2019年01月の記事
全14件 (14件中 1-14件目)
1
-

生徒実験:「コロイドの性質」生徒のレポート
生徒実験:「コロイドの性質」行いました→2019/1/25ブログの生徒レポートを評価しました。評価の高いレポートです。もう一つたくさんの生徒さんが質の高いレポートを書いてくれましたが、質問に正しく答えない。あるいは、答えられない生徒が多くいます。それは考察の⑤:「…セロファン膜の粒子の透過性について推測できることを記せ」という問いに対し、このような回答です。ここでは、「H+やCl-、未反応のFe3+がセロファン膜を通過する」ことに気がついてもらいたい。「存在する」ことがわかっても、そこからどんな結論が出るか書いて欲しいのです。それがない。このほか「推測できることを記せ」という質問が並んでいますが、どうもピント外れの回答が多いのが気になります。何を調べるための実験操作か?それを意識して実験してもらえるように、実験直前の説明で強調するのですが、手を動かしながら考えられないのでしょうか?私は、生徒実験をとても大切にしていますが、どうなんでしょうか?生徒にとっては、授業の方が身につくんでしょうかね〜…
2019.01.31
コメント(0)
-

反応熱の演示実験:チオ硫酸ナトリウムの溶解熱
授業で「化学反応とエネルギー」に入りました。今日は「反応熱の種類」で燃焼熱や中和熱などを紹介します。いつも、生徒には教室でチオ硫酸ナトリウム五水和物Na2S2O3・5H2Oの過飽和溶液から結晶が析出する時の発熱反応を体験してもらっています。寒い季節、小さな試験管が結晶析出とともに意外に熱くなるのが評判いいです。高さ10cmの小さな試験管に5g弱のチオ硫酸ナトリウムを入れて、振りながら15秒ほど加熱すると少し濁った過飽和溶液になります。結晶水に溶解します。そのまま、試験管立てに放置して15分ほどで人肌の温度に。30分もすると室温くらいに冷えてきました。これを教室に持っていき、列ごとに回覧したのち、結晶を落としてやるとすぐさま全体に結晶が析出します。チオ硫酸ナトリウムの溶解熱は吸熱です。従って結晶析出時は発熱となります。過飽和溶液ですので以下の式は当てはまりませんが、目安に載せておきます。Na2S2O3・5H2O + aq =Na2S2O3aq - 47.2kJ<後始末>・ホコリを入れないようにすれば何度でも使えます。・捨てるなら、大量の水で希釈して下水に流して構わないと思います。・そもそも、塩素の中和剤です。環境ではすぐに分解されるでしょう。・ラットのLD50も十分高いので安全データシートでは「区分外」となっています。動画はこちら溶解熱の演示…チオ硫酸ナトリウムの過飽和溶液→2021/10/13ブログ
2019.01.29
コメント(0)
-

生徒実験(①計画、実験テキスト):ヘスの法則
昨年の生徒実験「ヘスの法則」では、固体水酸化ナトリウムの溶解熱Q1水酸化ナトリウム水溶液と塩酸の中和熱Q2固体水酸化ナトリウムと塩酸の反応熱Q3を測定し、Q1+Q2=Q3になるというヘスの法則の検証を行いました。発泡ポリスチレンのカップを使って最高上昇温度をはかり、そこから発熱量Q1〜Q3を計算しました。生徒実験:反応に伴う熱の出入りとヘスの法則(予備実験)→18/1/31ブログ生徒実験:反応に伴う熱の出入りとヘスの法則(実施)→18/2/2ブログ生徒実験:反応に伴う熱の出入りとヘスの法則(生徒のレポート)→18/2/7ブログ今年は、発熱に伴う温度上昇を記録してグラフにし、外挿して温度上昇度Δtを求めるデータ処理を加えてみようと計画しました。以下生徒用のテキストです。テキストに従って予備実験をする予定です。
2019.01.28
コメント(0)
-

生徒実験:「コロイドの性質」行いました
本日、「コロイドの性質」の生徒実験を行いました。次に予備実験や昨年の生徒実験(予備実験〜生徒実験〜生徒レポート)のリンクも貼ってあります。生徒実験(予備実験):コロイドの性質19/1/22ブログさて、テキストです。実験室のホワイトボードです。これに従って実験して実験テキストの結果・考察を記入してもらい、次の授業(火曜日)に提出です。【実験2】[3]ブラウン運動は教卓に光学顕微鏡を2台置いて、uniPOSKAというマーキングペンインクに水を加えた液滴をホールスライドグラスに乗せて観察してもらいます。2台しかないので、実験中の待ち時間に自由に見てもらうことにしました。以下は、接眼レンズにスマホのカメラをくっつけて撮ったものです。ピントが甘いのですが、実際は小さな点が光ってぶるぶる動いています。昨年と変更したところは、Fe(OH)3コロイド溶液(疎水で正コロイド)の業績の実験です。上の写真で左は3mol/L,NaCl水溶液2mLでやっと沈殿が生じた中央は比較用に何も加えていない右は0.5mol/L,Na2SO4水溶液1滴で沈殿が生じた0.5mol/LのNa2SO4水溶液を1滴滴下すると、すぐに沈殿が生じますが、3mol/LのNaCl水溶液を2mLくらい滴下しないと沈殿が生じない。正コロイドは陰イオンを加えると凝析を起こします。その際、一価のCl-より二価のSO42-イオンがとても効果的なのをこの実験で確認できるでしょう。説明とFe(OH)3コロイド溶液を作る演示で15分、生徒実験に35分でした。洗って片付けに5分以上かかり、授業時間の50分を超えてしまいました。意外に時間がかかるのは、セルロースチューブを水中でほぐし、タコ糸で縛る作業。実験準備の時に、セルロースチューブを先にビーカーの水中に入れてふやかしておくと作業が早く進むかなと思いました。
2019.01.25
コメント(0)
-

生徒実験(予備実験):コロイドの性質
「コロイド溶液」の授業に入りました。生徒実験を行います。学習内容の確認実験をして、生徒への内容定着をはかります。以下、昨年の予備実験から生徒レポートまでの内容です。生徒実験:コロイド溶液の性質(予備実験)→18/1/25ブログ生徒実験:コロイド溶液の性質(実施)→18/1/29ブログ生徒実験:コロイド溶液の性質(レポート)→18/1/30ブログ今年も予備実験を行い、実験内容に変更を加えました。①50mLの沸騰純水に塩化鉄(Ⅲ)2mLを加えて、水酸化鉄(Ⅲ)コロイド溶液を作る操作を演示にしました。教卓に集めて、500mLのコロイド溶液を作り、冷ましたものを生徒に配布します。沸騰純水500mLにゆっくり20%塩化鉄(Ⅲ)溶液を滴下しました。とても濃いコロイド溶液になりますが、この後の実験で透析した純水に、BTB溶液、硝酸銀溶液、ヘキサシアニド鉄(Ⅱ)酸カリウムを加える実験で結果が昨年よりはっきり出ました。5分間静置して透析します。左から透析した純水にBTB溶液→H+の検出、硝酸銀溶液→Cl -の検出、ヘキサシアニド鉄(Ⅱ)酸カリウム溶液→Fe3+の検出と明確に確認できます。②水酸化鉄(Ⅲ)コロイド溶液(疎水コロイド)に0.5mol/LNa2SO4溶液を1滴加えるとすぐ沈殿してしまいますが、3mol/Lの塩化ナトリウム水溶液では2mLも加えないと沈殿しません。2価の硫酸イオンは1価の塩化物イオンよりはるかに効果的に凝析を起こすことを示す実験を加えました。中央が水酸化鉄(Ⅲ)コロイド溶液。右は0.5mol/LNa2SO4水溶液を1滴落としたコロイド溶液。左は3mol/LNaCl水溶液を濁りが出るまで加えたコロイド溶液、NaCl水溶液は2mLでやっと沈殿が出ました。<シュルツ・ハーディーの法則>水酸化鉄(Ⅲ)コロイドは疎水コロイドで正の電荷を持っています。凝析させるには陰イオンが必要です。その凝析力は陰イオンの電荷の価数が大きいほど強くなります。その凝析力はイオンの価数の6乗に反比例するそうです(経験則だそうです)。1価の陰イオンを基準にすると、2価では2^6=64倍、3価では3^6=729倍の凝析力があることになります。だから、昨年行った予備実験では0.5mol/LのNaCl溶液をいくら入れても濁らなかったのです。今年は試しに3mol/Lにしたら濁りが出ましたので、生徒実験に加えることにしました。
2019.01.22
コメント(0)
-
「凝固点降下で分子量を求める」生徒実験レポート
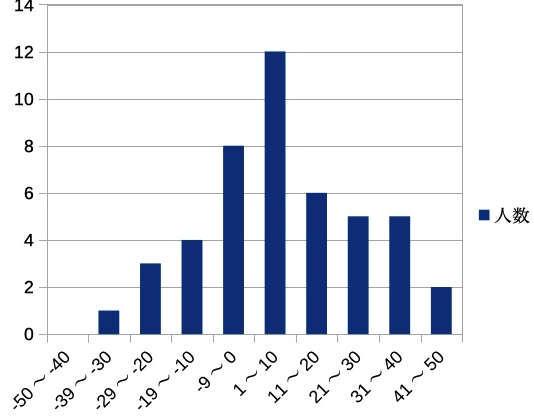
毎年、生徒実験「凝固点降下で分子量を求める」を行なっていますが、生徒実験の結果に満足いきません。溶質のナフタレンC10H8=128を実験結果から求めさせますが、誤差が大きいです。昨年は「凝固点降下で分子量を求める」⑤レポートに青ざめる→2018/1/9ブログにあるように、誤差の原因としてあげたのが以下でした①ナフタレンを溶かして溶液を作るときに、完全に溶解していない②グラフから凝固点を求める操作がわかっていない今年は、実験前の指導の時に上記①②を強調して話しました。さて、実験レポートなんですが、以下のように誤差が大きい縦軸人数、横軸誤差%です。−40%から+50%まで広がってしまいました。あいかわらず、グラフ処理を間違えたり、乱暴にやって誤差が大きくなる原因となっている生徒が多いです。しかし、「そもそも実験方法や温度計や天秤など装置に問題があるのでは」と不安になってきました。そこで、後からですが、①天秤(感量10mg)に分銅をのせ確認しました。これは問題なしです。②使い込んだ古いデジタル温度計は正確なのか?新しいものを購入する予定があるのでそちらに期待しています。③新たな実験方法を開発し直す。今年の最初のベンゼン屋の作業は③「凝固点降下で分子量を求める」生徒実験の開発に決まりました。多少の生徒の手抜きがあっても、分子量の誤差が少なくなるような実験を作っていこうと思います。色々アイディアがあります。試案ができたらまたアップします。さて、生徒のレポートの特徴的なものを掲載します。①まあまあ、良かったグラフです。②縦軸1℃を0.8cmにとったグラフ、記入しにくいし、読みにくい。ミスの元だと思います。縦軸の原点を0℃にする必要はないのです。これは、グラフ処理の時に注意しておいたのですが、聴き損ねたかな?③グラフを小さく書いていて、凝固点の読み取りに誤差が出やすい④どうにも意味不明な処理をしたグラフ以上ですが、これらのグラフについて今日の授業の冒頭で指導しました。生徒のグラフ処理の未熟さは大いにあります。しかし、実験をしっかり準備した上でないと、これらの指導を厳しくできません。
2019.01.18
コメント(0)
-

「凝固点降下で分子量を求める」③生徒実験
H30版「凝固点降下で分子量を求める」予備実験→1/13ブログ濃度はどこまで濃くてい良いか「凝固点降下で分子量を求める」予備実験②→1/15ブログ準備してきました「凝固点降下で分子量を求める」生徒実験を行いました。実験の概要とプリントは予備実験に示しましたので、冒頭のリンクから1/13のブログをご覧ください。シクロヘキサンは教卓で10mLくらい試験管に配布します。実験の流れをホワイトボードに、プリントとグラフの例をプロジェクターでホワイトボード右に示しました。以下のようなグラフ(こんな感じで書いてねという例です)を手書きでグラフ用紙に書いてもらって、明日提出です。考察は全てグラフ用紙の空いている部分に書いてもらい、グラフ用紙だけ提出してもらいます。実験の説明10分、生徒実験(片付け含む)25分、グラフの書き方、考察・計算の方法説明10分です。残り時間はグラフ作成に取り掛かってもらいました。2クラス行いました。さて、どうなるか評価し、概要を後ほどおしらせします。
2019.01.16
コメント(0)
-

濃度はどこまで濃くてい良いか「凝固点降下で分子量を求める」予備実験②
H30版「凝固点降下で分子量を求める」予備実験→1/13ブログで準備しましたが、事前にナフタレンの濃度について検討しました。希薄溶液というけれど、どこまで濃度を高くしても通用するのでしょう?化学部の生徒に実験してもらいました。ナフタレンC10H8のシクロヘキサン溶液の凝固点降下度からナフタレンの分子量を予備実験と同じ条件で実験します。ただし、様々な濃度でナフタレン(分子量128)の分子量を計算しました。横軸に質量モル濃度、縦軸に算出したナフタレンの分子量を示します。かなり高濃度まで、誤差なく分子量を算出できました。境界値0.2mol/Kgです。これ以上はバラついてきます。予備実験では、0.1mol/Kg前後です。誤差を考えると量が多い方(濃度が高い方)がいいのですが、高い濃度で何度も確認していないので、今年も0.1mol/Kgで行います。濃度については、今後も精査していきます。
2019.01.15
コメント(0)
-

H30版「凝固点降下で分子量を求める」予備実験
「希薄溶液の性質」の授業では、凝固点降下の実験を行います。予備実験をしながら、実験テキストを作り直し、指導法を再検討しました。特に、グラフの書き方と、凝固点の求め方について、指導を考えないといかんなー。昨年の予備実験です。「凝固点降下で分子量を求める」予備実験①→2018/1/11ブログ「凝固点降下で分子量を求める」予備実験②上手く結果を出すコツ→2018/1/11ブログこれを生かして、以下の注意をします。今年のテキストです。昨年と少し変えました(ほぼ同じなんですけど)。手書きの赤は生徒に、青はこちら側の準備に。注意事項です。実験の準備と実験です。5秒おきに4分はかりました。実験操作は30分。そして結果です。このデータに基づいて、生徒には手書きでグラフを書いてもらいますが、表計算で作りました。データが多いので横書きにしました。生徒には縦軸1cm=1℃で横書きをすすめようと思います。実験には、実習助手の先生も参加してもらい二人で9班を指導する予定です。予備実験では、指導の打ち合わせも行います。
2019.01.13
コメント(0)
-
数学X音楽:中島さち子氏の講演会へ行ってきました
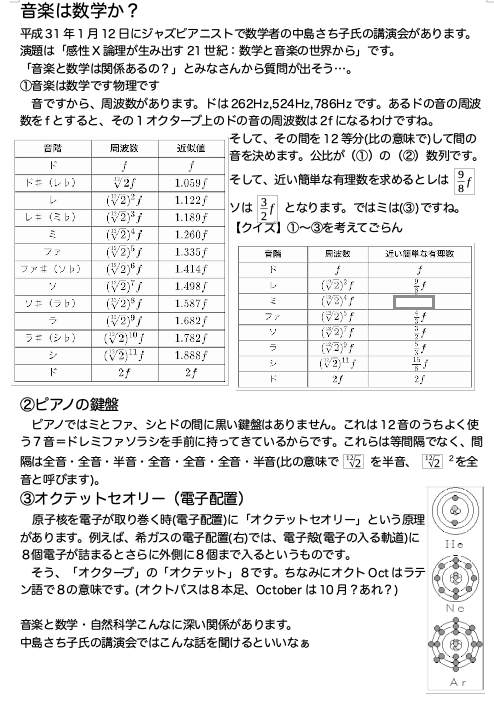
数学者でジャズピアニストの中島さち子氏の講演会へ行ってきました。学校の隣駅の市民会館の小ホールで行われました。生徒用に作った案内プリントです。中島さち子氏はピアニスト&作曲家・数学者・STEAMS教育者、というなんとも多彩。高校生の時は、国際数学オリンピックで金と銀を2年連続で取った方です。現在はフルブライト留学生でアメリカ在住です。STEM(Science/Tecnology/Engneering/Mathematics)の略でリアルな社会にどう役立つか、プロジェクトベースで、教科横断的に取り組もうという姿勢です。これに、A(Art)とS(Sports)を中島さんが取り入れて、学際的に取り組む教育を進めています。で、講演会の話の中心は(高校生向きなので)①音階と倍音②対称性(バッハの曲と図形の敷き詰め)でした。①音階と倍音音階の歴史と素数の歴史サインカーブである音に深みを与える音色には倍音が関わるなどの話。②対称性(バッハの曲と図形の敷き詰め)バッハのカノンの楽譜が示されて、音符の配置に縦横線対称と平行移動があること昔からバッハは大好きで、その心地よさはこの辺りにあったのかもしれない。私にとって新しい発見でした。さらに、「図形の敷き詰め」同じ図形を平行移動させたり、回転させたりして敷き詰めていきます。これも、アートと数学の融合です。平行移動、(様々な角度で)回転などを使って図形を隙間なく敷き詰めていくのですが、そのパターンは17種であると数学的に証明されているようです。実は、アルハンブラ宮殿のタイルの敷き詰め方も最大の17種。和服の模様の敷き詰めパターン最大の17種だそうです。過去の人たちの、すごいところですね。この「図形の敷き詰め」は、これも大好きなエッシャーのモチーフです。エッシャー展@上野の森美術館→2018/7/9ブログなんだかワクワクする講演会でした。内容が「アートと数学」であることが、私の趣味にあったのでしょう。なぜ、バッハやエッシャーが好きなのか、講演会で解きほぐしてもらえたような気がします。2:30-4:30までの講演会でしたが、あっという間に過ぎました。
2019.01.12
コメント(0)
-
モバイルルーターUQ Wimax2+にネット接続を変えました
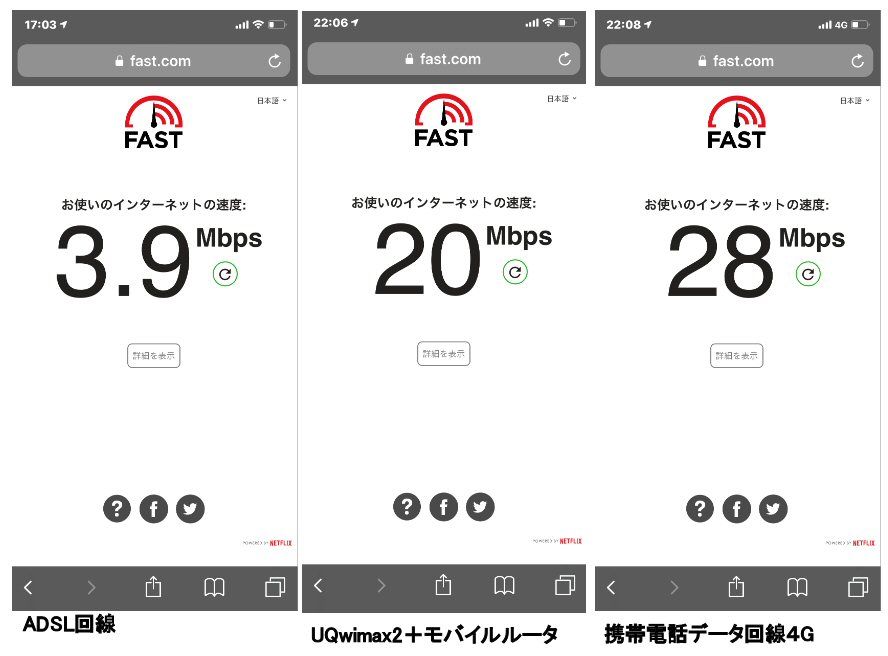
新年初仕事。我が家のネット環境を見直しました。理由は、これまで①家ではADSLで3.9Mbpsと遅くダウンロード・アップロードに時間がかかっていた②固定回線の電話はADSL接続のためにしか使われていない③学校でネット利用に制限があり、授業用動画などダウンロードできないそこで①NTTで固定回線の電話を解約し、プロバイダーでADSLを解約②携帯の更新時期だったので、データを2G→5Gに増量③携帯電話の通話時間無制限→5分に変更④モバイルルーターをGMOでUQ Wimax「ギガ放題」契約しました。上図のADSL回線がこれまでのもの。特にブログや写真などアップロードやソフトのバージョンアップに時間がかかっていました。2列目のモバイルルータにして5倍にスピードアップしました。回線がすいているときは40Mbpsくらいまで上がります。ちなみに、携帯電話の回線4Gは28Mbpsで我が家では最速。しかし、データ量の制限があり最大にするととても高い料金を取られます。光ケーブルにすると月額使用料がとても高くなり、初めから選択肢にありませんでした。そこで、UQ Wimax2+ という回線を選択しました。①ほぼデータ量無制限で、月額3600円程度。②小さくてポータブルなので家庭・学校・出先でiPadやMacNoteを使える③Wi-Fiルーターの機能があり、プリンタなど接続して使える④クレードルをつけると有線LANを1系統つなぐことができる 有線LANは我が家のメインのコンピューターWindows10につないであります⑤横17cm,縦5cmくらいの大きさで、小さめのスマホくらいの大きさと重さです。家庭で使わないときはクレードルから、すっと抜いて内蔵電池でつかいます。これで、これまでとほぼ同じ通信料金におさえることができそうです。<UQ Wimax2+の特徴>・データ量は「ギガ放題」で無制限。・ただし、3日で10GBの制限あり、超えると翌日18:00-2:00まで通信速度が1Mbpsになる。 ちょっと、3日10GBの制限を超すのではないかと不安が残りますが、超えた翌日でも2:00-18:00までは通常の高速でつかえますので、仕事には差し支えなさそうです。 また、携帯電話の制限を超えると0.12Mbpsに速度ダウンされてしまいますが、WiMAXでは1Mbpsなら何とか使えそうです。・電波が2.5GHzで障害物に弱く、部屋の奥では弱くなる(我が家では部屋の奥でアンテナ4本フルから3本。LTEや4Gでは800MHzで建物の奥まで届く)・光やADSLなど工事が不要・通信範囲が広い=いろいろな場所で使えるUQと直接契約する方法もありましたが、様々なMVMO(SO-NETなど)が特典付きでした。特典をかんがえて、今回はGMOというMVMOで契約しました。キャッシュバックが高かったからです。しばらく、これで使ってみようと思いますがあいかわらず不安があります。何か問題があったらレポートします
2019.01.07
コメント(0)
-

「日本を変えた千の技術博」上野科学博物館
上野公園、国立科学博物館の特別展「日本を変えた千の技術博」をみてきました。地味な特別展なので、正月土曜日も関わらず比較的空いていました。目指したのは、①日本初のブルドーサー太平洋戦争でフォリピンの飛行場を作るために小型のブルドーザーを作る必要があったので、小松製作所が作ったものです。戦後、アメリカ軍に海中に投棄されたのですが、回収されオーストラリアの農場で使われていたものを日本に戻したとのことです。戦時中ながらしっかりしたものづくりをしたからこそ、ちゃんと歴史を背負えるのですね。日本のものづくりに感動します。②アンモニア合成関連ハーバー・ボッシュ法で授業で扱われるアンモニア合成です。空気から窒素N2を取り出す際の装置「リンデ式空気液化分留機」です。これで、取り出したN2とH2を使って高温高圧でN2+3H2⇆2NH3アンモニアを合成するのです。肥料の原材料となって、農業生産性をとてもあげることができました。より低い温度・圧力で合成するために触媒を使うのですが、ここで高効率の触媒を日本人が作りました。ルテチウムを使った触媒です。詳しくは以下。③乾電池は日本人が作ったこれもまた、授業で扱う乾電池です。日本人が作りました。屋井乾電池です。それまで、電解質が液体だったので液漏れが問題だったのですがこれで持ち運びが便利になりました。この他、八木アンテナ、日本語ワープロ、ウォークマン、電卓、零戦のエンジンなど世界的な指標となる技術がたくさん。明治期から平成期までの技術が紹介されています。2019年3月3日までです。授業で使えるたくさんのものが展示されていました。
2019.01.06
コメント(0)
-
「なんで水銀は常温で液体なの?」②ーなんとか答えます
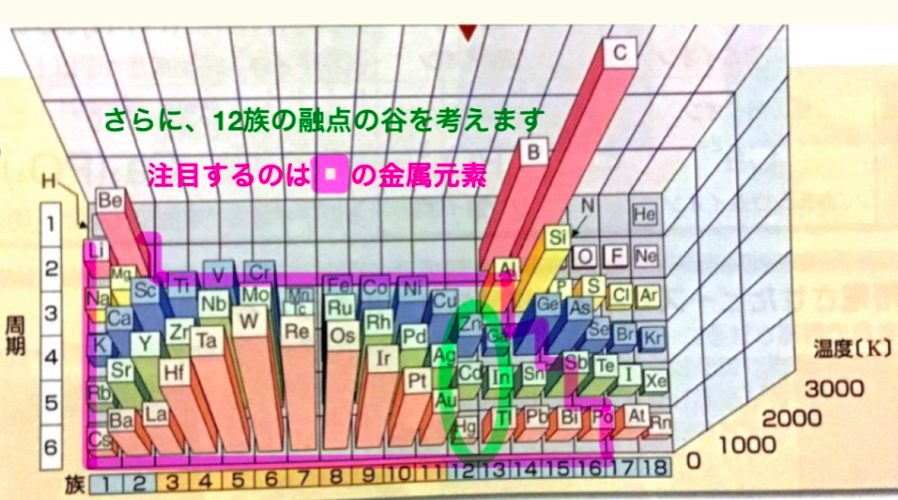
「なんで水銀は常温で液体なの?」①ー10歳の質問から→2017/12/29ブログ以来、高校生レベルまででどう説明するか、問題をどう切り分けて説明するか悩んできましたが、年越しちゃったし、ここでなんとか説明する努力をしてみたいと思います。2つの視点から説明してみようと思います。①今回注目するのは、金属元素のみです。上のグラフの赤枠。 5.6.7族を以外では、周期が大きくなるにつれて融点が下がっています。水銀Hgが液体(Zn-Cd-Hgと融点が下がる)傾向は金属元素の一般的傾向です。なぜそうなるのか、説明していきます。②13.14族に比べて12族は融点が特に低い(融点の谷のよう)。上のグラフの緑枠。 12族の最も外側の電子軌道はZn亜鉛N殻4s軌道、CdカドミウムO殻5s軌道、Hg水銀P殻6s軌道、それぞれ2つの電子が入っています。これが融点を下げる原因として説明できそうです。12/19のブログに続けて【4】から始めます。【4】融点と結合力の関係①温度が高くなると原子の振動は大きくなります。温度は原子の振動の目安です。②固体では原子が整然と並んでいますが、温度が高くなる(原子のブルブルが激しくなる)と並んでいた原子がほどけてバラバラになります。これが融点です。③融点は結合力(原子を並ばせておく引力)と温度(並んだ原子をバラバラにする運動)のバランスで決まります。「融点が高いということは結合力が強い」とわかります。【5】周期が大きくなると(周期表で下にいくほど)融点がさがる理由1族を例に話しします。どの族でも(Hgのある12族でも)同じです。周期が大きくなると、より外側の電子殻に電子が入るようになります。その結果、原子の半径(上の数字)は大きくなります。原子核はとても小さいので、原子の半径は周りを取り囲む雲のような電子集団の大きさです。上図上(1族)では原子が大きくなると、+とーの距離が離れて静電気的引力が弱まる様子を表しています。金属原子のサイズが大きくなる→結合力が弱まる→融点が下がる。最初の融点のグラフに現れるように、LI(融点180℃)-Na-K-Cs(28℃)と融点は下がっていきます。ついでに言うと、上図下(1族と2族)。1族では1つの原子から生じる自由電子とイオンは1つずつ。2族では1つの原子から2つの自由電子と2+の陽イオンが生じます。たくさんの自由電子により2+の陽イオンが引きつけられるのでより強い結合が生じます。したがって、1族と2族の融点を比べると2族の金属元素の融点はとても高いのです。【6】K.L.M.N…電子殻を構成するs.p.d.f電子軌道: 「12族、水銀Hgのなかまの融点はなぜ低いのか」を説明するには、電子殻を構成するs.p.d.f電子軌道の話をしなければなりません。s.p.d.f電子軌道のそれぞれには2つの電子が入ります。 K殻はs軌道によって作られています。s軌道に2つ電子が入っていっぱいです。 L殻はs軌道と3つのp軌道からなります。s軌道に2つ、3つのp軌道に6つ電子が入り、計8つの電子でL殻はいっぱいになります。 M殻はs軌道、3つのp軌道、5つのd軌道があり、18個の電子でいっぱいになります。 N殻はsと3つのp、5つのd、7つのfからできています。これらの軌道に電子が一つずつ入っていって色々な原子が作られます。その様子は以下の図で(ダイナミックワイド図説化学より)この図はK.L.M.N電子殻の電子軌道にどんな順で電子が詰まっていくかを表したものです。それぞれの電子軌道にぴったり電子が入ると原子は安定状態になります。例えば、Heヘリウムは1sに2つぴったり入り、電子の出し入れはしにくくなります(結合をつくらない)。Arアルゴンは3つのp軌道がちょうど満杯です。これも電子の出入りはしません。【7】12族、水銀Hgのなかまの融点はなぜ低いのか Hg水銀の融点の低さを説明するために、同じ12族Zn亜鉛の電子軌道の様子でお話しします。(Zn亜鉛ではN殻=1s(2)2s(2)2p(6)3s(2)…3d(10)4s(2))上の電子配置の図中Zn亜鉛をみてください(赤マーカー)。ちょうど、4s軌道にぴったり2つです。(Hg水銀ではP殻=1s(2)2s(2)2p(6)3s(2)…6d(10)6s(2))ちょうど電子が詰まると安定化し、電子を出したがらなくなる=自由電子が少なくなるので【5】で話したように結合力が弱まります。さらに、1s軌道や2s軌道は電子の運動スピードが速く(1sで光速の半分以上の速度)、光速近くで動く物体の質量はどんどん重くなり(相対論)、Hg水銀あたりでは電子は1s軌道で本来の質量の1.2倍になります(相対論効果)。相対論効果は原子番号の2乗に比例して大きくなります。相対論効果によれば、1sや2s軌道さらには2p軌道を回る電子はより原子核に近いところにあります。その周りにある電子軌道にも影響を与え、Zn亜鉛の4sやHg水銀の6s軌道もより原子核に近い=自由電子として離れ難い状態になっています。【8】まとめ:Hg水銀の融点が低い=常温で液体のわけ①原子が大きいので、自由電子(ー)と陽イオン(+)間の静電気力が弱い②6s電子軌道にちょうど電子が2つつまっていて、自由電子として放出しにくい(陽イオンにもなりにくい)③「相対論効果」により6s電子軌道が原子核に近く、原子核に束縛されやすくて自由電子として放出しにくい【9】お詫び この質問は説明するのに難しい。ずーっとどう答えるか悩んでいました。イメージとして伝えることができれば、小中高校生に伝わりやすいのですが、イメージが浮かんできません。量子力学や相対論は数学の世界です。これをビジュアライズすることは私にはできなかった。また、私自身の理解不足や勘違いもあるのではないか不安です。間違えていたらごめんなさい。もう少し、わかりやすい説明がありましたら教えてください。お願いします。
2019.01.02
コメント(0)
-

明けましておめでとうございます
昨年はたくさんの方にブログを見ていただき、また、模型をたくさん購入していただきありがとうございました。とっくに定年を過ぎて、今年から高校での講師生活が始まります。高校化学のの授業の中から、色々な実験方法や実験・講義の道具をたくさんの先生方に紹介したいとこのブログを始めたのが2017年の6月。以来、たくさんの方に見ていただき、アクセス数は10万5千を超えました。感謝しています。昨年の売上です。ありがとうございます。体心立方格子6.1cm42個、面心立方格子2億倍1個・6.1cm42個、ダイヤモンド2個NaCl型2億倍2個、CsCl型斜切り3個、体心立方格子斜切り3個、ZnS1個体心立方格子斜切りキット3個、ミニベンゼン3個、2億倍分子模型定規6枚これらの模型や定規はブログの左欄「フリーページ」に詳しくのせてあります。また、自分で作りたい方のために作りかたも詳しくのせてありますのでご覧ください。では、2019年も頑張ってアップしていきます。よろしくお願いします。
2019.01.01
コメント(0)
全14件 (14件中 1-14件目)
1










