PR
×
X
キーワードサーチ
▼キーワード検索
フリーページ
結晶構造模型の作り方
面心立方格子
体心立方格子
塩化セシウムCsCl斜め切りの詳しい作り方
体心立方格子斜め切り詳しい作り方
分子模型の作り方
ミニベンゼン8千万倍の作り方
2億倍分子模型の基本:H2O,CO2,NH3,CH4を作る
2億倍シクロヘキサンを作る・そのコツ
材料の入手:発泡スチロール球
発泡スチロール球の塗装
置換基入替え磁石付きベンゼンの作り方
置換基入替え磁石付き炭化水素基・水酸基の作り方
黒鉛2億倍の作り方
模型作りの道具
2億倍分子模型定規(1400円)
ニクロム線アクリル板曲げ機(キット300円)
販売中の結晶格子・分子模型
有機化合物2億倍フルキットの部分販売
金属とイオン結晶格子・分子模型
安価な生徒実験用機器
733円電池式速度可変スターラー
380円超小型スターラー
1500円で作る定電流電源(ファラデーの法則実験)
カレンダー
コメント新着
サイド自由欄
楽天プロフィールをフォローしていただくと
ブログの更新がすぐわかります
[問い合わせ] benzeneya☆yahoo.co.jp
☆→@
分子と人間 (SAライブラリー) [ ピーター・W.アトキンス ]
身近な分子たち 空気・植物・食物のもと
ブログの更新がすぐわかります
[問い合わせ] benzeneya☆yahoo.co.jp
☆→@
分子と人間 (SAライブラリー) [ ピーター・W.アトキンス ]
身近な分子たち 空気・植物・食物のもと
![[商品価格に関しましては、リンクが作成された時点と現時点で情報が変更されている場合がございます。] [商品価格に関しましては、リンクが作成された時点と現時点で情報が変更されている場合がございます。]](https://hbb.afl.rakuten.co.jp/hgb/15d15eb9.827daec8.15d15eba.0eddb21e/?me_id=1313796&item_id=10000071&m=https%3A%2F%2Fthumbnail.image.rakuten.co.jp%2F%400_mall%2Fkin-kyoto%2Fcabinet%2F04499399%2Facl_2_450_600.jpg%3F_ex%3D80x80&pc=https%3A%2F%2Fthumbnail.image.rakuten.co.jp%2F%400_mall%2Fkin-kyoto%2Fcabinet%2F04499399%2Facl_2_450_600.jpg%3F_ex%3D128x128&s=128x128&t=picttext)
|
アクリル 板 2mm厚 450×600mm アクリル アクリル板 プラスチック 透明 窓 パーテーション 棚 戸 扉 建具 コレクションケース ボード コレクションラック フィギュア ケース ガラス
|
結晶模型表面はアクリル板をカットして作ります
テーマ: 化学(351)
カテゴリ: 授業
「なんで水銀は常温で液体なの?」①ー10歳の質問から
以来、高校生レベルまででどう説明するか、問題をどう切り分けて説明するか悩んできましたが、
年越しちゃったし、ここでなんとか説明する努力をしてみたいと思います。
2つの視点から説明してみようと思います。
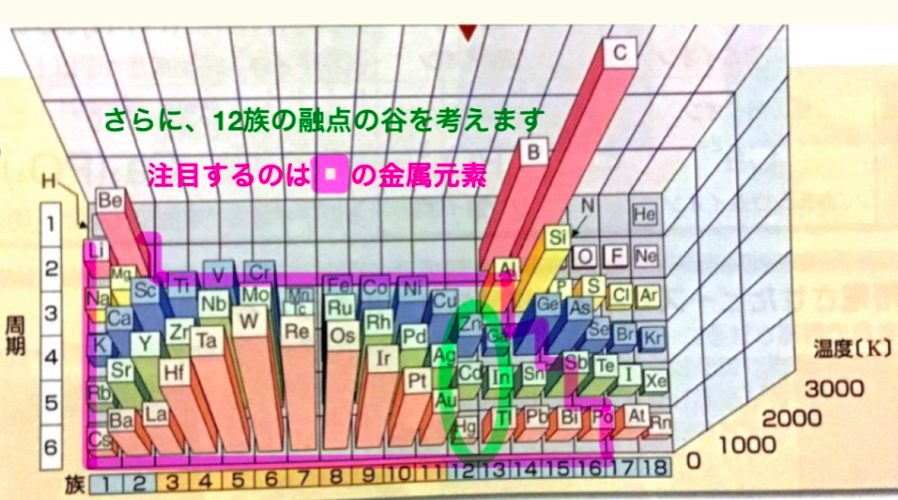
①今回注目するのは、金属元素のみです。上のグラフの赤枠。
5.6.7族を以外では、周期が大きくなるにつれて融点が下がっています。
水銀Hgが液体(Zn-Cd-Hgと融点が下がる)傾向は金属元素の一般的傾向です。
なぜそうなるのか、説明していきます。
②13.14族に比べて12族は融点が特に低い(融点の谷のよう)。上のグラフの緑枠。
12族の最も外側の電子軌道はZn亜鉛N殻4s軌道、CdカドミウムO殻5s軌道、Hg水銀P殻6s軌道、それぞれ2つの電子が入っています。これが融点を下げる原因として説明できそうです。
12/19のブログに続けて【4】から始めます。
【4】融点と結合力の関係
①温度が高くなると原子の振動は大きくなります。温度は原子の振動の目安です。
②固体では原子が整然と並んでいますが、温度が高くなる(原子のブルブルが激しくなる)と並んでいた原子がほどけてバラバラになります。これが融点です。
③融点は結合力(原子を並ばせておく引力)と温度(並んだ原子をバラバラにする運動)のバランスで決まります。
「融点が高いということは結合力が強い」 とわかります。
【5】周期が大きくなると(周期表で下にいくほど)融点がさがる理由

1族を例に話しします。どの族でも(Hgのある12族でも)同じです。
周期が大きくなると、より外側の電子殻に電子が入るようになります。
その結果、原子の半径(上の数字)は大きくなります。原子核はとても小さいので、原子の半径は周りを取り囲む雲のような電子集団の大きさです。
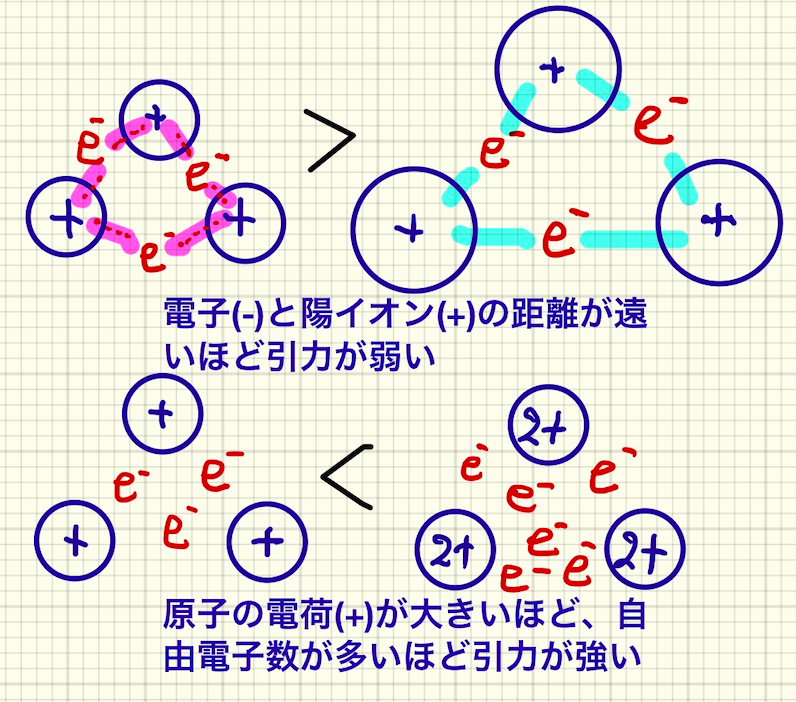
上図上(1族)では原子が大きくなると、+とーの距離が離れて静電気的引力が弱まる様子を表しています。
金属原子のサイズが大きくなる→結合力が弱まる→融点が下がる。
最初の融点のグラフに現れるように、LI(融点180℃)-Na-K-Cs(28℃)と融点は下がっていきます。
ついでに言うと、
上図下(1族と2族)。1族では1つの原子から生じる自由電子とイオンは1つずつ。2族では1つの原子から2つの自由電子と2+の陽イオンが生じます。たくさんの自由電子により2+の陽イオンが引きつけられるのでより強い結合が生じます。
したがって、1族と2族の融点を比べると2族の金属元素の融点はとても高いのです。
【6】K.L.M.N…電子殻を構成するs.p.d.f電子軌道:
「12族、水銀Hgのなかまの融点はなぜ低いのか」を説明するには、電子殻を構成するs.p.d.f電子軌道の話をしなければなりません。s.p.d.f電子軌道のそれぞれには2つの電子が入ります。
K殻はs軌道によって作られています。s軌道に2つ電子が入っていっぱいです。
L殻はs軌道と3つのp軌道からなります。s軌道に2つ、3つのp軌道に6つ電子が入り、計8つの電子でL殻はいっぱいになります。
M殻はs軌道、3つのp軌道、5つのd軌道があり、18個の電子でいっぱいになります。
N殻はsと3つのp、5つのd、7つのfからできています。
これらの軌道に電子が一つずつ入っていって色々な原子が作られます。その様子は以下の図で

(ダイナミックワイド図説化学より)
この図はK.L.M.N電子殻の電子軌道にどんな順で電子が詰まっていくかを表したものです。
それぞれの電子軌道にぴったり電子が入ると原子は安定状態になります。
例えば、Heヘリウムは1sに2つぴったり入り、電子の出し入れはしにくくなります(結合をつくらない)。
Arアルゴンは3つのp軌道がちょうど満杯です。これも電子の出入りはしません。
【7】12族、水銀Hgのなかまの融点はなぜ低いのか
Hg水銀の融点の低さを説明するために、同じ12族Zn亜鉛の電子軌道の様子でお話しします。
(Zn亜鉛ではN殻=1s(2)2s(2)2p(6)3s(2)…3d(10)4s(2))
上の電子配置の図中Zn亜鉛をみてください(赤マーカー)。ちょうど、4s軌道にぴったり2つです。
(Hg水銀ではP殻=1s(2)2s(2)2p(6)3s(2)…6d(10)6s(2))
ちょうど電子が詰まると安定化し、電子を出したがらなくなる=自由電子が少なくなるので【5】で話したように結合力が弱まります。
さらに、1s軌道や2s軌道は電子の運動スピードが速く(1sで光速の半分以上の速度)、光速近くで動く物体の質量はどんどん重くなり(相対論)、Hg水銀あたりでは電子は1s軌道で本来の質量の1.2倍になります(相対論効果)。相対論効果は原子番号の2乗に比例して大きくなります。
相対論効果によれば、1sや2s軌道さらには2p軌道を回る電子はより原子核に近いところにあります。
その周りにある電子軌道にも影響を与え、Zn亜鉛の4sやHg水銀の6s軌道もより原子核に近い=自由電子として離れ難い状態になっています。
【8】まとめ:Hg水銀の融点が低い=常温で液体のわけ
①原子が大きいので、自由電子(ー)と陽イオン(+)間の静電気力が弱い
②6s電子軌道にちょうど電子が2つつまっていて、自由電子として放出しにくい(陽イオンにもなりにくい)
③「相対論効果」により6s電子軌道が原子核に近く、原子核に束縛されやすくて自由電子として放出しにくい
【9】お詫び
この質問は説明するのに難しい。ずーっとどう答えるか悩んでいました。
イメージとして伝えることができれば、小中高校生に伝わりやすいのですが、
イメージが浮かんできません。量子力学や相対論は数学の世界です。
これをビジュアライズすることは私にはできなかった。
また、私自身の理解不足や勘違いもあるのではないか不安です。
間違えていたらごめんなさい。
もう少し、わかりやすい説明がありましたら教えてください。
お願いします。
以来、高校生レベルまででどう説明するか、問題をどう切り分けて説明するか悩んできましたが、
年越しちゃったし、ここでなんとか説明する努力をしてみたいと思います。
2つの視点から説明してみようと思います。

①今回注目するのは、金属元素のみです。上のグラフの赤枠。
5.6.7族を以外では、周期が大きくなるにつれて融点が下がっています。
水銀Hgが液体(Zn-Cd-Hgと融点が下がる)傾向は金属元素の一般的傾向です。
なぜそうなるのか、説明していきます。
②13.14族に比べて12族は融点が特に低い(融点の谷のよう)。上のグラフの緑枠。
12族の最も外側の電子軌道はZn亜鉛N殻4s軌道、CdカドミウムO殻5s軌道、Hg水銀P殻6s軌道、それぞれ2つの電子が入っています。これが融点を下げる原因として説明できそうです。
12/19のブログに続けて【4】から始めます。
【4】融点と結合力の関係
①温度が高くなると原子の振動は大きくなります。温度は原子の振動の目安です。
②固体では原子が整然と並んでいますが、温度が高くなる(原子のブルブルが激しくなる)と並んでいた原子がほどけてバラバラになります。これが融点です。
③融点は結合力(原子を並ばせておく引力)と温度(並んだ原子をバラバラにする運動)のバランスで決まります。
「融点が高いということは結合力が強い」 とわかります。
【5】周期が大きくなると(周期表で下にいくほど)融点がさがる理由

1族を例に話しします。どの族でも(Hgのある12族でも)同じです。
周期が大きくなると、より外側の電子殻に電子が入るようになります。
その結果、原子の半径(上の数字)は大きくなります。原子核はとても小さいので、原子の半径は周りを取り囲む雲のような電子集団の大きさです。

上図上(1族)では原子が大きくなると、+とーの距離が離れて静電気的引力が弱まる様子を表しています。
金属原子のサイズが大きくなる→結合力が弱まる→融点が下がる。
最初の融点のグラフに現れるように、LI(融点180℃)-Na-K-Cs(28℃)と融点は下がっていきます。
ついでに言うと、
上図下(1族と2族)。1族では1つの原子から生じる自由電子とイオンは1つずつ。2族では1つの原子から2つの自由電子と2+の陽イオンが生じます。たくさんの自由電子により2+の陽イオンが引きつけられるのでより強い結合が生じます。
したがって、1族と2族の融点を比べると2族の金属元素の融点はとても高いのです。
【6】K.L.M.N…電子殻を構成するs.p.d.f電子軌道:
「12族、水銀Hgのなかまの融点はなぜ低いのか」を説明するには、電子殻を構成するs.p.d.f電子軌道の話をしなければなりません。s.p.d.f電子軌道のそれぞれには2つの電子が入ります。
K殻はs軌道によって作られています。s軌道に2つ電子が入っていっぱいです。
L殻はs軌道と3つのp軌道からなります。s軌道に2つ、3つのp軌道に6つ電子が入り、計8つの電子でL殻はいっぱいになります。
M殻はs軌道、3つのp軌道、5つのd軌道があり、18個の電子でいっぱいになります。
N殻はsと3つのp、5つのd、7つのfからできています。
これらの軌道に電子が一つずつ入っていって色々な原子が作られます。その様子は以下の図で

(ダイナミックワイド図説化学より)
この図はK.L.M.N電子殻の電子軌道にどんな順で電子が詰まっていくかを表したものです。
それぞれの電子軌道にぴったり電子が入ると原子は安定状態になります。
例えば、Heヘリウムは1sに2つぴったり入り、電子の出し入れはしにくくなります(結合をつくらない)。
Arアルゴンは3つのp軌道がちょうど満杯です。これも電子の出入りはしません。
【7】12族、水銀Hgのなかまの融点はなぜ低いのか
Hg水銀の融点の低さを説明するために、同じ12族Zn亜鉛の電子軌道の様子でお話しします。
(Zn亜鉛ではN殻=1s(2)2s(2)2p(6)3s(2)…3d(10)4s(2))
上の電子配置の図中Zn亜鉛をみてください(赤マーカー)。ちょうど、4s軌道にぴったり2つです。
(Hg水銀ではP殻=1s(2)2s(2)2p(6)3s(2)…6d(10)6s(2))
ちょうど電子が詰まると安定化し、電子を出したがらなくなる=自由電子が少なくなるので【5】で話したように結合力が弱まります。
さらに、1s軌道や2s軌道は電子の運動スピードが速く(1sで光速の半分以上の速度)、光速近くで動く物体の質量はどんどん重くなり(相対論)、Hg水銀あたりでは電子は1s軌道で本来の質量の1.2倍になります(相対論効果)。相対論効果は原子番号の2乗に比例して大きくなります。
相対論効果によれば、1sや2s軌道さらには2p軌道を回る電子はより原子核に近いところにあります。
その周りにある電子軌道にも影響を与え、Zn亜鉛の4sやHg水銀の6s軌道もより原子核に近い=自由電子として離れ難い状態になっています。
【8】まとめ:Hg水銀の融点が低い=常温で液体のわけ
①原子が大きいので、自由電子(ー)と陽イオン(+)間の静電気力が弱い
②6s電子軌道にちょうど電子が2つつまっていて、自由電子として放出しにくい(陽イオンにもなりにくい)
③「相対論効果」により6s電子軌道が原子核に近く、原子核に束縛されやすくて自由電子として放出しにくい
【9】お詫び
この質問は説明するのに難しい。ずーっとどう答えるか悩んでいました。
イメージとして伝えることができれば、小中高校生に伝わりやすいのですが、
イメージが浮かんできません。量子力学や相対論は数学の世界です。
これをビジュアライズすることは私にはできなかった。
また、私自身の理解不足や勘違いもあるのではないか不安です。
間違えていたらごめんなさい。
もう少し、わかりやすい説明がありましたら教えてください。
お願いします。
お気に入りの記事を「いいね!」で応援しよう
[授業] カテゴリの最新記事
-
NotebookLMに教科書を読んでもらった 2026.05.09
-
ホームページを新しくしました 2026.04.27
-
気体の性質まとめ(ボイルシャルルから状態… 2026.01.26
【毎日開催】
15記事にいいね!で1ポイント
10秒滞在
いいね!
--
/
--
© Rakuten Group, Inc.




![[商品価格に関しましては、リンクが作成された時点と現時点で情報が変更されている場合がございます。] [商品価格に関しましては、リンクが作成された時点と現時点で情報が変更されている場合がございます。]](https://hbb.afl.rakuten.co.jp/hgb/15d44903.82c9af6a.15d44904.4dd050e5/?me_id=1278256&item_id=11652305&m=https%3A%2F%2Fthumbnail.image.rakuten.co.jp%2F%400_mall%2Frakutenkobo-ebooks%2Fcabinet%2F9056%2F2000000219056.jpg%3F_ex%3D80x80&pc=https%3A%2F%2Fthumbnail.image.rakuten.co.jp%2F%400_mall%2Frakutenkobo-ebooks%2Fcabinet%2F9056%2F2000000219056.jpg%3F_ex%3D128x128&s=128x128&t=picttext)






