公費 0
[医学の歴史] カテゴリの記事
全202件 (202件中 1-50件目)
-

ステミラック注
2018年札幌医科大の本望修教授らとニプロが開発した、脊髄損傷の治療に用いる自己骨髄間葉系幹細胞を使う細胞製剤「ステミラック注」の製造販売が、厚生労働省に条件及び期限付き承認された。ステミラック注(すてみらっくちゅう)は、ニプロと札幌医科大学が共同で開発した脊髄損傷の治療薬のこと。脊髄損傷への再生医療製品の販売承認としては世界初となる。概要患者自身の骨髄液から、神経や血管などに分化する能力を持つ間葉系幹細胞を採取。この細胞を約1万倍に増殖させ、5千万~2億個の幹細胞を生理食塩液で3倍以上に希釈しながら点滴注射する。投与は1回。対象は受傷後31日を目安に骨髄液採取の実施が可能な患者で、慢性的な患者への有効性は確認されていない。歴史2013年12月、札幌医科大学で治験開始。13人の患者が対象で13人中12人に身体の感覚が戻ったり手足が動いたりするなど目に見える効果が見られ、安全性も確認され、有意な副作用もなかった。2016年、「先駆け審査指定制度」の対象に指定される。2018年11月22日、厚生労働省の再生医療製品を審議する部会がニプロと札幌医科大学が開発した脊髄を損傷した患者の骨髄液から「間葉系幹細胞」を採取し、点滴で戻す「ステミラック注」の製造を承認した。治療の対象は自力で歩けないなど比較的重症の患者で、損傷から1カ月以内に骨髄を採取し、失われた感覚や運動機能の改善が期待されるとされる。2018年11月 札幌医科大学で慢性期患者対象の治験開始。2019年2月20日、中央社会保険医療協議会総会で、ヒト細胞加工製品(ヒト体性幹細胞加工製品)として「ステミラック注」の2019年2月26日付けで薬価基準収載が決定した。対象は、外傷性脊髄損傷で、ASIA機能障害尺度がA、B、又はCの患者に限られる。収載された薬価は、1回分14,957,755円。受注開始は2019年4月で、供給当初においては、札幌医科大学附属病院のみへの提供となる。批判2019年1月、イギリスの科学雑誌「ネイチャー」が、「投与群と非投与群の患者を比較して治療効果を科学的に評価するランダム化比較試験が実施されていない」、「静脈注射によって全身投与された間葉系幹細胞が脊髄の再生に繋がるという仮説自体が、今までのエビデンスに反している」などの点を指摘し、日本はより透明性の高いシステムを導入すべきだと批判した。出典: フリー百科事典『ウィキペディア(Wikipedia)』脊髄損傷者の看護 大事なポイントがすべてわかる!実践できる! 病態、合併症、リハビリテーション、看護まで/吉備高原医療リハビリテーションセンター看護部【3000円以上送料無料】
2021.07.15
コメント(0)
-

南方科技大学
2018年南方科技大学の賀建奎がヒト受精卵にHIVに感染しにくい遺伝子編集を施し、双子が誕生。賀の行為は生命倫理に反する行為として世界的な反発を招いた。南方科技大学(なんぽう-かぎ-だいがく、英語: Southern University of Science and Technology (SUSTech))は、中華人民共和国深圳市南山区に本部を置く中国の公立大学である。2011年に設置された。出典: フリー百科事典『ウィキペディア(Wikipedia)』CRISPR(クリスパー) 究極の遺伝子編集技術の発見 [ ジェニファー・ダウドナ ]
2021.07.14
コメント(0)
-
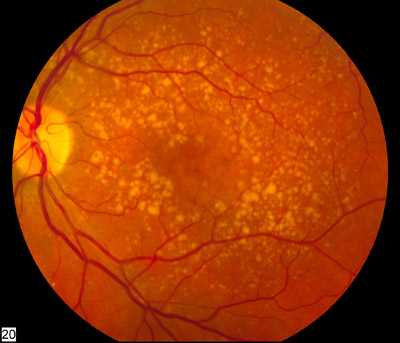
滲出型加齢黄斑変性
2014年理化学研究所と先端医療センター病院は、滲出型加齢黄斑変性患者に、iPS細胞から作った網膜の細胞を移植した。世界初のiPS細胞の臨床適用例。加齢黄斑変性(かれいおうはんへんせい、英: age-related macular degeneration、AMD)とは、加齢に伴い眼の網膜にある黄斑部が変性を起こす疾患である。失明の原因となり得る。以前は老人性円板状黄斑変性症と呼んでいた。またARMDと略していた頃もあった。症状としてはかすみ目や視野の中心に視覚障害を生じるが、初期は自覚症状がない事がよくある。しかし、時間の経過とともに、片方または両方の目に段階的な視力の低下を経験する場合もある。完全な失明になる事は少ないが、中心視力が失われることにより、顔の認識、運転、読書、その他の日常生活の活動が困難になる。視覚的な幻覚が見える場合があるが、これらは精神疾患によるものではない。黄斑変性は通常、高齢者に発生する。遺伝的要因と喫煙も起因となる。症状は網膜の黄斑の損傷によるものである。診断は精密な眼検査による[1]。重症度は、初期、中期、後期のタイプに分けられる。後期のタイプはさらに「萎縮型」と「滲出型」に分けられ、萎縮型が症例の90%を占める。予防法は、運動、バランスの取れた食事、禁煙などである[1]。一旦失われた視力を取り戻す治療法はない。滲出型は、眼への抗VEGF薬の注射、または、あまり一般的ではない光凝固法や光線力学療法により悪化を遅らせられる可能性がある[1]。抗酸化ビタミンとミネラルは予防に有用とは見做されない。しかし、栄養補助食品は、すでに病気に罹っている人の病状悪化を遅らせる可能性がある。2015年には、世界中で620万人が罹患した。2013年には白内障、早産、緑内障に次いで4番目に最も多い失明の原因であった。黄班変性は50歳以上の人に最も一般的に発生し、米国ではこの年齢層の視力喪失の最も一般的な原因である。黄班変性は50〜60歳の人の約0.4%が患っており、60〜70歳の人の0.7%、70〜80歳の人の2.3%、80歳以上の人の約12%に発生する。iPS細胞による治療の試み高橋政代(神戸理化学研究所網膜再生医療研究開発プロジェクト代表)は、2014年9月12日に自己由来のiPS細胞から作成した網膜を患者へ移植する臨床研究を世界で初めて実施した。これは加齢黄斑変性の治療を目的としたものである。これまで動物実験でのみ行われてきた人工的に作成した網膜を生体に移植する研究を実際に人体に応用した初期の例である。約1年後、該当する患者の視力はほとんど下がらず、腫瘍の発生もないと報告された。2017年2月には、神戸市立医療センター中央市民病院、大阪大学大学院医学系研究科、京都大学iPS細胞研究所、理化学研究所が申請していた他人由来のiPS細胞を使った滲出型加齢黄斑変性症の臨床試験に対し厚生労働省が計画を了承し、2017年4月から5人の患者に移植が実施された。2019年4月18日、理化学研究所らが他人由来のiPS細胞を使った滲出型加齢黄斑変性の治療を受けた5人の患者の術後1年の経過を報告。安全性が確認され、視力低下も抑えられた。5人とも移植細胞が定着しており、損なわれた目の構造が修復できたことも確認した。ただし、VEGF阻害剤投与では視力の改善が一般に見られるので、現在のところはVEGF阻害剤投与の方が施術の容易さ、コスト、視力回復の成績、の全てにおいて優れていると考えられる。出典: フリー百科事典『ウィキペディア(Wikipedia)』これで安心!中高年の目の病気 白内障・緑内障・加齢黄斑変性など/湯澤美都子/服部隆幸【3000円以上送料無料】
2021.07.13
コメント(0)
-
ニボルマブ
2014年ニボルマブ(商品名オプジーボ)がアメリカ、日本で承認される(ヨーロッパでは翌年)。世界初のヒトPD-1モノクローナル抗体医薬品。ニボルマブ(Nivolumab)は、当初悪性黒色腫治療を目的としており、現在では非小細胞肺癌などに適用拡大された分子標的治療薬の一つで、ヒト型抗ヒトPD-1モノクローナル抗体医薬品である。当時の京都大学医学部における本庶佑の研究チームが開発に貢献した。2014年7月に製造販売が承認され、2014年9月に小野薬品工業から発売が開始された。商品名オプジーボ。概要上皮性癌腫・非上皮性肉腫共に悪性腫瘍には、免疫系から逃れるための仕組みを持つ。悪性黒色腫と肺癌には、稀に自然治癒例が見られることがあり、免疫細胞により癌細胞が攻撃され、治癒することが示唆されていた。癌細胞は細胞表面にPD-L1を発現しており、リンパ球であるT細胞のPD-1と結合して免疫細胞の攻撃を免れている。ニボルマブは、癌細胞が免疫細胞から逃れるためのチェックポイント・シグナルPD-1を抑制する(だけでなく存在が示唆されている別な経路も利用する)ことにより、免疫細胞による癌細胞への攻撃を促進する。抗癌剤の多くは、核酸代謝や蛋白合成、細胞シグナル変換を阻害することにより作用する。しかし、ニボルマブは免疫そのものに作用する。悪性黒色腫に対して標準治療薬であるイピリムマブ(抗CTLA-4抗体)とニボルマブを併用することで、腫瘍への客観的反応は53%に見られた。2015年6月に同併用療法はFDAで承認された。出典: フリー百科事典『ウィキペディア(Wikipedia)』PDー1抗体でがんは治る 新薬ニボルマブの誕生【電子書籍】[ 本庶佑 ]
2021.07.12
コメント(0)
-
イピリムマブ
2011年イピリムマブ(商品名ヤーボイ)がアメリカ、ヨーロッパで承認される(日本では2015年)。世界初のヒトCTLA-4モノクローナル抗体医薬品であり、免疫力を高めることにより悪性腫瘍を攻撃する新しいタイプの抗がん剤。イピリムマブ(Ipilimumab)はCTLA-4を標的としたモノクローナル抗体で、免疫系の抑制解除による抗癌作用を狙った医薬品である。商品名ヤーボイ。開発コードMDX-010、MDX-101。細胞傷害性T細胞(CTL)は癌細胞を認識し破壊する能力を持つが、それを抑制するメカニズムが存在する。イピリムマブはそのメカニズムを解除して、CTLの機能を発揮させる。イピリムマブは皮膚癌の一種である悪性黒色腫の治療薬として2011年に米国FDAに承認された。欧州では2011年7月に、英国で2012年11月に、日本では2015年7月に承認を取得した。非小細胞肺癌(NSCLC)および小細胞肺癌(SCLC)、膀胱癌、転移性ホルモン治療抵抗性前立腺癌に対する治験が進行中である。出典: フリー百科事典『ウィキペディア(Wikipedia)』がん化学療法の薬−抗がん剤・ホルモン剤・分子標的薬・免疫チェック ポイント阻害薬・支持療法薬−はや調べノート これだけは押さえておきたい 2021・2022年版/古瀬純司【1000円以上送料無料】
2021.07.11
コメント(0)
-

ヨハネス13世 (ローマ教皇)
ヨハネス13世(Ioannes XIII、? - 972年9月6日)は、ローマ教皇(在位:965年10月1日 - 972年9月6日)。出自はローマ貴族のクレシェンツィ(クレッシェンティウス)家。教皇レオ8世の死(965年の2月 - 4月)ののちに選出される。これは神聖ローマ皇帝オットー1世の同意を得たもので、皇帝・ローマ貴族両者の歩み寄った結果の人選であったが、皇帝側からの支援を受けていることでローマ貴族側からは嫌われていた。そのため965年12月に反乱が起きて一時的に追放され、966年11月までローマに戻れなかった。帰還後、ヨハネス13世はマクデブルク大司教区の設立を含む教会機構の改革を皇帝とともに行った。さらに、東ローマ帝国や東方正教会の影響を排除するために南イタリアでの幾つかの大司教区の設置もした。967年の降誕祭の日、オットー2世を副帝として戴冠した。これは東西両教会の和睦ないし統一を目論んでの行為であったとされる。オットー2世はのちに東ローマ皇女テオファヌとの結婚も行っている。ヨハネス13世の死については、ヨハネス12世と同じく、密通相手の夫によって殺されたという逸話が残っている。出典: フリー百科事典『ウィキペディア(Wikipedia)』カトリックの装飾マドンナメアリー像の彫刻セットホーム教会の装飾
2021.07.10
コメント(0)
-

山中伸弥
2007年京都大学の山中伸弥らのグループが、ヒトの皮膚細胞に遺伝子を組み込むことにより人工多能性幹細胞(iPS細胞)を生成する技術を発表。また同日、ウィスコンシン大学のジェームズ・トムソンもほぼ同等の方法でiPS細胞を生成する論文を発表した。山中 伸弥(やまなか しんや、1962年〈昭和37年〉9月4日 - )は、日本の医師、医学者。学位は医学博士(大阪市立大学大学院・1993年)。京都大学iPS細胞研究所所長・教授。カリフォルニア大学サンフランシスコ校グラッドストーン研究所上席研究員。日本学士院会員。その他称号としては京都市名誉市民、東大阪市名誉市民、奈良先端科学技術大学院大学栄誉教授、広島大学特別栄誉教授、ロックフェラー大学名誉博士、香港大学名誉博士、香港中文大学名誉博士などを有する。文化勲章受章者。大阪府枚岡市(現・東大阪市枚岡地区)出身。「成熟細胞が初期化され多能性をもつことの発見」により、2012年のノーベル生理学・医学賞をジョン・ガードンと共同受賞した。出典: フリー百科事典『ウィキペディア(Wikipedia)』山中伸弥 人体を語る NHKスペシャル『人体』 / Nhkスペシャル「人体」 【本】
2021.07.10
コメント(0)
-

筋電義手
2005年筋電義手の実用化。アメリカ合衆国のジェシー・サリバンが世界で初めて意思で動く義手を装着した人間となった。筋電義手(きんでんぎしゅ)は、筋肉に発生する表面筋電位の出力量によって動作制御される義手である。通常、義手は「重い」「暑い」「人から注目を集めたくない」「反対の手で代用できる」といった理由から、軽量であることや外観の再現が中心となって製作されることが多い。これに対して、外観よりも機能の再現を目指して開発されたのが筋電義手である。仕組み筋肉は、脳から命令として発せられる微弱な電気的刺激を認識した神経から分泌されるアセチルコリンを受容体が受け止めることによって収縮する。この時、発生する電位は微弱ではあるものの、体表面でも検知することができる。これを「表面筋電位」と言い、筋電義手を動かすスイッチとなる。操作法は切断者によって異なるが、切断してしまった部分を動かす筋をスイッチとする場合が多い。例えば手首を切断した場合、手首の掌屈(掌側へ手首を曲げること)する時に発生する表面筋電位を「ものを掴む」、背屈(手の甲側へ手首を曲げること)する時に発生する表面筋電位を「ものを離す」といったように、義手の動きと表面筋電位の発生方法に一定のルールを設けることで操作を行う。このように表面筋電位を感知し、その出力が一定の閾値を超えることでスイッチをオン・オフさせて動作する筋電義手である。内蔵されたモーターにより、ものを掴む・離すという動作(把持)ができ、擬似的に本人の意思で動く手を再現する。開発・研究近年では表面筋電位の閾値ではなく、表面筋電位の波形そのものから義手が動作するような筋電義手も研究されている。しかし表面筋電位は極めて微弱であることから検知が難しく、誰でも使用可能というわけではない。また内蔵されたモーターが重く、価格も高価であるので、試用体験を通し、長所・短所をよく理解しなければならない。したがって切断に詳しい医師の診断と、経験豊富な作業療法士・義肢装具士のサポートが不可欠である。現在では筋肉の電気信号だけでなく脳波の読み取りや AI を併用することによって文字を書く、ピアノ を演奏するなどといった繊細な作業をこなすことができる。さらに、リハビリや練習などをしなくても 従来の義手よりもよりシームレスに動かすことができるほか、AI の学習により使用するほど自然な動作 が可能になる。世界初の商用の筋電義手は1964年にソ連のCentral Prosthetic Research Instituteによって開発され、イギリスのHangar Limb Factoryによって広められた。日本国内でも1968年から研究が行われたが、どれも試作段階で実用化されなかった。1979年に早稲田大学理工学部で加藤一郎教授が考案した「WASEDA ハンド」を元に今仙技術研究所のワイムハンドが完成した。2015年、電気通信大学の横井浩史教授らの研究チームによって思い通りに動かせる義手が開発された。1-2分の訓練で使いこなせるようになるのが特徴。問題点日本国内での普及率は低迷する。1998年に国内の主要な製作所で製作された義手 4417本のうち筋電義手はわずか8本だったという記録がある。 2015年現在、欧米では大人用だけでなく小児用の筋電義手も普及し始めているが、日本では障害者自立支援法の対象外である。また価格に関してもオットーボック(英語版)が世界の市場シェアをほぼ独占しているため競争が発生せず、価格が下がらない状況が続いている。これらの問題を解決するため、3Dプリンターやスマートフォンを利用することにより、低価格ながら柔軟性が高く外観の変更も容易な筋電義手の開発が進められている。日本のイクシーやイギリスのオープンバイオニクスではオープンソースによる開発が進められる。出典: フリー百科事典『ウィキペディア(Wikipedia)』【送料無料】 あったらいいな、こんな義手 楽しく知ろうバリアフリー からだをたすける道具 / 斎藤多加子 【全集・双書】
2021.07.09
コメント(0)
-

インクジェット技術による生きた細胞での3次元構造の作製
2003年富山大学の中村真人が、世界で初めてインクジェット技術による生きた細胞での3次元構造の作製に成功した。臓器プリンティング(ぞうきプリンティング、英: Organ printing)は、文字通り「臓器(器官)の印刷」であり、器官の代わりになる装置を3Dプリンターの技術を用いて作り出すことである。印刷される器官は、人工的に構成された装置であり、器官の代わりとして設計され、3Dプリンターの技術を用いて製造される。臓器プリンティングを行う第一の目的は移植に用いることである。現在、心臓、腎臓および肝臓の構造ならびに他の主要な器官についての研究が行われている。心臓のような複雑な器官では、心臓弁のような小さな構造物のみを印刷することもまた研究の対象となっている。いくつかの印刷された器官は、すでに臨床試験に達しており、主に、膀胱などの中空構造ならびに尿管などの管構造が該当する。3Dプリンターは、細胞が育つ足場となるような特定の器官の構造を、一層ずつ積み重ねて作製することができる。足場ができると、目的の細胞をその上に直接ピペットで「まく」ことができる。「まく」という過程を印刷と同時に行うために、細胞を印刷可能な材料、つまり「インク」自体に組み込む手法も探求されている。インクジェットプリンターを改良することで、3次元の生物学的組織を生成した研究がある。この手法においては、プリンターの「インクカートリッジ」は、生細胞の懸濁液とスマートゲルで満たされる。ゲルは構造を構築するために使用される。標準的なプリントノズルを用いて、ゲルと生きた細胞が交互に配置されるように印刷される。細胞は最終的に融合して組織を形成する。歴史クレムゾン大学のThomas Bolandが細胞のインクジェット印刷の使用について2003年に特許を取得し、細胞構造を生成するための3Dプリンターが初めて導入された。この工程は、基板上に配置された組織化された3次元のマトリクスへ細胞を配置する。Bolandの最初の発明以来、生体構造を3Dプリンターで作り出す手法、つまりバイオプリンティングがさらに開発され、細胞のマトリクスではなく組織や臓器構造を生成するに至った。さらに、押し出しバイオプリンティングのような印刷技術が研究され、その後製造手段として導入されている。臓器プリンティングは、臓器移植のドナー(提供者)の世界的な不足に対する解決策になりえるかもしれない。これまで実際に印刷されて臨床の場で使われた器官は、皮膚のような平坦なもの、血管のような管状のもの、または膀胱のような中空のものである。人工的な器官が移植のために準備されるときには、多くの場合レシピエント(受容者)自身の細胞でつくられる。より複雑な細胞構造からなる器官が研究されている。これらの器官には、心臓、膵臓、および腎臓が含まれる。十分に医療として使える臓器を導入できる時期の予測には幅がある。2013年にOrganovo社は3Dプリンターを使用してヒト肝臓を作製したが移植には適しておらず、主に薬物検査のために使用された。3Dプリンターの技術人工臓器の製造のための3Dプリンターの技術は、生物工学における重要な研究課題である。3Dプリンターによってもたらされるラピッドマニュファクチャリング技術がますます効率化しており、人工的に臓器をつくり出せる可能性がより顕著になった。3Dプリンターの主なメリットの一部は、細胞の足場となる構造を大量に生産できること、足場となる構造が高度に解剖学的な精度をもちうることにある。これにより、より効果的に天然の器官または組織構造の微細構造に、似た構築物をつくり出すことが可能になる。3Dプリンターを使用する臓器プリンティングは、様々な技法を使用して実施することができ、それぞれが特定の種類の臓器の生産に適した特有の利点がある。臓器プリンティングの最も代表的な2つの種類、液滴を用いるバイオプリントと押出バイオプリントである。他の技術も数多く存在するが、一般的に使用されていないか、まだ開発中である。液滴を使うバイオプリント(インクジェット)液滴を使う、つまりインクジェット方式のバイオプリントは、細胞を含む「インク」を液滴にし、細胞構築物を作製する。 基板表面と接触すると、各液滴が重合し、個々の液滴が合体し、大きな構造が形成される。重合を促進させるため、基質上のカルシウムイオンを「インク」中に拡散させ、固体ゲルを形成する。液滴を用いるバイオプリントは、速度が速いため、一般的に使用されるが、より複雑な臓器構造にはあまり適していない。押し出しバイオプリント押し出しバイオプリントは、特定の細胞株を含む「インク」を、移動式のプリントヘッドの一種である押し出し機から、一定の量を押し出し付着させる。これは、よく制御された穏やかな方法なので、3次元的に組織または臓器構造を構築するときに、細胞密度をより大きくすることができる。 しかし、印刷速度は遅い。押し出しバイオプリントは、「インク」を光重合させてより安定した構造物を形成するために、UVが使われることが多い。インク3Dプリンターの「インク」は、通常、細胞を物理的に付着する細胞接着分子と一体化されたアルギン酸またはフィブリンポリマーからなる。そのようなポリマーは、構造的安定性を維持し、細胞同士が結合していくように特別に設計される。 「バイオインク」という用語は、3Dバイオプリントで使われるインク材料を指す。「インク」は、いくつかの基準に適合しなければならず、最も重要なのは生体適合性である。3Dプリンターによって形成された足場は、物理的および化学的に細胞の増殖に適切でなければならない。生分解性はもう一つの重要な要素であり、人工的に形成された構造が、移植が成功すると分解され、完全に細胞構造に置き換えられるために必要である。3Dプリンターは、いろいろな形のものをつくれるというのがメリットであるため、使用される「インク」は、カスタマイズが可能であり、いろいろなものに応用でき、幅広い種類の細胞を扱え、いろいろな構造に適している必要がある。アルギン酸ハイドロゲルは、高度にカスタマイズ可能であり、天然の組織に特徴的な、機械的および生物学的特性に合わせて微調整することができるので、「臓器の印刷」の研究で最も一般的に使用される材料である。特定の要求に合わせて調整できる能力を持つヒドロゲルは、種々の組織または臓器構造および生理学的状態に適した足場の材料として応用が可能である。課題臓器の印刷の方法に関しては画期的な進歩が見られたが、複雑な臓器に関する臨床的な実施にはさらなる研究が必要である。バイオプリントでの細胞増殖は、自然な生物学的シグナル伝達やプロセスがない人工環境で行われる。これらの欠如は、適切な細胞の形態や分化を阻害する。自然な細胞増殖の過程をつくり出せれば、「印刷された臓器が造形された足場で成長する」という状態ではなく、もっと生体の臓器に近い、構造および機能を持ち得るだろう。もう1つの課題は、細胞を持続させるために、人工構造に血管を新生させる必要がある。血管構造などの管構造は、重要な栄養素および酸素の拡散を可能にする。しかし、それらの管構造はバイオプリント技術で、完全に再現されていない。出典: フリー百科事典『ウィキペディア(Wikipedia)』QIDI TECH Shadow 5.5 S 3D Printer, UV LCD Resin Printer with Dual Z axis Liner Rail, 3.5 Inch Touch Screen,Build Size 4.52"(L) X
2021.07.08
コメント(0)
-

ヒトゲノムプロジェクト
2003年ヒトゲノムプロジェクトの完成版が公開される。ヒトゲノム計画(ヒトゲノムけいかく、英: Human Genome Project)は、ヒトのゲノムの全塩基配列を解析するプロジェクト。1953年のDNAの二重らせん構造の発見から50周年となる2003年に完了した。プロジェクトは、各国のゲノムセンターや大学などによる国際ヒトゲノム配列コンソーシアムによって組織され、これまでにワーキング・ドラフトを発表し、その改良版の発表が継続して行われている。解読されたゲノムは、NCBIやUCSC、および Sanger Centerなどの研究機関で参照することができる。歴史このプロジェクトは1990年に米国のエネルギー省と厚生省によって30億ドルの予算が組まれて発足し、15年間での完了が計画されていた。発足後、プロジェクトは国際的協力の拡大と、ゲノム科学の進歩(特に配列解析技術)、およびコンピュータ関連技術の大幅な進歩により、ゲノムの下書き版(ドラフトとも呼ばれる)を2000年に完成した。このアナウンスは2000年6月26日、ビル・クリントン米国大統領とトニー・ブレア英国首相によってなされた。これは予定より2年早い完成であった。完全・高品質なゲノムの完成に向けて作業が継続されて、2003年4月14日には完成版が公開された。そこにはヒトの全遺伝子の99%の配列が99.99%の正確さで含まれるとされているプロジェクトが加速したもう一つの理由としてセレラ・ジェノミクス社による商業的なヒトゲノムプロジェクトの存在がある。この企業はショットガン・シークエンシング法という新しい方式でシークエンシングを行い、新たに発見された遺伝子を特許化しようとした。しかしこれは公的資金によって進められているヒトゲノムプロジェクト(こちらを以下HGPとする)と拮抗してしまうことから、調整を図る為にバミューダで会議が開かれることとなり、作成されたデータについては作成から24時間を基本として全て公開して全ての研究者が自由に利用できるようにするという項目を含む、バミューダ原則(1996年2月)という形で合意が成された。最終的には、このような競争はプロジェクトにとって非常に良いものであったことが証明されたといえる。ゲノムのドラフトは2000年6月に発表されたが、その詳細な情報についてはセレラ社もHGP側も翌年2月まで公表されなかった。2001年2月に、HGP側はNature誌の特別号で、セレラ社はScience誌でその配列に対する分析と、そのドラフトの構築に用いた手法の詳細が発表された。このゲノムのドラフトは全ゲノムのうちの約90%分の足場にはなると期待されており、そのギャップを埋めていくことで完成に近付けることになる。各ドラフト配列は最低でも4回から5回はチェックされ、シークエンシングの完成度と精度が向上していく。ドラフト配列では約47%が高品質配列であったが、完成版では7-8重のチェックがなされ、エラー率は10,000残基中で1残基程度まで抑えられているという。ヒトゲノムプロジェクトは、数ある国際ゲノムプロジェクトの一つに過ぎず、各ゲノムプロジェクトはそれぞれの生物のシークエンシングを行っている。ヒトのDNA配列の解読は確実な利益を我々にもたらす一方で、マウスやショウジョウバエ、ゼブラフィッシュ、酵母、線虫、また数多くの微生物や寄生虫などのモデル生物の配列解析の成果は生物学と医学の発展に重要な役割を果たすことが期待されている。プロジェクトのゴールHGPの目標は30億塩基対の高品質な配列を決定するだけでなく、この巨大なデータに含まれる遺伝子を見つけることも重要である。プロジェクトの予備調査では約22,000遺伝子が存在するとされているが、この数は多くの研究者の予測よりも遥かに少ないこともあり、現在でもこの調査は進行中である。HGPのもう一つのゴールはより高速かつ効率的なDNAシークエンシング法を開発し、それを産業化に向けて技術移転することにある。今日、ヒトのDNA配列情報はデータベースに蓄積され、インターネットを介して誰でも利用することができる。ただし、これらのデータは何らかの解釈を加えなければほとんど利用価値が無いことから、これらのデータを解析するコンピュータ・プログラムが数多く開発されている。単純なDNA塩基配列の中から遺伝子の境界を特定したり、何らかの特徴を見出す作業はアノテーションと呼ばれ、バイオインフォマティクスの得意とする分野である。現在でも最高品質のアノテーションを行うには生物の専門家に頼らねばならないが、その作業には大変な時間を要する。しかし、ゲノムプロジェクトのようなハイスループットなデータ生産の現場では、それに見合うペースでのアノテーションが必要とされたことから、コンピュータプログラムが利用されるケースが多くなってきたのである。現在、アノテーションに用いられている技術として最も役立っているのは、人間の言語の統計モデルをDNA配列解析に応用したものであり、形式文法などのコンピュータ・サイエンスから導入した手法を利用している。もたらされる利益ゲノムデータを解釈する作業は、まだ始まったばかりである。ゲノム情報の解明は、医学やバイオテクノロジーの飛躍的な発展に貢献することが期待されている。そしてやがてはガンやアルツハイマー病などの疾患の治療に役立つものになると思われる。例えば、ある研究者が何らかのガンについて調査していく過程で、ある遺伝子に着目したとする。この研究者はWWWのヒトのゲノム・データベースを訪れることで、他の研究者がこれまでにこの遺伝子について何を調査したのか、すなわち3次構造はどうなっているのか、どのような機能があるのか、他のヒトの遺伝子との進化上での関係はどうなっているのか、酵母やマウス、ショウジョウバエと比べてどうなっているのか、有害な突然変異が起こる可能性があるか、他の遺伝子と相互作用するのか、どの組織で発現しているのか、関連する疾患は何か…などについて調査することができる。 このような得られる情報の種類は数多くあり、これはバイオインフォマティクスが注目を浴びる一因となっている。特にゲノム学と関連して注目を集めている技術としてはマイクロアレイがある(マイクロアレイはDNAチップとも呼ばれる)。これはDNAのプローブが小さな板の上に規則的に配置されたもので、3万件以上の遺伝子について、同時にそれらのサンプル内における存在量を測定できるものである。この技術はこれからの医学・科学向けの診断用ツールとしての可能性を秘めていることから、大きな関心を集めている。また、ヒトゲノム計画の結果として今後も数多くの技術がここから派生すると見られている。生物間でのDNA配列比較分析が可能となったことで、進化の研究においては新たな道が切り開かれた。現在では進化に関わる問題は、多くの場合は分子生物学の手法によって研究を進めることができる。実に、リボソームの出現や細胞内小器官の出現、胚発生から各種器官への発達、脊椎動物の免疫系の出現までを分子レベルで関連付けできるのである。このプロジェクトのデータによって、ヒトとその近縁の種(霊長類や哺乳類)の違いや類似性に関する問題が解明されていくであろうと期待されている。出典: フリー百科事典『ウィキペディア(Wikipedia)』ヒトゲノムを解読した男 クレイグ・ベンター自伝 [ J.クレイグ・ベンター ]
2021.07.07
コメント(0)
-

カプセル内視鏡
2001年カプセル内視鏡が米FDAから認可される。カプセル内視鏡(カプセルないしきょう、英: Capsule endoscopy)は、小型カメラを内蔵したカプセル状の内視鏡。小腸・大腸の観察を目的とした内視鏡で、従来の内視鏡では不可能であった小腸の観察を可能とした製品。口から飲み込み、腸内の撮影を行い、肛門から排出される。低侵襲に消化管の検査を行うことができる機器で、日本では、小腸用と大腸用のカプセル内視鏡が、医療で使用されている。コヴィディエン製品のカメラ側。コヴィディエンの小腸用製品、オリンパスの製品は、カメラがカプセルの一方の先端部にある。歴史カプセル内視鏡は、1981年、イスラエル国防省の軍事技術研究機関 ラファエル研究所の電子/光学部門技術者ガブリエル・イダン等によって開発が始まり、1994年、The Los Angeles World Congress of Gastroenterologyにて、世界で初めてとなるカプセル内視鏡研究報告が、ラファエル研究所より発表された。1998年、カプセル内視鏡の開発、生産、販売を行う、ギブン・イメージングがイスラエルで設立。2000年、ネイチャーに臨床研究報告として掲載、カプセル内視鏡の存在が広く知れ渡ることとなった[2]。2001年、ギブン・イメージングの小腸用カプセル内視鏡が、欧州諸国でCEマークを取得、米国FDAより認可を受けている。日本では、2007年4月に薬事承認され[3]、フジノン(現・富士フイルムホールディングス)と販売、部品供給及び研究開発に関して提携し、同年10月に保険適用された。2012年、カプセル内視鏡検査を行う前に、消化管の開通性を評価する崩壊性のカプセル(パテンシーカプセル)が保険適用されたことで、クローン病を始めとする、全ての小腸疾患の患者に対して使用できるようになった。また、2013年7月、大腸用のカプセル内視鏡が日本で薬事承認され、2014年1月より保険適用となった。大腸用のカプセル内視鏡は、大腸内視鏡検査が回盲部まで到達できなかった場合や、器質的異常により下部消化管内視鏡検査が実施困難と判断された場合に限り、診療報酬が適用される。日本勢ではオリンパスやアールエフが、カプセル内視鏡の開発を進めており、オリンパスは、EU圏内で2005年より販売を開始している。日本では、2008年9月に製造販売承認を取得、同年10月に販売が開始された。なおギブン・イメージングは、医療機器メーカーであるコヴィディエンに2014年3月に買収されたため、日本でのカプセル内視鏡の販売は、メドトロニックグループのコヴィディエン ジャパン株式会社が行っている。構造カプセル内視鏡の形状は、薬のカプセルに類似しており、一般的な薬のカプセル剤よりも一回り程度大きい。 コヴィディエンの小腸用カプセルのサイズは、2.6cm×1.1cmで、1秒間に2枚または6枚撮影を行い、大腸用カプセルのサイズは、3.1cm×1.1cmで、1秒間に4枚または35枚の撮影を行う。また、オリンパス製品は、サイズが2.6cm×1.1cmで、1秒間に2枚撮影を行う。カプセルにはCMOSやCCDで構成されたカメラ及び無線装置を内蔵している。患者が口から飲み込んだ小腸用のカプセル内視鏡は、蠕動運動という臓器の収縮運動によって消化管内で運ばれ、前進しながら非侵襲的に腸内を撮影し、画像データを体外に送信する。画像データは、患者がたすき掛けで装着するデータ受信機が記録し、撮影を終えたカプセルは肛門より自然排出される。カプセルは使い捨てで、検査終了後は、医療廃棄物として処分される。製品日本で薬事認可されているものは、以下3つの製品がある。小腸の観察を目的とした製品PillCam®SB3カプセル:コヴィディエン小腸用カプセル内視鏡 OLYMPUS EC TYPE1:オリンパス大腸の観察を目的とした製品PillCam®COLON2:コヴィディエンその他、認可されていないが、以下の製品が存在する。PillCam®ESO2:コヴィディエン(主に食道の観察を目的とした製品)Sayaka®:アールエフ開発中アールエフが開発中のカプセル内視鏡は、他社製のものより小さく、バッテリーは内蔵せず電波により送電する方式を採用、外部コントローラによって移動やカプセルの向きを自由に指示・制御することができる、とされている。カメラは本体中央に配置され360度回転できるため、消化管内の全面をくまなく撮影することが可能である、とされている。なお、アールエフ製のカプセル内視鏡は、承認されておらず、市場流通はしていない。評価小腸用カプセル内視鏡カプセル内視鏡は、小腸病変の同定に有用かつ安全に施行できる検査として、施行数は増加しているが、腸管の狭窄を生じている場合、自然排出されない症例がごく稀にあるため、検査をするにあたってはIBD専門医への相談が必須であるという報告がされている。カプセル内視鏡には体内に2週間以上とどまる滞留があるが、その発生は341例中1例(0.29%、クローン病)という報告がされている。大腸用カプセル内視鏡大腸用のカプセル内視鏡を用いた検査直後に大腸内視鏡検査を実施する方法で、18歳以上の大腸疾患患者約300人を対象として行われた比較試験によれば[15]、嚥下から排出(口から肛門)までの所要時間は、平均で4時間51分、中央値は4時間1分。1例を除き、16時間以内に排出。90%以上の患者で嚥下から10時間以内にカプセルが排出された。また、カプセルは1〜2時間程度で大腸を通過する。腸管の洗浄状態と大腸通過に要する時間は無関係。通常の内視鏡検査とカプセル内視鏡検査の病変部位の検出感度は、有意な差がみられた。また、腸管の洗浄状態の影響を受け、洗浄状態が良好であるほど検出感度は上がる。と報告されている。その他、カプセル内視鏡が生体情報モニター機器と電波干渉を起こし、画像が記録されない現象が生じることが報告されており、専用電磁波防護服で、電波干渉を軽減している。出典: フリー百科事典『ウィキペディア(Wikipedia)』動画でわかるカプセル内視鏡テキスト [ 日本カプセル内視鏡学会 ]
2021.07.06
コメント(0)
-

ゲフィチニブ
1998年この頃、ゲフィチニブの臨床試験が始まる。分子標的治療薬は悪性腫瘍の化学療法に革命的変化をもたらした。ゲフィチニブ(Gefitinib)は、上皮成長因子受容体 (EGFR) のチロシンキナーゼを選択的に阻害する内服抗がん剤。癌の増殖などに関係する特定の分子を狙い撃ちする分子標的治療薬の一種である。 商品名はイレッサ (Iressa) で、アストラゼネカが製造・販売。褐色の錠剤で一錠250mgのゲフィチニブを含有する。ゲフィチニブ製剤は手術不能または再発した非小細胞肺癌に対する治療薬として用いられる。イレッサは2002年7月5日、世界に先駆けて日本で承認され、2003年5月5日、アメリカ食品医薬品局 (FDA) での承認[2]を含め、いくつかの国で承認を受けた。しかし、無作為比較臨床試験(ISEL試験、後述)の結果、プラセボと比較して生存期間を延長することができなかったため、2005年1月4日アストラゼネカは欧州医薬品局 (EMEA) への承認申請を取り下げ、また2005年6月17日、FDAは本薬剤の新規使用を原則禁止とした。その後2009年7月1日、欧州医薬品局は、後述のINTEREST試験とIPASS試験の2つの無作為化第III相臨床試験の結果をもとに、成人のEGFR遺伝子変異陽性の局所進行または転移を有する非小細胞肺癌を対象にイレッサの販売承認を行った。2009年現在イレッサを承認している国は、日本を含めたアジア諸国、欧州、オーストラリア、メキシコ、アルゼンチンである。ゲフィチニブは白色から黄白色の粉末。開発コード名ZD1839。作用機序変異型EGFRのチロシンキナーゼドメインとゲフェチニブの複合体構造。G719Sの変異は赤色で、T790Mの変異は黄色で示した。棒状の分子はゲフェチニブである。ゲフィチニブは、細胞の上皮成長因子受容体 (EGFR) のシグナル伝達を遮断することで、腫瘍の増殖抑制、アポトーシス(細胞死)を誘導する。EGFRのチロシンキナーゼのATP結合部位にATPと競合的に結合することで、EGFRの自己リン酸化を阻害し、シグナル伝達を遮断する。実験室レベルでは、正常構造のEGFRに対しても効果を示すが、実際の臨床では、腫瘍細胞のEGFR遺伝子が特殊な型の変異を伴っている場合に、ゲフィチニブは特に腫瘍縮小効果を示す。薬物動態学経口投与されたゲフィチニブは比較的緩徐に吸収され、内服後最高血中濃度までの時間 (Tmax) は3-5時間、バイオアベイラビリティ(生物学的利用能、吸収効率)は約60%で食事の影響を受けない。ゲフィチニブ225 mg/日内服後の最高血中濃度 (Cmax) は約320 ng/ml(約0.7 μmol/l)。血中濃度が定常状態に達するまで連日内服で7〜10日かかる[13]。血中半減期は48時間。主に肝代謝(シトクロムP450 3A4)により代謝され、糞便中に86%、尿中に4%未満が排泄される。血漿タンパク結合結合率は90%。効果要約非小細胞肺癌に対して、ゲフィチニブは約10%から20%の患者に腫瘍縮小効果を示す。東洋人、女性、非喫煙者、腺癌ではゲフィチニブが腫瘍縮小効果を示す割合が高く、これはEGFR遺伝子変異が関係している可能性がある。1種類から2種類の化学療法終了後の進行非小細胞肺癌に対して、ゲフィチニブはドセタキセルと同等の延命効果を示す可能性がある。対象を絞り、非喫煙者、腺癌、アジア人の未治療進行非小細胞肺癌を対象とした臨床試験では、ゲフィチニブは化学療法よりも無増悪生存期間を延長した。EGFR遺伝子変異をもつ非小細胞肺癌に対しては特にゲフィチニブは奏功し、70%から80%程度の患者に腫瘍縮小効果を示す。腫瘍縮小効果2000年から2001年に、既治療進行非小細胞肺癌を対象とした2つの第II相臨床試験(IDEAL1[15]とIDEAL2)が施行され、ゲフィチニブ単剤で奏功率9%から19%、1年生存率24%から36%の結果が得られた。また、ゲフィチニブの腫瘍縮小効果は、東洋人、女性、腺癌、非喫煙者で高い傾向がみられた。腫瘍縮小を示した非小細胞肺癌を調べた結果、癌細胞がEGFR遺伝子変異を持つ場合に、高率に腫瘍が縮小することが明らかとなり[9][10]、また、非喫煙者、腺癌、女性、東洋人ではEGFRの遺伝子変異をもつ割合が高いために腫瘍縮小率が高い可能性が示された。化学療法との併用また2000年から2001年に、未治療進行非小細胞肺癌に対して、初回治療に標準治療であるプラチナ製剤を含む化学療法にゲフィチニブを併用することにより、治療効果に上乗せがあるかどうかが検討された。ゲムシタビン・シスプラチン治療への上乗せ効果を検討したINTACT-1と、パクリタキセル・カルボプラチン治療への上乗せ効果を検討したINTACT-2[20]の二つの第III相無作為化比較試験が施行されたが、いずれも有意な併用効果はみられず、化学療法との併用は効果がないと考えられた。延命効果非小細胞癌全体を対象とした比較日本を含まない28か国、1,692例の既治療進行非小細胞肺癌患者を対象とした第III相臨床試験(ISEL試験、2003年7月15日から2004年8月2日に症例登録)においてゲフィチニブは、登録肺癌全症例に対して、および肺腺癌に対して、プラセボと比較して有意な生存期間の延長を示すことができなかった。しかし、サブセット解析では、アジア人、非喫煙者に対してはゲフィチニブはプラセボと比較して有意に生存期間を延長させた。全肺癌症例の生存期間中央値は、ゲフィチニブ群およびプラセボ群でそれぞれ5.6か月、5.1か月、P =0.11であり、肺腺癌症例ではそれぞれ6.3か月、5.4か月、P =0.07であった。規定のログランク検定 (Logrank test) では有意差がないものの、Cox回帰分析ではそれぞれP =0.030、P =0.033と有意差に達している。また東洋人の生存期間中央値は、ゲフィチニブ群およびプラセボ群でそれぞれ9.5か月、5.5か月、非喫煙者ではそれぞれ8.9か月、6.1か月であり、Cox回帰分析でそれぞれP =0.010、P =0.012であった。 その後さらに、既治療進行非小細胞肺癌に対する現在の標準療法であるドセタキセル療法と、ゲフィチニブ単剤療法の効果を比較した第III相無作為化比較臨床試験が2つ行われた。これら2つの試験は、すでに1 ~ 2種類の化学療法が行われた進行非小細胞肺癌患者にゲフィチニブ療法を行った場合の全生存期間が、ドセタキセル療法を行った場合の全生存期間よりも劣っていないこと(非劣勢)を証明することを目的として行われた。2003年から2006年の間に489例の患者を対象として日本で行われたV15-32試験[21]は、ゲフィチニブのドセタキセルに対する非劣性を証明できなかった(ただし劣っていることも証明されなかった)。しかし、2004年から2006年の間に、日本を含まない24カ国において1,466例の患者を対象として行われたINTEREST試験では、全生存期間中央値はゲフィチニブ群が7.6か月であったのに対しドセタキセル群は8.9か月、1年生存率はゲフィチニブ群が32%でドセタキセルは34%、ハザード比は1.020(96%信頼区間 0.905-1.150)であり、ドセタキセルとゲフィチニブは既治療進行非小細胞肺癌に対して同等の効果があることが初めて証明された。この2つの試験の違いとして、後治療の差が指摘されている。つまり、V15-32試験では、ドセタキセル群の53%もの患者がドセタキセル療法終了後にゲフィチニブ療法を受けていたために、ゲフィチニブの効果がドセタキセル群の患者にもあらわれた可能性である。ゲフィチニブ療法終了後にドセタキセル療法を受けた患者はゲフィチニブ群の36%であった。一方INTEREST試験では、ゲフィチニブ群の31%がゲフィチニブ療法終了後にドセタキセル療法を受け、ドセタキセル群の37%がゲフィチニブを含むEGFRチロシンキナーゼ阻害剤の投与を受けていた。対象を選別しての比較さらに、ゲフィチニブの効果が期待できる患者を選別して対象とした無作為化比較第III相臨床試験(IPASS試験)が行われた。この試験は、非喫煙か軽度の喫煙の経験者(15年以上禁煙)で腺癌のアジア人未治療進行非小細胞肺癌患者を、ゲフィチニブ治療群とカルボプラチンとパクリタキセルの併用化学療法群に無作為に振り分け、無増悪生存期間を評価する試験である。2006年5月から2007年10月の間に、日本人232人を含む1,217人が登録された。その結果、ゲフィチニブ治療がカルボプラチン/パクリタキセル併用化学療法よりも無増悪生存期間を延長することが証明されたと発表された(ハザード比 0.74、95%信頼区間 0.65 - 0.85)。ただし、投与開始後6か月間はゲフィチニブの方が疾患制御率が悪く、6か月以降は曲線が交差してカルボプラチン/パクリタキセルの方が悪くなっておりハザード比が大きく変動しているので、比例ハザード(ハザード比が一定を維持)を前提とした統計解析は誤りであり意味がない。事前に計画されていたバイオマーカーに基づくサブグループ解析では、無増悪生存期間はEGFR遺伝子変異陽性患者ではイレッサ群が化学療法群に比べ有意に長く(ハザード比 0.48、95%信頼区間 0.36 - 0.64)、逆にEGFR遺伝子変異陰性患者では化学療法群がイレッサ群に比べ有意に長い(ハザード比 2.85、95%信頼区間 2.05 - 3.98)ことが示された。このことより適切に症例を選択することにより、ゲフィチニブ治療は従来の化学療法よりも優れた効果を示すことが示された。ただし、全生存期間は有意差が付かなかった(ハザード比 0.90、95%信頼区間 0.79 - 1.02)。EGFR遺伝子変異を有する非小細胞肺癌に対する効果EGFR遺伝子変異を有する非小細胞肺癌に対して、ゲフィチニブはその70%から80%程度で腫瘍縮小効果を示すことが、いくつかの後ろ向き研究で指摘された。さらに、未治療非小細胞肺癌に対する前向き試験で、これらの患者の75%程度でゲフィチニブが腫瘍縮小効果を示すことが確認された。さらに、北東日本ゲフィチニブ研究グループで行われた、EGFR遺伝子変異を有する未治療進行非小細胞肺癌患者のみを対象とした無作為化比較第III相臨床試験の結果、ゲフィチニブ治療はカルボプラチン/パクリタキセル併用化学療法よりも有意に無増悪生存期間を延長することが示された。脳神経膠芽腫悪性再発脳神経膠芽腫(グリオブラストーマ)49例に対して、ゲフィチニブ(250 - 1,500 mg/日)またはエルロチニブ(150 - 500 mg/日)が投与され、49例中9例で、2方向計測で25%以上の腫瘍縮小がみられた。EGFRの細胞内領域の変異例はなく、EGFRvIIIとPTENの両者の発現がみられた例では有意に腫瘍縮小と相関がみられた。頭頸部扁平上皮癌52例の頭頸部扁平上皮癌に対するゲフィチニブ(500 mg/日)の効果を検討した第II相試験にて、奏功率10.6%、病勢制御率53%の効果を示した[27]。ゲフィチニブ250 mg/日による臨床試験では70例中1例で腫瘍縮小 (PR) がみられたのみであった。その他の癌31例の進行腎癌に対するゲフィチニブ(500 mg/日)の効果を検討した第II相試験にて、8例 (38%) で腫瘍の増大がみられなかったのみで、腫瘍の縮小はみられなかった。副作用急性肺障害・間質性肺炎を併発(1〜10%)することがあり、これにより死に至り得る。また、下痢、発疹、ざ瘡(にきび)、乾燥皮膚、かゆみ、爪周囲炎が起こることが多い。添付文書に記載されている重大な副作用は、上記のほか、重度の下痢(<1%)、脱水(<1%)、消化管穿孔(<1%)、消化管潰瘍(<1%)、消化管出血(<1%)、中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)(<1%)、皮膚粘膜眼症候群(Stevens-Johnson症候群)(<1%)、多形紅斑(<1%)、肝炎(<1%)、肝機能障害(AST(GOT)、ALT(GPT)、LDH、γ-GTP、Al-P、ビリルビン等の上昇 >10%)、黄疸(<1%)、肝不全(<1%)、急性膵炎(<1%)、血尿(<1%)、出血性膀胱炎(<1%)である。急性肺障害・間質性肺炎投与後4週間以内に発症しやすい。日本において、ゲフィチニブ投与後8週間以内の急性肺障害・間質性肺炎(以下肺障害)の発症率は約5.8%(193例/3322例)、肺障害による死亡率は2.3%(75例/3322例)であった。また PS (performance status) 2以上、喫煙歴のある人、すでに間質性肺炎を合併している人、化学療法を受けたことのある人、では肺障害が起こりやすいことが示唆された。また、ゲフィチニブ投与12週以内の肺障害の発症率は、化学療法による肺障害の発症率の1.9倍(4.0%対2.1%)、背景因子を調整すると3.2倍の高さであり、通常の化学療法に比べても肺障害がおこりやすいことが明らかとなった。ただし、欧米では肺障害はほとんど問題になっておらず、前述のISEL試験では、ゲフィチニブ投与群で3%、プラセボ投与群で4%の発症率であり、ゲフィチニブにより肺障害のリスクは増えていない。ゲフィチニブによる肺障害には民族差がある可能性がある。「薬害」について事実関係通常は他の薬の審査待ちで、1年ほどの審査期間が掛かるが、イレッサの場合は優先して審査したので、5か月ほどのスピード承認となった。当初は副作用が少ないと言われていたが、治験では3例で間質性肺炎を発症していずれも治療で回復したが、治験外使用では7例で間質性肺炎を発症したうちの3例が死亡している。承認前に判明していた間質性肺炎は、国内臨床試験で133人中3人、治験外使用では国内で296人中2人、海外を含めると1万人以上で10例前後だったとされる[35]。当初の添付文書の「重大な副作用」の4番目に「間質性肺炎(頻度不明):間質性肺炎があらわれることがあるので,観察を十分に行い,異常がみとめられた場合には,投与を中止し,適切な処置を行うこと」と記載されていた[36]。 販売後の情報収集体制強化を行う市販直後調査より、厚生労働省は同年10月15日、イレッサとの関連性が否定できない副作用26例、うち死亡13例を盛り込んだ緊急安全性情報(イエローレター)を発表。2002年10月(報告月)の1か月で51人、同年11月(報告月)で81人、同12月(報告月)で37人が、それぞれゲフィチニブ服用後の急性肺障害・間質性肺炎等での死亡が報告されたが、その後の死亡報告数は減少している。2006年3月までの累計で643人がゲフィチニブ服用後の急性肺障害・間質性肺炎等での死亡が報告された。2013年4月現在、日本において承認取消や使用制限は行なわれていない。2004年、患者の遺族達が国と製薬会社を相手取って大阪地方裁判所と東京地方裁判所に提訴した。地裁結審時の原告は計15人(大阪地裁側が患者4人[39]の遺族11人[40]、東京地裁側が患者3人の遺族4人)となった。判決2011年2月25日、大阪地裁は添付文書に警告欄を設けた2002年10月15日までに服用した患者3人について販売元企業であるアストラゼネカに賠償を命じ、同日以降に服用を始めた患者1人については賠償責任を否定した。その一方で、「死亡を含む重い副作用の危険が具体化すると高い可能性では認識できず、当時の医学、薬学的知見の下では著しく合理性を欠くとは言えない」として国の責任は否定した。2011年3月23日、東京地裁は第1版添付文書の記載に不備があるとして、この点についてのみであるが国と製薬会社双方の責任を認めた。2012年5月25日の大阪高等裁判所判決(大阪訴訟の控訴審)、2011年11月15日の東京高等裁判所判決(東京訴訟の控訴審)はいずれも製薬会社・国両方の賠償責任を認めず、一審判決を取り消して原告敗訴の判決を言い渡した。2013年4月12日、最高裁判所は各々の二審判決を支持、上告を棄却した。作用機序をめぐる変遷ゲフィチニブは、上皮成長因子受容体 (EGFR) チロシンキナーゼ阻害薬 (Epidermal Growth Factor Receptor-Tyrosine Kinase Inhibitor; EGFR-TKI) であり、EGFRのATP結合部位にATPと競合的に結合して自己リン酸化を阻害することによりシグナル伝達を遮断して、細胞の増殖や分化を抑制する薬として開発された[46]。実験室レベルでは、EGFRを発現する様々な癌細胞(卵巣癌、乳癌、大腸癌、非小細胞肺癌)に有効であることが示された。しかし、EGFRは非小細胞肺癌の40-80%で過剰発現がみられるのに対し、ゲフィチニブは非小細胞肺癌患者の10-19%にしか腫瘍縮小効果を示さず、EGFRは非小細胞肺癌のうち扁平上皮癌で過剰発現の頻度が高いのに対し、ゲフィチニブは腺癌で有効性が高く、また実際EGFRの発現とゲフィチニブの効果の間には相関がないことが示され、ゲフィチニブは非小細胞癌の一部で劇的な腫瘍縮小効果を示すもののその正確な作用機序は不明であった。2004年4月29日、ボストン・マサチューセッツ総合病院 (MGH) のトーマス・リンチらと、ボストン・ダナ・ファーバー癌研究所のギジェルモ・パエズらはそれぞれ同日に、ゲフィチニブにより縮小した肺癌のEGFRに遺伝子変異が認められ、この遺伝子変異とゲフィチニブの臨床効果の間に強い相関がみられたという衝撃的な発表を行った。遺伝子変異を持ったEGFRは、そのATP結合部位に構造変化が生じる結果、EGFRが恒常的に活性化して悪性度が高まる一方、ゲフィチニブとの親和性が高まり、EGFRの下流のシグナルが遮断されることによりアポトーシスが誘導され、腫瘍縮小効果を示すという。それまでゲフィチニブは非喫煙者、腺癌、女性、東洋人で有効性が高いことが報告されていたが、これらは非喫煙者、腺癌、女性、東洋人においてEGFRの遺伝子変異をもつ割合が高いことによる可能性が数々の後ろ向き研究で示された。また、このEGFR遺伝子変異にさらに二次的な遺伝子変異がおこると、ゲフィチニブ耐性となることが示された。これに対して、コロラド大学保健科学センターのフェレリコ・カプーゾおよびフレッド・ヒルシュらのグループは、FISH法により検出されるEGFR遺伝子コピー数の増加が、遺伝子変異よりも強く腫瘍縮小および予後と関連していると反論した。また、ゲフィチニブと同様の作用機序を示すエルロチニブを用いた二重盲検無作為化比較試験において、EGFR遺伝子変異は延命効果 (survival benefit) をもたらさず、またエルロチニブに対する腫瘍縮小効果はFISH法によるEGFRの遺伝子コピー数増加と相関していたもののEGFR遺伝子変異とは相関がなかったと報告された。しかし、EGFR遺伝子変異を有する未治療非小細胞肺癌に対する前向き試験によって、これらの患者の75%程度でゲフィチニブが腫瘍縮小効果を示すことが確認され、このEGFR遺伝子変異はゲフィチニブの腫瘍縮小を予測する因子であることは定説になりつつある。ただし、EGFR遺伝子変異がなくてもゲフィチニブが有効である症例も存在し、このEGFR遺伝子変異以外にも治療効果を規定する因子がある可能性は十分ある。一方、ゲフィチニブは、標準的化学療法との併用療法の意義を検証した第III相比較試験 (INTACT1&2) の事後解析では、標準化学療法のみの群でも、EGFR遺伝子変異例がEGFR遺伝子を持たない例よりも予後良好であることから、EGFR遺伝子変異自体が予後良好因子である可能性も指摘されており、ゲフィチニブがEGFR遺伝子変異を持つ非小細胞肺癌を縮小させることができても、それが予後を延長させることに結びついているのかどうかはまた未決着の問題であり、今後の研究が待たれる。EGFR遺伝子変異を有する症例を対象として、従来から標準治療とされてきたプラチナ製剤併用化学療法とゲフィチニブの比較試験が行われた。その結果、ゲフィチニブが無増悪生存期間で有意に優れていたことが報告され、現在では標準治療の1つとなっている。出典: フリー百科事典『ウィキペディア(Wikipedia)』がん化学療法の薬ー抗がん剤・ホルモン剤・分子標的薬・免疫チェックポイント阻害薬・支持療法薬ーはや調べノート2021・2022年版 (YORi-SOU がんナーシング別冊) [ 古瀬 純司 ]
2021.07.05
コメント(0)
-

リツキシマブ
1998年この頃、リツキシマブの臨床試験が始まる。分子標的治療薬は悪性腫瘍の化学療法に革命的変化をもたらした。リツキシマブ(Rituximab)は、抗ヒトCD20ヒト・マウスキメラ抗体からなるモノクローナル抗体であり、その製剤は分子標的治療薬のひとつとして抗がん剤・免疫抑制剤などとして使用されている。製剤としてのリツキシマブが注射剤であり、日本はリツキサン (Rituxan) の商品名で全薬工業[1]および中外製薬から発売されている。バイオシミラー後発品も日本では販売されている。(ファイザーとサンドより製造販売)リツキシマブは2011年には金額ベースにおいて世界でベストセラーの抗がん剤となっている。この背景には各国での治療適応疾患の拡大のほか、薬剤価格が高価であることがあり、日本でも1瓶(500mg/50mL)あたりの薬価(保険適用前)が約21万円(2008年薬価改正時点)に設定されている。2015年の全世界売上高は全医薬品で5位、抗がん剤では1位であった。2017年は売上高8位、抗がん剤としては依然1位であった。概要ヒトCD20はヒトリンパ球B細胞のみに発現し、正常・腫瘍細胞は問わず、preB~成熟B細胞にかけて細胞膜表面に認められる。preB、形質細胞にはCD20はみられない。ヒトCD20に対する抗体はヒトは持たないため、マウスのヒトCD20に対する抗体の可変領域Fabとヒト定常領域Fcをキメラとして、1991年米国のIDEC Pharmaceuticals社(現Biogen社)がリツキシマブを創製した。日本での健康保険適応は、CD20陽性のB細胞性非ホジキンリンパ腫、免疫抑制状態下のCD20陽性のB細胞性リンパ増殖性疾患、多発血管炎性肉芽腫症、顕微鏡的多発血管炎。非ホジキンリンパ腫、リンパ増殖性疾患の治療では単独での使用も行われるが、CHOP療法との併用も行われている。リツキシマブはANCA関連血管炎に対する治療薬のひとつで、好酸球性多発血管炎性肉芽腫症でも効果がみられている。ANCA関連血管炎に対する寛解維持療法でリツキシマブ群はアザチオプリン群に比べ有意に寛解維持できていた。また、臓器移植の際の拒絶反応治療や、腎炎などこれまで治療が困難であった一部の自己免疫疾患への効果も期待されており、関節リウマチ、全身性エリテマトーデス(SLE)については各国で治験が進んでいる。また日本では2008年より小児難治性ネフローゼ症候群、特発性血小板減少性紫斑病での治験が行われている。2014年、小児難治性ネフローゼ症候群にリツキシマブが効果を示すことが報告された。悪性リンパ腫に対しては、同効薬に90Y Ibritumomab, 131I Tositumomabなどがある。適応CD20陽性の非ホジキンリンパ腫 (NHL)CD20陽性の慢性リンパ性白血病 (CLL)免疫抑制状態下のCD20陽性のB細胞性リンパ増殖性疾患多発血管炎性肉芽腫症(GPA、旧称:ヴェゲナー肉芽腫症 (Wegener's granulomatosis))顕微鏡的多発血管炎 (MPA)難治性のネフローゼ症候群(頻回再発型あるいはステロイド依存性を示す場合)腎移植・肝移植におけるABO血液型不適合移植例に対する免疫抑制治療慢性特発性血小板減少性紫斑病 (ITP)インジウム (111In) イブリツモマブ・チウキセタン注射液およびイットリウム (90Y) イブリツモマブ・チウキセタン注射液投与の前投与副作用B型肝炎ウイルスキャリアの患者で、本剤の投与での免疫抑制によるウイルス活性化で劇症肝炎または肝炎増悪を生じることがある。出典: フリー百科事典『ウィキペディア(Wikipedia)』ゲノム医療時代のがん分子標的薬と診断薬研究 (実験医学増刊) [ 西尾 和人 ]
2021.07.04
コメント(0)
-
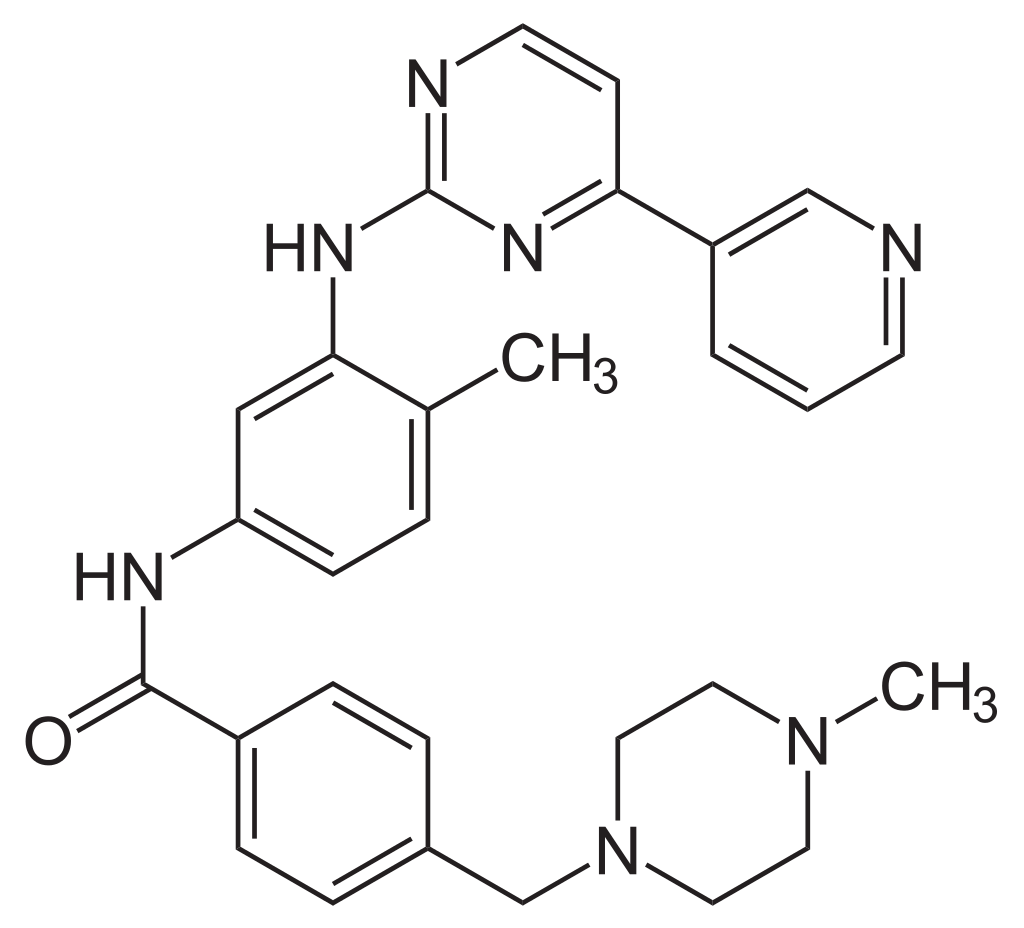
イマチニブ
2001年分子標的治療薬イマチニブがアメリカ合衆国で承認される。それまでは抗がん剤で38%、インターフェロンで53%、骨髄移植で63%だった慢性骨髄性白血病の5年生存率がイマチニブにより93%にあがった。イマチニブ(imatinib)は、フィラデルフィア染色体の遺伝子産物Bcr-Ablを標的とした分子標的治療薬としてブライアン・ドラッカーとスイスのノバルティスファーマ社により開発された抗悪性腫瘍剤(抗がん剤)。イマチニブ製剤は、慢性骨髄性白血病 (CML)、フィラデルフィア染色体陽性急性リンパ性白血病 (Ph+ALL) 、KIT (CD117) 陽性消化管間質腫瘍 (GIST) に対する治療薬として用いられる。投与はメシル酸塩で行われる。先発品の商品名は「グリベック(Glivec、米国でのみGleevec)」。販売までの経緯イマチニブは、欧米において1992年より非臨床試験が、1998年より臨床試験が開始され、Bcr-Ablチロシンキナーゼ活性を選択的に阻害し、慢性期、移行期ならびに急性期CMLにおける効果および安全性が確認されたことから、2001年5月に米国で承認された。日本においては、2000年7月より第I/II相試験が開始され、外国での使用成績が集積されていること、また、CMLという重篤かつ患者数が少ない疾患を対象とすることなどが加味され、2001年4月中間集計にて承認申請を行い、11月に輸入承認を受けた。更に適応追加として、2003年7月GISTに、2007年1月Ph+ALLに対して追加承認された。2014年には後発品の製造・販売承認が得られており、流通が始まっている。効能・効果慢性骨髄性白血病 (CML)KIT (CD117) 陽性消化管間質腫瘍 (GIST)フィラデルフィア染色体陽性急性リンパ性白血病 (ALL)FIP1L1-PDGFRα融合遺伝子陽性の慢性好酸球性白血病/特発性好酸球増加症候群 (CEL/HES)作用機序通常、骨髄造血幹細胞の増殖は遺伝子情報のシグナル伝達により正常にコントロールされている。しかし、CMLでは、第9番染色体と第22番染色体が相互転座し、abl遺伝子とbcr遺伝子が融合したbcr-abl遺伝子を持つ異常染色体(フィラデルフィア染色体)が形成されている。このフィラデルフィア染色体は、チロシンキナーゼ活性が亢進された210kDのBcr-Abl融合蛋白 (p210) を生成する。その結果細胞増殖のシグナル伝達に異常が起こり、過剰な細胞増殖が引き起こされCML病態が形成される。Ph+ALLにおいても同様に、異常染色体であるフィラデルフィア染色体によってBcr-Abl融合蛋白(p185あるいはp190)が形成され、細胞増殖のシグナル伝達の異常によりPh+ALL病態が形成される。イマチニブはBcr-Abl、v-abl、c-abl、PDGF受容体及びc-Kitチロシンキナーゼ活性を阻害するが、その抑制作用は、PDGF 受容体及びc-Kit のチロシンキナーゼ活性では、これらの自己リン酸化及び直接のリン酸化を阻害することによるものと考えられ、c-Ablチロシンキナーゼ活性では、ATPと競合拮抗することにより阻害することが示唆されている。GISTGISTは消化管間葉系腫瘍の一種であり、形態学的に平滑筋や神経への明瞭な分化を示さない腫瘍であることがわかってきている。さらに、免疫組織学的検討から平滑筋系腫瘍又は神経系腫瘍では認められないKIT (CD117) がGISTにのみ発現していると報告されている。またGISTの発症原因のひとつとしてc-kit遺伝子が機能獲得性突然変異を起こし、KITチロシンキナーゼ活性が亢進していることが考えられている。イマチニブはCMLで活性が亢進しているBcr-Ablチロシンキナーゼ活性を阻害するほぼ同等の濃度でKITチロシンキナーゼ活性も阻害し、GISTに対する抗腫瘍効果を発揮する。他にもc-abl、p185Bcr-Abl、Tel-Ablチロシンキナーゼに対しても同様な阻害作用機序を示す。出典: フリー百科事典『ウィキペディア(Wikipedia)』慢性骨髄性白血病治療症例集 分子標的治療薬 / メシル酸イマチニブ / 池田康夫 【本】
2021.07.03
コメント(0)
-

分子標的治療薬
1998年がんの分子標的治療薬の臨床試験が相次いで始まる。分子標的治療薬は悪性腫瘍の化学療法に革命的変化をもたらした。分子標的治療(ぶんしひょうてきちりょう、英: molecularly-targeted therapy)とは、ある特定の分子を標的として、その機能を制御することにより治療する療法。正常な体と病気の体の違いあるいは癌細胞と正常細胞の違いをゲノムレベル・分子レベルで解明し、がんの増殖や転移に必要な分子を特異的に抑えたり関節リウマチなどの炎症性疾患で炎症に関わる分子を特異的に抑えたりすることで治療する。従来の多くの薬剤もその作用機序を探ると何らかの標的分子を持つが、分子標的治療は創薬や治療法設計の段階から分子レベルの標的を定めている点で異なる。また、この分子標的治療に使用する医薬品を分子標的治療薬と呼ぶ。以下本項目では、分子標的薬の多くががん治療薬であることから、狭義の分子標的治療であるがん治療への分子標的治療薬を中心に記述する(自己免疫疾患についても触れる)。歴史がん(そのほか、自己免疫疾患、臓器移植など)治療で、特有あるいは過剰に発現している、特定の標的(分子)を狙い撃ちにしてその機能を抑える薬剤により治療する方法が、いわゆる「分子標的治療」である。この呼称はモノクローナル抗体の開発が始まった1980年代初頭より使用され始めた。1980年代にCEAなどの腫瘍関連抗原に対する抗体療法がマウスモノクローナル抗体で試みられたが成功しなかった。そこで、マウス抗体の定常領域をヒト由来のものに置き換えたキメラ抗体が開発され、1997年にリツキシマブとして、抗体医薬品が初めて承認された。しかし、その後ヒト抗キメラ抗体の出現や重篤なアレルギー反応が報告されたため、あらたにヒト化抗体が開発された。その後1990年代後半には完全ヒト化抗体が作成された。「分子標的治療」が一般的に使われ出したのは、メシル酸イマチニブやゲフィチニブなどの低分子化合物が臨床使用され始めた1990年代末からとされる。特に2001年に承認されイマチニブは、慢性骨髄性白血病 (CML) にたいして大きな効果を発揮し、分子標的薬の評価を飛躍的に高めた。また創薬期間は、イマチニブでは標的分子発見後40年を経て薬剤が承認されたが、BRAF阻害薬では標的分子発見から約10年で承認され、クリゾチニブでは承認までの時間が4年など、コンピューターとゲノム医学の進歩により標的分子発見後の創薬期間が短縮化される傾向にある。なお、分子標的薬はその効果を高めるため、抗体に細胞毒性物質のみならず放射性同位元素などを結合させた融合抗体(抱合薬)なども登場しており、その形を広げつつある。病態形成の本質たる原因分子標的が明らかになることによって、今後目覚ましい治療効果が得られるとされる。出典: フリー百科事典『ウィキペディア(Wikipedia)』分子標的治療薬マスターガイド [ 弦間昭彦 ]
2021.07.02
コメント(0)
-

細胞のカプセル化技術
1998年細胞のカプセル化技術の臨床応用が始まる。細胞のマイクロカプセル化技術は、ポリマーの半透膜で細胞を包み、細胞の移動を制限する技術である。その半透膜は、細胞代謝に必須の酸素、栄養素、成長因子などの分子の双方向の拡散は可能で、廃棄物および細胞が分泌する治療のためのタンパク質の外側への拡散は可能なものを使用する。同時に、膜は、カプセル内の細胞が外来の物質と認識され、免疫細胞や抗体によって、破壊されるのを防ぐ。細胞のカプセル化技術の主な目的は、組織工学の用途として、移植片への拒絶反応の問題を克服し、臓器移植後の免疫抑制剤の長期使用の必要性を低減することである。歴史1933年にVincenzo Bisceglieは、ポリマーの膜に細胞をカプセル化する最初の試みを行った。彼は、ブタの腹腔に移植されたポリマー膜の中の腫瘍細胞は、免疫系によって拒絶されることなく、長期間生存可能であることを実証した。30年後の1964年に、超薄型高分子膜のマイクロカプセル内に細胞を封入することで、細胞に免疫に対しての防御を与えるというアイデアが、Thomas Changによって提案された。[2] カプセル化された細胞は、免疫拒絶から保護されるだけでなく、体積に対する表面積が大きくなり、それが酸素と栄養素の良好な移動を可能にすることも、示唆している。20年後、このアプローチは、小動物をモデルにし、実践された。すい臓のランゲルハンス島(膵島)の細胞を、アルギン酸塩 - ポリリジン - アルギン酸(APA)マイクロカプセルで、固定化し、異種間移植された。 この研究では、マイクロカプセル化したすい臓のランゲルハンス島を、糖尿病のラットに移植すると、細胞が生存し、数週間にわたって血糖を制御し続けたことを実証した。カプセル化された細胞を利用したヒトへの試験は1998年に実施された。進行性の切除不能なすい臓がんの臨床試験として、抗腫瘍効果を局所的に発揮するために、シトクロムP450酵素を発現するカプセル化細胞が腫瘍部位に移植され、シトクロムP450に分解されて抗腫瘍効果を発揮するプロドラッグが患者に投与された。対照と比較して約2倍の生存期間が示された。出典: フリー百科事典『ウィキペディア(Wikipedia)』カプセル化時代のデザイン [ 柏木博 ]
2021.07.01
コメント(0)
-

ヒトES細胞
1998年ウィスコンシン大学のジェームズ・トムソンらにより、ヒトES細胞株の樹立に成功。胚性幹細胞(はいせいかんさいぼう、英: embryonic stem cells)とは、動物の発生初期段階である胚盤胞期の胚の一部に属する内部細胞塊より作られる幹細胞細胞株のこと。英語の頭文字をとって、ES細胞(イーエスさいぼう、ES cells)と呼ばれる。体細胞より作られる人工多能性幹細胞(iPS細胞)とは異なる。生体外にて、理論上すべての組織に分化する分化多能性を保ちつつ、ほぼ無限に増殖させることができるため、有力な万能細胞の一つとして再生医療への応用が期待されている。またマウスなどの動物由来のES細胞は、体外培養後、胚に戻し、発生させることで、生殖細胞を含む個体中の様々な組織に分化することができる。また、その高い増殖能から遺伝子に様々な操作を加えることが可能である。このことを利用して、相同組換えにより個体レベルで特定遺伝子を意図的に破壊したり(ノックアウトマウス)、マーカー遺伝子を自在に導入したりすることができるので、基礎医学研究では既に広く利用されている。作製法と性質その製法は受精卵が胚盤胞と呼ばれる段階にまで発生したところで取り出して、フィーダー細胞 (英: feeder cell、一般にはマウス胚線維芽細胞 (MEF) が使われる) という下敷きとなる細胞と一緒に培養をすると、内部細胞塊が増殖を始める。この内部細胞塊は、胎盤などの胚体外組織以外の、全ての身体の組織に分化してゆく細胞集団である。増殖した内部細胞塊由来の細胞をばらばらにしてフィーダー細胞に植え継ぐ操作を繰り返し、最終的に「ES細胞株」を樹立する。マウスの場合にはLIF (leukemia inhibitory factor) という分化抑制因子を加える。一方、ヒトES細胞株の場合にはLIFは必要ないが、bFGF (basic fibroblast growth factor) が必要になる。いずれにしても、自発的に分化しやすい細胞であり、分化多能性の状態を保ったままの継代には非常に注意を要する。ES細胞であることを示すマーカーには、Oct3/4, STAT3, Nanogなどの遺伝子の発現がある。歴史1964年、研究者らは現在は生殖細胞由来であることが知られている腫瘍であるテラトカルシノーマから単一の種類の細胞を単離した。テラトカルシノーマから単離されたこれらの細胞は、幹細胞として培地中で複製、成長し、現在は胚性腫瘍 (EC; embryonic carcinoma) 細胞として知られている[1]。形態学的ならびに分化能(多能性)の類似から、EC細胞は初期マウス発生のin vitroモデルとして使われるようになったが[2]、EC細胞は遺伝子変異やテラトカルシノーマの発達の間に蓄積する異常な核型をしばしば有している。これらの遺伝的異常は、内部細胞塊から直接的に多能性細胞を培養できるようになる必要性をさらに強調した。マーティン・エヴァンズ1981年、胚性幹細胞(ES細胞)が、マウスの胚から2つの研究グループによって独立に樹立された。ケンブリッジ大学遺伝学部門のマーティン・エヴァンズおよびマシュー・カウフマンが7月に初めて報告し、子宮内のマウス胚を培養し、ES細胞を樹立する新たな技術を明らかにした。カリフォルニア大学サンフランシスコ校解剖学部門のゲイル・R・マーティンは12月に論文を発表し、「胚性幹細胞」という用語を作った。彼女は、胚がin vitroで培養できること、これらの胚からES細胞を樹立できることを示した。1998年、ウィスコンシン大学マディソン校のジェームズ・トムソンによって率いられた研究者らが、ヒト胚性幹細胞を単離・培養する技術を初めて開発した。出典:フリー百科事典『ウィキペディア(Wikipedia)』最新ES細胞iPS細胞 再生医療、創薬、病気の解明……、新たな可能性にせまる【3000円以上送料無料】
2021.06.30
コメント(0)
-

子羊ドリー
1996年ロスリン研究所でイアン・ウィルムットらにより、体細胞クローンの子羊ドリー誕生。ドリー(Dolly、1996年7月5日 - 2003年2月14日)は、世界初の哺乳類の体細胞クローンである雌羊。スコットランドのロスリン研究所で生まれ育ち、6歳で死ぬ。ドリーの誕生は1997年2月22日に発表された。ドリーという名前は乳腺細胞由来にちなんで、飼育係がドリー・パートンを称えて提案したものである。ドリーは体細胞の核を除核した胚細胞に移植する技術によって誕生した。ドリーは1996年に6歳の雌羊の細胞からクローンされ、今日まで続く議論の的となっている。2003年5月9日、ドリーの剥製がエディンバラのスコットランド博物館へ陳列された。クローン羊の作り方羊(A)の乳腺から乳腺細胞を取り出し、通常の血清濃度の1/20で培養する。このことによって細胞の全能性が復活する。雌羊(B)の子宮から未受精卵を取り出し、核を除去する。未受精卵に、先ほど処理した乳腺細胞を1つだけ挿入し、電気刺激をかけ細胞融合させる。融合した細胞を代理母の雌羊(C)の子宮に移植する。ドリーは上記の手順を持って誕生した。議論1999年にネイチャー誌に、ドリーは生まれつき細胞内の染色体にあるテロメアが短くなっているので生まれつき老化しているという研究が発表された[2]。遺伝情報の元が6歳のヒツジであり、したがってドリーは誕生時に遺伝子が既に6歳であったと推測された。しかしながら、ジョン・トーマスは殆どのクローン動物が実際は通常の長さのテロメアを持ち、連続でクローンをする度にテロメアは実際には長くなっていく事を指摘した。この徴候は2002年1月、ドリーが5歳の時に報告された。異常な若さで関節炎を発症し衰弱していったのである。これは生まれつきの老化によって説明が可能であるが、リバプール大学獣医学部のダイ・グローヴ=ホワイトは「関節炎はクローンのせいと言えるし、せいではないとも言える。我々の知る限りでは、ドリーはゲートを飛び越えた時に足をけがし、関節炎を悪化させた。」と述べた。この関節炎によりこの形式のクローンは哺乳類に適していないのではと心配され、現状ではヒトのクローンを作る実験は未熟で倫理的でないということが専門家のみでなく全体の合意を得ている。この方法でのクローンの支持者達は、この技術は改良すればいいだけであると反論する。しかしながら、応用発生学の初歩の理解が非常に限られており、多くの遺伝子の活性のコントロールを科学者は出来ない、すべきでないとする主張がなされた。多くの専門家でない者は、このためにあらゆる形のクローン産生が倫理的に間違っており禁止すべきであると規定し始めた。死2003年2月14日にドリーが進行性の肺疾患を起こしていた事が公表された。検死の結果でそれは羊によくある病気、ヒツジ肺腺腫であることが確かめられた。農場の他の羊も同じ様な病気にかかっていたため、これはドリーがクローンである事と関連していないとロスリン研究所の科学者達は述べた。ドリーは安楽死させられた。遺産ドリーでの成功の後、ウマやウシといった大型哺乳動物のクローンが多く誕生していった。医療の進歩を約束するが危険も伴うクローン技術が、SFの世界のものではなく、現実となったのである。クローンは絶滅の危機に瀕した動物を保護したり、犬や猫などのペットの命を取り戻すための手段と期待されている。また、マンモスなどの先史時代の動物を復活させる計画も少しずつながら研究が進んでいる。ヒトの場合反対は続いているが、クローンが体外受精、代理母、養子そして従来の繁殖方法に加えて新たに妥当な繁殖戦略に加えられるかもしれない。議論の的となっている子供の遺伝子操作であるが、これを行う事が受け入れられる場合が、条件付きで考えられる。その一つは遺伝性疾患のリスクを取り除くため、二つ目が家族との幹細胞移植の互換性を確実にするため、そして寿命を延ばしたり、免疫を強化したり、知能を高めたりするために子供の遺伝子を改良する事もありえる[要出典]。身体能力や知能を向上させるといった、遺伝学的形質向上は、『世界保健機構(WHO)による遺伝医療に関するガイドライン』において遺伝医学上、生命倫理上「行われてはならない」ものとして否定されている。しかし実際にはあくまでも子供が持つであろう能力のポテンシャルを若干向上させるだけであって、仮にデザイナーベビーが誕生したとしても、生まれ付きの高い知力・体力や将来の劇的な能力向上を期待出来る訳ではないとした見方が一般的である。出典: フリー百科事典『ウィキペディア(Wikipedia)』ダイレクトリプログラミング 再生医療の新展開 [ 鈴木淳史 ]
2021.06.29
コメント(0)
-

HAART療法
1996年国際エイズ学会にて逆転写酵素阻害剤とプロテアーゼ阻害剤を併用することによって、劇的に治療効果が上がったことが発表され、HAART療法の有効性が認められる。HAART療法(ハートりょうほう、英語: highly active anti-retroviral therapy)とは、複数の抗HIV-1薬を各人の症状・体質に合わせて組み合わせて投与し、ウイルスの増殖を抑え後天性免疫不全症候群 (AIDS) の発症を防ぐ治療法である。用語的には「Therapy」と「療法」とで意味が重なってしまうため、単に「HAART」あるいは「ART」(anti-retroviral therapy)と呼ばれ、2007年以降は後者のほうが正式に使われている。また、複数の薬剤を組み合わせることから、以前は俗称的にカクテル療法とも呼ばれていた時期がある。歴史核酸の構成物質である、チミジンの水酸基の一つをアジドに置換したアジドチミジン (AZT) が、HIV-1の増殖を抑制することが判明し、1987年に米国で初めての抗HIV-1薬として認可される。薬剤のターゲットはウイルス酵素の一つである逆転写酵素 (RT) である。作用機序としてはウイルスの逆転写の際、偽物の核酸を取り込ませて逆転写を途中で止める事によって、ウイルスの増殖を抑制する。この事から、核酸を基本とした核酸系逆転写酵素阻害剤 (nucleoside analogue RT inhibitor: NRTI) の開発がされる。しかし、単一種の薬剤による治療では薬剤耐性ウイルスの出現が避けられず、また重篤な副作用により、治療を中断せざるを得ない状況が起こるようになった。そこで治療方法の幅を広げるため、1980年代後半にはHIVの再生産の時に働くウイルス酵素の一つである、プロテアーゼをターゲットとする薬剤の開発が行われるようになる。作用機序としては、プロテアーゼの活性中心に結合し、機能を阻害する物が開発された。1990年代前半にいくつかのプロテアーゼ阻害剤 (protease inhibitor: PI) が開発され、1995年に米国で最初のプロテアーゼ阻害剤であるサキナビルが正式に認可される。また1990年代前半に、それまでとは作用機序の異なる、逆転写酵素阻害剤の開発が始まった。それまでの逆転写酵素阻害剤とは異なり、逆転写を止めるのではなく、逆転写酵素の活性中心に結合し機能を阻害する、プロテアーゼ阻害剤と同じ発想の薬剤である。核酸を基本としないことから、非核酸系逆転写酵素阻害剤 (non-nucleoside RT inhibitor: NNRTI) と区別される。そして1996年に米国でネビラピンが認可される。この様にして、1990年代中頃には数種類の抗HIV-1薬が登場した。1996年国際エイズ学会にて逆転写酵素阻害剤とプロテアーゼ阻害剤を併用することによって、劇的に治療効果が上がったことが発表された。この事実からHIV感染症治療として、多数の薬剤を組み合わせてウイルスの増殖を抑える、多剤併用療法HAARTが行われるようになる。以後、先進諸国ではHAARTによりAIDSによる死亡率が顕著に低下し、患者予後が著しく改善された。用法HIV-1は突然変異を起こしやすいため、単一の薬剤ではすぐに薬剤耐性ウイルスを誘導してしまう。薬剤耐性変異は、各薬剤ごとに特異的な点変異を生じることがわかっており、薬剤それぞれの耐性変異が重ならないように薬剤を組み合わせて処方される。核酸系逆転写酵素阻害剤、非核酸系逆転写酵素阻害剤、プロテアーゼ阻害剤は、それぞれ全く異なる場所に耐性変異を生じるため、これら三種類の薬剤から一つないし二つずつ薬剤を選び、組み合わせて使われる。同種の薬剤には耐性変異が同じ場所に現れるものがあり、これを交叉耐性という。例えば核酸系逆転写酵素阻害剤の場合、AZTとd4Tは同じ場所に耐性変異が現れるので、同時に使われることは少ない。交叉耐性はプロテアーゼ阻害剤においても存在するため、薬剤を選択する際には、予想される耐性変異を考慮して組み合わせて処方する。一度に服用する錠剤の数を減らすため、始めから二種類の薬剤を合わせたコンビビル、エプジコム、ツルバダ、カレトラといった合剤が作られており、普及しつつある。また、薬剤耐性変異及び副作用が生じた場合は、薬剤の組み合わせの変更がなされる。問題点薬剤耐性近年の研究により、薬剤耐性ウイルスの出現前に、血中のウイルスを検出限界以下まで減らすことができるようになった。しかしながら、初回治療で感染者の血中ウイルス量が、検出限界以下までに抑えられる割合は60%ほどである。残りの40%は、何らかの原因で血中のウイルス量が、検出限界以下にならない。その原因の多くが、薬剤耐性ウイルスの出現である。薬剤の組み合わせを変更することにより、改善する場合もあるが、中には多数の薬剤に対して耐性を示し、現在認可されているすべての薬剤に対し耐性を示す症例も少なくない。一般的に薬剤の使用歴が長く、使用した薬剤の種類が多い感染者ほど、多くの薬剤に対して耐性を示すウイルスが現れる。また、薬剤耐性ウイルスは薬剤の血中濃度が十分でないときに出現するため、薬の飲み忘れをよくしてしまう(アドヒアランスの低い)感染者では、薬剤耐性ウイルスの出現度が高くなっている。HIVの増殖を抑えるように緻密な治療方法が考えられ、多くの感染者の予後を向上させているが、それでも薬剤耐性ウイルスの出現は避けられず、根本的な解決には至っていないのが現状である。副作用すべての薬剤がそうであるように、HAARTにおいても副作用が存在し、それは死に至るまで重症化することがある。長期にわたって薬剤を服用するため、様々な副作用が起こっている。核酸系逆転写酵素阻害剤によって引き起こされる、ミトコンドリア障害に起因する乳酸アシドーシス、脂肪肝は特に重大な副作用である。その結果、肝機能障害を引き起こし死に至る場合もある。プロテアーゼ阻害剤では、体脂肪分布異常や脂質異常症など、リポジストロフィーといわれる体脂肪異常が起こる。その結果、動脈硬化などの血管疾患を引き起こす。このような副作用が出た場合は薬剤の変更が検討されるが、先の薬剤耐性との関連もあり、治療の選択肢が広いとはいえない。治療によるメリットと副作用によるデメリットを考慮して、治療を中断することもある。治療費高額な薬剤費用のため、後進国では十分にHAARTによる治療を行うことができない。コピー薬の認可政策や価格を抑えた治療薬等の対策も行われているがまだ十分ではない。出典: フリー百科事典『ウィキペディア(Wikipedia)』平成3年5月2日,後天性免疫不全症候群にて急逝された明寺伸彦博士,並びに,【完全版】【電子書籍】[ 石黒達昌 ]
2021.06.28
コメント(0)
-
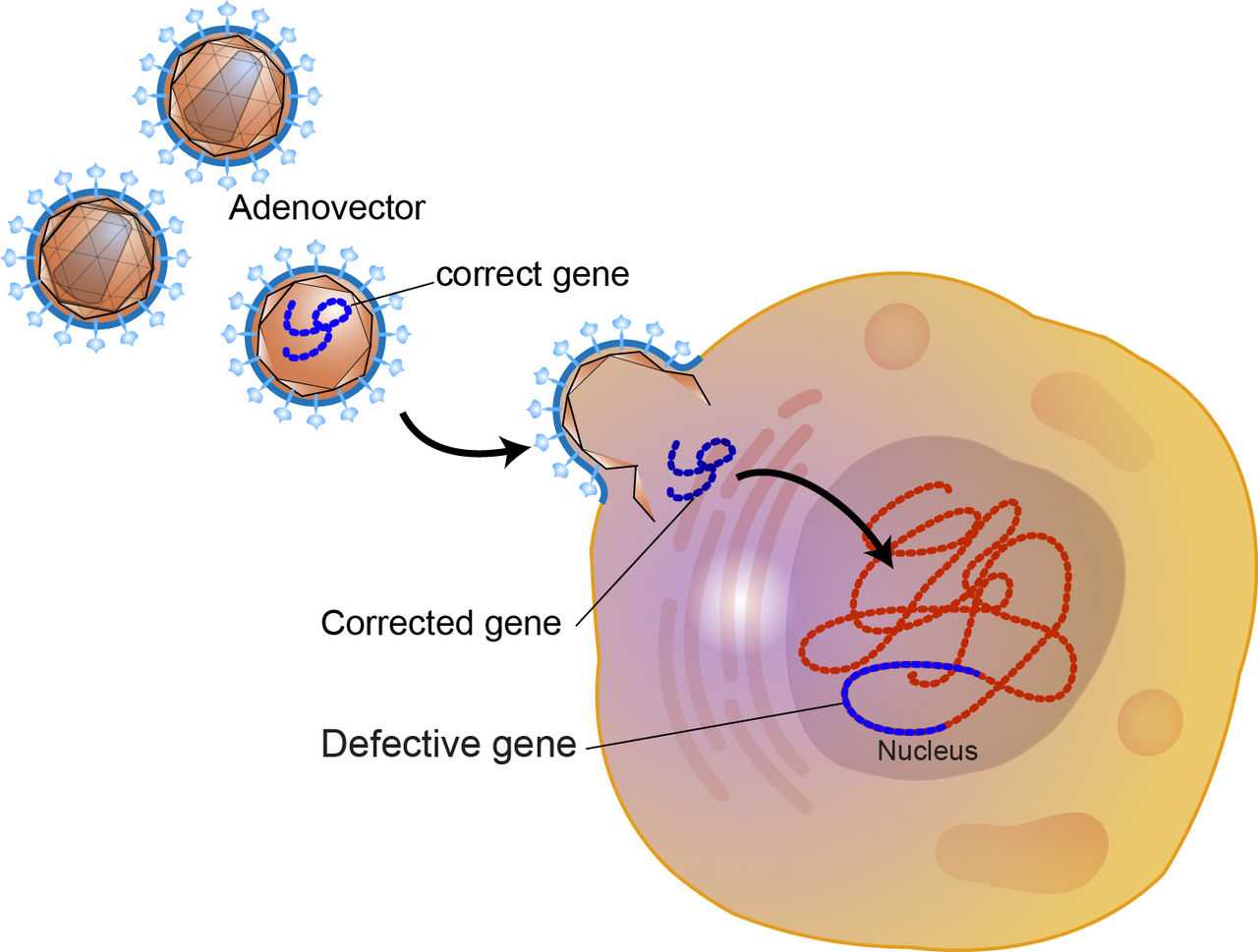
遺伝子治療
1990年アメリカ合衆国で、世界初の遺伝子治療。アデノシンデアミナーゼ欠損症による重度免疫不全患者に対する治療が行われた。遺伝子治療は、患者の遺伝子の一部を置き換えることにより治療する実験技術である。多くの場合、患者が持っている欠陥のある遺伝子へと、健常なコピーを導入することにより行われる。遺伝子治療(いでんしちりょう)とは、異常な遺伝子を持っているため機能不全に陥っている細胞の欠陥を修復・修正することで病気を治療する手法である。代表的なものでは、治療用の遺伝子情報を組み込んだレトロウイルスを異常な遺伝子を持つ細胞内に浸入させる手法がとられているが、成功例は少なく、より画期的なDNA導入法が期待される。ベクターを注射、吸入、塗布などで患部組織に注入するか、患者自身の血球などを一度取り出し、体外でベクターを作用させてから、患者に戻す方法などがある。具体例として、1990年アメリカにおいてアデノシンデアミナーゼ欠損症による重度免疫不全患者に対する初の遺伝子治療に成功し、その後日本でも1995年北海道で同様の成果が得られた。課題遺伝子治療の研究として1990年代に臨床試験が開始されたものの、次のような課題により盛衰を繰返した。送達の問題 - DNAの帯電した分子に細胞膜と核膜を通過させるのが困難。ベクターとしてウイルスを使うことになるが制御が困難。機能の問題 - DNAを標的細胞に入れたとしても、機能として発現させるのが困難。タンパク質へと転写・翻訳される見込みが薄い。免疫反応の問題 - ウイルスが異物として免疫系からみなされることになるので、長期のウイルス投与になるほど困難。1999年には死亡事故が起こり、また白血病を患うことになった患者も存在する。このような事情により、ES細胞やiPS細胞を中心とした幹細胞治療へと、研究の方向性は広がっていった。2010年代に入ると、ZFN、TALEN、CRISPR/Cas9を中心としたゲノム編集と呼ばれる高効率の遺伝子改変技術が登場することになった。2015年にはCRISPR/Cas9を用いた世界初のヒト受精卵の遺伝子操作が中華人民共和国で行われ、国際的な波紋を起こした。これにより2015年現在、ヒト受精卵に対するゲノム編集技術の倫理的規制が新たな課題となっている。出典: フリー百科事典『ウィキペディア(Wikipedia)』図解・最先端治療 がん遺伝子治療のことがわかる本 [ 石田 幸弘 ]
2021.06.27
コメント(0)
-
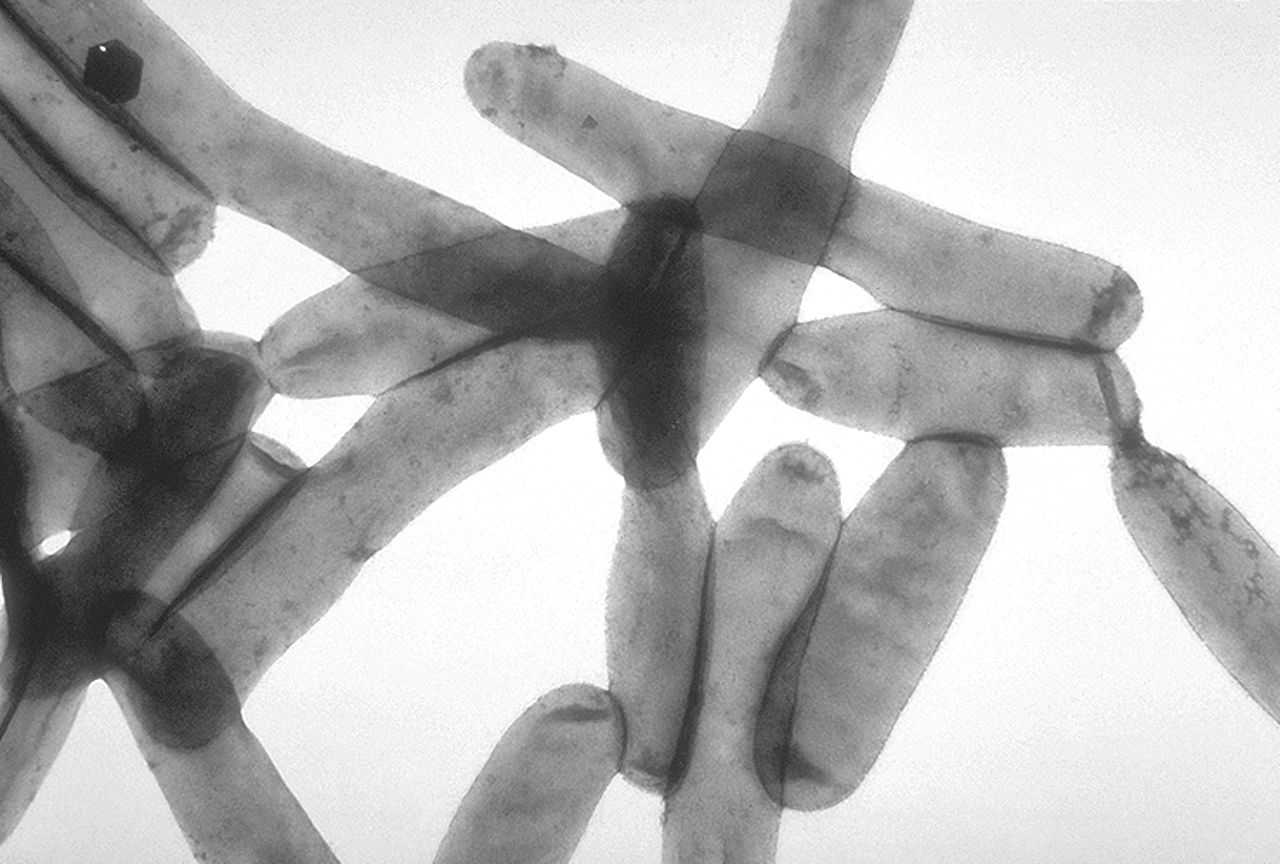
レジオネラ
1986年レジオネラの発見。レジオネラ (Legionella) は、レジオネラ属に属する細菌の総称であり、グラム陰性の桿菌。レジオネラ肺炎(在郷軍人病)等多くのレジオネラ症を引き起こす種を含む。少なくとも46の種と、70の血清型が知られている。通性細胞内寄生性菌である。発見1976年にアメリカ合衆国ペンシルベニア州米国在郷軍人会(英語版)の大会が開かれた際、参加者と周辺住民221人が原因不明の肺炎にかかり、一般の抗生剤治療を行なったが34人が死亡した。ウイルス、リケッチア等が原因の候補に挙げられたがそれらしいものは検出されず、新種のグラム陰性桿菌が患者の肺から多数分離された。発見された細菌は在郷軍人 (legionnaire) にちなんで Legionella pneumophila と名づけられた。種形容語の pneumophila は、本菌が肺に感染することから、「肺(ギリシア語でpneumōn)を好む (-phil)」を意味する。この集団感染事例は、在郷軍人会の大会会場近くの建物の冷却塔から飛散したエアロゾルに起因していたとされている。特徴レジオネラ属菌は2 - 5µm位の好気性グラム陰性の桿菌で、一本以上の鞭毛を持っている。通常の細菌検査用培地では生育しないが、これはグルコースなどの糖を利用できない事に起因する。このため培養の際にはレジオネラがエネルギー源および炭素源として利用できるシステインやセリン、スレオニンなどの特定のアミノ酸を加える必要がある。特にシステインは必須である。脂肪酸により発育阻害を受けるためこれらを除去しなければならない。また、有機鉄も要求する。培養条件は厳しく、pHが6.7〜7.0でないと増殖せず、至適温度は36°Cである。分裂周期は数時間で、増殖には時間がかかり、バンコマイシン等の抗生物質を加え他の菌の生育を抑えて培養する。環境中では人工培地とは異なり幅広い環境で生育可能である。主に沼や河川などの水の中や、土壌に存在している自然環境中の常在菌の一種としても知られる。レジオネラは通性細胞内寄生性であり、これらの場所ではアメーバなどの原生生物など他の生物の細胞内に寄生したり、藻類と共生しており、これによってさまざまな環境での生育が可能になっている。上記の人工培養条件下で必要とされる厳しい栄養要求は、当然のことながら他の生物の細胞内では容易に得られるものである。水中でも長期間( - 数年)生存できる。ヒトの生活する環境においても、大量の水を溜めて利用する場所でレジオネラが繁殖する場合が知られている。特に Legionella pneumophila は、空調設備に用いる循環水や入浴施設においてよく見られ、しばしばこれらの水を利用する際に発生する微小な水滴(エアロゾル)を介してヒトに感染する。レジオネラを含んだエアロゾルがヒトに吸入されると、レジオネラは肺胞に到達し、そこで肺胞のマクロファージに貪食される。しかし、レジオネラは通性細胞内寄生性であり、その殺菌機構を逃れてマクロファージ内で増殖することが可能である(→サルモネラのマクロファージでの増殖参照)。レジオネラはマクロファージに取り込まれる際に出来る食胞に作用し、食胞膜の性質を変化させてリソソームとの結合性を失わせるとともに、その変化した食胞 (LCV, Legionella containing vesicle) 内で増殖する。LCVは、粗面小胞体と同様にリボソームが表面に結合した、多重の膜構造を持つ小胞であり、この小胞を形成することでレジオネラは分解されることなく細胞内に感染することが可能だと考えられている。人工環境では、レジオネラはしばしばアカントアメーバなどのアメーバ類に寄生していることが知られているが、この生活様式が衛生学上、レジオネラを除去しにくいことに関わっている。これらの自由生活アメーバは浴槽などの表面に形成されるバイオフィルムに付着して生活していることが多いため、循環式のろ過処理設備から逃れて増殖可能である。レジオネラ自身、単独でもバイオフィルムの形成が可能である。またバイオフィルムの存在と、アメーバの細胞内に寄生していることによって、レジオネラに対して消毒薬が直接到達しにくいため、消毒薬の効果が妨げられる。さらに自由生活アメーバの中には、生育環境が悪化するとシスト(嚢子、のうし)と呼ばれる、耐久型の構造を形成するものがあり、この状態では熱や消毒薬に対する抵抗性が増加するため、内部のレジオネラが保護される形になって完全な除菌が難しくなるという問題が生じる。病原性レジオネラは環境中に普通に存在する菌であり、通常では感染症を引き起こすことは少ない。しかしながら感染しやすい環境に示すような環境下では、特に高齢者等抵抗力の少ない人々にとって、主にレジオネラ属の一種、L. pneumophila が、ヒトのレジオネラ感染症(レジオネラ肺炎およびポンティアック熱)の原因になる。出典: フリー百科事典『ウィキペディア(Wikipedia)』レジオネラ感染症ハンドブック [ 斎藤厚 ]
2021.06.26
コメント(0)
-
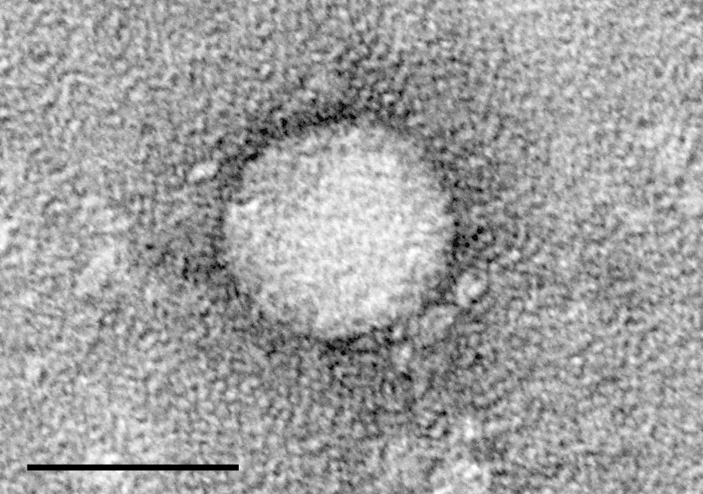
C型肝炎
1986年C型肝炎ウイルスの発見。C型肝炎(Cがたかんえん、英: Hepatitis C)とは、C型肝炎ウイルス (HCV) に感染することで発症するウイルス性肝炎の一つ。かつては非A非B型肝炎輸血後肝炎・血清肝炎と呼ばれていた。疫学現在の日本のHCV感染者数は約200万人、世界では1億7千万人(世界人口の3パーセント近く)がキャリアであると見られている。日本ではインターフェロン治療が効きにくい1b型が70 - 85パーセントを占め、以降2a型が10 - 15パーセント、2b型が約5パーセントで、他はまれである。ただし、血友病患者では1a型が多い。これは、血友病患者がC型肝炎に罹患する原因となった、血液製剤の輸入元であるアメリカ合衆国では、1a型が最も多いことに由来する。U.S. Preventive Services Task Forceは、1945〜1965年生まれの全てのアメリカ人に対して、C型肝炎スクリーニングを推奨することとした。感染経路HCVは血液が主な感染経路で、かつては輸血による感染が多かった。ディスポーザブル注射器の普及により現在においては先進国では検査体制が確立したためほとんど見られない。現在は針刺し事故や、鍼、ピアス、入れ墨(刺青)、覚醒剤注射の回し打ちなどが主である。カミソリの共用、歯ブラシの取り違え、コンタクトスポーツでも感染者の血液や唾液の付着による感染リスクがある。血液製剤(フィブリノゲン製剤、第IX因子製剤)の投与によるC型肝炎感染については、非血友病患者に対する投与に対して、日本国政府と製薬会社を相手とする訴訟(薬害肝炎訴訟)が起こされている。出典: フリー百科事典『ウィキペディア(Wikipedia)』[書籍のメール便同梱は2冊まで]/肝炎のすべてがわかる本 C型肝炎・B型肝炎・NASHの最新治療 イラスト版[本/雑誌] (健康ライブラリー) / 泉並木/監修
2021.06.25
コメント(0)
-
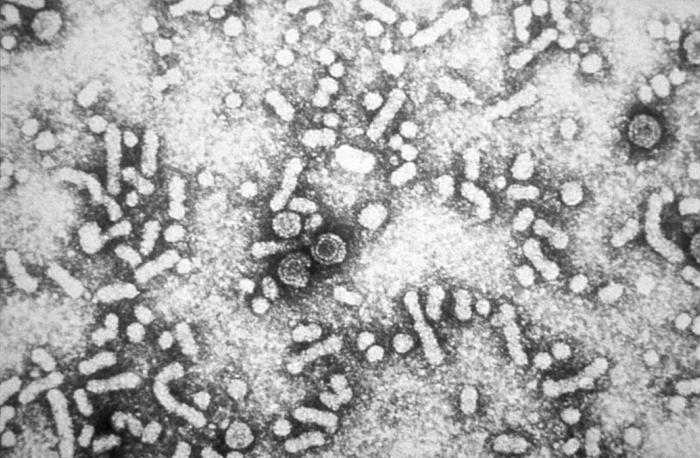
B型肝炎
1981年B型肝炎ウイルスの最初のワクチンが開発された。B型肝炎(Bがたかんえん、英: Hepatitis B)とは、B型肝炎ウイルス (HBV) に感染することで発症するウイルス性肝炎の一つ。血液を介して感染するため、従来の検査体制が確立されない時期に輸血を介して、または1986年に母子間ブロックが実施されるようになる前には母子感染で感染した。感染の予防策としては、注射器を共用しない。主な治療法は、インターフェロンや核酸アナログ製剤を用いた抗ウイルス療法がある。日本においてB型肝炎ウイルス保有者(キャリア)は、150万人程度といわれている。その内の約95%は自然治癒するが、約5%は肝炎発症となり、慢性肝炎、肝硬変、肝臓ガンへと進行することがある。疫学2002年のB型肝炎による人口10万人当たりの障害調整生存年数(en: disability-adjusted life year)。 ≤ 10 10–20 20–30 30–40 40–50 50–80 80–100 100–120 120–150 150–200 200–500 ≥ 500近年、日本ではあまり見られなかったジェノタイプA(北米、欧州、アフリカ中部に多く分布する)のB型肝炎ウイルス感染が広がりつつある。ジェノタイプAのB型肝炎ウイルスに感染した場合、その10%前後が持続感染状態(キャリア化)に陥る。本来、日本に多いジェノタイプCのB型肝炎ウイルスは、成人してからの感染では、キャリア化することはまれであったことから、ジェノタイプAのB型肝炎ウイルス感染の拡大には、警戒が必要である。感染B型肝炎ウイルスは、血液や体液の飛沫を介して感染する。感染経路は主に以下がある。成人以降での水平感染の多くは、一過性であることが多い。垂直感染:母子感染水平感染:輸血・臓器移植・刺青・針刺し事故・注射器の使い回し・コンタクトスポーツ等2002年4月、佐賀中部保健所に急性B型肝炎の届出があり、保育所で25名の集団感染が疑われた[2]。感染源は、HBVキャリアである元職員が疑われたが全例で特定することはできなかった[2]。日常生活の中でも感染が起こりうることを確認し、その感染様式には出血及び滲出液を伴う皮膚疾患が関与している可能性と、感染防御策にワクチン接種を加えることが有効であることが示唆された[2]。かつては幼児期(7歳まで)の輸血による感染が多かったが、現在では先進国では検査体制が確立したため、ほとんど見られない。針刺し事故や注射針の回し打ち・刺青での針の再使用などもある。日本では、戦後から1988年頃まで行われた、幼児期の集団予防接種における注射針や注射筒の使い回しにより、B型肝炎ウイルスが蔓延した。日本国政府は1948年には注射針・注射筒の連続使用の危険性を認識していたが、40年にわたり使い回しの現状を放任していた。2011年現在、推定150万人の持続感染者(キャリア)の内、集団予防接種による感染者は30%前後と言われており、この集団感染訴訟は、2011年6月28日に国と原告との間で基本合意が締結し、2012年(平成24年)1月13日に特定B型肝炎ウイルス感染者給付金等の支給に関する特別措置法が施行され、裁判上の和解が成立した者に対し、日本国政府は法に基づく給付金を支給することになった。出典: フリー百科事典『ウィキペディア(Wikipedia)』[書籍のメール便同梱は2冊まで]/B型肝炎被害とは何か 感染拡大の真相と被害者救済[本/雑誌] / 岡多枝子/編著 片山善博/編著 三並めぐる/編著
2021.06.24
コメント(0)
-
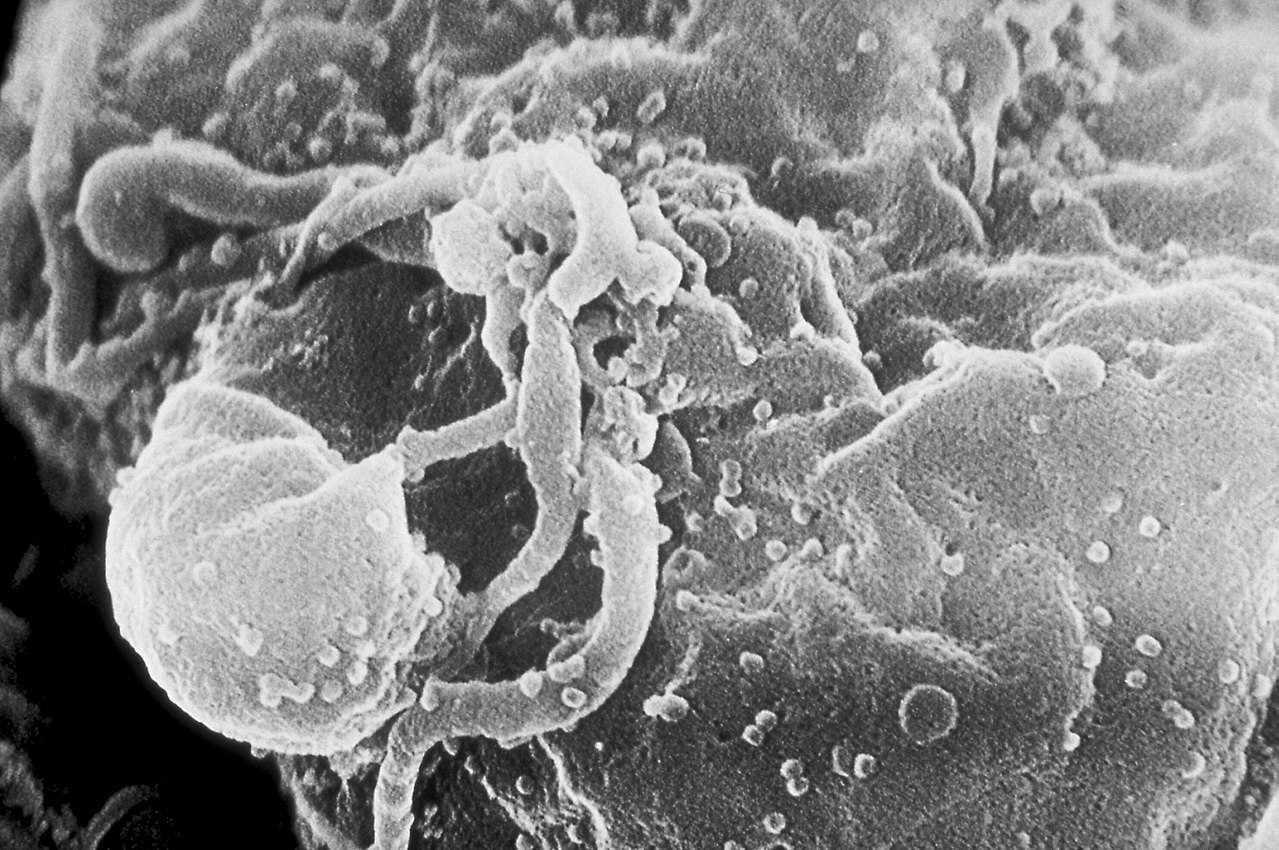
HIV(ヒト免疫不全ウイルス)
1982年HIV(ヒト免疫不全ウイルス)の発見。ヒト免疫不全ウイルス(ヒトめんえきふぜんウイルス、英語: Human Immunodeficiency Virus, HIV)は、人の免疫細胞に感染してこれを破壊し、最終的に後天性免疫不全症候群 (AIDS)を発症させるウイルス。1983年に分離された。日本では1985年に感染者が認知された。歴史1983年に、パスツール研究所のリュック・モンタニエとフランソワーズ・バレシヌシらによってエイズ患者より発見され「LAV (Lymphadenopathy-associated virus)」と命名された。1984年に、アメリカ国立衛生研究所 (NIH)のロバート・ギャロらも分離に成功しており、「HTLV-III (Human T-lymphotropic virus type III)」と命名した。続いて、カリフォルニア大学サンフランシスコ校のレヴィらも分離に成功し、「ARV (AIDS-associated retrovirus)」と命名した。LAV、HTLV-III及びARVは、後にいずれも同じウイルスである事が明らかとなりHIV-1と改称され、1985年には、モンタニエらが、エイズ患者から新たな原因ウイルスを分離し、「LAV-2 (Lymphadenopathy-associated virus-2)」と命名し、LAV-2はその後HIV-2と改称された。最初の発見者を巡って、モンタニエとギャロの仏米の研究チームが長年にわたって対立し、1994年に両者が共に最初であるとして決着したが、長期の対立はエイズ治療薬の特許が絡むもので、治療薬の発売を遅らせないための政治的決着であった。2008年10月6日、フランスのモンタニエとバレシヌシの2人がウイルスの発見者として、2008年のノーベル生理学・医学賞を授与された。カリフォルニア大学バークレー校教授のピーター・デュースバーグ (en:Peter Duesberg) などのように、AIDSの原因がHIVであると認めないエイズ否認主義は科学界で明確に否定されている。起源ウイルスの分類上は、エンベロープを持つプラス鎖の一本鎖RNAウイルスであるレトロウイルス科レンチウイルス属に属する。以下の2つが存在する。HIV-1 (Human Immunodeficiency Virus type1)HIV-2 (Human Immunodeficiency Virus type2)霊長類を自然宿主とするサル免疫不全ウイルス (Simian Immuno-deficiency Virus: SIV)が、突然変異によってヒトへの感染性を獲得したと考えられている。ウイルスの塩基配列を比較すると、「HIV-1」はチンパンジーから分離されたSIVcpzに近く、「HIV-2」はマカクやマンガベーなどのサルから分離されたウイルスSIVmacやSIVsmmに近い。以上から、SIVに感染したサルからヒトへと感染し、HIVに進化したと考えられている。「HIV-1」と「HIV-2」の基本的な遺伝子の構造はほぼ同じであるが、塩基配列の類似性は低く60%ほどであり、最も大きな遺伝子の相違として、「HIV-1」にはvpuが、「HIV-2」にはvpxがそれぞれに存在し、この相違はSIVcpzとSIVsmmの間にも見られることから、「HIV-1」と「HIV-2」はそれぞれ独立した祖先から、人間に感染する能力を持ったウイルスに進化したものと考えられている。出典: フリー百科事典『ウィキペディア(Wikipedia)』【送料無料】 病院内 / 免疫不全関連感染症診療の考え方と進め方 第2集 IDATEN感染症セミナー実況中継 / Idatenセミナーテキスト編集委員会 【本】
2021.06.23
コメント(0)
-
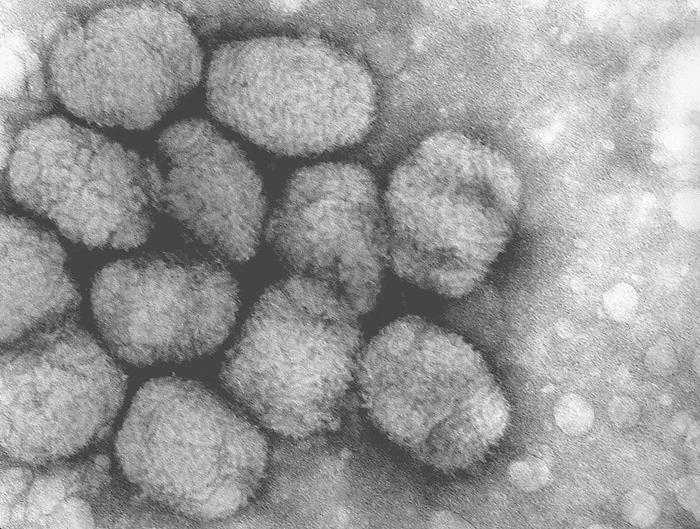
天然痘
1980年WHO第33回総会において天然痘撲滅宣言がおこなわれた(最終症例は1977年、ソマリアにおいて)。これが疾病制圧の最初の例となった。天然痘(てんねんとう、英語: Variola、Smallpox)は、天然痘ウイルスを病原体とする感染症の一つである。疱瘡(ほうそう)、痘瘡(とうそう)ともいう。医学界では一般に痘瘡の語が用いられた。疱瘡の語は平安時代、痘瘡の語は室町時代、天然痘の語は1830年の大村藩の医師の文書が初出である。ヒトに対して非常に強い感染力を持ち、全身に膿疱を生ずる。致死率が平均で約20%から50%と非常に高い。仮に治癒しても瘢痕(一般的にあばたと呼ぶ)を残す。天然痘は人類史上初めてにして、唯一根絶に成功した人類に有害な感染症である(2021年現在)。天然痘ウイルス天然痘ウイルス (Variola virus) は、ポックスウイルス科オルソポックスウイルス属に属するDNAウイルスである。直径200ナノメートルほどで、数あるウイルス中でも最も大型の部類に入る。天然痘の原型となるウイルスはラクダから人類へと入り、そこで変化を起こして天然痘ウイルスが成立した可能性が高いと考えられている。ヒトのみに感染、発病させるが、膿疱内容をウサギの角膜に移植するとパッシェン小体と呼ばれる封入体が形成される。これは天然痘ウイルス本体と考えられる。また、牛痘やサル痘、ラクダ痘といった近縁種の病気が存在する。サル痘はしばしば重篤化して人の命を奪うことがあるが、牛痘やラクダ痘などほかの近縁種の病気は人類に感染しても軽い発熱や水疱が出る程度で、非常に軽い症状で済むうえ、できた免疫は天然痘と共通する。この性質を利用して、牛痘をあらかじめ人類に接種する種痘法が確立され、天然痘の撲滅が達成されることとなった。天然痘は独特の症状と経過をたどり、古い時代の文献からもある程度その存在を確認し得る。大まかな症状と経過は次のとおりである。飛沫感染や接触感染により感染し、7 - 16日の潜伏期間を経て発症する。40℃前後の高熱、頭痛・腰痛などの初期症状がある。発熱後3 - 4日目に一旦解熱して以降、頭部、顔面を中心に皮膚色と同じまたはやや白色の豆粒状の丘疹が生じ、全身に広がっていく。7 - 9日目に再度40℃以上の高熱になる。これは発疹が化膿して膿疱となる事によるが、天然痘による病変は体表面だけでなく、呼吸器・消化器などの内臓にも同じように現われ、それによる肺の損傷に伴って呼吸困難等を併発、重篤な呼吸不全によって、最悪の場合は死に至る。2 - 3週目には膿疱は瘢痕を残して治癒に向かう。治癒後は免疫抗体ができるため、二度とかかることはないとされる。天然痘ウイルスの感染力は非常に強く、患者のかさぶたが落下したものでも1年以上も感染させる力を持続する。天然痘の予防は種痘が唯一の方法であるが、種痘の有効期間は5年から10年程度である。何度も種痘を受けた者が天然痘に罹患した場合、仮痘(仮性天然痘)と言って、症状がごく軽く瘢痕も残らないものになるが、その場合でも他者に感染させることはある。「種痘」というワクチン接種による予防が極めて有効。感染後でも3日以内であればワクチン接種は、発症あるいは重症化の予防に有効であるとされている。また化学療法を中心とする対症治療が確立されている。出典: フリー百科事典『ウィキペディア(Wikipedia)』最後の天然痘地帯ーエチオピアー 若き隊員たちの「感染症」との苦闘の記録 [ 矢嶋和江 ]
2021.06.22
コメント(0)
-

ルイーズ・ブラウン
1978年 世界初の体外授精児(ルイーズ・ブラウン)誕生。ルイーズ・ジョイ・ブラウン(Louise Joy Brown、1978年7月25日 - )は、世界初の「試験管ベビー」として知られるイギリスの女性。人物・来歴父ジョンと母レズリーは9年間子供を授かろうと努めていたものの、レズリーの卵管に異常があったため自然妊娠はかなわず、体外受精に望みを託した[1]。この体外受精技術は、ケンブリッジ大学のロバート・エドワーズ教授と婦人科医パトリック・ステップトーが12年に渡る研究の末に完成させたもので、1977年11月10日に母体から採取された卵子を体外受精させ、2日半後、受精卵を母の子宮へ移し、その後は普通に成長した。この技術には非難も多く、ロンドンでは連日集会が開かれた。一方で、自宅には祝福する手紙も多く届けられた。1978年7月25日午後11時47分、イングランド北部のオールダム総合病院で、帝王切開により世界初の体外受精技術による子供として誕生した。出生時の体重は5ポンド12オンス(2608グラム)だった。ルイーズの誕生はその後の不妊治療の大きな希望となり、世界中の注目を集めた。両親はステップトーにミドルネームの命名を依頼した。ステップトーは「これから全世界の人々と喜びを分かち合う」ということで「Joy(喜び)」と名付けた。4歳の頃に両親から産まれた時のフィルムを見せられて事情を説明され、他の人と違う方法で産まれてきたことや常にマスコミが興味を示してくる理由を理解したという。看護師をした後、現在はイングランド南西部ブリストルの郵便局で働いている。2002年3月に警備員をしていた男性ウェズリー・マリンダーと出会い、2004年9月4日に結婚。ブリストルの教会で行った結婚式にはエドワーズ教授も招待された(ステップトーはルイーズが10歳の時に他界)。2006年7月11日、自然妊娠していることが発表された。2006年12月21日に男の子を出産した。2013年に次男を出産した。ちなみに、ルイーズの妹ナタリーも1982年、体外受精で誕生している。ナタリーは1999年5月、最初に子供を産んだ試験管ベビーとなり、「体外受精で生まれた女性は将来、健康な子供を産むことができない」というそれまでの懸念を覆した。2010年にロバート・エドワーズ教授がノーベル生理学・医学賞を受賞し、ルイーズは「素晴らしいニュースです」とコメントを寄せた。父ジョンは2007年に死去。母レズリーは体調を崩しブリストルの病院に入院していたが、2012年6月6日に64歳で亡くなった。5人の孫に恵まれていた。2018年5月20日、日本に招かれ六本木ヒルズで講演した[2]。その折に『読売新聞』によるインタビューで、自分は「ごく普通」の人間であるが、体外受精への理解を深めるため、マスメディアで積極的に話すようにしている旨を語っている[7]。出典: フリー百科事典『ウィキペディア(Wikipedia)』体外受精と顕微授精〈2020〉 i-wishママになりたい/不妊治療 体外受精 顕微授精 本 不妊治療情報センター 【本】【発行元】
2021.06.21
コメント(0)
-

アシロマ会議
1975年 -アメリカ合衆国でアシロマ会議が開かれ、遺伝子組み換えのガイドラインが議論された。アシロマ会議 (Asilomar conference) は遺伝子組換えに関するガイドラインが議論された会議。1975年開催。アメリカ合衆国カリフォルニア州アシロマにおいて開催されたことからこう呼ばれる。28か国から140人ほどの専門家が参加した。科学者自らが研究の自由を束縛してまでも自らの社会責任を問うたことで科学史に残る。歴史的経緯当時は DNA の二重らせん構造が明らかにされたことを受けて分子生物学が爆発的な成長を遂げつつあった。制限酵素、ライゲーション、形質転換など遺伝子組み換えの基礎となる技術が樹立され、大腸菌を用いて発ガン性ウイルスの研究などが着手されつつあった。科学者の中には無限の可能性を手に入れたと驚喜する者がいる一方で、この新たな技術が重大な危険性をはらんでいることを指摘する者もいた。例えば大腸菌のように人の体内で生育する細菌が新たな病原性を獲得した場合、それらは容易に広まりうる可能性をもっている。またこの技術は細菌兵器などに容易に応用されうる。生物によるこのような災害をバイオハザードという。当時公害に関する規制は強化されつつあったものの、生物実験施設に対する規制はなかった。発端は組み換え技術を開発したポール・バーグが腫瘍学者のロバート・ポラックにその危険性を指摘されたことに始まる。最初は反発したバーグだったがポラックに説得され、米科学雑誌サイエンスにジェームズ・ワトソンらなどと連名で遺伝子組み換えのガイドラインに関する国際会議を行うことを呼びかける。この会議はアシロマの国際会議場で開催された。会議は「生物学的封じ込め」によって合意をみる。また各国はこの会議に基づいて「物理学的封じ込め」などのガイドライン制定を行った。日本では「組換えDNA実験指針」が取り決められた。遺伝子組み換え生物による生物多様性の破壊を防ぐためにカルタヘナ議定書が2003年11月21日に締結された。日本ではこれに対応するための国内法(カルタヘナ法)が制定され、組換えDNA実験指針に代わって規制の中心となっている。生命倫理の観点から科学者が自ら束縛を許容した背景には、当時の分子生物学者には戦後に核物理学から転向した者が多く、自分達の科学技術が原子爆弾に応用されたことへの反省もあったと思われる。現在の生物学・生命科学は様々な倫理的問題を潜在的・顕在的に抱えており、アシロマ会議は生物学における倫理規制の古典的な例として引き合いに出されることも多い。出典: フリー百科事典『ウィキペディア(Wikipedia)』植物改良への挑戦 メンデルの法則から遺伝子組換えまで [ 鵜飼保雄 ]
2021.06.20
コメント(0)
-

ポール・ラウターバー
1973年ポール・ラウターバー、核磁気共鳴画像法の研究を発表。MRIによる画像撮影に成功する。ポール・クリスチャン・ラウターバー(Paul Christian Lauterbur、1929年5月6日 - 2007年3月27日)は、アメリカ合衆国の化学者。核磁気共鳴画像法(MRI)の開発を可能にする発見で、ピーター・マンスフィールドと共に2003年のノーベル生理学・医学賞を受賞した。彼のオリジナルのMRIは、ロングアイランドにあるニューヨーク州立大学ストーニーブルック校にある。オハイオ州シドニー生まれ。1969年よりニューヨーク州立大学ストーニブルック校、1985年よりイリノイ大学アーバナ・シャンペーン校の教授を歴任した。2007年にイリノイ州アーバナで死去。享年77年。主な受賞歴生物物理学賞(1983年)ラスカー・ドゥベーキー臨床医学研究賞(1984年)ガードナー国際賞(1985年)ハーヴェイ賞(1986年)IEEE栄誉賞(1987年)アメリカ国家科学賞(1987年)ハイネケン賞(1989年)Bower Award and Prize for Achievement in Science(1990年)ディクソン賞科学部門(1992年)京都賞先端技術部門(1994年)ノーベル生理学・医学賞(2003年)出典: フリー百科事典『ウィキペディア(Wikipedia)』【送料無料】 骨軟部疾患の画像診断 画像診断別冊 第2版 / 上谷雅孝 【本】
2021.06.19
コメント(0)
-
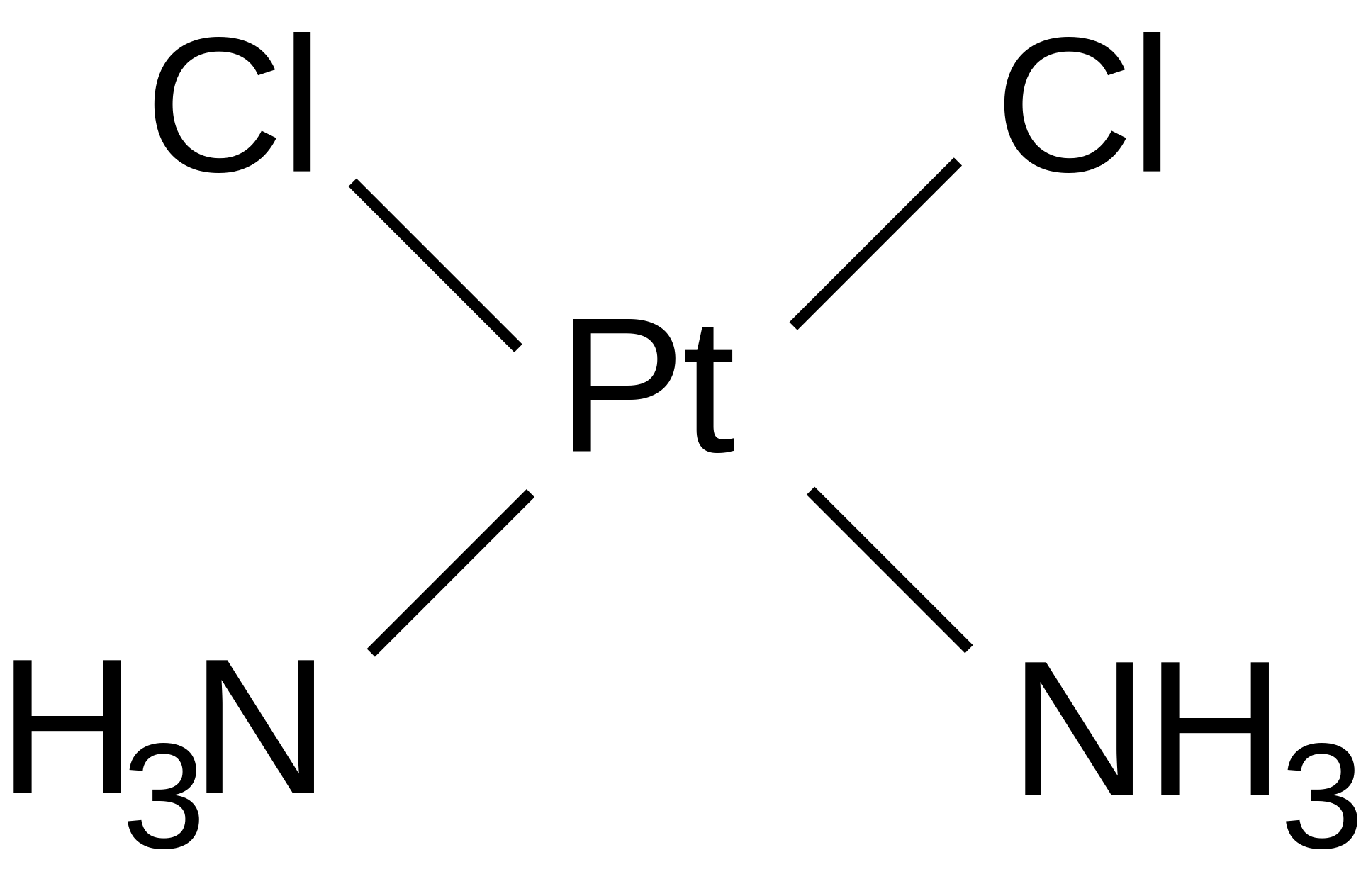
シスプラチン
1972年 抗がん剤シスプラチンの臨床試験が始まる。白金製剤と言われる抗がん剤のはしりだが、強い腎毒性のため承認は1978年までずれこんだ。シスプラチン(英語: cisplatin、略称:CDDP)は、白金錯体に分類される抗悪性腫瘍剤(抗がん剤)。シスプラチンの「シス」は、立体化学の用語のシスに由来する。錯体の中心金属は白金、配位子はアンミンと塩化物イオンであり、物質名はシス-ジアミンジクロロ白金(II)(cis-diamminedichloro-platinum(II)、cis-[PtCl2(NH3)2])である。なお、日光によって分解されるため、直射日光を避けて保存する必要があり、点滴にかかる時間を長く取る必要がある場合は点滴容器の遮光が必要となることもある。世界保健機関 (WHO) の下部組織によるIARC発がん性リスク一覧のグループ2に属する。ヒトに対する発癌性の限られた証拠、動物実験での十分な証拠がある。商品名は、ブリプラチン(ブリストル・マイヤーズ)、ランダ(日本化薬)など。白金製剤としては、ほかにカルボプラチン、ネダプラチン、オキサリプラチンがある。 薬理作用を発現するのはシス型だけでトランス型は抗がん作用を示さない。出典: フリー百科事典『ウィキペディア(Wikipedia)』やさしくわかる抗がん剤の副作用とその対処法 いつもと同じ日常を過ごすために
2021.06.18
コメント(0)
-
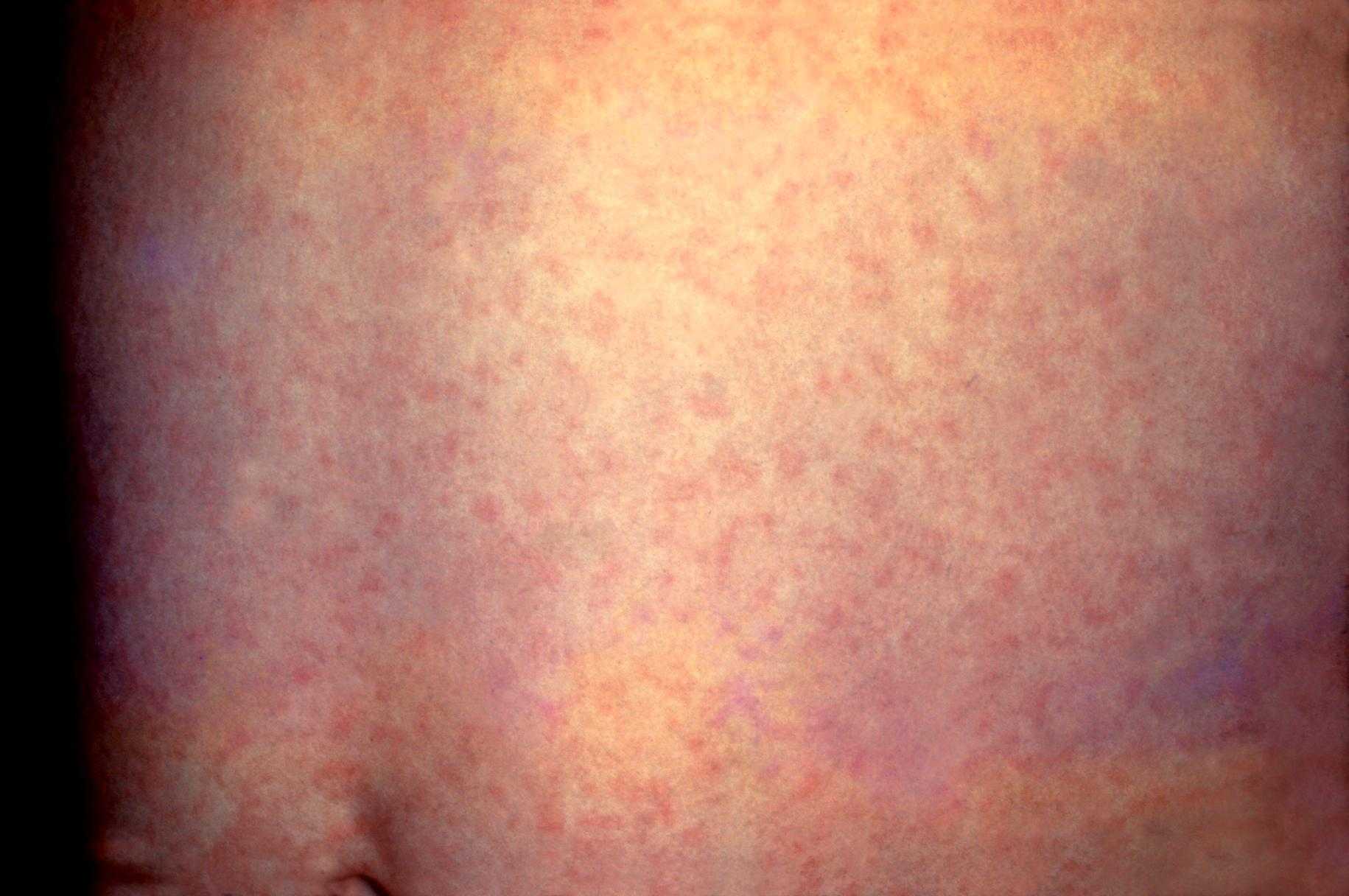
風疹
1970年 風疹の最初のワクチンが開発された。風疹(ふうしん、英: Rubella)とは、ウイルス感染症の一種で、風疹ウイルスによる急性熱性発疹性感染症。一般に日本では「三日はしか」「三日ばしか」としても知られ、英語では「German measles(ドイツはしか)」とも呼ばれている。日本では「風しん」(「疹」が常用漢字に含まれていないため)として、感染症法に基づく五類感染症に指定して届出の対象としている。伝染力は、水痘(水疱瘡)、麻疹(はしか)、ノロウイルス感染症よりは弱いが、インフルエンザより強い。日本ではワクチン接種を受けていない成人男性の患者が多い。効果的な治療法は無く、症状に応じた対症療法が行われる。発症防止策はワクチンによる予防接種のみで、妊娠初期に妊婦が感染した場合の先天性風疹症候群が問題となる。出典: フリー百科事典『ウィキペディア(Wikipedia)』風疹をめぐる旅~消される「子ども」・「笑われる」国~ [ 金子あつし ]
2021.06.17
コメント(0)
-
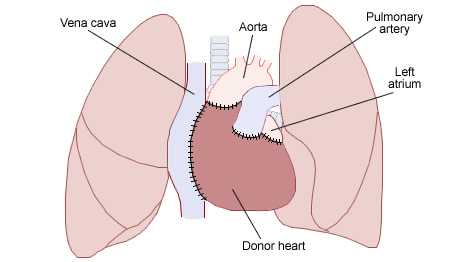
心臓移植
1967年世界初の心臓移植がケープタウンで行われる。心臓移植(しんぞういしょく、英: Heart transplantation)または心移植(しんいしょく)とは、重症心不全など他に代替治療手段の無い末期心疾患に罹患している患者である移植希望者(レシピエント)に対し、脳死状態にある臓器提供者(ドナー)の体から提供された心臓を移植する手術である。レシピエントの心臓を摘出してドナーの心臓を移植する術式(同所性心移植)が一般的であるが、レシピエント心を残し、ドナー心は別の場所に移植する術式(異所性心移植)も存在する。移植後は拒絶反応、感染症を予防するために種々の薬剤を服用する必要があるが、救命と余命の延長、クオリティ・オブ・ライフ(QOL)の向上を図り、最終的に社会復帰が期待できる治療法である。出典: フリー百科事典『ウィキペディア(Wikipedia)』ヒト移植臓器拒絶反応の病理組織診断基準 鑑別診断と生検標本の取扱い(図譜) 腎臓移植,肝臓移植,膵臓移植,心臓移植,および肺移植
2021.06.16
コメント(0)
-
流行性耳下腺炎
1967年流行性耳下腺炎の最初のワクチンが開発された。流行性耳下腺炎(りゅうこうせいじかせんえん、英: Mumps)は、ムンプスウイルスの感染によって発生するウイルス性の感染症。一般にはおたふく風邪として知られる。英語でマムプスといわれる。1967年にワクチンが開発される以前は、小児の疾患として全世界で一般的であり、今日でも開発途上国では脅威となっている。発生に季節性は無く、感染しても症状が出ない不顕感染の場合もある。しかし、一般的に成人が感染すると症状が重い場合が多い。日本では、ワクチン接種が任意となり接種率は約20%から30%とされている。このため初感染が高年齢となり、合併症を伴う成人ムンプスの増加が懸念されている。また、突発性難聴を示した患者の中には、抗ムンプスIgM抗体陽性者があり不顕感染でありながら突発性難聴を生じた可能性が示されている。症状主症状耳下腺の腫れを主症状とする。両側の耳下腺が同時に腫れる場合が多いが、片側の耳下腺だけが腫れる場合、片方の耳下腺が腫れた後にもう一方の耳下腺が腫れてくる場合もある[5]。顎下腺まで腫れる場合もある。顔面の疼痛発症から12 - 24時間以内に唾液腺(耳下腺)の腫脹(60 - 70%で発生)。耳下腺の腫れは3 - 7日でゆっくり消失するが、約10日に及ぶ場合もある。発熱38 - 39℃の発熱が3 - 5日間。発熱を伴わない場合もある。頭痛咽頭痛こめかみや顎の腫脹。但し、約30%の患者ではこの腫脹が認められないとする報告がある。膵炎合併症無菌性髄膜炎10人に1人と合併症としては最多(40%が耳下腺の腫脹無しで発生)。基本的に後遺症はないが稀に髄膜脳炎を伴う(6,000人に1人程度)。難聴(ムンプス難聴)重篤な難治性難聴が後遺症として残ることがある。頻度は教科書的には希もしくは1万5000人に1人程度とされていることが多いが、2004年の報告では高頻度としており、184 - 533人に1人とする調査結果もある。国立感染症研究所は、2001年の1年間の全国のムンプス難聴受療患者数は 650人と推計している。2018年5月に発表された日本の疫学調査では、おたふくかぜにかかった人の282人に1人が合併症で難聴になっており、これまでの報告よりもはるかに高い確率であることが示された。睾丸の痛み、拡大思春期以降に感染した男性の約20%で、精巣炎・副精巣炎。両方の精巣が侵されることは少ないため、不妊症になることもあるが、頻度は高くない。陰嚢腫脹原因原因はパラミクソウイルス科のムンプスウイルスで、飛沫感染、ならびに接触感染により感染する。2歳から12歳の子供への感染が一般的であるが、他の年齢でも感染することもある。通常耳下腺が関わるが、上記年齢層よりも年上の人間が感染した場合、耳下腺、睾丸、卵巣、中枢神経系、膵臓、前立腺、胸等、他の器官も関わることがある。場合によっては、治った後も生殖機能に後遺症が残る。潜伏期間は12-25日、通常は16-18日である。診断身体検査で唾液腺の腫脹を確認する。通常この病気は臨床の根拠で診断され、試験室での確定検査は必要ないが、一般的には血清学的診断を行う。RT‐PCR 法でウイルス遺伝子を検出すれば、ワクチン株と野生株の鑑別ができる。類似の耳下腺炎症状を呈する他感染症は、パラインフルエンザウイルス、コクサッキーウイルスなどによるもので、軽度の痛みの耳下腺腫脹を繰り返し、1 - 2週間で自然に軽快する。『流行性耳下腺炎に何度もかかる』という場合、疑う必要がある(#免疫)。治療流行性耳下腺炎の特異的治療法は存在しない。首やほかの腫脹箇所を冷やしたり暖めたりする対症療法で症状が軽減される場合もある。また、アセトアミノフェンやイブプロフェンを鎮痛のために経口投与する(ライ症候群発症の可能性のため、アスピリンをウイルス性疾患(英語版)を持つ子供には投与しない)。また、暖かい塩水のうがい薬、柔らかい食物、および特別な流動食は、兆候を軽減するかもしれない。発熱による脱水症状を軽減するため水分の摂取を行う。酸味のある果実ジュースは、飲み込む際に耳下腺の痛みを感じさせる場合がある。膵炎により強い吐き気や嘔吐が生じた場合は輸液を行う。予防ワクチン接種幼児期の予防接種が欠かせない全世界105カ国(2004年時点)では、MMRワクチン(麻しん・おたふくかぜ・風しんの混合ワクチン)として定期接種を行っているが、日本では1981年より国産おたふくかぜワクチンが任意の予防接種として使用されていて、MMRワクチン接種の行われた1988年から1993年迄の約5年間を除き、任意接種として単独接種が行われており、一部の自治体では公費助成が行われている。2015年度感染症流行予測調査では、成人の約70~85%が接種歴不明者となっている。国立感染症研究所は、「水ぼうそうやおたふくかぜなどは、大人になってからかかると、重症になることが知られているため、予防接種を受けたことがなく、またかかったこともないのであれば、予防接種を受けておかれると良い」としている。おたふくかぜワクチンの抗体陽転率は、90 - 98%と他のワクチンと比べて低いが、流行時の有効率は星野株で約90%とされている。ワクチン接種後のおたふくかぜ罹患の多くは、二次性ワクチン不全と考えられており、MMRワクチンを接種する国家では2回接種により、二次性ワクチン不全を防いでいる。予防効果ワクチンの2回接種率が高い米国で、2006年1月から年末までに、18 - 24歳の大学生を中心に計6,584人が発症、85人が入院、死亡0人と言う20年ぶりの流行が発生した。疫学的な調査の結果、ワクチン2回接種でも予防効果は不十分である事が示唆された。レポートによれば、18 - 24歳で1,020人中858人(84%)が2回接種を受けていたが発症している。詳細はNEJM誌2008年4月10日号に掲載されている。予後予後は一般的によい。耳下腺の腫脹がなくなれば感染力はなくなる。高度感音性難聴になることがあるが、頻度は1万分の1から数百分の1と、文献により異なる。男性が不妊症になることもある。疫学免疫流行性耳下腺炎はムンプスウイルス感染症であり、基本的に一度かかると免疫ができる。繰り返しているようにみえても、実際には耳下腺炎をおこす他のウイルスや細菌が原因の別の感染症の場合がある。また未だ原因ははっきりしてないが数週間から数年おきに耳下腺の腫脹を繰り返す反復性耳下腺炎の場合もある。以上のように一般に、ワクチン接種や一度野生株に自然感染すると一生有効な免疫を獲得するとされている。しかし、再感染例も報告されている。抗体価の減少による再感染の理由として、かつては周期的な小流行に伴う刺激により抗体価が維持されてきたが、流行による刺激が無くなり徐々に抗体価が下がってきたのではないかと考える専門家もいる。日本日本において、流行性耳下腺炎の予防接種は任意接種である。また、学校保健安全法上の学校感染症に指定されており、感染時は出席停止などの処置が執られる。5類感染症定点把握疾患指定。イタリアイタリアでは、新三種混合ワクチンと自閉症の関連性に関する噂が根強く残り、予防接種を受ける子供が減ったため、2017年より6歳までの子供への接種が義務化された。出典: フリー百科事典『ウィキペディア(Wikipedia)』ワクチン 基礎から臨床まで [ 日本ワクチン学会 ]
2021.06.15
コメント(0)
-

フランク・パントリッジ
1965年 フランク・パントリッジ(Frank Pantridge, 北アイルランド)が、最初の携帯用の細動除去器を導入。出典: フリー百科事典『ウィキペディア(Wikipedia)』AED 自動体外式除細動器【P4倍+10000オフクーポン6月台数限定】日本光電 AED-3100 一式+【8年保証パック】2点セット【価格と実績のAED専門店】【日本製】【AED 60日間返金保証】お見積もり無料【法人様限定 請求書払い対応商品】
2021.06.14
コメント(0)
-
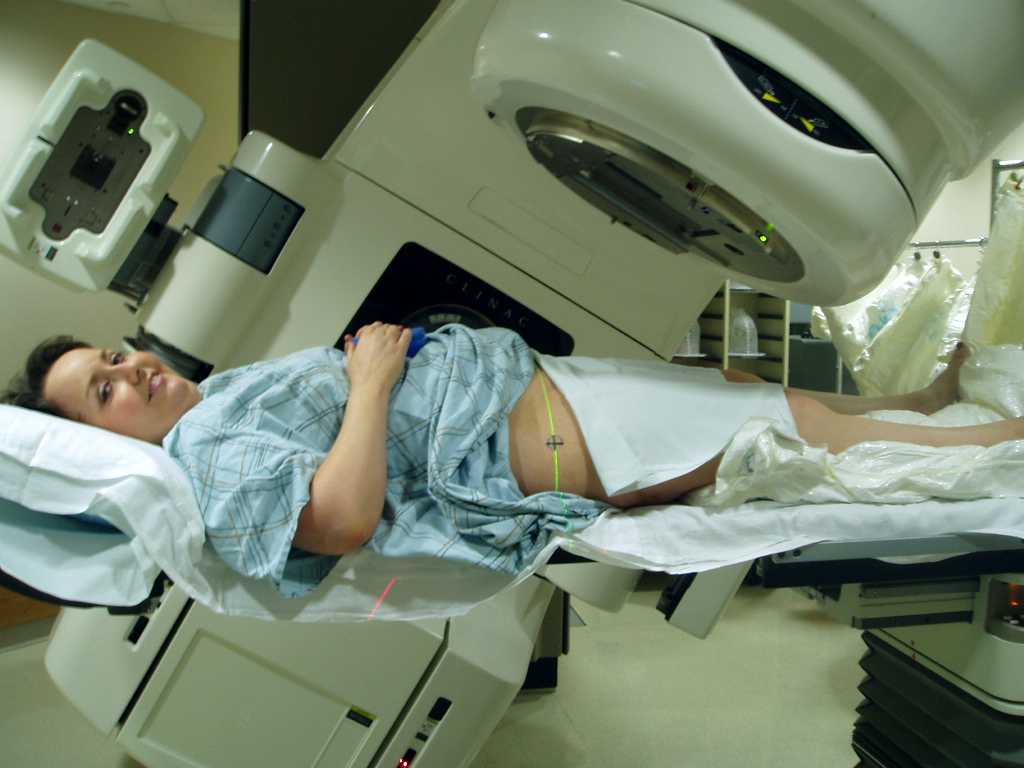
粒子線治療
1964年がんの粒子線治療の試みが始まる。当時は病巣の位置を正確に把握することが困難で、実用化はX線CTが普及してからである。放射線療法(ほうしゃせんりょうほう、英語: radiation therapy / radiotherapy)は、放射線を患部に体外および体内から照射する治療法である。手術、抗がん剤治療とともに、癌(がん)に対する主要な治療法の一つである。概要同じく固形腫瘍の根治療法である外科療法と比較し、放射線療法による治療では、がんが発生した臓器の機能と形態をある程度からほぼ維持することが可能であることが最大のアドバンテージである。とはいえ、これは放射線療法がむやみに危険であることを示すものではなく、放射線療法の有害事象は、実は完全に放射線腫瘍医のさじ加減で、ほとんどゼロにすることもできる。しかし、癌を治すことが目的で治療を行なうのであるから、癌を根治するの確率を上げるため、許容されうる最大の有害事象が起こるだけの大線量を照射しているのが実情であり、上記のように有害事象も憂慮する必要があるのである。日本では癌患者がその生涯で放射線治療を受けるのは4人に1人であり、アメリカでの3人に2人と比べると少ない。放射線療法の歴史は19世紀末のエックス線、ラジウムの発見を始まりとし、抗生物質、抗がん剤の開発および外科手術や麻酔法の確立がなされていなかった当時の癌治療はほとんど放射線療法のみであった。癌治療の目標には根治(完治)、延命、緩和があるが、放射線療法はこの全てに利用される。固形がんを根治させる可能性があるのは手術のほかは放射線療法だけであり、さらに放射線療法は患者の負担が少ない優しい治療法で、耐術能に乏しい高齢者にも適用できる。局所療法のため副作用は比較的少なく、それも大部分は治療後一か月から二か月で自然に治まる。これは、上述のごとく、有害事象を考慮した線量で治療していることと関連が深く、予定調和的な軽度の有害事象とその快癒である。使用される放射線のエネルギーが、正常組織に対して無視できない影響を与えると、後述するように放射線障害と呼ばれる有害事象を起こし、その内容は部位により多彩であるものの、この影響は放射線治療のメリットに比べて十分小さい。繰り返しにあるが、そうなるように放射線治療医が、適切に線量を選択しているのである。放射線療法は、放射線により生物の細胞が死滅する効果を利用しているが、この作用は細胞分裂の盛んな細胞に対して効果が大きく、分裂の盛んながん細胞により大きな影響を与えると経験的に知られ、例外はあるもののベルゴニエー・トリボンドウの法則として知られている。放射線は、がん細胞のみならず正常細胞にも障害を与えるが、がん細胞は放射線による障害からの回復能力が乏しいため放射線療法は分割照射という形式を取ることが多いが、これはある照射から次の照射までに、正常細胞がダメージから回復する時間を与え、ダメージから回復できないがん細胞だけが効果的に死滅させるようにする照射技術である。がん細胞の数が減少すると免疫細胞側が優勢となり、残ったがん細胞すべてを処分することができるようになる。また、ふだんは免疫細胞が見逃しているがん細胞も放射線照射によってその存在が知られ、免疫細胞はがん細胞の場所に移動し、ただちにこれを処分する。照射されているがん細胞ばかりか、遠隔転移しているがん細胞への免疫細胞の攻撃力が高まり、転移巣が治癒することもあり、アブスコパル効果と呼ばれている。出典: フリー百科事典『ウィキペディア(Wikipedia)』【送料無料】 がん・放射線療法 2017 / 大西洋 【本】
2021.06.13
コメント(0)
-
麻疹
1964年麻疹の最初のワクチンが開発された。麻疹(ましん、英: measles, rubeola、痲疹、別名:はしか)とは、麻疹ウイルスによる急性熱性発疹性感染症。中国由来の呼称で、発疹が麻の実のようにみえる。罹患すると、医療が整った先進国であっても死亡することもある。日本では「麻しん」として感染症法に基づく五類感染症に指定して届出の対象としており、疹が常用漢字でないため、平仮名を用いている。江戸時代以降の日本語でははしか(漢字表記は同じく麻疹)と呼ばれる。古くから「はしかのようなもの」の慣用句があり、「一度罹患すると二度はかからないため通過儀礼のようなもの」という意味で2度なし病とも呼ばれたが、麻疹ワクチンが普及した2000年代以降は言われなくなった。麻疹は、麻疹ウイルスによるものであり、その感染力は極めて強く、同じ空間に患者と居るだけで感染してしまい、マスクや手洗いでもウイルス侵入は防げない。感染経路は空気感染、飛沫感染、接触感染と多彩である。麻疹に関して麻疹ワクチンを含んだ予防接種は、効果がある唯一の予防法であり、世界では予防接種の実施により、麻疹による死亡を2000-2013年の間に75%減少させた。世界のおよそ85%の児童は予防接種を受けている。患者に接触してから3日以内であれば、麻疹ワクチンの接種により発病を予防できる可能性があり、患者に接触してから6日以内であれば、ガンマグロブリンの注射により発病を予防できる可能性がある。一度罹患するかワクチンによって抗体価があるうちに感染すると、症状は出ず抗体価が再び上昇するブースター効果がかかる。一方で、現代では抗体価が減少し続けて、麻疹に再感染することがある。ワクチンによる獲得免疫の有効期間は約10年とされるが、ブースター効果による追加免疫が得られないこともある。発病(発症)してからの治療法はなく、対症療法が行われる。先進国における栄養状態の改善、対症療法の発達によって死亡率は0.1-0.2%である。世界の患者数は年間20万人ほどであり、主にアジア・アフリカの途上国である。世界保健機関(WHO)は、2018年の感染者が少なくとも22万9000人おり、未報告分を含めると200万人以上と推計している。持続的な流行が一定期間ない「排除状態」とWHOに認定された国でも、再流行により認定が取り消されることもある。流行株の変異によって、麻疹ワクチンで獲得した抗体での抑制効果が低くなることが懸念されている。定期的に流行しており、江戸時代でも13回の大流行があり、ワクチン時代の2007-2008年に、日本で1万人の罹患者を超える大流行が起きた。出典: フリー百科事典『ウィキペディア(Wikipedia)』ワクチン鎖国ニッポン 世界標準に向けて (学びやぶっく) [ 大西正夫 ]
2021.06.12
コメント(0)
-

チャールズ・ドッター
1964年チャールズ・ドッター、カテーテルを用いた血管内治療を開発する。血管内治療(けっかんないちりょう、Vascular IVR)とは、血管内に挿入した医療機器によって行われる治療である。血管内手術(けっかんないしゅじゅつ、Intravascular surgery)とも呼ばれ、治療に際してカテーテルが多用されるので、俗にカテーテル治療や低侵襲的手術、内科的手術とも呼ばれる。カテーテルは元来画像診断の為に導入された医療機器であったが、今日の血管内治療では画像診断のみならず治療器具としても使用されており、種々の目的や形態を持ったカテーテルが開発されている。沿革カテーテルの導入により選択的血管造影が可能になった。画像診断のために利用したほか、内分泌領域では血管毎に採血をしてホルモン産生腫瘍の部位同定に役立てたり、血液ガス分析にて動静脈短絡(シャント)や心室心房中隔の部位を確定する診断が行われたりするようになった。その後、造影剤だけではなく、抗がん剤や血栓溶解剤の局所投与も可能になった。また、出血が著しいときは、意図的に塞栓を生じさせ血行を遮断する手法も取り入れられた。血管拡張の方法としては、バルーン(風船状の医療機器)を用いる方法があるが、ステントが開発されて以降、ステントにより内腔を保持する方法が主流となった。大動脈解離では挿入したステントで内腔を保持して手術を回避することも可能になった。さらに血管のないところに血管を造ってしまう経頚静脈的肝内門脈肝静脈シャント形成術(TIPS : Transjugular Intrahepatic Portosystemic Shunt)もうまれた。出典: フリー百科事典『ウィキペディア(Wikipedia)』血管内治療のための血管解剖外頚動脈 [ 清末一路 ]
2021.06.11
コメント(0)
-

アリック・アイザックス
1957年アリック・アイザックス(イギリス)ら、インターフェロンを発見・命名。アリック・アイザックス(英: Alick Isaacs、1921年7月17日 - 1967年1月26日)はイギリスのウイルス学者。スコットランド・グラスゴー生まれ。彼はインターフェロンについての研究で最もよく知られていて、1964年から1967年までの間、国立医学研究所(National Institute for Medical Research)のインターフェロン研究所の所長だった。彼は1966年に王立協会の会員に選ばれたのだが、それは彼の死の少し前のことだった。出典: フリー百科事典『ウィキペディア(Wikipedia)』肝臓の病気を治す正しい知識 インターフェロンや抗がん剤が合わない患者さんのための 肝炎から肝硬変、肝がんでも、肝機能を改善する方法
2021.06.10
コメント(0)
-

クロルプロマジン
1952年クロルプロマジンに向精神作用が発見される。精神病院の「閉鎖病棟」を開放する大きな動機づけとなった。クロルプロマジン(英語: Chlorpromazine)は、フランス海軍の外科医、生化学者アンリ・ラボリ (Henri Laborit, 1914-1995) が1952年に発見した、フェノチアジン系の抗精神病薬である。精神安定剤としてはメジャートランキライザーに分類される。メチレンブルー同様、フェノチアジン系の化合物である。塩酸塩が医薬品として承認され利用されている。日本においてクロルプロマジンは劇薬に指定されている。商品名はウインタミン、コントミン。沿革1950年、フランスの製薬会社ローヌ・プーラン(Rhône-Poulenc、現サノフィ・アベンティス)により、抗ヒスタミン薬として開発されたものの、鎮静作用が強すぎる上、抗ヒスタミン作用が少ないと当時は評価された(整理番号は4560RP)。ドパミン遮断剤のほか、古くからヒベルナシオン (hivernation) という麻酔前投与剤として知られていた。1952年2月、外科医であったアンリ・ラボリが、麻酔とクロルプロマジンを併用したところ、精神症状の変化に気づき、精神科治療での有用性を示唆した。同年3月に精神疾患患者でのクロルプロマジンの効果がみられ、その後1年の間にフランス全土で統合失調症に用いられるようになった。翌年にはヨーロッパ全土で用いられるようになった。クロルプロマジンが、薬理作用としてドパミン遮断効果(その作用機序は、脳内の中枢神経系で、興奮や妄想を生み出すと考えられている、神経伝達物質ドパミンのD2受容体の回路を遮断する事にある)を有することは、ラボリの発見まで知られていなかった。約12.5 mg程度で、乗り物酔いの防止効果と悪心の防止効果を生じ、精神神経疾患に対しては、アメリカ合衆国では1日あたりの投与量が 1,000 mg 程度のいわゆる『1キロ投与』が、統合失調症の精神障害者治療に発明当初から広く使用された。ヒベルナシオンとしての麻酔前投与も古くから行なわれ、この用途では前記発明以前から知られていた。日本では、大阪地方裁判所(昭和33年9月11日言渡:判例時報162号23頁)で、クロルプロマジンの被告製法が迂回方法にならない(すなわち非侵害)と判断された。吉富製薬がその迂回発明に拠る製法特許を取得し、市場の西半分はコントミンが占有し販売されている。ノバルティスの輸入品はウインタミン(塩野義製薬取次)の商標を使用している。クロルプロマジンの発明が、統合失調症における薬物治療の幕開けと、精神科病院の閉鎖病棟を開放する、大きな動機づけとなったことは良く知られている。ドパミン遮断薬としては最も歴史が古く、その塩の成分により、前者の迂回発明による吉富製薬迂回製法によるクロルプロマジン剤と、塩野義製薬の正規輸入クロルプロマジン剤とで多少の差異があるものの、薬効には差異はみられない。なお、吉富製薬(現「田辺三菱製薬」)は、この当事者系特許侵害訴訟(塩野義製薬が原告で請求棄却)に勝訴し、日本でのクロルプロマジンの市場を寡占状態近くにまで伸ばし、旧来の一流製薬企業に比肩することになった。塩野義製薬は、1957年にクロルプロマジンとフェノバルビタール、プロメタジンを含む、処方箋医薬品の合剤『ベゲタミン』を発売した。赤玉、白玉の名で知られたが、強力な副作用やオーバードースが問題視されて、2016年12月に発売を終了した。適応統合失調症・躁病・神経症における不安・緊張・抑うつ悪心・嘔吐・吃逆・破傷風に伴う痙攣麻酔前投薬・人工冬眠催眠・鎮静・鎮痛剤の効力増強基本的な注意点重要な副作用は、パーキンソン症候群である。初期は手がふるえ、綺麗な文字が筆記できなくなり(くずしたような文字になる)、痙攣(振戦)が生じ、横隔膜の痙攣(しゃっくり)なども生ずることが報告されている。美容上では色素沈着などが生じ、その結果そばかす状の汚点などが生じる。眼科では網膜に色素沈着が生ずることも知られている。抗パーキンソン薬(ビペリデン「biperiden」、商標:アキネトン、タスモリン、ビカモール)をクロルプロマジンと同時に投与(1mg/日、から3-6mg/日)する方法で前記の「パーキンソン症候群」を防止することができるが、最悪は「遅発性ジスキネジア」のビペリデンのリバウンドを防ぐことができないので、「抗パーキンソン薬」を安易に投与せず、1日の投薬量を600mg以下の適量まで減薬し、パーキンソン症候群のリバウンドを生じさせない処方への切り替えが呼びかけられている。副作用クロルプロマジンの使用で、特に頻繁に遭遇する副作用は以下の通りである。循環器(血圧降下、頻脈、不整脈、心疾患悪化)血液(白血球減少症、顆粒球減少症、血小板減少性紫斑病)消化器(食欲亢進、食欲不振、舌苔、悪心・嘔吐、下痢、便秘)内分泌(体重増加、女性化乳房、乳汁分泌、月経異常、糖尿)精神神経系(錯乱、不眠、眩暈、頭痛、不安、興奮、易刺激、痙攣)錐体外路症状(パーキンソン症候群、ジスキネジア、ジストニア、アカシジア)クロルプロマジンの本来の作用と反対の効果、つまり、易興奮性、筋痙攣等が見られることがあるかもしれない。これを「奇異反応」という。こうした反応があった場合、上記のような副作用が現れた場合には、減量または投与を中止すること。外来患者にクロルプロマジンを処方する場合、眠気・注意力・集中力・反射運動能力などの低下が起こることがあるので、投与中の患者には、自動車の運転など危険を伴う機械の操作に従事させないように注意すること。制吐作用を有するため、他の薬剤に基づく中毒、腸閉塞、脳腫瘍などによる嘔吐症状を不顕性化することがある。抗精神病薬において、肺塞栓症、静脈血栓症等の血栓塞栓症が報告されているので、不動状態・長期臥床・肥満・脱水状態などの危険因子を有する患者に投与する場合には注意が必要である。睡眠時無呼吸発作を有する患者には、呼吸抑制作用によって呼吸停止と死を招く可能性がある。重大な副作用ほとんどが頻度不明となっているが、報告されている重大な副作用は以下の通り。悪性症候群、遅発性ジスキネジア、遅発性ジストニア、SLE様症状横紋筋融解症、麻痺性イレウス、抗利尿ホルモン不適合分泌症候群(SIADH)突然死、心室頻拍、肝機能障害、黄疸肺塞栓症、深部静脈血栓症、再生不良性貧血、溶血性貧血、無顆粒球症、白血球減少眼色素沈着過量摂取クロルプロマジンをオーバードースした人は、傾眠から昏睡までの中枢神経系の抑制、血圧低下と錐体外路症状等の徴候を示す。その他には、激昂と情緒不安、痙攣、口渇、腸閉塞、心電図変化および不整脈などがあらわれる可能性がある。クロルプロマジンの過量摂取は、医学的な緊急事態であり、救急医学関係者による迅速な処置が必要である。処置としては、本質的には対症療法かつ補助療法である。早期の胃洗浄は、有効であることが認められている。なおクロルプロマジンは、血中半減期が長いため、対症療法を続けながらの経過観察が必要である。酒や中枢神経抑制剤との併用は、致死的となる恐れがある。相互作用クロルプロマジンを他の薬剤と併用投与する場合、薬理学的な相互作用の可能性に注意を払わなければならない。とりわけバルビツール酸塩・フェノチアジン・麻薬・アルコールなどのクロルプロマジンの効果を高める薬には注意が必要である。禁忌クロルプロマジンの禁忌には以下のようなものがある。絶対禁忌アドレナリンを投与中昏睡状態,循環虚脱状態フェノチアジン系化合物およびその類似化合物に対し過敏症、アレルギーバルビツール酸誘導体・麻酔剤等の中枢神経抑制剤の強い影響下にある場合皮質下部の脳障害(脳炎,脳腫瘍,頭部外傷後遺症等)の疑いがある併用禁忌アドレナリンアドレナリンの強心作用を逆転させ、重篤な低血圧発作を引き起こすことがある。アドレナリンはアドレナリン作動性α・β-受容体の両方を作用し効用を発揮するが、クロルプロマジンにはα-受容体遮断作用があり、アドレナリンのβ-受容体への作用が優位となり、重篤な低血圧発作を引き起こすことがある。慎重投与肝障害または血液障害褐色細胞腫、動脈硬化症あるいは心疾患の疑い重症喘息、肺気腫、呼吸器感染症等てんかん等の痙攣性疾患またはこれらの既往歴高温環境にある者脱水・栄養不良状態等を伴う身体的疲弊幼児、小児 - 処方は、痙攣の治療、および鎮静を除いては通常指示されない。妊婦、産婦、授乳婦等への投与クロルプロマジンのアメリカ合衆国アメリカ食品医薬品局 (FDA)・胎児危険度分類 (pregnancy category) はカテゴリー「C」である。これは、動物実験では胎児への有害作用が証明されているが、その薬物の潜在的な利益によって、潜在的なリスクがあるにもかかわらず妊婦への使用が正当化されることがありうることを意味する。しかし動物実験では、胎児死亡、流産、早産等の胎児毒性が報告されている。また、妊娠後期に抗精神病薬が投与されている場合、新生児に哺乳障害、傾眠、呼吸障害、振戦、筋緊張低下、易刺激性等の離脱症状や錐体外路症状があらわれたとの報告がある。なお、クロルプロマジンは母乳中へ移行することが報告されているため、授乳中の婦人には投与しないことが望ましいとされる。出典: フリー百科事典『ウィキペディア(Wikipedia)』精神科治療学 34巻12号〈特集〉抗てんかん薬の持つさまざまな向精神作用 [雑誌]
2021.06.09
コメント(0)
-

ペル・イングヴァール・ブローネマルク
1952年ペル・イングヴァール・ブローネマルクによって、チタンが骨と結合することが発見される。ペル・イングヴァール・ブローネマルク(Per-Ingvar Brånemark [pɛːr iŋgvar broːnəmark] 1929年5月3日 - 2014年12月20日)はスウェーデンの整形外科医、医学者、歯学者。デンタルインプラントにブレークスルーを起こしたオッセオインテグレーションの発見者であり、世界的に著名なデンタルインプラントシステムであるブローネマルクインプラントシステムの開発者。『現代の父』と呼ばれる。エピテーゼの研究者でもある。来歴・人物スウェーデンのルンド大学医学部で1952年、ウサギの脛にチタン製の生体顕微鏡を取り付け微少循環の観察実験を行っていた。その器具を外そうとした際チタンと骨がくっつき外せなくなったことより、チタンと骨の組織が拒否反応を起こさず結合する現象であるオッセオインテグレーションを発見した。その後ヨーテボリ大学に移籍し、研究を続け1965年に現在主流となる世界初の純チタンによるデンタルインプラントシステムの臨床応用を開始。最初の患者は先天性歯牙欠損に悩むヨスタ・ラーソンという名前の34歳の男性で、彼は上下顎にデンタルインプラント手術を行い、そのインプラントはその後彼が亡くなるまで41年間問題なく機能した。1989年にはオッセオインテグレーション技術の普及のため、スウェーデンのヨーテボリにブローネマルク・オッセオインテグレーション・センター(BOC)を設立。BOCはその後ブラジル、東京など世界9ヵ国に設立され現在に至る。現在はブラジルサンパウロ州バウルーに在住し、デンタルインプラントの治療、指導を行っている。近年はインプラントを使って固定したエピテーゼの研究も行っており、それに関した著書も多数執筆している。上記の業績に対し、数々の賞を受けている。1992年にミニノーベル賞とも呼ばれる、『the Swedish Engineering Academy's equally prestigious medal for technical innovation』を受賞[4]。また、ハーバード歯科医学校よりアメリカ合衆国におけるデンタルインプラントの業績に対し表彰され、生前はヨーロッパと北米で30以上の名誉職についていた。息子のリカードも外科医であり人工関節付きの義足、指の再建の等の研究を行っている。出典: フリー百科事典『ウィキペディア(Wikipedia)』インプラントの潮流を考える オッセオインテグレイション・スタディクラブ・オブ・ (クインテッセンス デンタル インプラントロジー 別冊) [ 岡田隆夫 ]
2021.06.08
コメント(0)
-

ジョナス・ソーク
1952年ジョナス・ソークが、最初の小児麻痺(ポリオ)ワクチンを開発。ジョナス・ソーク(Jonas Salk /sɔːlk/、本名:Jonas Edward Salk、1914年10月28日 - 1995年6月23日)は、アメリカ合衆国の医学者。ポリオワクチンを開発した。ポリオワクチンの開発に際しては安全で効果的なものをできるだけ早く開発することだけに集中し、個人的な利益は一切求めなかった。テレビのインタビューで「誰がこのワクチンの特許を保有しているのか」と聞かれたのに対して「特許は存在しない。太陽に特許は存在しないでしょう。」と述べた。略歴1914年、ニューヨーク州ニューヨークにて、貧困のロシア系ユダヤ人家庭に生まれる。ニューヨーク市立大学シティカレッジ卒業後、1939年にニューヨーク大学から医学博士号を取得。ニューヨークのMount Sinai School of Medicineで勤務の後、1947年にピッツバーグ大学に移る。1950年代に、初めてポリオワクチンのテストに成功する。1962年、カリフォルニア州ラホヤにソーク研究所を創設し、分子生物学と遺伝学の研究所として世界的に知られるようになり、この研究所から数多くのノーベル賞学者を輩出した。日本ではポリオワクチンにより、1960年代に年間5000人ほどいた患者が激減した結果、1980年の1人を最後に野生ポリオウイルスによる発症は1件も報告されていない。また、2012年時点で世界的にもほぼ根絶され、現在の常在国はナイジェリア、パキスタン、アフガニスタンの3か国のみとなった。2014年10月28日には生誕100周年を迎え、Googleのトップページがソークを称える特別なロゴになった。出典: フリー百科事典『ウィキペディア(Wikipedia)』夢ありき。 Dream Big Dreams! 脳性小児麻痺の息子あっての人生ドラマ
2021.06.07
コメント(0)
-

ジョージ・オットー・ゲイ
1951年ジョージ・オットー・ゲイにより、ヒト由来の最初の細胞株であるHeLa細胞が培養される。この細胞のドナーであるヘンリエッタ・ラックスが死亡。ジョージ・オットー・ゲイ(George Otto Gey、1899年7月6日-1970年11月8日)は、HeLa細胞の株を確立したことで知られるアメリカ合衆国の生物学者である。伝記ゲイはペンシルベニア州で生まれた。両親はドイツ出身である。1921年にピッツバーグ大学で学士号を取り、ここで動物学を教えた。1926年頃、彼はウィスコンシン州出身のマーガレット・K(1900年-1989年)と結婚した。1930年までに、彼らはボルチモアのセントポールストリートに転居し、1950年代中頃に彼らは、ジョンズホプキンス大学で組織培養研究所を始めた。ハワード・ジョーンズ博士から提供されたヘンリエッタ・ラックスの子宮頸部の細胞のサンプルを用いて、不滅のヒト細胞株を確立した。ゲイは、ローラードラムの開発者でもある。この機械は、細胞培養を育てるのを助ける最初の機械の1つである。ローラードラムは、様々な組織とその適切な生育基質が配置される複数の穴から構成される。ドラムは、基質を攪拌し、また1時間に1度、培養物を環境に晒すために回転する。ゲイはさらに、細胞の分裂と成長を最初にフィルムに収めた人物の1人でもある。彼は、温度制御インキュベーター付きの低速度撮影カメラを考案した。ゲイは、膵臓癌で死去した。彼の癌の緊急処置を行っている際、医師は、癌がリンパ節、肺、心臓にも転移していることを発見し、治療は不可能であった。ゲイは、肝臓から癌の切片を切り出して、研究用の細胞株とすることを望んだ。しかし医師は彼の要望を聞き入れず、ゲイは手術後に目覚めた時に激怒した。出典: フリー百科事典『ウィキペディア(Wikipedia)』目的別で選べる細胞培養プロトコール 培養操作に磨きをかける!基本の細胞株・ES・iPS細胞の知っておくべき性質から品質検査まで/中村幸夫【1000円以上送料無料】
2021.06.06
コメント(0)
-

ガイ・ヘンリィ・ファジェット
1943年ガイ・ヘンリィ・ファジェットはスルフォン剤のプロミンがハンセン病に有効なことを発表した。その後、スルフォン剤の開発が進んだ。ガイ・ヘンリィ・ファジェット (Guy Henry Faget, 1891年 - 1947年) は、アメリカの医師。世界で初めてハンセン病の薬・プロミンの有効性を発見し (1943年)、サルファ剤合成品の開発など、医学に革命的貢献をした。名前の発音ファジェットの発音以外にフランス語流にファジェと記載した文献もあるが、ここではファジェットと記載する。生涯22歳より、米国公衆衛生の医師として活躍。1940年に海軍のハンセン病療養所カーヴィルの病院長。結核の薬で副作用が多く人間には使用されていなかったsulfanilamide、prominを研究し、前者では少々有効性があったが、まだ使用不可のという成績であったが(1942)、後者では明瞭な有効性を認め発表した。(1943)その後いくつかの薬を検討している。1946年リオデジャネイロで開かれた汎アメリカらい会議でスルフォン剤の顕著な効果を発表。1947年7月17日、心臓病を患ったが、直接的には新しい職場の開いた窓の下で死亡しているのを発見された。死後1958年の東京の第7回国際らい学会、1994年のカーヴィルの100年祭で表彰されている。Sulfanilamideの有効性1942年に発表した論文である。20例のうち6例有効、2例も有効であったが、これは改善中の患者であった。1例は不変。10例は進行(無効)、1例は別の病気で死亡。しかし副作用が強く、らい腫型にも斑紋型にも使えないと言明している。らいのpromin治療原著によると、副作用を慎重に検討し、尿と血液を頻繁に検査すれば使用可能と断定している。22例中有効15例(68%),不変6例(27%),悪化1例(5%),菌陰性化5例(23%)。印象深い改善前後の写真を掲載している。最初に使われたのは1941年3月10日、彼のゴーサインで、フランク、マクリアリー医師が6人の被験者希望者にプロミンを注射した。ゆっくりながら劇的な効果が現れた。出典: フリー百科事典『ウィキペディア(Wikipedia)』ハンセン病の社会史 日本「近代」の解体のために [ 田中 等 ]
2021.06.05
コメント(0)
-
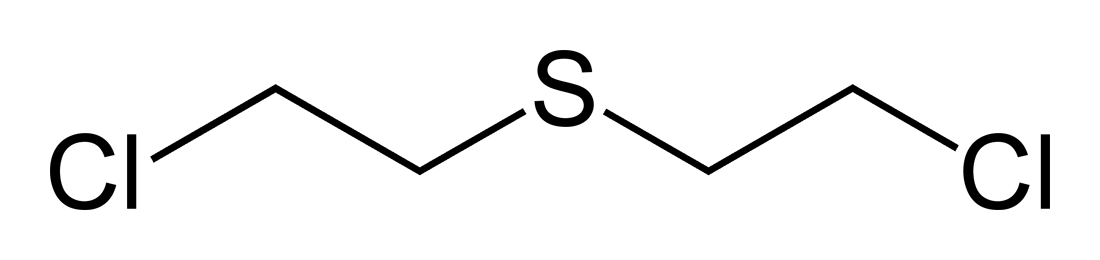
ナイトロジェンマスタード
1942年 マスタードガスの誘導体であるナイトロジェンマスタードが、悪性リンパ腫に有効であることが示され、抗癌剤の第1号となった。マスタードガス(Mustard gas)は、化学兵器のひとつ。2,2'-硫化ジクロロジエチル(2,2'-Dichloro Diethyl Sulfide)という化合物を主成分とする。びらん剤(皮膚をただれさせる薬品)に分類される。硫黄を含むことから、サルファマスタード(Sulfur mustard gas)とも呼ばれる。概要主にチオジグリコールを塩素化することによって製造される。また、二塩化硫黄とエチレンの反応によっても生成される。純粋なマスタードガスは、常温で無色・無臭であり、粘着性の液体である。不純物を含むマスタードガスは、マスタード(洋からし)、ニンニクもしくはホースラディッシュ(セイヨウワサビ)に似た臭気を持ち、これが名前の由来である。他にも、不純物を含んだマスタードガスは黄色や黄土色といった色がついているために、マスタードの名が付けられたという説や、さらに皮膚につくと傷口にマスタードをすりこまれるぐらいの痛さという説もある。第一次世界大戦のイープル戦線で初めて使われたため、イペリット(Yperite)とも呼ばれる。実戦での特徴的な点として、残留性および浸透性が高いことが挙げられる。特にゴムを浸透することが特徴的で、ゴム引き布を用いた防護衣では十分な防御が不可能である。またマスクも対応品が必要である。気化したものは空気よりもかなり重く、低所に停滞する。マスタードガスは遅効性であり、被害を受けても気づくのが遅れる。皮膚以外にも消化管や、造血器に障害を起こすことが知られていた。この造血器に対する作用を応用し、マスタードガスの誘導体であるナイトロジェンマスタードは抗がん剤(悪性リンパ腫に対して)として使用される。ナイトロジェンマスタードの抗がん剤としての研究は、第二次世界大戦中にアメリカ合衆国で行われていた。しかし、化学兵器の研究自体が軍事機密であったことから、戦争終結後の1946年まで公表されなかった。一説には、この研究は試作品のナイトロジェンマスタードを用いた人体実験の際、白血病改善の著効があったためという。人体への作用マスタードガスは人体を構成する蛋白質やDNAに対して強く作用することが知られており、蛋白質やDNAの窒素と反応し(アルキル化反応)、その構造を変性させたり、DNAのアルキル化により遺伝子を傷つけたりすることで毒性を発揮する。このため、皮膚や粘膜などを冒すほか、細胞分裂の阻害を引き起こし、さらに発ガンに関連する遺伝子を傷つければガンを発症する恐れがあり、発癌性を持つ。また、抗がん剤と同様の作用機序であるため、造血器や腸粘膜にも影響が出やすい。人体への影響は非常に長く続く。イラン・イラク戦争でマスタード・ガスの被害に遭った民間人は、30年以上経過してもなお後遺症に悩まされている。歴史1859年、ドイツの化学者アルベルト・ニーマンにより初めて合成。彼は皮膚への毒性を報告するが、2年後に中毒が原因と思われる肺疾患により死去。翌1860年にはイギリスのフレデリック・ガスリーも合成して毒性を報告している。1886年、ドイツの研究者ヴィクトル・マイヤーが農薬開発の過程で合成法を完成。彼はその毒性に手こずり、実験を放棄。1917年7月12日、第一次世界大戦中にドイツ軍がカナダ軍に対して実戦で初めて使用し、約3500人の中毒者のうち89人が死亡。その後、同盟国・連合国の両陣営が実戦使用した。大戦中のドイツ・フランス・イギリス・アメリカの4ヶ国での生産量は計1万1千tに及んだ。1943年12月、イタリア南部のバリ港にて、アメリカの貨物船「ジョン・ハーヴェイ号」がドイツ空軍の爆撃を受け、大量のマスタードガスが流出し、アメリカ軍兵士と一般市民617名が負傷、83名が死亡した(ジョン・ハーヴェイ号事件)。旧日本陸軍も「きい剤」の名称で、マスタード-ルイサイトを保有していた。イラン・イラク戦争時、イラク軍はイラン軍および自国のクルド人に対し、マスタードガス、サリン、タブンを使用したと言われる(ただし異説あり)。このうちクルド人に対して行なわれたものを、事件の起こった町の名を取って「ハラブジャ事件」と呼ぶ。出典: フリー百科事典『ウィキペディア(Wikipedia)』抗がん剤10の「やめどき」【電子書籍】[ 長尾和宏 ]
2021.06.04
コメント(0)
-

エガス・モニス
1936年エガス・モニスが、精神病治療にロボトミー手術を提唱した。エガス・モニス(António Caetano de Abreu Freire Egas Moniz, 1874年11月29日 - 1955年12月13日)は、ポルトガルの政治家、医者(神経科医)である。ロボトミーという名前で良く知られる精神外科手術、前頭葉切断手術を精神疾患を根本的に治療する目的で考案した。これが功績として認められ、1949年にスイスの神経生理学者ヴァルター・ルドルフ・ヘスとともにノーベル生理学・医学賞を受賞した。受賞の理由は「ある種の精神病に対する前頭葉白質切截術の治療的価値に関する発見」である。人物・生涯ポルトガル中部大西洋岸のアヴェイロ県エスタレージャ北郊のアヴァンカに生まれた。モニスは医学を故郷に近いコインブラ大学で学び、神経学をフランスのボルドーとパリで学んだ。1902年コインブラ大学に神経学科の主任教授として戻る。リスボン大学教授となり、20年以上務めた。その間、政治の世界に入る。政治家としてはポルトガルの国会議員を1903年から1917年の間務め、1917年外務大臣となる。1918年から1919年まで第一次世界大戦後に開かれたパリ講和会議の首席代表となった。スペイン大使を1917年から1919年まで(第一次共和制)務める。その後、政治家を辞めて、1944年までの間はリスボン大学で神経学の教授となる。その間、1927年にX線を利用した脳血管造影法を開発する。像の陰影で脳の腫瘍や動静脈奇形などの神経性の病気の原因を診断する方法を考案する。ロボトミー (Lobotomy)1936年、モニスと同僚のアルメイダ・リマ (Almeida Lima) は、当時すでに知覚を脳に伝える部分として知られていた視床と、知性と感情をつかさどる部分とされていた皮質に繋がる神経繊維を、外科手術で切断することに世界で初めて成功する。この手術は、それから10年程で世界で広く行なわれるようになった。モニスの方法をアメリカ合衆国のウォルター・フリーマンとジェームス・W・ワッツ(英語版)が改良し、前部前頭葉白質切截法(ロボトミー)として確立した。それによりモニスは世界で広く知られ、名声はノーベル医学賞受賞という形で最高潮に達する。65歳のとき、自分の患者に銃撃されて脊髄を損傷し、身体障害者になった。1955年、ポルトガルのリスボンで死去した。81歳没。ロボトミーは、主に統合失調症の治療に用いられたが、患者から人間性を不可逆的に奪う深刻な副作用が問題視されて、1975年頃にはまったく行なわれなくなった。現在では悪評の高い手術となっており、薬物療法が一般的となっている。アメリカ合衆国などでは、現在でもロボトミー手術の被害で廃人になった当事者と、その家族たちが、エガス・モニスのノーベル生理学・医学賞受賞取り消しのための運動を行っている。出典: フリー百科事典『ウィキペディア(Wikipedia)』精神科医は腹の底で何を考えているか【電子書籍】[ 春日武彦 ]
2021.06.02
コメント(0)
-
黄熱病
1935年黄熱病の最初のワクチンが開発された。黄熱(おうねつ、英: yellow fever)は、ネッタイシマカ (Aedes aegypti) などのカ(蚊)によって媒介されるフラビウイルス科フラビウイルス属に属する黄熱ウイルスを病原体とする感染症。ウイルス性出血熱のひとつ。感染症法における四類感染症。黄熱病と同義。発熱を伴い、重症患者に黄疸が見られることから命名された。熱帯アフリカと中南米の風土病である。黒色嘔吐(吐血)を起こすことから通称を「黒吐病」という。日常生活におけるヒトからヒトへの直接感染はない。症状潜伏期間は3 - 6日で、突然の発熱、頭痛、背部痛、虚脱、悪心・嘔吐、下痢で発症する。発症後3 - 4日で症状が軽快し、そのまま回復することもある。しかし、重症例では、数時間から2日後に再燃し、出血熱を引き起こす。発熱(高熱)、腎障害、鼻や歯根からの出血、黒色嘔吐(吐血)、血便(下血)を伴う下痢、子宮出血、黄疸(肝障害)などがみられる。黄熱病の死亡率は、30 - 50%とされている。これはエボラ出血熱に匹敵し、非常に危険な感染症である。治療罹患した場合の特効薬は無い。対症療法にて投薬治療する方法しかない。なお罹患前であれば、1回接種の黄熱ワクチン (17D) の予防接種を受けることで予防可能。疫学感染する可能性がある国、地域アフリカ(五十音順):アンゴラ、ウガンダ、エチオピア、カメルーン、ガーナ、ガボン、ガンビア、ギニア、ギニアビサウ、ケニア、コンゴ共和国、コンゴ民主共和国、コートジボワール、シエラレオネ、スーダン、セネガル、赤道ギニア、中央アフリカ、チャド、トーゴ、ナイジェリア、ニジェール、ブルキナファソ、ブルンジ、ベナン、マリ、南スーダン、リベリア、モーリタニア 。アメリカ(五十音順):アルゼンチン、エクアドル、ガイアナ、コロンビア、スリナム、パナマ、フランス領ギアナ、ブラジル、ペルー、ベネズエラ、ボリビア、トリニダード・トバゴ(トリニダード島のみ)、パラグアイ 。なお同じく、蚊が媒介するデング熱とは異なり、アジアでの発生は見られない。予防接種流行地域や流行可能地域は、出入国管理に際して国家機関発行による国際予防接種証明書(イエローカード)が求められる。かつて、イエローカードの有効期間は、接種10日後から10年間とされてきたが、世界保健機関は、2016年7月11日より、生涯有効に延長することを勧告した。これに伴い、日本で発行される黄熱予防接種証明書の有効期間も、1回の接種で生涯有効となった[3]。なお2016年(平成28年)7月11日の時点で、既に有効期限が切れているイエローカードも有効として取り扱われる。日本では、イエローカードの発行権限の関係から、検疫所、日本検疫衛生協会及び厚生労働省から指定を受けた医療機関(国立国際医療研究センター等)でのみ予防接種を受けられる。日本で薬事承認を受けているワクチン(YF-VAX)は、発育鶏卵に接種して作られている。このため、接種予定者が卵アレルギーであれば、予防接種を受けることが出来ないが、代替処置として禁忌証明書が発行される。なお、イエローカードとは異なり、入国の際、禁忌証明書を提示しても上陸拒否を受ける場合がある。研究キューバで開業した医師カルロス・フィンレーは蚊による媒介と伝染を提唱している。このような蚊を媒介と想定したモスキート仮説は研究初期から存在したが、当時は人から人へ伝染るものとする論者も多かった。1900年、アメリカ軍の軍医だったウォルター・リードは、モスキート仮説に立った実証実験のためにキューバに医師団を派遣した[5]。最初は参加した医師や軍人で蚊を使った媒介実験を行ったが、死亡者が続出したため、スペイン系移民労働者に謝礼金と医療補償を与える条件で実験を継続し、モスキート仮説は証明された。リードの行った集団実験は、自分の意志で参加した被験者と、契約の上で行われた史上初の人体実験の例とされている。その後、パナマ運河建設に際し、蚊の駆除を中心とした防疫対策を行い効果を挙げたことから、フィンレーの蚊媒介説の正しさが証明された。更に、野口英世によって黄熱の研究が手がけられるものの、その中途で感染し死亡した。その後、南アフリカ出身でアメリカ合衆国の微生物学者マックス・タイラー(Max Theiler、サイラーとも)が黄熱ワクチンを開発。このワクチン開発の功績によりタイラーは、1951年にノーベル医学生理学賞を受賞した。出典: フリー百科事典『ウィキペディア(Wikipedia)』イエロー・ジャック(黄熱病)[本/雑誌] (単行本・ムック) / 三瓶眞弘/著
2021.06.01
コメント(0)
-

ウェンデル・スタンリー
1935年ウェンデル・スタンリーがタバコモザイクウイルスの結晶化に成功した。ウェンデル・メレディス・スタンリー(Wendell Meredith Stanley, 1904年8月16日 – 1971年6月15日)はアメリカ合衆国の生化学者、ウイルス学者。初めてウイルスを分離・結晶化したことで知られ、1946年のノーベル化学賞受賞者。経歴インディアナ州リッジヴィル出身。アーラム・カレッジ(英語版)で学士号を取得し、1927年にはイリノイ大学で修士号を得る。1929年には化学分野で博士号を取得した。この年に彼は結婚している。その後1931年まで米国学術研究会議の一員としてミュンヘンで過ごした。帰国後ロックフェラー研究所の助手となり、1948年までその地位にあった。後にカリフォルニア大学バークレー校で生化学の教授となり、1958年には生化学部の部長となった。彼の業績にはビフェニルの立体化学やステロールの化学があげられるが、最も重要なものとして、タバコモザイクウイルスの単離、結晶化が挙げられる。この結果により、ウイルスはたんぱく質と核酸のみからできているということが判明した。数グラムのタバコモザイクウイルスを得るために要したタバコの葉は数トンであったといわれる。ノーベル賞以外にも多くの賞を受け、パリ大学やハーバード大学、プリンストン大学あるいはイェール大学から名誉職に任ぜられた。カリフォルニア大学バークレー校には彼の名にちなんだスタンリーホールがある。スペインのサラマンカで客死した。出典: フリー百科事典『ウィキペディア(Wikipedia)』京大おどろきのウイルス学講義/宮沢孝幸【1000円以上送料無料】
2021.05.31
コメント(0)
-

ゲルハルト・ドーマク
1932年 ゲルハルト・ドーマクが、連鎖球菌に対する化学療法を発見。ゲルハルト・ドーマク(Gerhard Domagk, 1895年10月30日 - 1964年4月24日)は、ドイツの病理学者、細菌学者の医師。1939年にノーベル生理学・医学賞を受賞した。しかしながら、ナチス・ドイツ政権によりドイツ人の入賞が禁じられていたため辞退した。1947年、第二次世界大戦後にあらためて受賞した。生涯ドイツ帝国東部ラゴウ(現在のポーランドルブシュ県ワグフ)に生まれる。1913年ユトランド半島にあるキール大学に入学するが、第一次世界大戦開戦により、従軍する。1915年に負傷し、学業に戻る。1921年に卒業し、医学博士号を取得後、1924年にグライフスヴァルト大学の病理学講師となる。1925年にはミュンスター大学病理学講師に代わる。1927年デュッセルドルフにあったIG・ファルベン社の実験病理学細菌学研究所の実験病理学と細菌学の研究主任を大学と兼任する。1928年にはミュンスター大学一般病理学・病理解剖学特任教授となる。そして1939年、プロントジルに化学抗菌作用が存在することを発見したという理由でノーベル生理学・医学賞を受賞する。1956年パウル・エールリヒ&ルートヴィヒ・ダルムシュテッター賞受賞。1958年にミュンスター大学一般病理学・病理解剖学教授となり、1959年にはロンドン王立協会外国人会員に選ばれた。ドーマクの発見は1927年にIG・ファルベン社における研究から始まった。同社は細菌の化学療法に利用できる薬剤の開発をねらっており、ドーマクにすべてがまかされた。1932年、赤色アゾ染料の一種、赤色プロントジルを調べたところ、レンサ球菌に感染したマウスを治療できた。レンサ球菌による感染症は重篤なものも多く、ヒトに対して効果があれば貴重な薬品となる。このとき、ドーマクの娘がレンサ球菌感染症に罹患し、他の治療がすべて効果を発揮しない段階に至って赤色プロントジルを投与したところ完治した。1935年、服用量などを確認後、赤色プロントジルが世界初のサルファ剤系合成抗菌薬として発表された。これを受けて、官能基などを置換し、より安価で安全な数千種にも及ぶサルファ剤誘導体が生まれた。これにより肺炎などを起こす細菌の他、真菌・原虫などのさまざまな微生物感染症に対する有力な武器が手に入ったことになる。1951年、抗結核性のイソニアジド(イソニコチン酸ヒドラジド)を発見し、ストレプトマイシンとの併用により結核に対して高い効果を発揮した。チオセミカルバジドも彼が開発した結核の化学療法薬である。1964年、バーデン=ヴュルテンベルク州ケーニヒスフェルトで没した。出典: フリー百科事典『ウィキペディア(Wikipedia)』【送料無料】 サルファ剤、忘れられた奇跡 世界を変えたナチスの薬と医師ゲルハルト・ドーマクの物語 / トーマス・ヘイガー 【本】
2021.05.30
コメント(0)
-

ハンス・ベルガー
1929年 ハンス・ベルガーが人の脳波診断(electroencephalography)を確立した。ハンス・ベルガー(Hans Berger, 1873年5月21日 - 1941年6月1日)は、ドイツの神経科学者、精神科医。生涯テューリンゲン州コーブルク近郊のノイゼスに生まれ、当初は天文学を志していた。1890年代はじめにドイツ軍で働いていた折、乗っていた馬が堤防を転げ落ち、騎砲の車輪に轢き殺されそうになるという出来事があった。この時、彼の姉[1]ははるか離れた土地にいたにもかかわらずベルガーの危険を感じ取り、父に頼んで電報を打たせた。この出来事はベルガーを非常に驚かせ、心理学へと転向するきっかけになった。ベルガーはイェーナ大学で医学を学び、1897年に博士号を得たのち、1900年に同大学の精神・神経科医院の院長であるオットー・ビンスヴァンガー (1852 - 1929) の助手として職を得た。そこで2人の高名な科学者かつ医師、オスカー・フォクト (1870 - 1959) とコルビニアン・ブロードマン (1868 - 1918) の脳機能局在に関する共同研究に参加した。1906年に教授となり、1919年にビンスヴァンガーの後任となった。のちイェーナ大学の学長を務め (1927 - 1928)、最終的には、1938年に心理学の名誉教授となったが、公的・私的生活が第二次世界大戦とナチズムによって妨げられたことにより、1941年6月1日に縊首自殺した。研究体験したテレパシー現象の衝撃と脳神経機能への興味から、彼は神経学において多くの面で研究意欲を示したが、中でも脳における循環器、神経生理学、脳温度の研究を行った[3]。 しかし医学と神経学における彼の最大の貢献は、人間の脳における電気活動を系統的に研究し、脳波 (EEG) 研究を発展させたことである。これはイギリスでリチャード・カートン (1842 - 1926) が動物で行った草分け的研究の後を継いたものである。1924年にベルガーは人間では初めてとなる脳波記録を行い、これを Electroencephalogram(脳波)と名付け1929年に発表した[4]。また彼はこの脳波を用い、健常者や患者の脳から得られる、様々なパターンの波形やリズムを初めて記述した。具体的には、ベルガー波としても知られるアルファ波 (8-12 Hz) の存在、および被験者が開眼した時にそれが(より速いベータ波によって)抑制されること、いわゆる「アルファ・ブロケード」を指摘した。彼はまた、てんかんのような脳障害における脳波の変容の性質について初めて記述した。彼の手法は、前頭と後頭に各一箇所ずつ、患者の頭皮下へ銀製のワイヤを挿入するというものだった。彼は後に、銀箔を施した電極をゴムバンドで頭部へ装着させる手法を用いた。記録装置としては、彼はまずガブリエル・リップマンの毛細管電位計を用いたが、満足な結果を得られなかった。次いで彼は単線検流計を用い、後にシーメンス製の二重コイル記録検流計を用いた。これによって彼は1万分の1ボルトという微小電圧を記録できるようになった。最長3秒にわたる波形出力は助手によって写真撮影された。ベルガーによる初期の脳波記録1935年の時点で、ベルガーは同僚からドイツの精神科医として高く評価されていたとは言えず、どちらかというと変人扱いされていた。私の印象としては、彼は謙虚かつ威厳があり、ユーモアを解し、世間から認められない時も、後に名声を獲得した時も平静さを失なわなかった。しかし彼には一つ致命的な欠点があった。彼は自らの手法の技術的・身体的な基盤について全く知識を欠いていた。彼は力学や電気学に関しては何も分かっていなかった。—W.G. ウォルター、『生きている脳』懸田克躬・内薗耕二訳、岩波書店、1959年ベルガーは後に国際的な評価を得るようになった。彼の実験結果はエドガー・エイドリアンらイギリスとアメリカの科学者達によって確認された。ベルガーは 1937 年に国際会議に招かれ研究発表を行い、そこで彼の発見の重要性と革新性が顕彰された。出典: フリー百科事典『ウィキペディア(Wikipedia)』[書籍のメール便同梱は2冊まで]/脳波の発見 ハンス・ベルガーの夢[本/雑誌] (岩波科学ライブラリー) / 宮内哲/著
2021.05.29
コメント(0)
-
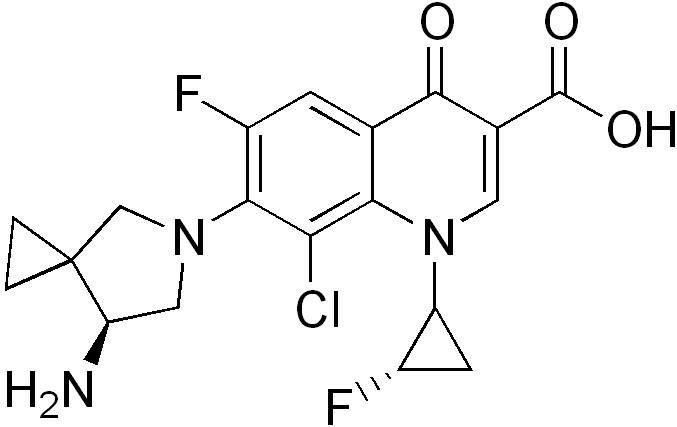
シタフロキサシン
2008年キノロン系合成抗菌薬、シタフロキサシン(Sitafloxacin:STFX)が開発された。シタフロキサシン(Sitafloxacin、別名:DU-6859a、商品名:グレースビット)はニューキノロン系の合成抗菌薬。第一三共により創成され、2009年現在は日本のみで上市されている。薬理シタフロキサシンは細菌のDNAジャイレース及びトポイソメラーゼIVに対して阻害活性を示し、DNA複製を阻害し、殺菌的に作用する。シタフロキサシンは、従来のキノロン耐性菌由来酵素に対しても強い阻害活性を示した。シタフロキサシンは生物由来でないため、正確には抗生物質ではなく、合成抗菌薬に分類される。特長抗菌活性の強い化合物であり、他剤に比べて低いMIC濃度で抗菌活性を示す。同社の発売しているオフロキサシン、レボフロキサシンに比べ、マイコプラズマやクラミジアに対しても十分な活性をもつ。ピロリ菌に対しても抗菌活性を示すため、3次除菌薬として除菌試験の途中で販売中止となったガチフロキサシンの代替薬として有望視されている。適応症同世代のガレノキサシンやモキシフロキサシンがレスピラトリー・キノロンとして上気道・呼吸器感染症にしか適応症がないのに比べ、広い適応症をもつ。上気道・呼吸器感染症咽頭・喉頭炎、扁桃炎、急性・続発性気管支炎、肺炎尿路感染症膀胱炎、腎盂腎炎、尿道炎婦人科領域子宮頸管炎耳鼻咽喉科領域中耳炎、副鼻腔炎歯科領域歯周組織炎、顎炎出典: フリー百科事典『ウィキペディア(Wikipedia)』エビデンスに基づくQ&Aでわかる皮膚感染症治療
2021.05.28
コメント(0)
-

ガレノキサシン
2007年 キノロン系抗菌剤、ガレノキサシン(Garenoxacin:GRNX)が開発された。ガレノキサシン(Garenoxacin, 略号: GRNX)は、富士フイルム富山化学(旧富山化学工業)で創製されたキノロン系経口抗菌剤である。商品名はジェニナック® (Geninax)。発売はアステラス製薬、販売提携は大正製薬。海外での販売権はMSD(旧シェリング・プラウ)が持つ。適応症幅広い菌種に効能をもち、レジオネラ・マイコプラズマ・クラミジアにも感受性を持つ。上気道: 咽頭・喉頭炎、扁桃炎、扁桃周囲膿瘍下気道: 急性気管支炎、肺炎、慢性呼吸器病変(慢性気管支炎・気管支拡張症など)の二次感染耳鼻科領域: 中耳炎、副鼻腔炎適応菌種ブドウ球菌属、レンサ球菌属、肺炎球菌(ペニシリン耐性肺炎球菌;PRSPを含む)、モラクセラ・カタラーリス、大腸菌、クレブシエラ属、エンテロバクター属、ヘモフィルス・インフルエンザ、レジオネラ・ニューモフィラ、クラミジア・ニューモニエ、マイコプラズマ・ニューモニエ抗菌活性Campylobacter jejuni: MIC50は0.032で、GFLXと同等、LVFXの2倍高い。Helicobacter pylori: MIC90は0.008で、GFLX・TVFXの4倍高い。阻止率は3者とも≦1μg/mLで100%。出典: フリー百科事典『ウィキペディア(Wikipedia)』[書籍のメール便同梱は2冊まで]/サンフォード感染症治療ガイド 日本語版 2020 / 原タイトル:THE SANFORD GUIDE TO ANTIMICROBIAL THERAPY 原著第50版の翻訳[本/雑誌] / DavidN.Gilbert/編集 HenryF.Chambers/編集 MichaelS.Saag/編集 AndrewT.Pavia/編集 菊池賢/日本語版監修
2021.05.27
コメント(0)
全202件 (202件中 1-50件目)











