公費 0
[医学の歴史] カテゴリの記事
全202件 (202件中 51-100件目)
-

ダプトマイシン
2003年 リポペプチド系抗生物質、ダプトマイシン(daptomycin)が開発された。ダプトマイシン(Daptomycin, DPT)はリポペプチド系の抗菌薬のひとつ。 ほとんどの抗菌薬が効かないMRSA感染による皮膚軟部組識感染や敗血症、感染性心内膜炎などの治療薬として利用される。歴史ダプトマイシンは放線菌 Streptomyces roseosporus が生成する物質より発見された。 1980年代に Eli Lilly and Company が発見した(LY146032)が、臨床試験で高用量投与時に筋炎などの副作用が発症したため、試験中止となっていた。その後LY 146032の開発権利は1997年にCubist Pharmaceuticalsに引き継がれた。 2003年に18歳以上の患者に対しての適応がFDAで承認されアメリカで販売された。その後キュビシン(Cubicin)という商品名でEUなどでも利用されている。 日本では2011年よりMSD(旧万有製薬)が販売している。 作用機序ダプトマイシンはグラム陽性菌の細胞膜にカルシウムイオン濃度依存的に結合し、細胞膜中で多量体(オリゴマー)を形成し、膜電位の脱分極を引き起こし、カリウムイオンを流出させる。その結果、蛋白質、DNA及びRNAの合成を阻害し、細胞融解を引き起こすことなく細菌を死滅させる。耐性耐性をもたらす伝達性因子は知られていない。また他の抗生物質・抗菌薬に対する交差耐性はみられていない。効能効果<適応菌種>ダプトマイシンに感性のメチシリン耐性黄色ブドウ球菌(MRSA)<適応症>敗血症、感染性心内膜炎、深在性皮膚感染症、外傷・熱傷及び手術創等の二次感染、びらん・潰瘍の二次感染出典: フリー百科事典『ウィキペディア(Wikipedia)』[書籍のメール便同梱は2冊まで]/2019 JAID/JSC感染症治療ガイド[本/雑誌] / JAIDJSC感染症治療ガイド・ガイドライン作成委員会/編集
2021.05.26
コメント(0)
-

リネゾリド
2000年 オキサゾリジノン系抗生物質、リネゾリド(linezolid)が開発された。リネゾリド(INN:linezolid)は、抗菌薬の1種である。分子構造にオキサゾリジノン骨格を持つため、オキサゾリジノン系合成抗菌薬に分類される。注射以外に経口投与でも使用可能である。概要リネゾリドはグラム陽性菌に対して有効な抗菌薬である。バンコマイシンに対する薬剤耐性を獲得したバンコマイシン耐性腸球菌(Vancomycin-resistant Enterococci, VRE)およびバンコマイシン耐性黄色ブドウ球菌(Vancomycin-resistant Staphylococcus aureus, VRSA)に有効な新たな抗菌薬として、リネゾリドは開発された。オキサゾリジノン系合成抗菌薬に分類され、日本では約20年ぶり、欧米では35年ぶりの新しい系統の抗菌薬として登場した。ただし、新たな抗菌薬をすれば、その耐性菌が必ず出現してきた歴史が有り、リネゾリドの場合も耐性菌の発現が予想されたため、当初から安易な使用を避け、適正使用するよう呼びかけられていた。しかし、2008年にスペインのICUで、リネゾリド耐性MRSAのアウトブレイクが発生した事が報告された、そして、日本でもリネゾリド耐性を有するメチシリン耐性黄色ブドウ球菌の出現が数多く報告されている。作用機序リネゾリドは、細菌のリボソームの50Sサブユニットに結合する事により、リボソームが70S開始複合体を形成する事を阻害する[1][注釈 1]。これによって、細菌がタンパク質の合成を開始できないようにして、細菌の増殖を抑制する。なお、ヒトなどの真核生物が持つリボソームは、細菌のような原核生物の持つリボソームとは異なるため、この機序の抗菌薬をヒトに対して使用できる。適用リネゾリドを含むオキサゾリジノン系合成抗菌薬は、従前に存在した抗菌薬との交叉耐性を示さない。一方で、グラム陰性菌に対しては充分な効果が望めない。リネゾリドは従前に存在した抗菌薬に耐性のグラム陽性菌の菌株を含む、下記の菌種などグラム陽性菌に対して、比較的低いMICを示す。レンサ球菌属(Streptococcus)- グラム陽性の通性嫌気性の球菌である。腸球菌(Enterococcus属のE. faecalis、E. faecium)- グラム陽性の球菌である。ブドウ球菌属(Staphylococcus)- グラム陽性の通性嫌気性の球菌である。ペプトストレプトコッカス属(Peptostreptococcus)- グラム陽性の嫌気性の球菌である。コリネバクテリウム属(Corynebacterium)- グラム陽性の好気性または通性嫌気性の桿菌である。根拠に基づく医療の観点からは、リネゾリドはVREによる肺炎、菌血症、腹腔内感染症、髄膜炎に有意な効果を示した。一方で、VREによる感染性心内膜炎に対しては効果を証明できていない。MRSAに対しては、バンコマイシンと同等の効果を得られる事が、3つのランダム化比較試験で証明された。なお、VRSA感染症については、臨床試験を行うほどの患者数がいないため、効果を証明できていない。副作用副作用として2週間以上の使用で、血小板減少、白血球減少、貧血など可逆性の骨髄抑制が 3パーセントの投与者に生じる。相互作用リネゾリドはMAOの阻害作用も有するため、チラミンを含有する食品を同時に摂取すると、チラミンの影響が強く出る。歴史アメリカ合衆国では2000年4月に VRE感染症や院内肺炎などを適応とした治療薬として承認された。しかし、その約1年後には、リネゾリドに対する耐性菌の登場が報告された。リネゾリドに対する耐性獲得のメカニズムとしては、23S rRNAのG2576U変異が原因の1つだと判明した。日本では、2001年4月に、バンコマイシン耐性腸球菌を適応として承認された。その後、2006年4月20日付でリネゾリド製剤について、メチシリン耐性黄色ブドウ球菌感染症の効能・効果の追加が承認された。出典: フリー百科事典『ウィキペディア(Wikipedia)』エビデンスに基づくQ&Aでわかる皮膚感染症治療
2021.05.25
コメント(0)
-

モキシフロキサシン
1999年キノロン系抗菌剤、モキシフロキサシン(Moxifloxacin:MFLX)が開発された。モキシフロキサシン (Moxifloxacin) は、第IIIa世代キノロン系抗菌薬のひとつ。商品名はアベロックス、点眼薬としてベガモックスがある。販売ドイツの製薬メーカーバイエルが開発し、かつて日本では塩野義製薬が販売していた。2010年7月1日より、バイエル薬品の日本法人が製造販売している。また、富士フイルムファーマが販売元として医薬品添付文書に記載されている。点眼薬として商品名ベガモックスで、アルコンが販売しており、日本ではノバルティスファーマ傘下アルコンファーマが取り扱っている。特徴PK/PD理論から一日一回内服投与として発売された。また、レスピラトリーキノロンとして当初発売されたが、適応症を皮膚感染症・外傷/熱傷の二次感染に対しても取得している。点眼薬としては1日3回の点眼となる。点眼薬には等張化剤、pH調節剤が添加されている。適応症表在性皮膚感染症、深在性皮膚感染症、外傷・熱傷及び手術創等の二次感染、咽頭・喉頭炎、扁桃炎、急性気管支炎、肺炎、慢性呼吸器病変の二次感染、副鼻腔炎眼瞼炎、涙嚢炎、麦粒腫、結膜炎、瞼板腺炎、角膜炎(角膜潰瘍を含む)、眼科周術期の無菌化療法出典: フリー百科事典『ウィキペディア(Wikipedia)』日本語版 サンフォード感染症治療ガイド2020(第50版) [ David N. Gilbert ]
2021.05.24
コメント(0)
-
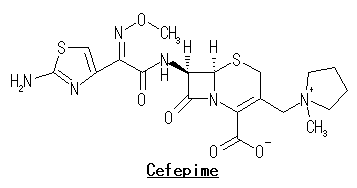
セフェピム
1994年 セファロスポリン系抗生物質、セフェピム(cefepime:CFPM)が開発された。出典: フリー百科事典『ウィキペディア(Wikipedia)』感染症治療のエッセンス&ピットフォール [ 竹末 芳生 ]
2021.05.23
コメント(0)
-

レボフロキサシン
1993年キノロン系抗菌剤、レボフロキサシン(levofloxacin:LVFX)が開発された。レボフロキサシン (Levofloxacin, LVFX) は、ニューキノロン系の合成抗菌薬(抗生物質)。日本の第一三共によって発明され、先発薬名はクラビット。様々な細菌感染症に適応があり、急性細菌性副鼻腔炎、肺炎、尿路感染症、慢性前立腺炎、ある種の胃腸炎に使用される。また他の抗生物質と併用し、結核、髄膜炎、骨盤腹膜炎の治療にも使用される。投与ルートは、経口、静注、点眼剤で利用可能。1996年にアメリカ合衆国で医療承認された。名前の由来は「英語: CRAVE(熱望する、切望する)IT」から CRAVIT とし、待ち望まれた薬剤であることを表現した。現在はWHO必須医薬品モデル・リストに収録され、後発医薬品も利用可能である。適応菌種本薬剤に感受性のある、ブドウ球菌、連鎖球菌、腸炎球菌、淋菌、結核菌、大腸菌などによる感染症。嫌気性菌を含むグラム陽性菌群及びグラム陰性桿菌マイコプラズマ属 (注射剤のみ)クラミジア属 (注射剤のみ)主な適応疾患肺炎、慢性呼吸器病変の二次感染、急性気管支炎、乳腺炎、肛門周囲膿瘍、咽頭・喉頭炎、扁桃炎(扁桃周囲炎、扁桃周囲膿瘍を含む)、腎盂腎炎、前立腺炎(急性症、慢性症)、精巣上体炎(副睾丸炎)、尿道炎、感染性腸炎、腸チフス、パラチフス、コレラ、涙嚢炎、麦粒腫、瞼板腺炎、外耳炎、中耳炎、副鼻腔炎、化膿性唾液腺炎、歯周組織炎、歯冠周囲炎、顎炎、炭疽、ブルセラ症、ペスト、野兎病、Q熱[5]、結核膀胱炎、表在性皮膚感染症、深在性皮膚感染症、リンパ管・リンパ節炎、慢性膿皮症、痤瘡(化膿性炎症を伴うもの)、外傷・熱傷および手術創などの二次感染、胆管炎、胆のう炎、バルトリン腺炎、子宮内感染及び付属器炎、子宮頸管炎(錠剤のみ)他の薬剤と併用しヘリコバクター・ピロリ (Helicobacter pylori) の除菌に用いられる事がある。主な副作用アナフィラキシー中毒性表皮壊死融解症横紋筋融解症クレアチンキナーゼ上昇QT延長急性腎不全間質性腎炎間質性肺炎偽膜性大腸炎関節痛胸部不快感倦怠感低血糖アキレス腱炎、腱断裂譫妄過敏性血管炎主な相互作用他の薬剤との併用により、自身の効力減弱や増強または併用している薬剤の効力に変化を及ぼす相互作用が報告されている。フェニル酢酸系又はプロピオン酸系非ステロイド性消炎鎮痛薬 - 痙攣を起こすおそれアルミニウム又はマグネシウム含有の制酸薬等、鉄剤 - 効果の減弱クマリン系抗凝固薬 - ワルファリンの作用を増強異性体オフロキサシン (Ofloxacin, OFLX) は光学異性体である (S) - (−) 体、(R) - (+) 体を含むが、レボフロキサシンは薬効のある (S) - (−) 体(=L体)のみを含有している。作用機序レボフロキサシンはグラム陽性菌とグラム陰性菌の両方に活性がある、薬効範囲の広い抗生物質である。すべてのキノロン系抗菌薬のように、DNAジャイレースやIV型トポイソメラーゼと呼ばれる二つのタイプのDNAトポイソメラーゼを阻害することにより働く。出典: フリー百科事典『ウィキペディア(Wikipedia)』JAID/JSC感染症治療ガイド 2019/JAIDJSC感染症治療ガイド・ガイドライン作成委員会【3000円以上送料無料】
2021.05.22
コメント(0)
-

セフジニル
1991年セファロスポリン系抗生物質、セフジニル(cefdinir:CFDN)が開発された。セフジニル(Cefdinir、商品名セフゾン)とは、第三世代セファロスポリンに属する抗生物質である。日本では第三世代セフェムと呼ばれることも多い。この薬剤は半合成で作られ、広い抗菌スペクトルを持っている。米国では1997年2月にFDAの承認を受けた。日本では藤沢薬品工業(現・アステラス製薬)が1991年11月に発売した。作用機構作用機構は他のセファロスポリン系抗生物質と同じである。使用対象セフジニルは中耳炎、皮膚炎、咽頭炎、静脈洞炎、感染性肺炎、気管支炎などの治療に用いられている。日本でも風邪などの治療薬として処方される。セフジニルはグラム陽性菌およびグラム陰性菌が原因の感染症の治療に用いられる。以下のような細菌に対して作用する。グラム陰性菌Haemophilus influenzae (インフルエンザ菌)Moraxella catarrhalisEscherichia coli (大腸菌)Klebsiella spp.Proteus mirabilisグラム陽性菌Staphylococcus aureus (黄色ブドウ球菌)Streptococcus pneumoniaeStreptococcus pyogenes大部分の第三世代セファロスポリン(セフジニルを含む)は、緑膿菌には効果的ではない。投与方法と投与量セフジニルは通常カプセルとして経口投与される。投与期間は感染症の種類によって異なる。出典: フリー百科事典『ウィキペディア(Wikipedia)』感染と抗菌薬(18-3) 特集:これからを見据えた呼吸器感染症治療
2021.05.21
コメント(0)
-

クラリスロマイシン
1990年マクロライド系抗生物質、クラリスロマイシン(clarithromycin:CAM)が開発された。クラリスロマイシン (Clarithromycin, CAM) はマクロライド系抗生物質のひとつ。咽頭炎、扁桃炎、慢性気管支炎の急性増悪、肺炎(特にマイコプラズマ肺炎とクラミジア肺炎)、皮膚感染症、非結核性抗酸菌、レジオネラによる感染症の治療、ヘリコバクター・ピロリの除菌療法に用いられる。歴史1970年代に大正製薬が創製し、1991年にアメリカ合衆国のアボット社によって市販された。マクロライドの化学合成はたいへん難しく、クラリスロマイシンはエリスロマイシンの修飾によって生まれた半合成マクロライドである。作用機序クラリスロマイシンは微生物のリボゾームの、50Sサブユニットという部分に結合して、タンパク質の合成を阻害する。マクロライドの作用は主に静菌作用(増殖の抑制)である。クラリスロマイシンは原型薬のエリスロマイシンと類似の抗菌活性を有しているが、レジオネラなど一部の菌にはより強い抗菌活性を持ち、ほぼ全ての点でエリスロマイシンよりも優れている。高濃度ではインフルエンザ菌、肺炎球菌、淋菌などの一部の菌に殺菌的にも作用する。薬物動態学エリスロマイシンとは異なり、クラリスロマイシンは酸に対して安定で、コーティングなどで胃酸から保護しなくても経口投与できる。ほとんどが腸から吸収され、かなり初回通過効果(肝臓での代謝)の影響を受けるので、生物学的利用度は50〜55%である。これをわかりやすく言うと、口から投与した量の半分ぐらいが、クラリスロマイシンの作用点にあたる部位に到達して作用する、と考えればよい。最高血中濃度は、投与を開始してから2時間程度で得られる。基本的にはエリスロマイシン同様に、時間依存性の抗生物質と考えられているので、徐放製剤も米国では利用できる(Biaxin XL:1日1回の投与でよい。日本では未認可)。白血球などの食細胞に蓄積する作用があるため、能動的に病変部へ輸送され、全身の組織内では血中濃度の10倍以上の濃度を得ることができる。もっとも高濃度になるのは肝臓と肺である。主に肝臓で代謝されるが、代謝産物の中で14-ハイドロキシクラリスロマイシンはクラリスロマイシンのほぼ2倍の活性を持っている。クラリスロマイシンの半減期は5時間で、14-ハイドロキシクラリスロマイシンのそれは7時間である。これは、エリスロマイシンの血中半減期の数倍に相当する。従って、徐放化されていなくても一日2(〜3)回の内服で良い。クラリスロマイシンとその代謝産物は、尿と胆汁へと排泄される。もっとも、相当重症(クレアチニンクリアランスで30未満)で無い限り、腎不全で投与量を修飾する必要は無い。薬物相互作用肝代謝酵素シトクロムP450(CYP3A4)阻害作用を有する。従って、CYP3A4で代謝される薬剤と併用したとき、併用薬剤の代謝が阻害され血中濃度が上昇する薬物相互作用が生じる可能性がある。適応クラリスロマイシンに限らず、マクロライドの基本的な用途はペニシリン系やキノロン系がアレルギーなどにより禁忌であるヒトに対する、連鎖球菌などのグラム陽性菌感染症の代替薬である。さらに、第一選択となる主なものにはベータラクタム系が無効のマイコプラズマ・リケッチア・クラミジアによる感染症がある。原型薬のエリスロマイシンがかなり臨床的な使いづらさのある薬剤(一日4〜6回も飲まなければならない、消化器症状が強いなど)であるため、クラリスロマイシンは多くのマクロライドの用途において、アジスロマイシンなどと並んで「マクロライドの顔」として広く用いられている。ほか、インフルエンザ菌への活性はエリスロマイシンよりも優れている。主な適応咽頭炎・細菌性肺炎・急性中耳炎、副鼻腔炎などの、起因菌としてグラム陽性球菌が想定される感染症基本的にはペニシリン系が用いられない場合に限るべき。静菌的な薬剤でもあり、臨床的な「切れ味(効果)」の面で明らかに劣る。非定型肺炎基本的には、マイコプラズマとクラミジアによる肺炎の総称。第一選択。ウィルス性肺炎と鑑別しがたい場合も、重症度によってはやむを得ず用いられる[3]。トラコーマ、性器クラミジア感染症などのクラミジア感染症後者には服薬コンプライアンス面でアジスロマイシンが優れるとの考えが主流。発疹チフスなどのリケッチア感染症、ツツガムシ病基本的にはテトラサイクリン系を優先するが、小児や妊婦では第一選択になりうる。百日咳(第一選択)カンピロバクター腸炎(第一選択)レジオネラ感染症(第一選択)非結核性抗酸菌の予防・治療(第一選択)2008年5月より保険適応となった。ヘリコバクター・ピロリの除菌療法(第一選択)前述の様に呼吸器感染症の治療に用いられることから、小児のクラリスロマイシン耐性菌保有も見られる。アジスロマイシンやロキシスロマイシンとどちらが優れているかは大変難しい問題である。非定型抗酸菌やヘリコバクター・ピロリのようにクラリスロマイシンによる治療が確立しているものに、理由も無くアジスロマイシンを代替薬として用いる必要はないだろう(新しい薬がいい薬、とは限らない)。しかし、一方でアジスロマイシンの薬物動態学的特性(飲ませる期間が短く、回数も1日1回でよい、見かけの分布容積がとても大きい)は魅力的であり、マクロライドという服薬コンプライアンスが悪く(つまり味が悪く)、耐性菌の問題が深刻になっている薬剤では重要な利点である。時に、一般論としてアジスロマイシンの優位性を主張する識者も存在する。処方例成人での一日量は400mg/日。非結核性抗酸菌症に対しては800mg/日。一般にはクラリス/クラリシッド錠(200mg) 2錠 一日2回(AIDS患者の非結核性抗酸菌症(NTM)の治療などでは増量)。各感染症について、何日投与を続けるかは疾患や病状、医師により異なる。概して咽頭炎では10日が推奨されている。胃潰瘍・十二指腸潰瘍におけるヘリコバクター・ピロリの除菌で7日間他剤と併用が日本では保険適応とされている。期間も重要であるが、耐性菌の問題もあるので、服薬コンプライアンスに注意を払う必要がある。ことに解熱後の、症状がとれてきた時期が問題である。小児では、クラリス/クラリシッドドライシロップ(ないし錠剤)で10〜15mg/kg/日 一日2〜3回。剤形クラリスロマイシン錠 200mgクラリス/クラリシッド錠(200mg・50mg小児用)クラリス/クラリシッドドライシロップ(10%)小児用その他、ジェネリック医薬品(後発医薬品)の各剤形が各社から発売されている。副作用他のマクロライドと同様で、重篤なものは少ない。多いのは消化器症状(下痢・悪心(吐き気)・嘔吐)である。消化器症状の頻度はエリスロマイシンよりも少なくなっている。まれに発疹・頭痛・倦怠感などを呈する。アレルギー反応はごくまれに重篤になるが、多くはない。クラリスロマイシンにより心臓死が増加することが報告されている(ロキシスロマイシンでは同様の影響はみられなかった)。安定冠動脈疾患患者におけるクラリスロマイシンの投与は心血管疾患死を有意に上昇させた報告がある。禁忌クラリスロマイシンの禁忌は、「本剤にアレルギー反応を持つ者」、「ピモジド、エルゴタミン含有製剤、スボレキサント、ロミタピドメシル酸塩、タダラフィル〔アドシルカ〕、チカグレロル、イブルチニブ、アスナプレビル、バニプレビルを投与中の患者」、「肝臓又は腎臓に障害のある患者で、コルヒチン服用者」。米国FDAの胎児危険度分類はクラス「C」である。禁忌ではない。動物実験レベルでクラリスロマイシンの催奇形性を示唆する報告が出ているが、大量投与を用いた実験であり臨床上の意義が明らかでない(一般的には、マクロライドは比較的安全である)。しかし、FDA基準ではアジスロマイシンやエリスロマイシンがクラス「B」としてより安全なクラスに入れてあるので、妊婦に対してアジスロマイシンやもっとも使用年数の長いエリスロマイシンの投与を優先することは十分考えうる選択肢である。FDAの授乳危険度分類は。「注意深く用いること」である。禁忌ではない。出典: フリー百科事典『ウィキペディア(Wikipedia)』【送料無料】 JAID / JSC感染症治療ガイド2019 / Jaid / Jsc感染症治療ガイド・ガイドライン作成委員 【本】
2021.05.20
コメント(0)
-

アルベカシン
1990年アミノグリコシド系抗生物質、アルベカシン(arbekacin:ABK)が開発された。アルベカシン(日局アルベカシン硫酸塩、Arbekacin, ABK)は、アミノグリコシド系抗生物質の一つである。硫酸塩(硫酸アルベカシン)が明治製菓より「ハベカシン」という商品名で上市されているほか、後発品が有る。効能・効果アルベカシンに感性のメチシリン耐性黄色ブドウ球菌 (MRSA) による敗血症、肺炎作用機序細菌のタンパク質合成を阻害することにより抗菌作用を示し、その作用は殺菌的である。緑膿菌を含むグラム陽性菌及びグラム陰性菌に対して広い抗菌スペクトラムを有する。特に、アミノグリコシド不活性化酵素に高い安定性を示し、MRSAに対する抗菌力が認められている。販売までの経緯梅澤濱夫らは、カナマイシン耐性菌の耐性機構の研究から、カナマイシン耐性菌に有効なジベカシンをベカナマイシン(カナマイシンB)を原料として合成し、さらにジベカシン耐性菌にも有効なアルベカシンをジベカシンから1973年に合成した。 アルベカシンは日本で1990年9月にMRSA感染症の敗血症、肺炎を適応症として成人用に承認され、1998年12月に小児への適応が追加承認された。副作用他のアミノグリコシド系抗生物質と同様に、内耳神経、腎臓に対する毒性を持ち、腎障害、聴力障害等の副作用が生じる恐れがある。副作用の発現は最低血中濃度と相関性があることが知られており、副作用発現防止のため、薬物血中濃度モニタリング(TDM)を必要とする。出典: フリー百科事典『ウィキペディア(Wikipedia)』感染症治療のエッセンス&ピットフォール [ 竹末 芳生 ]
2021.05.19
コメント(0)
-
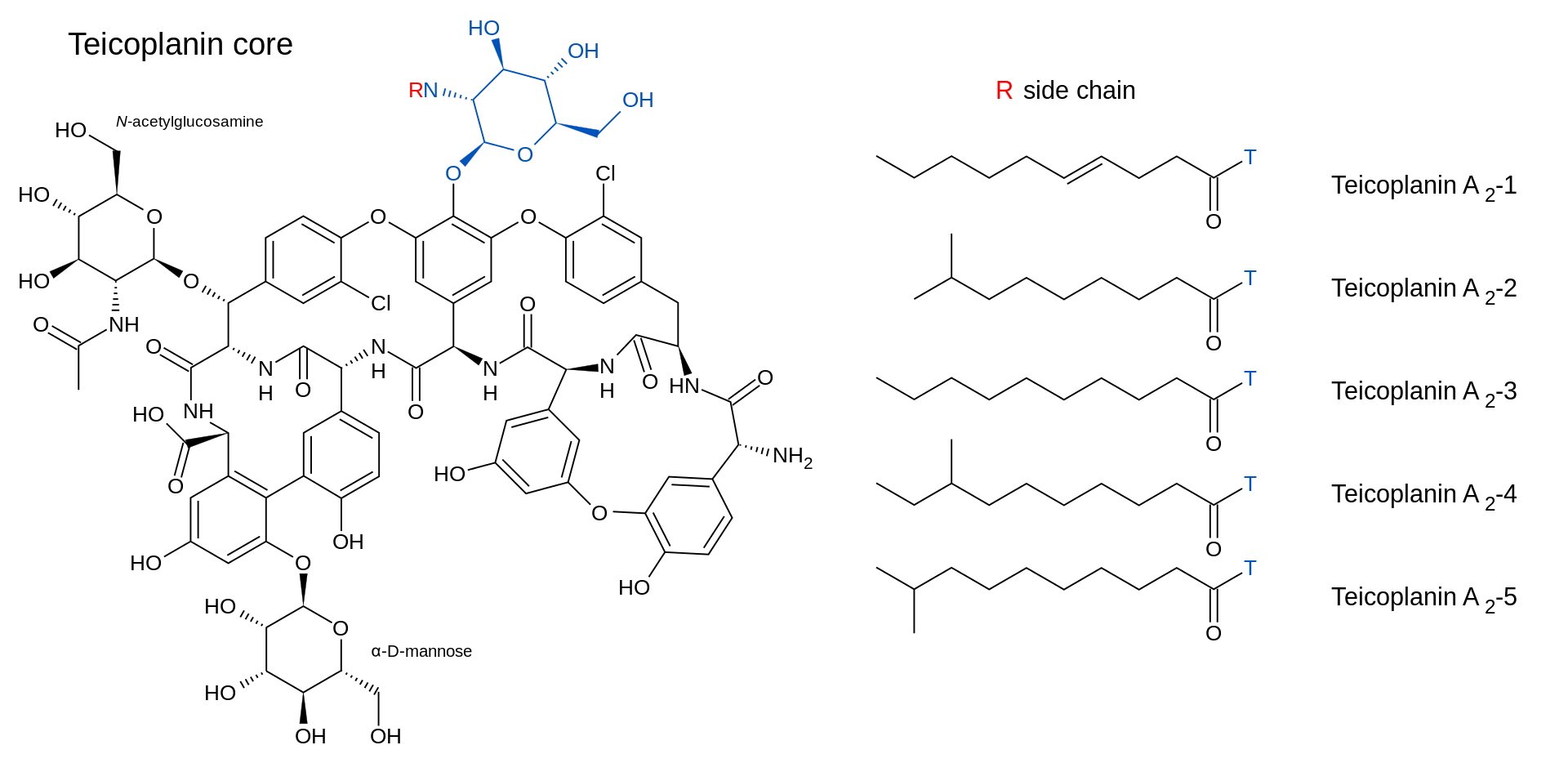
テイコプラニン
1988年グリコペプチド系抗生物質、テイコプラニン(teicoplanin:TEIC)が開発された。【送料無料】 小児感染症治療ハンドブック2020-2021 / 尾内一信 【本】
2021.05.18
コメント(0)
-

アジスロマイシン
1988年マクロライド系抗生物質、アジスロマイシン(azithromycin:AZM)が開発された。アジスロマイシン(azithromycin)は、15員環マクロライド系抗生物質である。分子量は785.02。日本での商品名は「ジスロマック」、略号は「AZM」。2009年現在15員環マクロライド系抗生物質はアジスロマイシンのみである。特徴長時間体内に留まる特徴がある。これは15員環に窒素原子が入っているという構造に由来し、血中濃度より10〜100倍の組織、細胞内濃度を得ることができるため半減期が68.1時間(500 mg投与時)ときわめて長い。また、クラリスロマイシンなどでみられる薬物相互作用はほとんど無い。おもな適応症は、深在性皮膚感染症、リンパ管・リンパ節炎、咽頭・喉頭炎、扁桃炎、急性気管支炎、肺炎、肺膿瘍、慢性呼吸器病変の二次感染、尿道炎、子宮頸管炎、骨盤内炎症性疾患、副鼻腔炎、歯周組織炎、歯冠周囲炎、顎炎、HIV/AIDS患者の非結核性抗酸菌症適応菌種アジスロマイシンに感性のブドウ球菌属、レンサ球菌属、肺炎球菌、淋菌、モラクセラ(ブランハメラ)・カタラーリス、インフルエンザ菌、レジオネラ・ニューモフィラ、ペプトストレプトコッカス属、プレボテラ属、クラミジア属、マイコプラズマ属その他他のマクロライド系抗生物質でもみられるQT延長症候群について、アジスロマイシンに対しても米国のFDAは2013年3月12日に警告を強化した。軽症の呼吸器感染症に関しては米国にて500 mg×3日間が有効という研究があるが、クラミジア肺炎やレジオネラ肺炎ではより長期の投与が必要ではとの意見もある。オートファジーの阻害作用が報告されており、嚢胞性線維症患者においてはマイコバクテリア感染症の罹患リスクを向上させる可能性が指摘されている。おもな相互作用マクロライド系薬剤であるためチトクロームP450に影響を与え薬物相互作用を生じる。シクロスポリン、ワルファリン、ジゴキシン制酸剤水酸化マグネシウム、水酸化アルミニウムにより、最高血中濃度低下出典: フリー百科事典『ウィキペディア(Wikipedia)』救急集中治療領域と外科領域における実例に学ぶ重症感染症治療
2021.05.17
コメント(0)
-

シプロフロキサシン
1987年キノロン系抗菌剤、シプロフロキサシン(ciprofloxacin:CPFX)が開発された。シプロフロキサシン (英語: ciprofloxacin、略称:CPFX) とは、ニューキノロン系の抗生物質のひとつ。バイエルよりシプロキサン、シプロの商品名で販売されているほか、後発医薬品も存在する。フッ素を持ち、フルオロキノロン薬に分類される。活性シプロフロキサシンは広域抗生物質であり、グラム陰性、グラム陽性のいずれのバクテリアにも活性である。デオキシリボ核酸二本鎖の切断・再結合を行う酵素であるDNAジャイレース(DNAトポイソメラーゼの一種)に結合し、DNAの複製を阻害することで抗菌作用を示す。DNAの複製が阻害されることで、バクテリアは細胞分裂ができなくなる。主な副作用は他の抗生物質と同様、消化器への刺激である。一般的な安全性と効力と広域性から、シプロフロキサシンは耐性菌への感染に対する最終手段として用いられる。しかし使用回数や使用期間とともにシプロフロキサシン耐性菌が病院内で増える結果となる。細胞の培養では、シプロフロキサシンはマイコプラズマへの感染に対処するために用いられる。相互作用フラボノイドの一種のクエルセチン(ニンニクやリンゴに含まれる)は、フルオロキノロン薬と相互作用する可能性がある。クエルセチンはバクテリアのDNAジャイレースに競合して結合するためである。フルオロキノロン薬の効果が阻害されるか高められるかは明らかになってはいない。注意アルミニウム、マグネシウム、カルシウム、鉄(II)、亜鉛などの金属のカチオンはフルオロキノロン系の抗生物質とキレート錯体を作り吸収を阻害すると考えられている。アルミニウムを含むスクラルファートはシプロフロキサシンの生物学的利用能を約4%まで低下させる[2]。シトクロムP450系で代謝される薬物の毒性がキノロン薬によって高められる。キノロン薬はまた、GABAA受容体に作用して神経系の病徴(痙攣など)を引き起こすことがある。その作用は非ステロイド性抗炎症薬との相互作用により強められる[3]。特にジクロフェナクの併用で痙攣例がある。効能・効果<適応菌種>本剤に感性のブドウ球菌属、腸球菌属、炭疽菌、大腸菌、クレブシエラ属、エンテロバクター属、緑膿菌、レジオネラ属<適応症>敗血症、外傷・熱傷および手術創などの二次感染、肺炎、腹膜炎、胆嚢炎、胆管炎、炭疽出典: フリー百科事典『ウィキペディア(Wikipedia)』【送料無料】 エビデンスに基づくQ & Aでわかる皮膚感染症治療 / 宮地良樹 【本】
2021.05.16
コメント(0)
-

アズトレオナム
1986年モノバクタム系抗生物質、アズトレオナム(aztreonam:AZT)が開発された。アズトレオナム(Aztreonam)は、アザクタム(Azactam)などの商品名で販売される、緑膿菌のようなグラム陰性菌によって引き起こされる感染症の治療に用いられる抗生物質である。アズトレオナムを用いて治療される感染症には、骨髄炎、子宮内膜炎、腹腔内感染症、肺炎、尿路感染症、敗血症などがあげられる[1]。投与法は点滴静脈注射、筋肉内注射、または霧状に噴射による口からの吸入である。注射投与による一般的な副作用には、注射部位の痛み、嘔吐、発疹などがあげられる[1]。吸入した場合の一般的な副作用には、喘鳴、咳、嘔吐などがあげられる[1]。重度の副作用には、クロストリジウム・ディフィシル感染症やアナフィラキシーなどのアレルギー反応などがあげられる。他のβ-ラクタムに対してアレルギーがある人は、アズトレオナムに対してのアレルギー反応率は低い。妊娠中の人への投与は安全とみられる。アズトレオナムはモノバクタムに属する医薬品である。アズトレオナムは通常、細胞壁の合成を阻害することにより殺菌する効果がある。アズトレオナムは、1986年に米国で医薬品として承認された。アズトレオナムは、2019年に世界保健機関の必須医薬品リストから削除された。後発医薬品として入手できる[1]。英国の国民保健サービスにかかる費用は、1日分の注射薬は約28.20ポンド、一貫の治療に使われる吸入剤は約2,182.00ポンドである。アズトレオナムは、クロモバクテリウム・ビオラセウム細菌から製造される化学物質である。出典: フリー百科事典『ウィキペディア(Wikipedia)』[書籍のメール便同梱は2冊まで]/サンフォード感染症治療ガイド 日本語版 2020 / 原タイトル:THE SANFORD GUIDE TO ANTIMICROBIAL THERAPY 原著第50版の翻訳[本/雑誌] / DavidN.Gilbert/編集 HenryF.Chambers/編集 MichaelS.Saag/編集 AndrewT.Pavia/編集 菊池賢/日本語版監修
2021.05.15
コメント(0)
-

オフロキサシン
1985年キノロン系抗菌剤、オフロキサシン(ofloxacin:OFLX)が開発された。オフロキサシン(Ofloxacin)は、第2世代ニューキノロン系の抗菌薬である。錠剤のほか、点眼液、眼軟膏、点耳液がある。1980年頃に第一製薬が初めて合成し、1985年4月に日本で、1990年12月に米国で承認された。オフロキサシンはラセミ体であり、薬理学的活性体であるレボフロキサシンを50%とその鏡像異性体であるデキストロフロキサシンを50%含んでいる。オフロキサシンの副作用として、腱障害(腱断裂を含む)や末梢神経炎(英語版)(時に不可逆性)が知られている。腱障害は治療終了後長期間経ってから生じ、生涯にわたる障害が残る可能性もある。WHO必須医薬品モデル・リストに収載されている。効能・効果日本で承認されている適応症は、表在性皮膚感染症、深在性皮膚感染症、リンパ管・リンパ節炎、慢性膿皮症、外傷・熱傷および手術創などの二次感染、乳腺炎、肛門周囲膿瘍、咽頭・喉頭炎、扁桃炎、急性気管支炎、肺炎、慢性呼吸器病変の二次感染、膀胱炎、腎盂腎炎、前立腺炎(急性症、慢性症)、精巣上体炎(副睾丸炎)、尿道炎、胆嚢炎、胆管炎、感染性腸炎、腸チフス、パラチフス、子宮頸管炎、バルトリン腺炎、子宮内感染、子宮付属器炎、涙嚢炎、麦粒腫、瞼板腺炎、角膜炎(角膜潰瘍を含む)、眼瞼炎眼製剤のみ、結膜炎眼製剤のみ、眼科周術期の無菌化療法眼製剤のみ、外耳炎点耳液のみ、中耳炎、副鼻腔炎、歯周組織炎、歯冠周囲炎、顎炎、ハンセン病である。(眼製剤:点眼液・眼軟膏) 錠剤のみに承認を有する疾患は特記しない。米国では、下記の疾患について承認されている。慢性閉塞性肺疾患患者の急性感染症市中肺炎合併症のない皮膚・皮膚構造感染症非淋菌性尿道炎(英語版)と子宮頸管炎(英語版)尿道および子宮頸部の混合感染症急性骨盤腹膜炎単純性尿路感染症複雑性尿路感染症前立腺炎急性単純性尿路・子宮頸部淋菌感染症オフロキサシンは梅毒には無効である。多用されて薬剤耐性がついたため、淋病への第一選択薬ではない。感性菌種オフロキサシンに感性の下記の菌種に対して使用可能である。グラム陽性菌ブドウ球菌属レンサ球菌属肺炎球菌腸球菌属癩菌(らいきん)ペプトストレプトコッカス属ミクロコッカス属(眼のみ)コリネバクテリウム属(眼のみ)アクネ菌<(眼のみ)グラム陰性菌淋菌大腸菌赤痢菌チフス菌パラチフス菌シトロバクター属肺炎桿菌エンテロバクター属セラチア属プロテウス属モルガネラ・モルガニープロビデンシア属インフルエンザ菌緑膿菌アシネトバクター属カンピロバクター属クラミジア・トラコマチスモラクセラ属(眼のみ)クレブシエラ属(眼のみ)ヘモフィルス・エジプチウス(眼のみ)シュードモナス属(眼のみ)バークホルデリア・セパシア(眼のみ)ステノトロホモナス・マルトフィリア(眼のみ)禁忌製剤成分に過敏症を持つ患者のほか、内服薬では動物実験(幼若犬、幼若ラット)で関節異常が認められたため、妊婦または妊娠している可能性のある婦人ならびに小児等には禁忌とされている。前項でも述べた通り、一部の性病では薬剤耐性菌が増加しており、オフロキサシンは禁忌とされている。肝疾患を有する患者が使用する際には注意が要る。重度の肝機能障害(肝硬変(腹水の有無にかかわらない)等)ではオフロキサシンの排泄が遅延する。オフロキサシンの主な排泄経路は腎臓であるので、重度の腎機能障害を有する患者では減量等を考慮すべきである。腎機能正常の場合は血中濃度の半減期t1/2=4.5時間、中等度障害でt1/2=5.3時間、重度障害でt1/2=12.6時間である。精神病やてんかんなどの痙攣性疾患を有する患者の場合も注意が必要である。妊産婦オフロキサシンは妊娠ラット対する超高用量(810mg/kg/日:mg/m2換算でヒトへの推奨最高投与量の11倍、mg/kg換算で50倍)あるいはウサギに対する高用量( 160 mg/kg/日:推奨最高量の4倍または10倍)でも催奇性を示さない。またラットに360mg/kg/日(最高用量の5倍または23倍)経口投与した研究でも、後期胚、分娩、授乳や、新生児の状態や成長には異常は見られなかった。しかし、50倍(ラット)と10倍(ウサギ)の投与量で胎児毒性(胎児体重減少、胎児死亡率増加)が見られた研究もある。810mg/kg/日(ラット)で骨格の非定型が報告されている。ヒトの妊婦を対象とした管理された臨床試験は実施された事がない。オフロキサシンを妊婦に服用させる際には、有益性が有害性を上回る場合にのみ留めるべきである。小児(LVFX)筋骨格系の副作用が起こるので小児への全身投与は承認されていない。ある研究では、3つの臨床試験に参加した計1,534名の若年患者(6-16歳)を治療終了後12ヶ月まで追跡調査したところ、レボフロキサシン(LVFX)を投与したこれらの患者での12ヶ月間の筋骨格系有害事象の累積発現率は3.2%で、他の抗生物質を使用した893名の1.8%よりも高い発生率であった。LVFX投与群ではこれら筋骨格系の有害事象の2⁄3は最初の60日以内に発生しており、86%は軽度、17%は中等度で、全て長期間の後遺症なく回復した。712名の小児でLVFXとアジスロマイシンまたはセフトリアキソンの市中肺炎への有効性を比較した臨床試験の結果、LVFX群で6%の有害事象が発生し、比較群では4%であった。これらの有害事象のほとんどはLVFXとの因果関係は“無し”か“疑わしい”であった。LVFX群で2名が死亡したが、治療関連死とは考えられなかった。米国食品医薬品局(FDA)への自発報告システムには、2011年9月20日の時点で筋骨格系有害事象が39件(筋断裂5件を含む)、中枢神経系有害事象が19件(5件の痙攣を含む)報告されていた。特に2005年4月から2008年3月に掛けて報告の頻度が高かった。同期間内には11万2千名の小児患者にLVFXが処方されたと推測される。副作用錠剤の添付文書に記載されている重大な副作用は、ショック、アナフィラキシー、過敏性血管炎、中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)、QT延長、心室頻拍(Torsades de pointesを含む)、急性腎不全、間質性腎炎、劇症肝炎、肝機能障害、黄疸、無顆粒球症、汎血球減少症、血小板減少、溶血性貧血、間質性肺炎、好酸球性肺炎、偽膜性大腸炎などの血便を伴う重篤な大腸炎、横紋筋融解症(急激な腎機能悪化を伴う事がある)、低血糖、アキレス腱炎、腱断裂などの腱障害、痙攣、錯乱・せん妄・抑うつなどの精神症状、重症筋無力症の悪化である。点眼液と眼軟膏には、これらの内、ショックとアナフィラキシーのみが記載されている[8][9]。点耳液には重大な副作用は設定されていない[10]。頻度の多い副作用は、消化器症状2.4%―腹痛、下痢、嘔気、食欲不振等精神神経系症状0.7%―不眠、眩暈等過敏症状0.5%―発疹、瘙痒等である。一般に、ニューキノロン系抗生物質(FQ)の忍容性は高く、ほとんどの副作用は軽度か中等度であるが、時折重篤な副作用が発生する。ニューキノロン系抗生物質で治療された患者の全般副作用発現率は他の系統の抗生物質を用いた場合の発現率と概ね同程度である。米国の疾病予防管理センター(CDC)の研究では、ニューキノロン系の副作用はセファロスポリン系やマクロライド系の抗生物質の副作用よりも重篤性が高く、救急科に掛かる割合が多いが、ペニシリン系、クリンダマイシン系、スルホンアミド系、バンコマイシンよりは低く少ないとされた。製造販売後調査であらゆるFQについて多くの種類の稀で重篤な副作用の事例が収集された。これらの内、腱障害と神経系疾患である重症筋無力症の症状増悪の2点が米国向け添付文書の黒枠警告に記載された。ニューキノロン系で見られる重篤腱障害のほとんどは「腱断裂」で、その内のほとんどは「アキレス腱断裂」であった。若い患者ほど回復が早く、高齢の患者では永続的に障害が残る症例があった。シプロフロキサシンまたはレボフロキサシンに関連するアキレス腱断裂の全般的な発生頻度は、10万治療中17治療である。発生の危険性は、高齢、ステロイド系抗炎症薬の局所または全身投与、で増加する。ニューキノロン系関連腱断裂のほぼ1⁄3でステロイド系抗炎症薬が併用されていた。腱障害はFQ投与終了後1年間が経過するまでは発生し得る。FQは電位駆動型カリウムチャネルを遮断してQT延長を惹起させる。QT延長は命を脅かすトルサード・ド・ポワントの原因となるが、最も頻繁に用いられるシプロフロキサシンとレボフロキサシンではQT延長が最小限に抑えられている。Clostridium difficile が原因で発生する下痢(偽膜性大腸炎)は、色々な抗生物質、特にスペクトルが広域なクリンダマイシン、セファロスポリン系、ニューキノロン系で多く見られる。ニューキノロン系の偽膜性大腸炎リスクは、広域セファロスポリンと同等か、低い。FQを服用すると特に有害なクロストリジウム属が定着、繁殖し易くなる。米国の添付文書では、時に末梢神経炎が後遺症を残す事があると記載されている[41]。他の精神神経系症状として、不眠、不穏、稀に痙攣、精神病が起こるとされる。稀な精神神経系症状は他にもあるが、研究により異なる。過量投与時に急性症状を呈することはほとんどないが、腎不全や痙攣発作が起こり得る。小児や高齢者は感受性が高く、治療域の使用量でも副作用の発生率は高い。相互作用オフロキサシンや一部のニューキノロンは薬物代謝酵素を阻害するので、シクロスポリンやテオフィリン、ワルファリンなどの薬剤の血中濃度が上昇する。その結果、これらの薬剤による副作用リスクが増大する。オフロキサシン等をスルホニルウレア系の抗糖尿病薬と併用する場合には、血糖値を慎重に確認することが勧められる。非ステロイド系抗炎症薬を(ニュー/オールド)キノロン系抗生物質と併用するは、中枢神経刺激が増加して痙攣発作が起こり易くなる。ニューキノロンはアセノクマロール、アニシンジオン、ジクマロールの抗凝固活性を増加させる。さらに、ジヒドロキニジン、バルビツール酸系睡眠薬、キニジンなどの心血管リスクや不整脈リスクを増加させる。ステロイド系抗炎症薬を同時にまたは過去に使用していると、特に高齢者で、ニューキノロン服薬時のアキレス腱断裂のリスクが上昇する。過量投与オフロキサシンを過量投与した場合の情報は限られている。現状で推奨される手当は、胃洗浄と水分補給である。血液透析や腹膜透析は効果が薄い。過量投与で中枢神経毒性、心血管毒性、腱・関節毒性、肝毒性、腎毒性、痙攣が見られるとの報告がある。また、オフロキサシン常用量でも重篤な精神病症状が発現したとの報告もある。薬物動態錠剤の場合、オフロキサシンの生物学的利用能は約98%である。服用の1〜2時間後に血中濃度が最高になり、半減期は4〜5時間である。ただし、高齢者では6.4〜7.4時間に延長する。65〜80%が未変化体のまま腎臓から排泄される。肝臓(胆嚢)からも4〜8%が排泄される。代謝200mgと300mgを繰り返し投与して定常状態に達した時、最高血中濃度はそれぞれ2.2µg/mLと3.6µg/mLである。in vitro では、オフロキサシン分子の約32%が血漿蛋白質と結合している。体組織に広範囲に分布し、水疱液、子宮頸部、肺組織、卵巣、前立腺液、前立腺組織、皮膚、喀痰からも検出される。ピリドベンザキソジン環がある事で、母化合物よりも代謝され難い。脱メチル体またはN-オキシド体は尿中排泄の5%未満、糞中排泄の4〜8%である。内因性の多くの化合物がオフロキサシンで阻害、機能変化、枯渇される。作用機序オフロキサシンは広域スペクトル抗生物質であり、グラム陽性菌とグラム陰性菌の両方に有効である。ほとんどの原核生物、特に細菌で必須のII型トポイソメラーゼ(トポイソメラーゼIV)であるDNAギラーゼを阻害して]DNAの複製を妨げ、細菌の分裂増殖を妨害する。用法・用量英語版の添付文書ではオフロキサシンの投与量は感染症毎に細かく定められている。腎機能障害または肝機能障害がある場合には、血中濃度が上がり過ぎて致死的な事象が発生しない様に注意しなければならない。オフロキサシンは主に腎臓から排泄されるが、一部は代謝され、一部は肝臓から排泄される。腎・肝機能障害がある場合、特に重症腎機能障害がある場合には、用量調節が必須である。腎臓が主な排泄経路であるので、腎機能障害の方が肝機能障害よりも影響が大きい。服用期間は疾病の治療上必要な最小限の期間とされており、多くの場合7〜14日間である。抗生物質の乱用と薬物耐性菌の出現オフロキサシンや他のフルオロキノロンに対する耐性は、通常の治療期間中にも速やかに形成される。黄色ブドウ球菌、腸球菌、化膿連鎖球菌など、多数の病原体について全世界で耐性が出現していることが知られている。フルオロキノロンは2002年時点では米国内で成人に最も多く処方される抗生物質であった。医療研究・品質調査機構の調査に拠れば、処方箋の42%が米国食品医薬品局に承認されていない疾患に処方されていた。細菌感染症であると確認される前に(ウイルス感染症などに)処方される事も多々あるが、効果は保証されていない。開発の経緯オフロキサシンは、最初のキノロン系抗生物質であるノルフロキサシンに次ぐ広域抗生物質として1980年代前半に開発された。1985年4月に日本で錠剤が承認され、点眼液・眼軟膏は1987年6月に、点耳液は1992年3月に承認を受けた。米国では1990年12月に承認された。海外では上記の他に内用液、注射液、原虫感染症治療薬オルニダゾールとの合剤がある。出典: フリー百科事典『ウィキペディア(Wikipedia)』救急集中治療領域と外科領域における実例に学ぶ重症感染症治療
2021.05.14
コメント(0)
-

セフトリアキソン
1982年セファロスポリン系抗生物質、セフトリアキソン(ceftriaxone:CTRX)が開発された。セフトリアキソン(Ceftriaxone)はセフェム系の抗生物質。先発商品名はロセフィンで、日本では中外製薬が製造販売していた。第三世代セファロスポリンの一つであり、細菌の細胞壁合成を阻害して抗菌作用を発揮する。概要多数の細菌感染症に処方される抗生物質である[1]。処方される細菌感染症は中耳炎、心内膜炎、髄膜炎、肺炎、骨と関節の感染症、腹腔内感染症、皮膚感染症、尿路感染症、淋病、骨盤腹膜炎などがある。また、手術前や咬傷後の感染症予防などにもしばし用いられる。 セフトリアキソンの投与法は点滴または筋肉注射である。セフトリアキソンは1980年代初めにホフマン・ラ・ロシュによって発見された。WHO必須医薬品モデルリストに含まれ、最も効果的で安全な医療制度で必要とされる医薬品である。すでに特許は切れており、後発医薬品として入手できる。2014年の先進国では1投与の価格は約$0.20-$2.32米ドルである。米国での治療費は通常$25米ドル以下である。日本では中外製薬がロシュからライセンスを受けて販売していたが、特許切れに伴い販売権を2018年末までに太陽ホールディングスに売却した。適応症適応菌種セフトリアキソンに感受性のあるブドウ球菌属、レンサ球菌属、肺炎球菌、淋菌、大腸菌、シトロバクター属、クレブシエラ属、エンテロバクター属、セラチア属、プロテウス属、モルガネラ・モルガニー、プロビデンシア属、インフルエンザ菌、ペプトストレプトコッカス属、バクテロイデス属、プレボテラ属(プレボテラ・ビビアを除く)適応症敗血症、咽頭・喉頭炎、扁桃炎、急性気管支炎、肺炎、肺膿瘍、膿胸、慢性呼吸器病変の二次感染、膀胱炎、腎盂腎炎、精巣上体炎(副睾丸炎)、尿道炎、子宮頸管炎、骨盤内炎症性疾患、直腸炎、腹膜炎、腹腔内膿瘍、胆嚢炎、胆管炎、バルトリン腺炎、子宮内感染、子宮付属器炎、子宮旁結合織炎、化膿性髄膜炎、角膜炎(角膜潰瘍を含む)、中耳炎、副鼻腔炎、顎骨周辺の蜂巣炎、顎炎副作用一般的な副作用は注射患部の痛みとアレルギー反応である。その他の副作用にはクロストリジウム・ディフィシル関連の下痢、溶血性貧血、胆石、てんかん発作などがある。ペニシリンによってアナフィラキシー を起こす人には勧められないがアレルギー反応が軽度な人には使用される。静脈点滴注射投与の場合、カルシウム点滴の併用は避けるべきである。セフトリアキソンは妊娠中や授乳中でも比較的安全に投与できることが暫定的に証拠づけられてる。出典: フリー百科事典『ウィキペディア(Wikipedia)』【送料無料】 エビデンスに基づくQ & Aでわかる皮膚感染症治療 / 宮地良樹 【本】
2021.05.13
コメント(0)
-

ラタモキセフ
1981年オキサセフェム系抗生物質、ラタモキセフ(latamoxef:LMOX)が開発された。出典: フリー百科事典『ウィキペディア(Wikipedia)』サンフォード感染症治療ガイド 日本語版 2018 ライフサイエンス出版 デーヴィド・N.ギルバート /
2021.05.12
コメント(0)
-

ピペラシリン
1980年ペニシリン系抗生物質、ピペラシリン(piperacillin:PIPC)が開発された。ピペラシリン(Piperacillin)は広域スペクトラムの β-ラクタム抗生物質 、中でもウレイドペニシリン・クラスのひとつ。 日本での製品名は「ペントシリン」(富山化学工業製造販売)。ピペラシリンとその他のウレイドペニシリンの化学構造は、極性側鎖を持つ。これはグラム陰性菌に対して高い浸透性と、グラム陰性菌βラクタマーゼによる分解感受性を低下させる。 これらの性質は病院での重要な病原菌である緑膿菌に対する活性を持つ。 このような性質から、ピペラシリンはときに「抗緑膿菌ペニシリン」と呼ばれる。ピペラシリンは単独で用いられる時には 黄色ブドウ球菌のなどのグラム陽性菌への強い活性を持たない。またβ-ラクタム構造は細菌の β-ラクタマーゼで加水分解される。ピペラシリンは最も一般的には β-ラクタマーゼ阻害剤であるタゾバクタム(Piperacillin/Tazobactam)(製品名「ゾシン」「タゾシン」「Zosyn」または「Tazocin」)とピペラシリンとの組み合わせで用いられる。タゾバクタムは多くのβラクタマーゼを阻害する。ピペラシリン・タゾバクタムの合剤は MRSAに対しては投与されない。他のペニシリン/βラクタム系抗生物質同様、MRSAのペニシリン結合蛋白に結合しないからである。薬理抗菌作用ピペラシリンは緑膿菌を含むグラム陰性菌、腸球菌属を含むグラム陽性菌、またバクテロイデス属を含む嫌気性菌に対し効果があり、幅広い抗菌スペクトルを有する。グラム陰性のインフルエンザ菌に対するMIC90は2μg/mL、グラム陽性の肺炎球菌に対するMIC90は2μg/mLであり、セフェム系のフロモキセフより優れた抗菌力を示した(in vitro)。作用機序細菌の細胞壁合成を阻害し、殺菌作用を有する。医療ピペラシリンは、βラクタマーゼ阻害剤タゾバクタムとの組み合わせで、深刻な院内感染でしばしば用いられる。 この組み合わせのが最も広く使用されている。低コストの後発医薬品を用いているにもかかわらず、米国の非連邦病院では総額388百万ドルが使われている。ピペラシリン・タゾバクタムは、多剤耐性菌の院内感染が疑わる場合の推奨されている三剤処方の一つである。またこれは嫌気性グラム陰性桿菌の感染症に対する推奨される抗菌剤の一つである。ピペラシリン・タゾバクタムはNIHにより、好中球減少に伴う敗血症の初期経験的治療に推奨されている。副作用ピペラシリン・タゾバクタム合剤の最も一般的な副作用は、下痢、便秘、吐き気、頭痛や不眠である。あまりみられない副作用には、アナフィラキシー、Stevens-Johnson症候群、 Clostridium difficile 関連下痢等がある。投与ピペラシリンは経口投与では吸収されず、 静脈内 または 筋肉内注射により投与される。持続投与と間欠投与の特徴も検討されている。出典: フリー百科事典『ウィキペディア(Wikipedia)』抗菌薬ポケットガイド これで安心感染症治療のコツ
2021.05.11
コメント(0)
-

チカルシリン
1975年ペニシリン系抗生物質、チカルシリン(ticarcillin:TIPC)が開発された。出典: フリー百科事典『ウィキペディア(Wikipedia)』エビデンスに基づく感染症治療マニュアル
2021.05.10
コメント(0)
-

バカンピシリン
1975年ペニシリン系抗生物質、バカンピシリン(bacampicillin:BAPC)が開発された。バカンピシリン(Bacampicillin)とはペニシリン系抗生物質の一つ。アンピシリンのプロドラッグであり、バイオアベイラビリティが改善されている。Spectrobid (ファイザー)とenglobe (アストラゼネカ)の商品名で販売されている。出典: フリー百科事典『ウィキペディア(Wikipedia)』救急集中治療領域と外科領域における実例に学ぶ重症感染症治療
2021.05.09
コメント(0)
-

フォスフォマイシン
1973年 フォスフォマイシン(fosfomycin:FOM)が開発された。ホスホマイシン(Fosfomycyn、Phosphomycin、Phosphonomycin)とは、ストレプトマイセス属の真正細菌が産生する抗菌スペクトルの広い抗生物質の一つである。商品名ホスミシン。カルシウム塩が経口剤、ナトリウム塩が注射剤と点耳剤として製造されている。構造は単純で類似構造を持つ抗生物質は未だに確認されていない。禁忌製剤成分に過敏症の既往を有する患者のほか、低張性脱水症の患者は脱水が増悪する可能性があるので注射剤は禁忌である。副作用経口剤の添付文書に記載されている重大な副作用は、血便を伴う重篤な大腸炎(偽膜性大腸炎等)である。注射剤にはそれに加えて、ショック、アナフィラキシー様症状、汎血球減少、無顆粒球症、血小板減少、肝機能障害、黄疸、痙攣が記載されている。点耳剤に重大な副作用は設定されていない。効能・効果ホスホマイシンが有効な以下の菌株グラム陽性菌:ブドウ球菌属☆※*、グラム陰性菌:大腸菌☆※、セラチア属☆※、プロテウス属☆※*、モルガネラ・モルガニー☆※、プロビデンシア・レットゲリ☆※、緑膿菌☆※*、赤痢菌※、サルモネラ属※、カンピロバクター属※が原因である敗血症☆、急性気管支炎☆、肺炎☆、肺膿瘍☆、膿胸☆、慢性呼吸器病変の二次感染☆、膀胱炎☆※、腎盂腎炎☆※、感染性腸炎※、腹膜炎☆、バルトリン腺炎☆、子宮内感染☆、子宮付属器炎☆、子宮旁結合織炎☆、深在性皮膚感染症※、涙嚢炎※、麦粒腫※、瞼板腺炎※、中耳炎※*、外耳炎*、副鼻腔炎※☆:注射剤に記載、※:経口剤に記載、*:点耳剤に記載ホスホマイシンは各種の尿路感染症に短期間大量投与される。単回経口多量投与の報告もある。 トブラマイシンとの合剤が嚢胞性線維症患者の肺感染症治療に応用された。ホスホマイシンの忍容性は高く、副作用は少ないとされるが、治療中の耐性の出現率が高く、重症感染症の治療継続ができない場合が多い。小児ならびに75歳以上の高齢者には推奨されない。さらなる使用方法が提案されている。 世界的な耐性菌出現が近年問題視されている。動物用医薬品としては、牛の大腸菌性下痢症及びサルモネラ症に使用され、飼料添加物としても使用されている。また、すずき目魚類の類結節症及びエドワジェラ症に対して飼料添加物として使用される。作用機序ホスホマイシンはMurAと呼ばれるUDP-N-アセチルグルコサミンエノールピルビン酸トランスフェラーゼ酵素を失活させる事で殺菌的に作用する。MurAはペプチドグリカンの生合成過程の内、ホスホエノールピルビン酸(PEP)をUDP-N-アセチルグルコサミンの3'位の水酸基へ移動させる役割を持っており、このピルビン酸基はペプチドグリカンのペプチド部分とグリカン部分を繋ぐ役目を果たす。ホスホマイシンはPEPの代わりにMurAに結合し、その活性部位であるシステイン残基(Escherichia coli の場合は115番)をアルキル化して作用を封じる[12]。この様にホスホマイシンは、細菌の細胞壁のペプチドグリカン合成を阻害することにより抗菌力を発揮する。βラクタム系の様に細胞壁のムレイン架橋を阻害するのではなく、ムレイン単体生合成を阻害することが特徴である。ムレイン単体合成阻害薬には他にバンコマイシンがある。ホスホマイシンはバクテリア体内へグリセロールリン酸輸送体にて取り込まれる。抗菌スペクトルと感性ホスホマイシンの抗菌活性はグラム陽性菌とグラム陰性菌の両方に対して有効であり、E. faecalis、E. coli、シトロバクター属、プロテウス属等のグラム陰性菌を殺菌できる。低pH環境下ではより活性が強く、尿中に未変化の活性体が排泄されるので尿路病原菌起因性の予防・治療に適している。 注目すべき点は、S. saprophyticus、クレブシエラ属、エンテロバクター属に対する活性一定ではないので、最小発育阻止濃度(MIC)を確認した上で用いるべきである点であろう。他の抗生物質と交差耐性を持たないので、基質特異性拡張型βラクタマーゼ(ESBL)を産生する病原体に対する活性は、特にESBL産生型E. coli において良好または著効である。 ホスホマイシンに感性の起因菌による単純性尿路感染症に対する臨床データがある。しかし、感性の判断基準である64mg/Lは全身性感染症については適用すべきでない。欧州抗菌薬感受性試験委員会(EUCAST)は、感性の基準として32mg/Lを採用している。急性毒性LD50:1,200mg/kg(ナトリウム塩、マウス投与時)耐性非必須なグリセロールリン酸輸送体の不活性化によってホスホマイシン耐性が出現する。ホスホマイシン耐性酵素ホスホマイシンの耐性に寄与する酵素群の遺伝子が、染色体とプラスミドの両方から見付かっている。ホスホマイシン耐性に関する3つの遺伝子(FosA、FosB、FosX)はグリオキシラーゼに分類される酵素をコードする。これらの酵素はホスホマイシンの1位の炭素に求核反応してエポキシ環を開き、ホスホマイシンを不活化させる。求核反応に用いる基質に応じてFosA(グルタチオン)、FosB(バシリチオール)、FosX(水(H2O))に分類されている。一般にFosAおよびFosXはグラム陰性菌が、FosBはグラム陽性菌が産生する。FosCはホスホマイシンにATPのリン酸基を転移させる酵素であり、この反応によってもホスホマイシンは不活化される。生合成遺伝子群Streptomyces fradiae が持つホスホマイシンを生合成する遺伝子群を全てStreptomyces lividans に移植する試みが2006年に成功した。開発の経緯ホスホマイシンは最初、土壌サンプルの培養液中に含まれていたStreptomyces fradiaeから、発育中のバクテリアをスフェロプラスト化させた事から発見され、1969年に出版された論文集の中で報告された。1971年に工業的に生産される様になった。出典: フリー百科事典『ウィキペディア(Wikipedia)』小児感染症治療ハンドブック2020-2021 [ 尾内 一信 ]
2021.05.08
コメント(0)
-
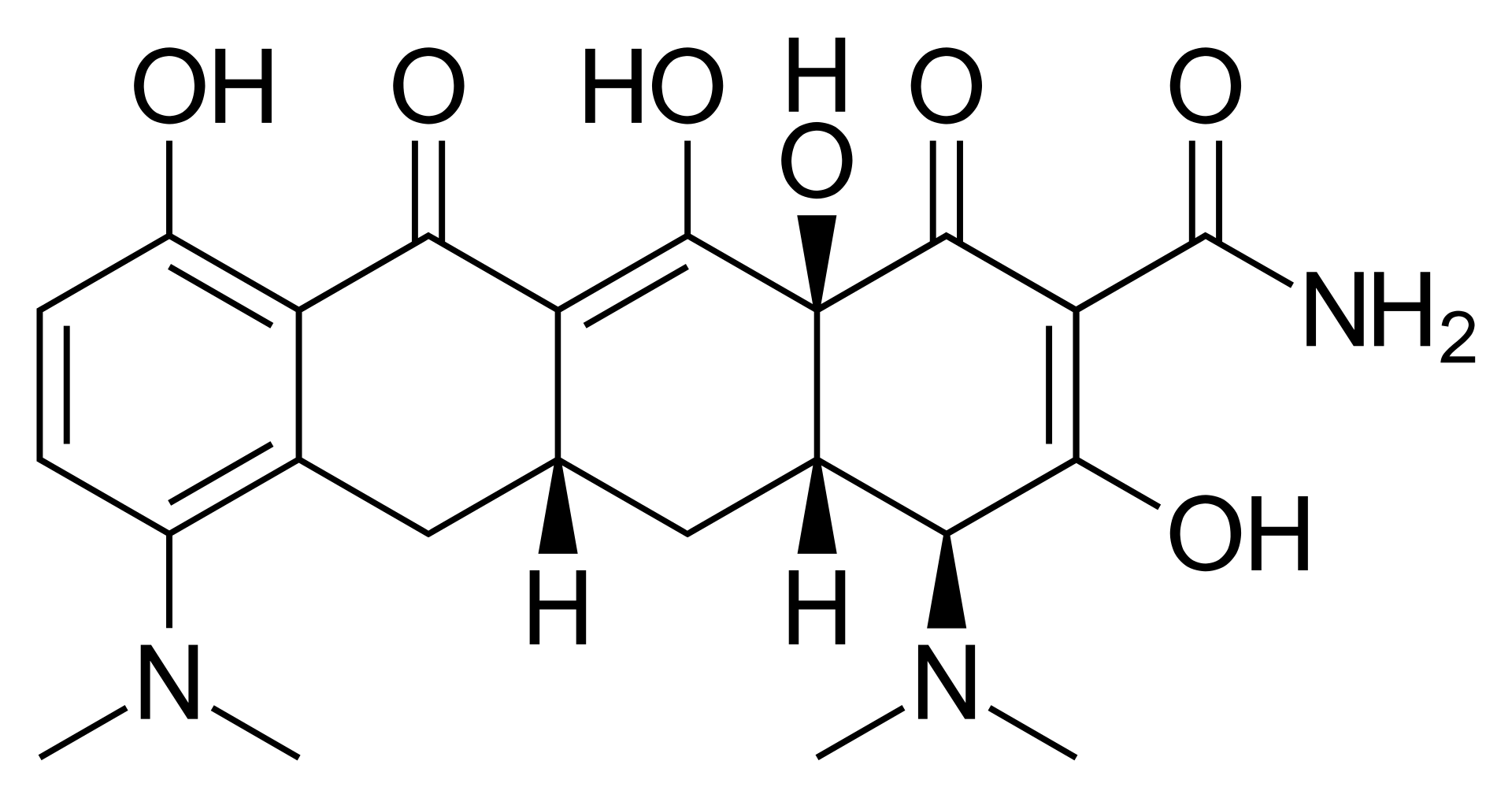
ミノサイクリン
1972年テトラサイクリン系抗生物質、ミノサイクリン(minocycline:MINO)が開発された。ミノサイクリン(英: Minocycline)は、広域スペクトル性のテトラサイクリン系抗生物質であり、静菌性の抗生物質に分類される。テトラサイクリン系としては脂溶性が高く、組織移行性が良好で生体内半減期も長い。経口摂取時の生物学的利用能が100%に近い。動物用医薬品としても使用される。アメリカ食品医薬品局FDAは、2008年に甲状腺疾患、小児自己免疫疾患など重篤な副作用との関連が見出している。コクラン・レビューもある種の自己免疫疾患の発症リスクの上昇を見出した。天然に存在する抗生物質ではなく、1966年に米国のレダリー研究所によって天然テトラサイクリンから半合成された物質[2]。特徴抗菌作用主に皮膚感染症やライム病の治療に使用され、テトラサイクリン系抗生物質の中でも第一選択となることが多い。これはドキシサイクリンと並び生体内半減期が長いため、1日の服薬回数が少なくて済むことと、テトラサイクリン系抗生物質に対する耐性菌にも効果が期待できるためである。β-ラクタム系耐性菌に有効な場合があり、β-ラクタム耐性アシネトバクターによる疾患や、一部のMRSA感染症の治療に使用されることもある。髄膜炎菌への活性も有するなど、他のテトラサイクリン系よりも幅広い抗菌スペクトルであるが、予防投与は副作用(目眩や光線過敏)の問題と耐性のつきやすさのために現在は推奨されていない。動物のリボソーム80Sには作用せず、細菌のリボソーム70Sに特異的に作用すると報告されている、細菌のリボソーム30Sサブユニットに特異的に作用することから、選択毒性を有すると報告されている。適応妊娠中や妊娠の可能性がある場合は他のテトラサイクリン系と同様に選択されない。小児に対しては第一選択とならない。特に8歳未満の小児において歯牙の着色やエナメル質形成不全、また、一過性の骨発育不全などを起こす可能性があるためである。しかし耐性などの問題で本剤以外に選択肢がない場合は例外となりうる。ミノサイクリンに感受性のある菌種は、ブドウ球菌属、レンサ球菌属、肺炎球菌、腸球菌属、淋菌、炭疽菌、大腸菌、赤痢菌、シトロバクター属、クレブシエラ属(肺炎桿菌を含む)、エンテロバクター属、緑膿菌、梅毒トレポネーマ、リケッチア属、クラミジア属、マイコプラズマ、アメーバ性赤痢、炭疽症、コレラ、淋病(ペニシリンが投与できない場合)、融合性細網状乳頭腫症(グジュロー・カートイド症候群)、ライム病、腺ペスト、歯周病、肺炎など呼吸器疾患、ロッキー山紅斑熱、梅毒、尿路感染症、直腸の感染症、ある種の微生物感染による子宮頚部の症状など。適応だけを見ればそうだが、実際には例えば淋病では2016年には7-8割の例で耐性を持つため、治療薬剤としての推奨にはない。主な適応症皮膚/骨格系表在性皮膚感染症、深在性皮膚感染症、リンパ管・リンパ節炎、外傷・熱傷及び手術創による二次感染、乳腺炎、骨髄炎呼吸器系咽頭炎、喉頭炎、扁桃炎、気管支炎、肺炎、肺膿瘍、慢性呼吸器病変の二次感染泌尿器系/生殖器系膀胱炎、腎盂腎炎、前立腺炎、精巣上体炎、尿道炎、淋菌感染症、梅毒、外陰炎、細菌性膣炎、子宮内感染消化器系/腹腔内臓器腹膜炎、感染性腸炎感覚系器官涙嚢炎、麦粒腫、外耳炎、中耳炎、副鼻腔炎、化膿性唾液腺炎歯科領域歯周組織炎、歯冠周囲炎、上顎洞炎、顎炎全身性感染症炭疽、つつが虫病、オウム病ほかエイズ患者のトキソプラズマ症に対する 土壇場治療薬としても使用されている。アメリカ合衆国ではリウマチ学会のホームページに他の治療より効果的でないため一般的には使用されないが、たまに使用されることがあると記される。動態アルミニウム・カルシウム・マグネシウムを含有している制酸剤、または鉄含有製剤によって損なわれるが、乳製品を含む食事と同時にミノサイクリンを摂取しても、吸収の程度と時間は、絶食条件下との差は認められなかった。出典: フリー百科事典『ウィキペディア(Wikipedia)』AMINOMYSIN 30mg【アミノマイシン】
2021.05.07
コメント(0)
-

アモキシシリン
1972年ペニシリン系抗生物質、アモキシシリン(amoxicillin:AMPC)が開発された。アモキシシリン (Amoxicillin) は、細菌感染症の治療に用いられる、近年開発されたβ-ラクタム系抗生物質の一つである。ペニシリン系抗生物質に属する。構造は、ほとんどアンピシリンと同じだが、腸からの吸収性が良いことから、経口摂取薬として用いられる。アモキシシリンはβ-ラクタマーゼ産生微生物による分解を受けやすく、分解を避けるためにクラブラン酸と一緒に供されることがある。1972年にビーチャム(現在のグラクソ・スミスクライン)によって開発された。日本では協和発酵キリンがパセトシン、アステラス製薬がサワシリンの商品名で販売するほか、様々な後発医薬品が存在する。作用機構アモキシシリンは、微生物の細胞壁の合成を阻害することによって効果を発揮する。これは、グラム陽性菌の細胞壁の主成分であるペプチドグリカン鎖間の架橋を阻害する。出典: フリー百科事典『ウィキペディア(Wikipedia)』感染と抗菌薬(18-3) 特集:これからを見据えた呼吸器感染症治療
2021.05.06
コメント(0)
-

セファレキシン
1970年 セファロスポリン系抗生物質、セファレキシン(cephalexin:CEX)が開発された。セファレキシン(Cefalexin)は、多数の細菌感染症に用いられる抗生物質である。グラム陽性菌と一部のグラム陰性菌の細胞壁の成長を攪乱(かくらん)することにより殺菌する。セファレキシンは第一世代のセファロスポリンのβ-ラクタム系抗生物質である。 同じ第一世代のセファロスポリン、静脈内投与のセファゾリンと同様の作用があるが投与法は経口である。セファレキシンは特定の細菌感染症:中耳炎、骨髄炎、関節炎、皮膚炎、尿路感染症などの治療に用いられる。 また特定の肺炎、レンサ球菌咽頭炎、感染性心内膜炎の予防にも使用される。 セファレキシンはメチシリン耐性黄色ブドウ球菌(MRSA)、腸球菌、 シュードモナス属による感染症には効果はない。その他の抗生物質と同じく、セファレキシンはウイルス感染症などのインフルエンザ、風邪、急性気管支炎には効かない。 セファレキシンは軽度から中度のペニシリンアレルギーの人にも投与できる。しかし、重度のペニシリンアレルギーの人への投与は推奨されていない。よくある副作用は吐き気や下痢である。アレルギー反応、クロストリジウム・ディフィシル腸炎の感染、一種の下痢をすることもありえる。現在までに、妊娠中または授乳中の女性が摂取することによる赤ちゃんへの悪影響は発見されていない。子供でも65歳以上でも安全に使える抗生物質である。腎不全の人は量を減らして摂取する必要がある。セファレキシンは2012年のアメリカで最も処方された薬トップ100のひとつである。 2013年のカナダでは5番目に最も処方された抗生物質である。オーストラリアでは最も処方される薬トップ15のひとつであるセファレキシンが開発されたのは1967年であり、1969年から1970年にグラクソ・スミスクラインとイーライリリー・アンド・カンパニー がKeflex と Ceporexという名で他多数の企業と最初に市販した。 ジェネリック医薬品バージョンが複数の商号で安価で入手できる。 セファレキシンは医療制度に必要とされる世界保健機関の必須医薬品リストで最も重要な医薬品である。出典: フリー百科事典『ウィキペディア(Wikipedia)』小児感染症治療ハンドブック2020-2021 [ 尾内 一信 ]
2021.05.05
コメント(0)
-
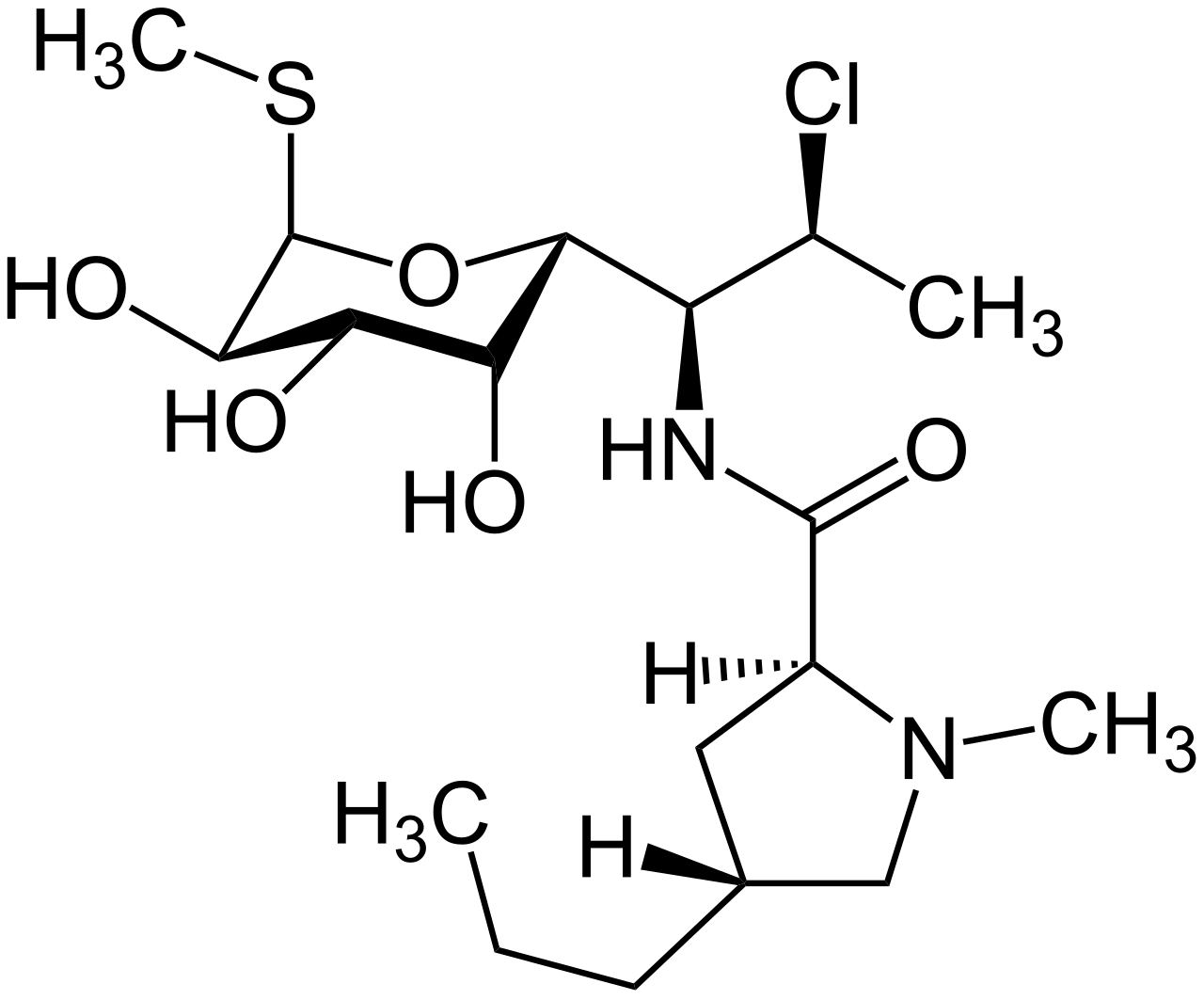
クリンダマイシン
1968年 リンコマイシン系抗生物質、クリンダマイシン(clindamycin:CLDM)が開発された。クリンダマイシンは、リンコマイシン系の抗生物質。 商品名としては先発品にダラシン、ダラシンTゲル、ミドシンなどがある。薬理リボソームの50Sサブユニットを阻害して細菌のタンパク質の合成を阻害する。蛋白合成阻害薬として、機序はマクロライド系抗生物質と同じだが、化学的構造は全く異なる。スペクトラム細菌において、グラム陽性菌、嫌気性菌、マイコプラズマに効能を持つが、グラム陰性菌には効かない。マラリア(キニーネと併用)トキソプラズマ(ピリメタミンと併用)ニューモシスチス(プリマキンと併用)適応症クリンダマイシンは嫌気性菌への抗菌活性のため誤嚥性肺炎や、他の抗菌薬の併用剤として用いられることが多い。中枢神経系への移行は極めて悪く、嫌気性菌による脳膿瘍・髄膜炎などでは用いられない。誤嚥性肺炎グラム陽性菌と嫌気性菌をカバーする。口腔内はレンサ球菌と嫌気性菌が多いため原因菌をカバーできる可能性が高い。口腔内感染症ペニシリンアレルギーがある場合の咽頭炎や副鼻腔炎腹腔内感染症CA-MRSA(市中獲得型MRSA)感染症表在性皮膚感染症、深在性皮膚感染症中耳炎、外耳炎顎骨周辺の蜂巣炎創傷感染症ではグラム陽性球菌であるブドウ球菌が主となることが多いが、クリンダマイシンとST合剤の効果には有意差はなく、ともに有効であった[3]。副作用かつては偽膜性腸炎の原因となることで有名であったが、現在はその他の抗生物質でもほぼ同様に起こりえるため強調されなくなった。苦味が強いため小児では扱いにくい。出典: フリー百科事典『ウィキペディア(Wikipedia)』感染と抗菌薬(18-3) 特集:これからを見据えた呼吸器感染症治療
2021.05.04
コメント(0)
-

リファンピシン
1967年抗結核剤、リファンピシン(rifampicin:REP;リファンピン、rifampin)が開発された。リファンピシン (rifampicin) は抗生物質の一種。分子式C43H58N4O12、分子量822.95の有機化合物。リファンピン (rifampin) ともいう。製品名はリファジン®カプセル150mg(第一三共製造販売)。放線菌の一種 Streptomyces mediterranei が生産するリファマイシンから半合成される。作用機序細菌のRNAポリメラーゼに直接作用してRNA合成の開始反応を阻害することにより抗菌力を発揮する。薬物相互作用リファンピシンは薬物代謝酵素であるCYP3A4の誘導を行うため、この薬物相互作用に対して注意を要する(この酵素によって代謝される薬物の血中濃度を低下させるため、この酵素で代謝される薬が効きにくくなる)。効能・効果適応菌種本剤に感受性を持つマイコバクテリウム属適応症肺結核及びその他の結核症マイコバクテリウム・アビウムコンプレックス(MAC)症を含む非結核性抗酸菌症(NTM)ハンセン病臨床応用結核やハンセン病の治療に用いられることがある。副作用としては肝機能障害などが挙げられる。多剤耐性緑膿菌や多剤耐性アシネトバクター・バウマニの感染症に対してコリスチンとの併用療法に用いられることがある(この場合、保険適用外使用となるため健康保険が効かない)。コリスチンとリファンピシンの併用療法はin vitro及びin vivoで相乗効果があることが確認されている。CYP3A4で代謝される薬は薬物相互作用に気をつけなければならない。特にHIVプロテアーゼ阻害薬、デラルビシン、ボリコナゾール、プラジカンテルは併用禁忌となっている。日本では第一製薬(現第一三共)、科研製薬、日本チバガイギー(現ノバルティス)などから販売されており、1996年に厚生大臣より希少疾病用医薬品の指定を受けた。分子生物学での利用リファンピシンは他の抗生物質に比べ自然耐性をもたれやすい。そのため、大腸菌の可逆的リファンピシン耐性変異株を利用することで、in vivoにおけるRNA合成を開始段階で同調させることができる。また、RNAの伸長反応は阻害しないので、オペロンの構造分析にも利用できる。認知症への応用大阪市立大学の富山貴美研究教授が1994年に「リファンピシン」という薬に、アルツハイマー病の原因となるタンパク質「アミロイドβ(ベータ)」の蓄積を抑える作用があると発表。研究のきっかけとなったのは、92年に報告された、日本のハンセン病患者に関する論文。端的に言うと、ハンセン病患者の人たちは高齢になっても認知症を発症する頻度が極めて低かった。ご承知の通り、ハンセン病患者は当時の国の政策によって長期にわたって外界から隔絶され、しかも、同じ薬を投与され続けてきた。主な薬はダプソン、クロファジミン、そしてリファンピシン。これらの薬を入手して「アミロイドβ」の凝集を防げるか調べたところ、最も顕著に効果が現れたのがリファンピシンだった。その後、原因タンパク質の小さな集合体であるオリゴマーの形成を抑えることができるかを調べると、ここでもリファンピシンが断トツで優れた結果をもたらした。さらに研究を重ね、リファンピシンはアミロイドβだけでなく、タウやαシヌクレインといった、様々な原因タンパク質のオリゴマー形成も抑制することが判明。これにより、リファンピシンがアルツハイマー病だけでなく、脳の神経細胞が徐々に失われることで発症する、他のタイプの認知症にも効く可能性が示された。出典: フリー百科事典『ウィキペディア(Wikipedia)』[書籍のゆうメール同梱は2冊まで]/抗生物質と人間 マイクロバイオームの危機[本/雑誌] (岩波新書 新赤版 1679) / 山本太郎/著
2021.05.03
コメント(0)
-

ドキシサイクリン
1966年 テトラサイクリン系抗生物質、ドキシサイクリン(doxycycline:DOXY)が開発された。ドキシサイクリン(英: Doxycycline)は、メタサイクリンから化学的に合成されたテトラサイクリン系の抗菌薬である。日本での先発品は、ファイザーのビブラマイシン。グラム陽性菌やグラム陰性菌、リケッチア、マイコプラズマ、クラミジアなどへ、広い抗菌作用を示す。細菌の蛋白合成を阻害し、静菌性の抗生物質に分類される。特に脂溶性が強く、経口投与での吸収が極めて良好、組織内移行も良好で長時間持続する。一般的な副作用は、消化器系(食欲不振や悪心、嘔吐、腹痛、下痢など)と皮膚障害(発疹や蕁麻疹、光線過敏など)である。可逆的な遺伝子発現調整の実験系であるTet on/offシステムに用いられる。特徴ドキシサイクリンは、その化学構造からテトラサイクリン系の抗菌薬に分類される。経口用の薬剤100 mg、1錠当たりの卸売価格は、0.01-0.02アメリカドルと非常に安価な薬剤として知られる。なお、放出制御によって徐放化された製剤も存在する 。作用機序ドキシサイクリンの抗菌作用の作用機序は、他のテトラサイクリン系抗菌薬と同様に、細菌に取り込まれたものが、細菌の持つリボソームの30Sサブユニットに可逆的ながら比較的強く結合し、タンパク質の合成に阻害をかけることによる。すなわち、細菌のリボソームを一時的に使用不能にして、細菌に必要なタンパク質を生合成できないようにすることによって、細菌の増殖を一時的に阻止する。なお、細菌などの原核生物のリボソームは30Sと50Sサブユニットから成っているのに対して、ヒトなど真核生物のリボソームは40Sと60Sであるため、真核生物のリボソームに対しては、その機能を効果的に阻害することは難しい。したがって、ドキシサイクリンは原核生物に対して選択毒性を持つ。ドキシサイクリンに対して耐性を持たない細菌に対する最小発育阻止濃度(MIC)は、0.03 (μg/ml)から0.12 (μg/ml)程度である。ただし、ドキシサイクリンに対して耐性を持つ細菌も存在する。薬物動態吸収ドキシサイクリンをヒトに対して空腹時に経口投与した場合の吸収は速やかであり、最高血中濃度到達時間は約3時間とされる。ところで、一般的なテトラサイクリン系の抗菌薬は、その化学構造からカルシウムイオンなどと難溶性の複合体を生成しやすく、例えばカルシウムを多く含む食品と同時に摂取すると、吸収が阻害される。しかし、ドキシサイクリンの場合は他のテトラサイクリン系の抗菌薬とは異なり、乳汁や食物と同時に摂取しても、最高血中濃度到達時間こそ空腹時よりも遅くなるものの、ドキシサイクリンの吸収自体には支障が起こらない。分布体内に吸収されたドキシサイクリンは、腎臓への移行性が最も高い[2]。ただ、ドキシサイクリンは、その化学構造上の特徴のために、他のテトラサイクリン系の抗菌薬と比べても比較的脂溶性が高いとされており、同じテトラサイクリン系抗菌薬のミノサイクリンほどではないものの、ドキシサイクリンもまた中枢移行性がテトラサイクリン系抗菌薬の中では比較的高い。脳中濃度は血中濃度の約30%とも言われる[7]。また、血中濃度の11-56%が脳脊髄液中に移行する報告もある。この他、ドキシサイクリンはタンパク結合率も高く、したがって、過量投与時に血液透析を行っても効果的に除去できない。代謝・排泄ヒトにおけるドキシサイクリンの血中濃度半減期は12時間前後と、テトラサイクリン系の抗菌薬としては比較的長い。このため、ドキシサイクリン感受性の細菌に対しては、1日1回投与で充分に効果を上げられるとされている。参考までに、健康なヒトに対する200 mg経口単回投与の72時間後の血中濃度ですら、約0.07 (µg/ml)であった。これは、上記のドキシサイクリン感受性菌の最小発育阻止濃度に近い値である。このように経口投与72時間経過後でも感受性菌の最小発育阻止濃度を下回るか下回らないかといった血中濃度が維持されるため、ヒトにおいてはドキシサイクリンの効果は長時間持続すると考えられる。なお、ドキシサイクリンは腎臓への移行性が最も高く、健康なヒトでは主に尿中に排泄されるものの、尿中の他に、胆汁中にも排泄される。このためドキシサイクリンは、腎不全のヒトに対しても、投与量を減量する必要のないテトラサイクリン系の抗菌薬とされる。適応適応菌種ブドウ球菌属、レンサ球菌属、肺炎球菌、淋菌、炭疽菌、大腸菌、赤痢菌、肺炎桿菌、ペスト菌、コレラ菌、ブルセラ属、Q熱、リケッチア(コクシエラ/ブルネティ)、クラミジア属適応症皮膚/骨格系感染症表在性皮膚感染症(丹毒など)、深在性皮膚感染症(蜂窩織炎など)、リンパ管炎・リンパ節炎、慢性膿皮症、外傷/熱傷及び手術創等の二次感染、乳腺炎、骨髄炎上気道/下気道感染症咽頭炎、喉頭炎、扁桃炎、急性気管支炎、肺炎、慢性呼吸器病変の二次感染尿路感染症/生殖器感染症膀胱炎、腎盂腎炎、前立腺炎、尿道炎、淋菌感染症、子宮内感染、子宮付属器炎(骨盤腔内感染)消化器感染症感染性腸炎、コレラ感覚器感染症眼瞼 膿瘍、涙嚢炎、麦粒腫、角膜炎、中耳炎、副鼻腔炎、歯冠周囲炎、唾液腺炎全身性感染症猩紅熱、炭疽、ブルセラ症、ペスト、Q熱、オウム病応用マラリア予防:マラリア原虫に対してもある程度の効果があり、予防内服あるいは他の抗マラリア剤と併用して治療に用いられることもある。メフロキンの副作用を倦厭して、その代替薬として使用される場合もある。ただし、「副作用の節」に書かれているように、第1選択薬としてはドキシサイクリンを使わない。有効性2016年改定の日本皮膚科学会による尋常性ざ瘡治療ガイドライン2016において、「推奨度 A」で強く推奨されている。1970年の文献を根拠に、ドキシサイクリン50mgとミノサイクリン100mgの同等性が示されているとした。EUのガイドラインではミノサイクリンよりも推奨されていると紹介されている。副作用は光線過敏があるが、中止により軽快し、その他の腹痛や頭痛などは軽微なものであるとした。なお、ドキシサイクリンは痤瘡(にきび)の適応はない。性感染症の尿路へのクラミジアトラコマティス感染に対して、アジスロマイシンは97%に有効であり、ドキシサイクリンは100%に有効であった。出典: フリー百科事典『ウィキペディア(Wikipedia)』【指定第2類医薬品】テラ・コートリル軟膏a 6G赤ニビキなどに
2021.05.01
コメント(0)
-
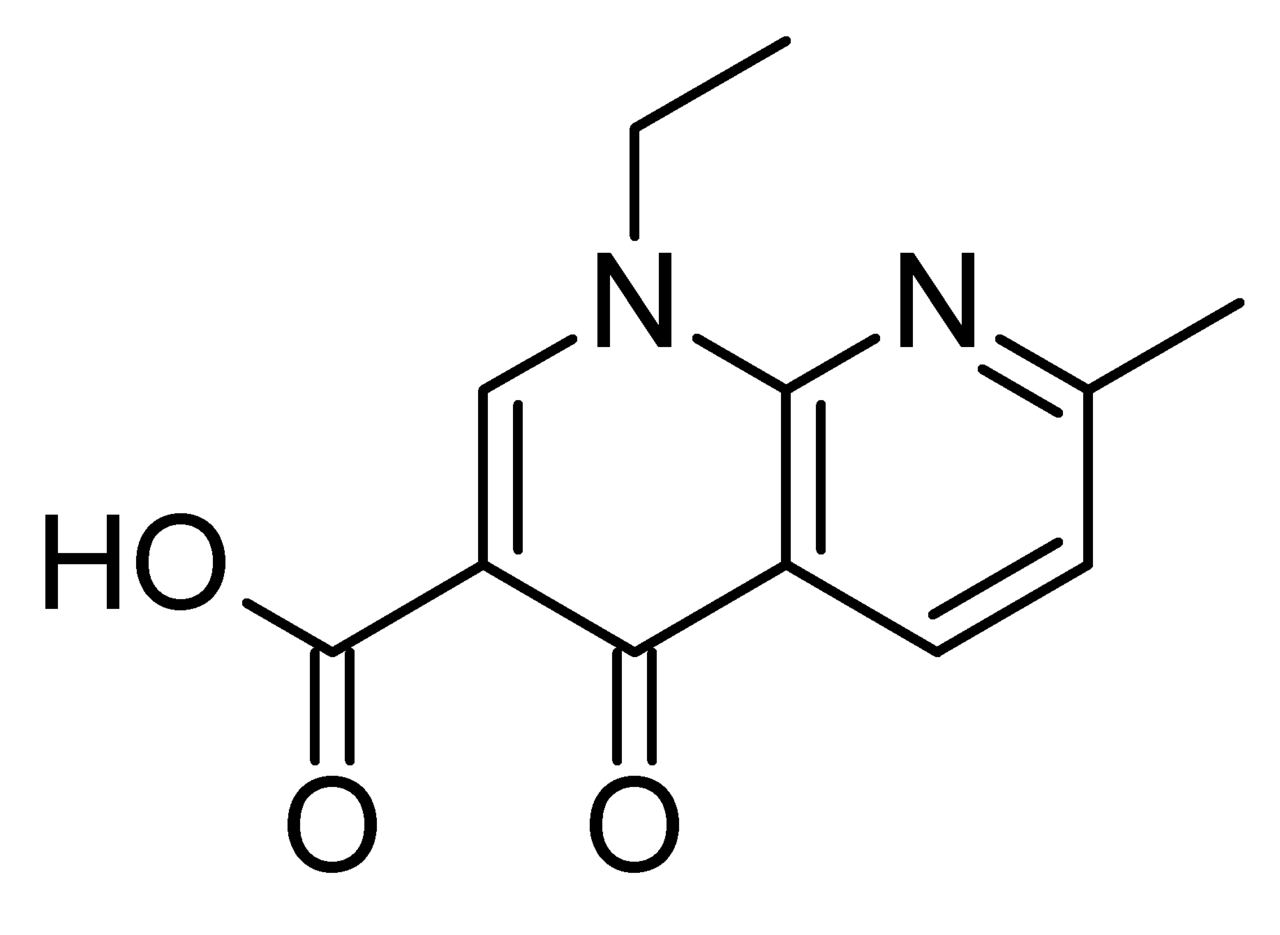
ナリジクス酸
1964年キノロン系抗菌剤、ナリジクス酸(nalidixic acid:NA)が開発された。ナリジクス酸(ナリジクスさん、Nalidixic acid)とは、1962年にウィンスロップ・ラボラトリー社により開発(化学合成)された抗菌剤の一種である。日本では第一製薬によりウイントマイロンという商品名で販売された(現在は第一三共製造販売ののちに販売中止」)。社名(ウインスロップ社、Winthrop)由来の前半と、抗生物質と区別するために後半をマイシン(mycin)ではなくマイロン(mylon)として、ウイントマイロン(WINTO+MYLON)と命名された。この化合物は最初に発見されたキノロン系抗菌剤であり、第一世代キノロンに分類されている。ナリジキシン酸(ナリジキシンさん)とも呼ばれる。主にグラム陰性菌に対して効果を発揮するが、のちにレボフロキサシンをはじめとする、グラム陽性菌にも効果を発揮するニューキノロンと呼ばれる抗菌薬群も開発された。活性ナリジクス酸は他の多くのキノロン系抗菌剤と同じように、DNAジャイレースを阻害することによって効果を発揮する。DNAジャイレースが阻害されると、染色体中のDNAは正常な二重らせん構造を取れず、DNAの複製と転写が阻害される。その結果、細菌はタンパク質を合成できなくなり、死に至る。しかし、細菌がナリジクス酸に対する耐性を獲得するスピードが早かったため、現在ではやや時代遅れの薬剤である。アメリカでは、他に毒性が低く抗菌作用の高いニューキノロン系薬剤があるという理由から、すでに臨床利用されていないが、日本でも2017年11月末をもって販売中止となった。主な用途尿路感染症に対する治療薬として用いられる。グラム陽性菌のみを選択培養する時にも有効である。効能・効果(以下は販売されていた当時の適応症。現在は販売されていない。)適応菌種本剤に感性の淋菌,大腸菌,赤痢菌,サルモネラ属(チフス菌,パラチフス菌を除く),肺炎桿菌,プロテウス属,腸炎ビブリオ適応症膀胱炎,腎盂腎炎,前立腺炎(急性症,慢性症),淋菌感染症,感染性腸炎副作用重篤な副作用がおこることはあまりない。約5%の患者に消化管副作用(悪心、嘔吐、食欲不振など)が起こる。5%未満の患者に中枢神経系副作用(軽度の頭痛、睡眠障害、めまいなど)が起こる。中枢神経系障害のある患者に用いてはならない。出典: フリー百科事典『ウィキペディア(Wikipedia)』レスピラトリーキノロン系薬最前線改訂版 [ 渡辺彰(医学) ]
2021.04.30
コメント(0)
-

ゲンタマイシン
1964年アミノグリコシド系抗生物質、ゲンタマイシン(gentamycin:GM)が開発された。ゲンタマイシン(英: gentamicin, gentamycin)は、アミノグリコシド(アミノ配糖体)系抗生物質である。英語名称は、正式にはgentamicinという。同じアミノグリコシドのtobramycin、streptomycin、kanamycinとは意図的に異なる綴りが与えられている。これは、これらのStreptomycesに由来する薬物に-mycinの名を与えたのに対し、Micromonospora由来のゲンタマイシンには-micinの名を与えたからである。また、ゲンタマイシンは熱に安定な抗生物質の一つであり、高温高圧滅菌後においても活性を持つ。そのため、ある種の微生物培地の調製に使われる。作用機序ゲンタマイシンは殺菌性の抗生物質で、細菌のリボソーム 30S サブユニットに結合して、蛋白合成を阻害する。他のアミノグリコシド系抗生物質と同様経口投与では無効である。これは、小腸にて吸収された後、門脈を経由して肝臓に到達し、不活化されるためである。そのため、静脈注射、筋肉注射、局所投与。および、軟膏による皮膚への塗布にて利用される。臨床応用ゲンタマイシンは、グラム陰性桿菌による感染症にほぼ専門的に用いられる。殺菌能の高い薬剤で、緑膿菌などの日和見感染症の起炎菌による敗血症に対する効果が高い。また、広範囲の薬剤が無効である腸球菌に対しても、ペニシリン系薬剤と併用することによって相乗効果を発揮する。緑膿菌のほか、大腸菌、インフルエンザ桿菌、クレブシエラ菌、セラチア菌、アシネトバクター、シトロバクター、エンテロバクターなど血液感染の原因となるようなグラム陰性桿菌はほぼ網羅する抗菌スペクトラムを有する。ゲンタマイシンは黄色ブドウ球菌などのグラム陽性菌や、淋菌・髄膜炎菌 のようなグラム陰性球菌、またレジオネラ菌 による感染症には効果がない。アミノグリコシド系抗生物質には、他の抗生物質に比較すると非常に耐性化しにくいという特徴がある。よく似たトブラマイシンとは、ゲンタマイシンが緑膿菌を得意とするに対し、トブラマイシンはセラチア菌により活性が高いという違いが知られている(どちらもよく効く)。緑膿菌に対しては、有効性、また耐性化の予防の観点から、かならずセフタジジムなど他の抗緑膿菌活性を持った薬剤との併用が行われる。敗血症のほかは、腎盂腎炎に主に用いられる。組織移行性が低いので、肺炎などといった主要臓器の感染症に用いられることは少ないが、上記の日和見感染症に対する効果を期待し用いることはある。一方血液脳関門を通過できないため、静脈注射では、髄膜炎には完全に無効である。髄腔内投与を行う場合もあるが、この効果を積極的に支持する科学的根拠はない。また、軟膏製剤もあるが、この使用を正当化するような科学的根拠も乏しい。副作用すべてのアミノグリコシド系抗生物質は耳に対し毒性を持つ。前庭神経に対する毒性は平衡感覚障害をきたし、一方蝸牛神経に対する障害は聴覚障害をおこし、まれに聾にいたる。アミノグリコシドの中で、ゲンタマイシンの聴覚毒性は最も強い。聴覚障害は、薬剤中止によってもあまり改善しない。ゲンタマイシンは高い腎毒性をもち、場合によっては急性腎不全に至ることがある。腎障害は、薬剤中止によって改善することが多い。腎毒性の発症頻度は、ゲンタマイシンの血中最低濃度(トラフ)と相関する。腎障害を予防するため、体重により投与量を調節する。欧米では、ゲンタマイシンの投与量の計算式があるが、日本の保険医療の範囲内でこれに従うことは、よほど体が小さくない限り難しい(投与量が上限をこえてしまう)。治療中は血清中のゲンタマイシン濃度を監視する。出典: フリー百科事典『ウィキペディア(Wikipedia)』感染と抗菌薬(18-3) 特集:これからを見据えた呼吸器感染症治療
2021.04.29
コメント(0)
-

セファロスポリン
1964年セファロスポリン系抗生物質、セファロスポリン(cephalosporin:CEP)が開発された。セファロスポリン(Cephalosporin)は、β-ラクタム系抗生物質の一つの種類で、セファマイシン類やオキサセフェム類と共にセフェム系抗生物質と総称される。ベータラクタム環(四員環ラクタム)にヘテロ六員環がつながった形をしている。抗菌力・抗菌スペクトルの改善が重ねられてきたため、現在では多種多様なセフェム系抗生物質が販売使用されている。消化管吸収は一般に良く、副作用が少ないため頻用される。その反面、耐性菌の出現が問題となっている。歴史セファロスポリンが最初に発見・単離されたのは、サルデーニャ島の排水溝で採取されたCephalosporium acremoniumの培地から1948年にイタリア人科学者ジュゼッペ・ブロツによってである。彼は、腸チフスの原因となるチフス菌に対して効果がある物質を産生する培地に注目していた。1960年代にイーライ・リリー社によりセファロスポリンは上市された。他の多くのセファロスポリンの開発は抗菌剤の年表に詳しい。 また、上記のようにセファロスポリンを始めとする第一世代セフェムなどの薬剤に対して、そのβラクタム環を加水分解、失活させてしまうグラム陰性菌の表層酵素のセファロスポリナーゼが問題視されている。作用機序セファロスポリンはペニシリンと同様な機序で細菌の細胞壁のペプチドグリカン合成に干渉して、架橋のために必要な最終段階のペプチド間結合反応を阻害する。すなわち、ペニシリンの場合はペプチドグリカン合成阻害により、細胞膜が浸透圧に抗しきれず溶菌現象を経て「殺菌作用」として働く場合が多いのに対して、セファロスポリンの場合は、細胞壁の変性により細胞分裂を阻害することで細菌の増殖を抑える場合が多いのでこの作用は「静菌作用」と呼ばれる。両者の違いは阻害する酵素の違いと、ペニシリンが主にグラム陽性菌に対して利用され、グラム陽性菌の細胞壁の場合は溶菌しやすいことにもよる。特徴原型であるセファロスポリンCとペニシリンGとを比べた場合、ペニシリンがほとんどグラム陰性菌に対して作用しないのに対して、セファロスポリンは一部グラム陰性菌にも作用を持つ。また、安定性の面ではセファロスポリンはもともと酸に対する安定性が高く、またペニシリン分解酵素にもある程度の耐性を持つ。1950年代当時は、ペニシリンが細菌感染症治療の主力であったが、ペニシリンは酸に不安定で注射剤以外の利用は困難であり、院内での治療にのみ使用されるのみであった。また1960年代頃からペニシリンは耐性菌の問題が発生し始め、その当時の耐性発現は主にペニシリナーゼによるものであったため、ペニシリナーゼによる不活化を生じないセファロスポリンは徐々にペニシリンと置き換えられるようになった。また、セファロスポリンの場合はペニシリンショックのような重篤なアレルギー症状の発現頻度が低いと言われていた点も挙げられる。第二世代セファロスポリンの頃から、酸に安定な性質から経口剤が開発されるようになり、グラム陰性菌への抗菌スペクトル拡大と共に、通院治療にも利用できる万能感染治療薬としての地位を固め、1980年代以降はセファロスポリンが抗菌剤の主力となった。1980年代に入ると、グラム陽性菌にやや作用の弱い第三世代セフェムに抵抗するメチシリン耐性黄色ブドウ球菌が台頭し、特に大手術で免疫機能の低下した患者に、日和見感染を引き起こす院内感染が問題とされるようになった。すなわち、セフェムが静菌的であり第三世代がグラム陽性菌にやや作用が弱いことで、風邪など軽症患者をも含めたセファロスポリンの多用が、人体とその周囲に常在するグラム陽性菌の中から、耐性菌を選抜する状況を引き起こしたとも考えられている。副作用セファロスポリン側鎖にチオテトラゾールを持つものは、代謝により遊離するチオテトラゾール類がアルデヒドデヒドロゲナーゼを阻害するので、少量のアルコール摂取でも酩酊するので飲まないこと。またペニシリンにアレルギーを持つ者の十数パーセント(5〜15%と言われる)は、セファロスポリンにも感作している。また、偽膜性腸炎を起こしやすいことが知られている。クリンダマイシン(CLDM、リンコマイシン系抗菌薬、商品名ダラシン)などが有名だが、セファロスポリンも同程度の頻度で起こすことが知られている。生合成産生菌におけるセファロスポリンの生合成は、途中まではペニシリン生合成過程と同一であり、ペニシリンNより生合成される。すなわち、ACVトリペプチド (δ-(L-α-amino-adipate)-L-cysteine-D-valine)を出発原料として酵素isopenicillin-N-synthetase (EC 1.21.3.1)によりセファロスポリン類も生合成されている。また3位アミノ側鎖のカルボン酸成分は基質特異性の低い酵素N-acyltransferaseの作用により交換され、Cephalosprin C、P等のセファロスポリン類が生成する。出典: フリー百科事典『ウィキペディア(Wikipedia)』感染と抗菌薬(18-3) 特集:これからを見据えた呼吸器感染症治療
2021.04.28
コメント(0)
-

フシジン酸
1962年合成抗菌薬フシジン酸(fusidic acid:FA)が開発された。フシジン酸 (フシジンさん、fusidic acid) は、クリームおよび点眼剤の形で局所的に使用されることが多い抗生物質であるが、錠剤または注射剤の形で全身投与することも可能である。近年、抗菌剤耐性の獲得が国際的に問題となる中、その使用に新たな関心が向けられている。薬理フシジン酸は、翻訳伸長因子 EF-G のリボソームからの解離を防ぐことで、細菌のタンパク質合成阻害剤として機能する。フシジン酸は、主にブドウ球菌属 (Staphylococcus) やレンサ球菌属 (Streptococcus)、コリネバクテリウム属 (Corynebacterium) などのグラム陽性細菌に効果的である。フシジン酸は、細菌の翻訳を阻害するが菌を殺さない、静菌作用を持つ。フシジン酸は、Fusidium coccineum という菌類に由来するステロイド系の抗生物質である。デンマークのレオファーマ社によって開発され、1960年代に臨床での使用が解禁された。フシジン酸は、Mucor ramannianus や Isaria kogana といった他の菌類からも単離される。薬剤はフシジン酸ナトリウムとして使用が認可されており、韓国、日本、イギリス、カナダ、ヨーロッパ、オーストラリア、ニュージーランド、タイ、インド、台湾で承認されている。化合物のPK/PDプロファイルに基づいた、異なる経口投与レジメンが Taksta としてアメリカ合衆国で臨床開発中である。使用フシジン酸は in vitro で黄色ブドウ球菌 (Staphylococcus aureus) をはじめとして、ほとんどのコアグラーゼ陽性のブドウ球菌、コリネバクテリウム属の種、ほとんどのクロストリジウム属 (Clostridium) の種に対して活性がある。一方、エンテロコッカス属 (Enterococcus) やほとんどのグラム陰性細菌 (ただしナイセリア属 (Neisseria)、モラクセラ属 (Moraxella)、レジオネラ (Legionella pneumophila)、バクテロイデス (Bacteroides fragilis) を除く) に対しては、有用な活性がないことが知られている。フシジン酸は、in vitro でも臨床においても、らい菌 (Mycobacterium leprae) に対して活性があるが、同属の結核菌 (Mycobacterium tuberculosis) に対してはわずかな活性しか示さない。フシジン酸の臨床での利用において重要な点の1つは、メチシリン耐性黄色ブドウ球菌 (MRSA) に対する活性である。MRSA やコアグラーゼ陰性黄色ブドウ球菌を含む、いくつかの米国株の細菌種を対象とした in vitro 感受性試験において、フシジン酸の強力な活性が示されている。薬剤耐性獲得の遺伝的障壁は低い (1ヶ所の点変異で耐性が獲得される) ため、深刻な MRSA 感染の治療に対しては、ヨーロッパやカナダなどで承認されている経口または局所的投与のレジメンで単独で用いてはならず、リファンピシンのような他の抗菌剤と組み合わせて用いるべきである。一方で、病原体が高い薬剤濃度に曝露されているときには耐性選択は低い。高用量の経口投与による単剤療法がアメリカ合衆国で開発中である。フシジン酸の局所的投与は、尋常性痤瘡 (ニキビ) の治療に用いられることがある。ニキビの治療において、フシジン酸はその症状を部分的に改善する効果があることが多い。一方で、フシジン酸のアクネ菌 (Cutibacterium (Propionibacterium) acnes) に対する活性は、ニキビの治療によく用いられる他の抗生物質ほどには高くないことが研究で示されている。また、フシジン酸は他の皮膚や眼用の製品 (Fucibet など) にも含まれていることがあるが、こうした目的での使用については議論がある。フシジン酸は、皮膚感染症以外の適応症についても試験がなされている。フジジン酸が人工関節に関連した慢性骨髄炎患者の治療に効果がある可能性がある、という特例使用事例に基づくエビデンスが存在する。用量フシジン酸は黄色ブドウ球菌の感染に対し、低用量で単独で用いるべきではない。一方で、フシジン酸は高用量での単剤療法としての可能性がある。フシジン酸を含有する局所製剤 (スキンクリームや眼軟膏) の使用は薬剤耐性の獲得と強く関連しており、フシジン酸の単剤療法の継続的使用には反対の声がある。ヨーロッパで用いられている局所製剤は、多くの場合フシジン酸とゲンタマイシンが混合されており、耐性獲得の防止が図られている。フシジン酸ナトリウムの成人用量は、処方される症状に応じて、1日2回 250 mg から最大1日3回 750 mg である (皮膚に用いる場合はより少ない用量である)。錠剤または懸濁液の状態で利用可能である。アメリカ合衆国で臨床開発中の経口投与レジメンは、1日目に 1500 mg を2回、その後は1日2回 600 mg の用量である。In vitro モデルでは、このレジメンでの微生物の耐性選択の可能性は低いことが示されている。静注用製剤も存在するが、静脈に刺激性であり静脈炎を引き起こす。ほとんどの場合は経口服用で非常によく吸収されるので、患者が嚥下可能であれば、たとえ心内膜炎 (心腔の感染) の治療であっても、静脈注射をする必要性はほとんどない。注意妊娠時の安全性のエビデンスは不十分である。動物実験と多年の臨床経験からはフシジン酸には催奇性がないことが示唆されるが、フシジン酸は胎盤関門を通過する。副作用フシジン (Fucidin) の錠剤と懸濁液 (主成分はフシジン酸ナトリウム) は、肝臓に異常を引き起こすことがあり、黄疸 (皮膚や白目が黄色くなること) が引き起こされることがある。これらの症状はフシジンの投与が終了すると回復する。他の関連する副作用には、暗色の尿と通常より軽い便などがある。これらも治療が完了すると元へ戻る[17]。これらの副作用に気づいたときは、医師に相談すべきである。薬剤耐性フシジン酸に対する耐性獲得のメカニズムは、黄色ブドウ球菌でのみ詳細な研究がなされている。最も重要なメカニズムは、染色体上で EF-G をコードする fusA 遺伝子中の点変異である。変異によって EF-G は、フシジン酸が結合できないよう変化する。フシジン酸が単独で用いられている場合、耐性は容易に獲得され、多くの場合治療中に獲得される。他のほとんどの抗生物質と同様、フシジン酸への耐性は他の薬剤と併用時には頻繁には発生しない。これが深刻な黄色ブドウ球菌感染の治療にフシジン酸を単独で用いるべきではない理由である。しかしながら、少なくともカナダの病院で1999年から2005年にかけて集められたデータからは、MRSA やメチシリン感受性黄色ブドウ球菌が耐性を獲得する確率はむしろ低く、局所的に用いられる抗生物質としてはムピロシンのほうがより問題であることが判明した。また、細菌は「fusB型」の耐性を示すこともある。耐性は、プラスミド上に見つかる fusB、fusC、fusD 遺伝子によるものである[21]。fusB型耐性遺伝子の産物は213残基のタンパク質で、EF-G に 1:1 の比で相互作用する。 FusB型タンパク質はフシジン酸とは異なる領域に結合し、EF-G のコンフォメーション変化を引き起こす。これによって EF-G はフシジン酸から解放され、別のリボソームのトランスロケーションに参加できるようになる。FusB型の耐性は MRSA の臨床分離株によく見られ、いくつかのコホートでは70%以上で観察されている。相互作用フシジン酸は、キノロンと拮抗するため併用するべきではない。リファンピシンとの併用によって、フシジン酸の作用は相加的または相乗的となる。2008年8月8日、アイルランド医薬品委員会 (Irish Medicines Board) は、59歳のアイルランド人男性がアトルバスタチンとフシジン酸の併用後に横紋筋融解症を発症して死亡した事例と、類似の3件の事例について調査を行っていると報告した。2011年8月、イギリスの医薬品・医療製品規制庁はで「重篤で致死の可能性のある横紋筋融解症の危険性があるため、フシジン酸 (フシジン) はスタチンと同時に全身投与されるべきではない」と警告する医薬品安全対策情報を出した。出典: フリー百科事典『ウィキペディア(Wikipedia)』抗菌薬の考え方,使い方 ver.4 魔弾よ、ふたたび…
2021.04.27
コメント(0)
-

アンピシリン
1961年ペニシリン系抗生物質、アンピシリン(ampicillin:ABPC)が開発された。アンピシリン(Ampicillin)とは、1961年から感染症の治療に用いられているβ-ラクタム系抗生物質の1種である。アミノペニシリングループに属し、抗菌スペクトルや活性はアモキシシリンとほぼ同じである[1]。また、アレルギーを起こすことがあり、程度は発疹などの軽度なものからアナフィラキシーのように重度なものまで様々である。作用機序赤く色をつけた部分がアンピシリンにおいてペニシリンGに付加されたアミノ基である。アンピシリンはペニシリンと同じβ-ラクタム系抗生物質の1種であり、アミノペニシリンファミリーの一つである。アンピシリンはペニシリンGにアミノ基を付加したものであり、このアミノ基によってグラム陰性菌の外膜を透過するようになった(外膜については細胞壁を参照)。そのため、アンピシリンはグラム陽性菌およびグラム陰性菌の一部に有効である。しかし、耐性の高い緑膿菌には効かない。アンピシリンは細菌の細胞壁を作るために必要なペプチド転移酵素のDD-トランスペプチダーゼを拮抗阻害する。したがって、細胞壁合成の第3ステージ、および最終ステージを阻害し、最終的に溶菌させる。使用対象感染症アンピシリンの作用はアモキシシリンとよく似ており、尿路感染症、中耳炎、感染性肺炎、サルモネラ、リステリア髄膜炎などの治療に用いられる。蜂巣炎の治療にはβ-ラクタム系抗生物質のフルクロキサシリン(Flucloxacillin)と併用して用いられる。これはフルクロキサシリンが黄色ブドウ球菌に作用し、同時にアンピシリンがA群連鎖球菌に作用することで治療するためである。この併用剤はCo-fluampicilという名前で販売されている。シュードモナス属全種、クレブシエラ属とエアロバクター属の大部分はアンピシリンに対して抵抗性を示す。アンピシリン自体はペニシリンの次に発見された2番目のβラクタムであることから、昨今はスルバクタムとの合剤で使用することが多い。血液脳関門を通過することを期待しての使用では単体でも使用される。研究アンピシリンは細菌に遺伝子(プラスミドなど)が取り込まれたことを確認するためにも用いられる(選択マーカー)。導入する遺伝子にアンピシリン耐性をコードする領域(通常大腸菌においてはβ-ラクタマーゼをコードするTEM-1遺伝子)を持たせ、大腸菌に組み込む。その大腸菌をアンピシリンを含む培地で培養し、菌が増殖した場合はアンピシリン耐性を持っているため、遺伝子が正常に組み込まれたと判断できる。出典: フリー百科事典『ウィキペディア(Wikipedia)』ペニシリンはクシャミが生んだ大発見【電子書籍】[ 百島祐貴 ]
2021.04.26
コメント(0)
-

メトロニダゾール
1960年イミダゾール系合成抗菌薬・抗原虫薬、メトロニダゾール(metronidazole)が開発された。メトロニダゾール(英: metronidazole)はニトロイミダゾール系の抗原虫薬、抗菌薬のひとつ。日本では商品名フラジールなどで知られる。当初はトリコモナス感染症治療薬であったが、様々な微生物への殺作用が確認され、適応は広がった。開発と販売当初トリコモナス感染症治療薬として開発されたが、膣トリコモナス症治療に伴う歯肉炎の改善効果発見によって嫌気性菌に対する抗菌活性が見出され、他の感染微生物に対しても開発が進められた。欧米では嫌気性菌等にも広く用いられていたが、日本では長くトリコモナス感染症の薬剤としてしか認可されていなかった。現在ではヘリコバクター・ピロリ菌の2次除菌療法における薬剤としても認可を受けている。そのほか、ランブル鞭毛虫、赤痢アメーバなどの嫌気性環境に寄生する原虫類や各種嫌気性菌に対しても、2012年公知申請により日本でも健康保険の適用対象となった。さらに、がん性皮膚潰瘍部位で増殖するグラム陽性およびグラム陰性嫌気性菌の殺菌目的にも使用される。日本での商品名は内服薬は「フラジール」(塩野義製薬)および「アスゾール」(富士製薬)、外用薬は「フラジール膣錠」「ロゼックス・ゲル」(ガルデルマ製造販売)、注射薬は「アネメトロ点滴静注液500mg」(ファイザー製造販売)。適応症トリコモナス症ヘリコバクター・ピロリ感染症アメーバ赤痢、肝膿瘍ジアルジア症以下の嫌気性菌感染症深在性皮膚感染症(蜂窩織炎など)外傷・熱傷および手術創等の二次感染骨髄炎肺炎、肺膿瘍腹膜炎、骨盤内炎症性疾患 (PSI)がん性皮膚潰瘍感染性腸炎(偽膜性大腸炎を含む。嫌気性菌であるクロストリジウム・ディフィシル感染に対して)歯科領域では、3MIX(3種混合抗菌薬)の成分として、歯内療法に使用される。3MIXとは、メトロニダゾール、セファクロム、シプロフロキサシンの3種の抗菌薬を混和したものである。 獣医学領域では、イヌの腸鞭毛虫症や豚赤痢に対して有効である。また、イヌやネコの嫌気性細菌による感染症の治療にも使用される。薬理嫌気性菌やトリコモナスなど、嫌気性環境下で増殖する病原微生物がもつ特異的なニトロ還元酵素系(ニトロレダクターゼ)によって還元され、メトロニダゾールはニトロソ化合物 (R-NO)に変化する。この変化体がフリーラジカルとしてDNA二重鎖切断などの細胞傷害活性を有すため、殺菌作用を示すといわれている。副作用比較的副作用は少ない。軽度なものとして消化器症状(悪心、心窩部不快感など)、金属味、舌苔、暗赤色尿などが指摘されている。また、まれに中枢性・末梢性の各種神経学的合併症(痙攣、小脳症状、末梢神経障害(可逆的)など)が指摘されており、重篤例も含まれる[8]。このため、肝機能不全、長期投与や高用量投与の際には特に注意が必要である。薬物相互作用メトロニダゾールによる治療中にアルコールを摂取するといわゆる「二日酔い・悪酔い」(ジスルフィラム様作用)をひきおこすことがあるため、投与期間中のアルコールの摂取は控える必要があり、アルコールを含む薬剤(リトナビルなど)との併用時も注意が必要である。ジスルフィラムはアルコール中毒症治療薬であり、アルコールの代謝に関わるアルデヒド脱水素酵素(acetaldehyde dehydrogenase; ALDH)の活性を阻害することにより血中アセトアルデヒド濃度を上昇させ、上記の症状をきたす。一般に薬物相互作用におけるジスルフィラム様作用は、薬物がジスルフィラムと同様にALDHを阻害することによるが、本剤は、投与によるアルコール摂取時の血中アセトアルデヒド濃度上昇もアルデヒド脱水素酵素に対する直接の阻害活性自体も見られない一方で、本剤によるモノアミン酸化酵素(monoamine oxidases; MAO)阻害作用の報告等もあることから、本剤とアルコールとの相互作用はジスルフィラムによるアルコール不耐性とは作用が異なり、同様の症状(意識状態の変様、自律神経障害、神経筋興奮等)を示すセロトニン症候群によるものとする報告もなされている 。そのほか、CYP2C9阻害作用による薬物相互作用(ワルファリンの作用増強(出血傾向)など)にも注意が必要である。環境への放出使用されたメトロニダゾールが下水道、下水処理場を経て、または直接河川へ流出してなお、検出されるレベルになっていることがある。バングラデシュのある川では、メトロニダゾールの濃度が環境中で安全とされる限界値を300倍も上回っていた調査結果がある。出典: フリー百科事典『ウィキペディア(Wikipedia)』
2021.04.25
コメント(0)
-

メチシリン
1960年ペニシリン系抗生物質、メチシリン(methicillin)が開発された。出典: フリー百科事典『ウィキペディア(Wikipedia)』菌株(ペニシリン)はよみがえる【電子書籍】[ 山崎光夫 ]
2021.04.24
コメント(0)
-

バージニアマイシン
1959年ストレプトグラミン系抗生物質、バージニアマイシン(virginiamycin)が開発された。バージニアマイシンは、プリスティナマイシンとキヌプリスチン/ダルフォプリスチンに似たストレプトグラミン抗生物質です。プリシュティナマイシンIIA(バージニアマイシンM1)とバージニアマイシンS1の組み合わせです。 バージニアマイシンは、微生物汚染を防ぐために燃料エタノール産業で使用されます。また、農業、特に家畜において、動物の成長を加速し、感染症を予防・治療するためにも使用される。USDAの調査によると、抗生物質は若い豚の飼料コストも30%も節約できるが、豚が年を取るにつれて節約は薄れる。 出典: フリー百科事典『ウィキペディア(Wikipedia)』よくわかる最新抗菌薬の基本と仕組み 「はじめて」でもよくわかる抗菌薬入門/深井良祐/中尾隆明【1000円以上送料無料】
2021.04.23
コメント(0)
-
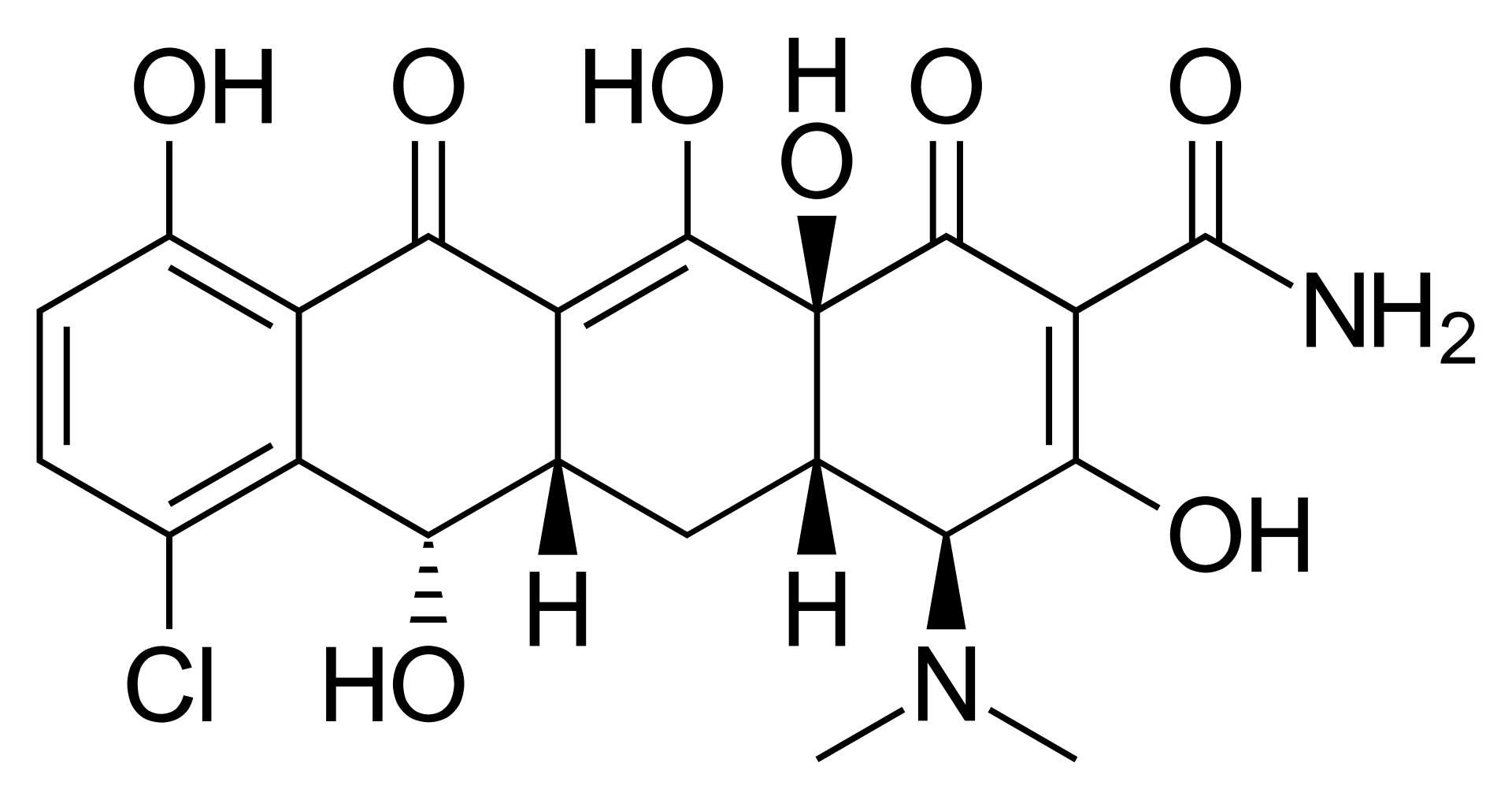
デメチルクロルテトラサイクリン
1958年テトラサイクリン系抗生物質、デメチルクロルテトラサイクリン(demethylchlortetracycline、、デメクロサイクリン、レダマイシン®)が開発された。デメクロサイクリン(INN、BAN、USAN)(ブランド名デクロマイシン、デクロスタチン、レデルマイシン、ビオテルシクリン、デガノール、デテクロ)は、ブランド名デトラビス、メシクリン、メキソシン、クロルテトリン、ストレプトマイセス・アウレオフィレンスの変異株に由来するテトラサイクリン系抗生物質である。 編集デメクロサイクリンは、細菌感染症の様々なタイプの治療のために正式に示されています. ライム病の治療において抗生物質として使用され、にきび、5つ気管支炎が挙げられる。 抵抗は、しかし、徐々に一般的になってきている,とデメクロキシンは現在、感染症の治療にほとんど使用されていない。 これは、水分制限だけでは効果がない場合、不適切な抗利尿ホルモン(SIADH)の症候群による低ナトリウム血症(低血中ナトリウム濃度)の治療に広く使用されています(米国を含む多くの国ではオフラベルです)。 生理的に、これはADHに集める細管細胞の応答性を低下させることによって働く。 SIADH での使用は、実際には副作用に依存します。デメクロサイクリンは、腎性糖尿病のインシピダ(尿を集中できないことによる脱水)を誘導する。 SIADHでのデメクロサイクリンの使用は1975年に最初に報告されました、そして、1978年に、より大きな研究では、当時唯一利用可能な治療である炭酸リチウムよりも効果的で耐容性が高いことが判明しました。 デメクロサイクリンは、SIADHを治療するための選択の薬であることが使用されます。一方、バソプレシン受容体拮抗薬、例えばトルバプタンが利用可能になった。 禁忌他のテトラサイクリンと同様に, デメクロサイクリンは、子供や妊娠中または授乳中の女性で禁忌.このクラスのすべてのメンバーは骨の発達を妨げ、歯を変色させるかもしれません。 副作用と相互作用これらは他のテトラサイクリンの物と似ています。日光との皮膚反応が報告されている。 他の数個の既知のテトラサイクリン誘導体と同様に、デメクロサイクリンはネクロ原性糖尿病を起こす さらにデメクロサイクリンは、リチウムに似た向精神性副作用を有する可能性がある。 テトラサイクリンは、カルシウム、鉄(経口投与時)、マグネシウムなどのカチオンに結合し、胃腸管に不溶性および不吸刺激性を与える。デメクロサイクリンは食品(特に牛乳やその他の乳製品)や制酸剤と一緒に服用しないでください。 アクションのメカニズム関連するテトラサイクリン系抗生物質と同様に、デメクロサイトリンは、細菌によるタンパク質合成を損なうアミノアシルtRNAの結合を阻害する30Sリボソームサブユニットに結合することによって作用する。それは静菌性です(細菌の増殖を損ないますが、細菌を直接殺すものではありません)。 デメクロサイクリンは、腎臓におけるバソプレシンV2受容体にホルモンが結合した後の細胞内第2のメッセンジャーカスケード(具体的には、アデニルシクラーゼ活性化を阻害する)を妨害することによって抗利尿ホルモンの腎作用を阻害する。 デメクロサイクリンがこれを行う正確な方法はまだ解明されていません。 出典: フリー百科事典『ウィキペディア(Wikipedia)』【メール便送料無料】【第2類医薬品】 テラマイシン軟膏a 6g 1個皮膚の薬 しっしん・かゆみ(4987123701693)二つの抗生物質が化膿に効く化膿性皮膚疾患用薬です。
2021.04.22
コメント(0)
-
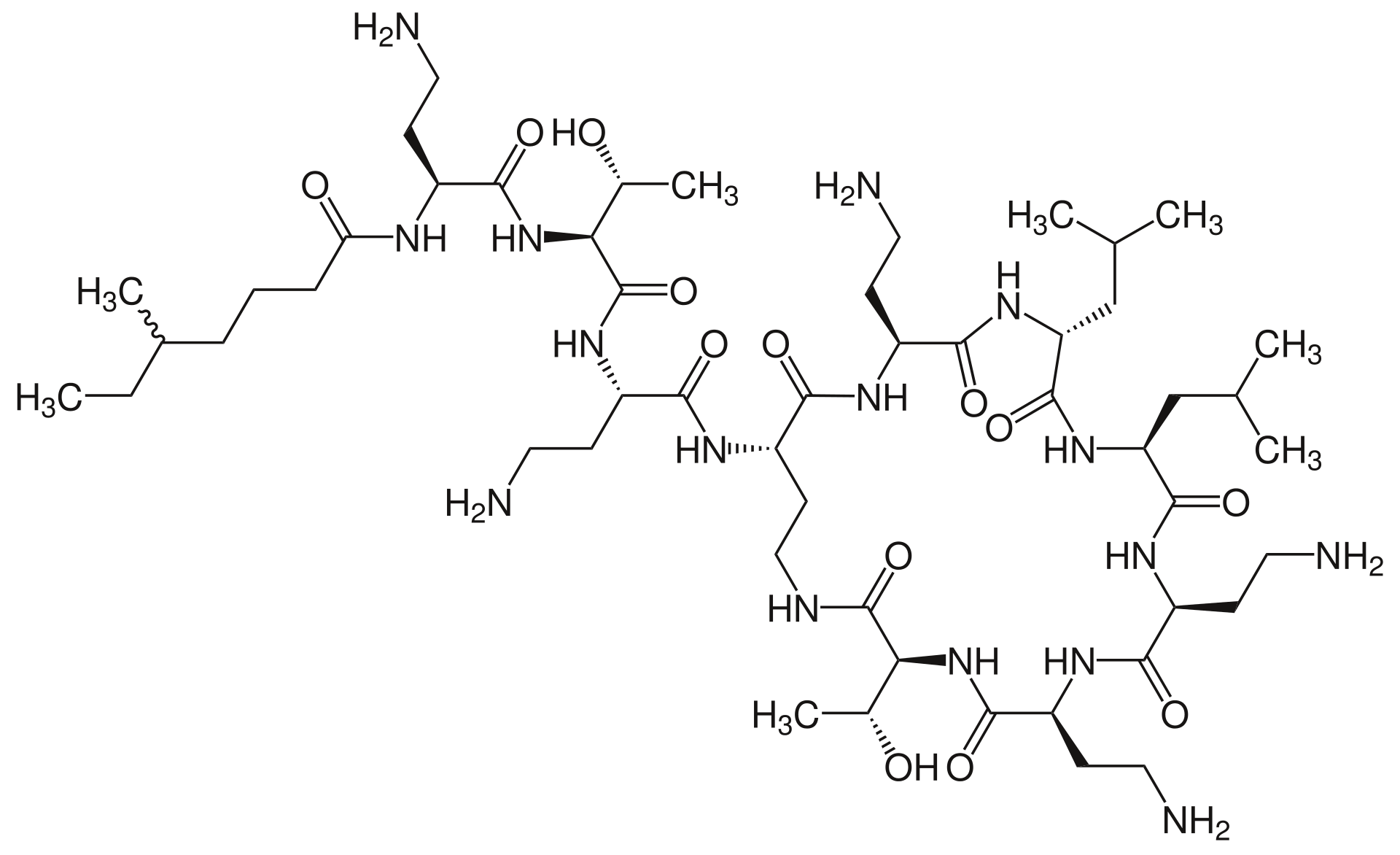
コリスチン
1958年ポリペプチド系抗生物質、コリスチン(colistin:CL)が開発された。コリスチン(別名 ポリミキシンE、英: colistin)は、7つのアミノ酸からなる環状ペプチド系抗生物質。商品名オルドレブ点滴静注用、コリマイシン散(ポーラファルマ製造販売)。塩基性の陽イオン性界面活性剤であり、細胞質膜を傷害することにより殺菌的に作用する。グラム陰性菌に対して優れた抗菌作用を示し、緑膿菌感染症や細菌性赤痢に対して有効。腎毒性、神経毒性が強いが、多剤耐性グラム陰性桿菌に対する最終手段として用いられる。点滴静注用製剤が2015年3月に日本で承認された。歴史コリスチンは、1950年にライオン製薬(現ポーラファルマ)の小林細菌研究所の小山康夫、黒沢秋雄らによって、福島県掛田町の土壌中の芽胞桿菌Bacillus polymyxa var. colistinus が産生する物質から発見された。日本では1951年に硫酸塩(硫酸コリスチン)が医薬品として発売され、1960年にはコリスチン誘導体ナトリウム塩のコリスチンメタンスルホン酸ナトリウムが発売された。また、米・ワーナー・ランバート(現ファイザー)に輸出されるなど、米国を始め海外でも医薬品として発売され使用された。コリスチンは1960年代から1970年代にかけて用いられたが、副作用の頻度が高いこと、他により安全性が高い抗菌薬が開発されたことなどにより、その後日本では使用されなくなった。2015年、多剤耐性を有するグラム陰性菌に対する抗生物質として見直され、改めて希少疾病用医薬品として承認された。近年、コリスチンは多剤耐性緑膿菌(MDRP)などの多剤耐性グラム陰性桿菌感染症に比較的有効な貴重な治療薬の一つとして欧米で見直されており、日本でも2010年10月に厚生労働省の薬事・食品衛生審議会が多剤耐性菌への使用に限り許可する方針を固めるなど見直しが始まっている。2015年、コリスチン耐性を持つ細菌が発見された。薬効薬理抗菌作用コリスチンは、グラム陰性桿菌に対して殺菌的に作用する。菌種 コリスチン感受性緑膿菌 3.13μg/mLで約71%発育抑制大腸菌 1.56μg/mLで100%発育抑制赤痢菌 1.56μg/mLで100%発育抑制薬剤耐性耐性を獲得し難く、他種抗生物質との間には交叉耐性がないため他種抗生物質耐性菌にも有効である。作用機序グラム陰性細菌の細胞質膜の障害である。(グラム陽性細菌の細胞質膜には効果が期待できない)効能・効果オルドレブ〈適応菌種〉コリスチンに感性の大腸菌、シトロバクター属、クレブシエラ属、エンテロバクター属、緑膿菌、アシネトバクター属で、他の抗菌薬に耐性の菌株。〈適応症〉各種感染症。コリマイシン<適応菌種> コリスチンに感性の大腸菌、赤痢菌<適応症> 感染性腸炎副作用治験で認められた副作用は、腎機能障害が21%で神経系障害が2%であった。重大とされている副作用は、腎不全、腎機能障害、呼吸窮迫、無呼吸、偽膜性大腸炎である。出典: フリー百科事典『ウィキペディア(Wikipedia)』【第2類医薬品】【定形外郵便】ゼリア新薬工業 ドルマイシン軟膏 6g<ケガの化膿予防・治療。できものに>(コリスチン硫酸塩・バシトラシン軟膏)
2021.04.21
コメント(0)
-
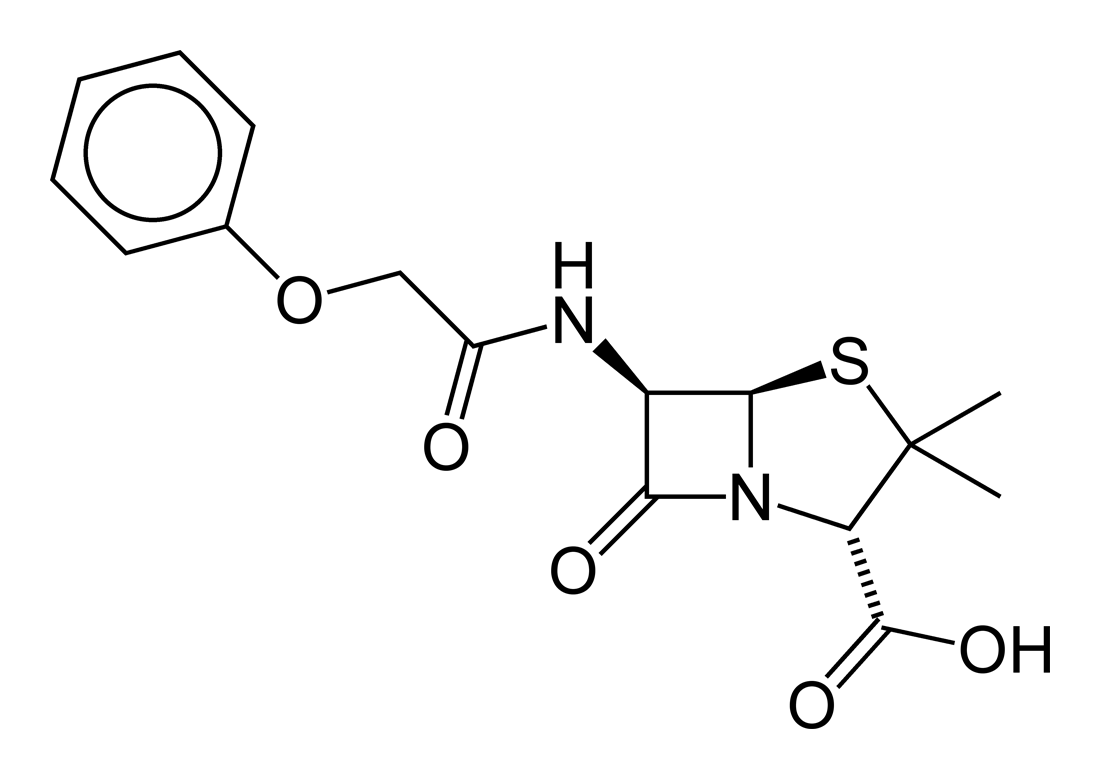
フェノキシメチルペニシリン
1956年 ペニシリン系抗生物質、フェノキシメチルペニシリン(phenoxymethylpenicillin;Penicillin V)が開発された。フェノキシメチルペニシリンは、ペニシリンV(PcV)およびペニシリンVKとしても知られており、多くの細菌感染の治療に有用な抗生物質である。 具体的には、レンサ球菌の喉、中耳炎、および蜂の炎の治療に使用される。またリウマチ熱を予防し、脾臓の除去後の感染症を予防するためにも使用される。 経口投与される。 副作用には、下痢、吐き気、アナフィラキシーを含むアレルギー反応などがあります。 ペニシリンアレルギーの既往歴のある人には推奨されません。 妊娠中の使用に比較的安全です。 ペニシリンとβラクタム科の薬です。 通常、細菌死を生じる。 フェノキシメチルペニシリンは、最初にイーライリリーによって1948年に作られました. 世界保健機関(WHO)の必須医薬品リストに載っています。 ジェネリック医薬品として入手可能です。2017年には、米国で242番目に一般的に処方された薬で、200万以上の処方箋が発行された。出典: フリー百科事典『ウィキペディア(Wikipedia)』菌株(ペニシリン)はよみがえる【電子書籍】[ 山崎光夫 ]
2021.04.20
コメント(0)
-
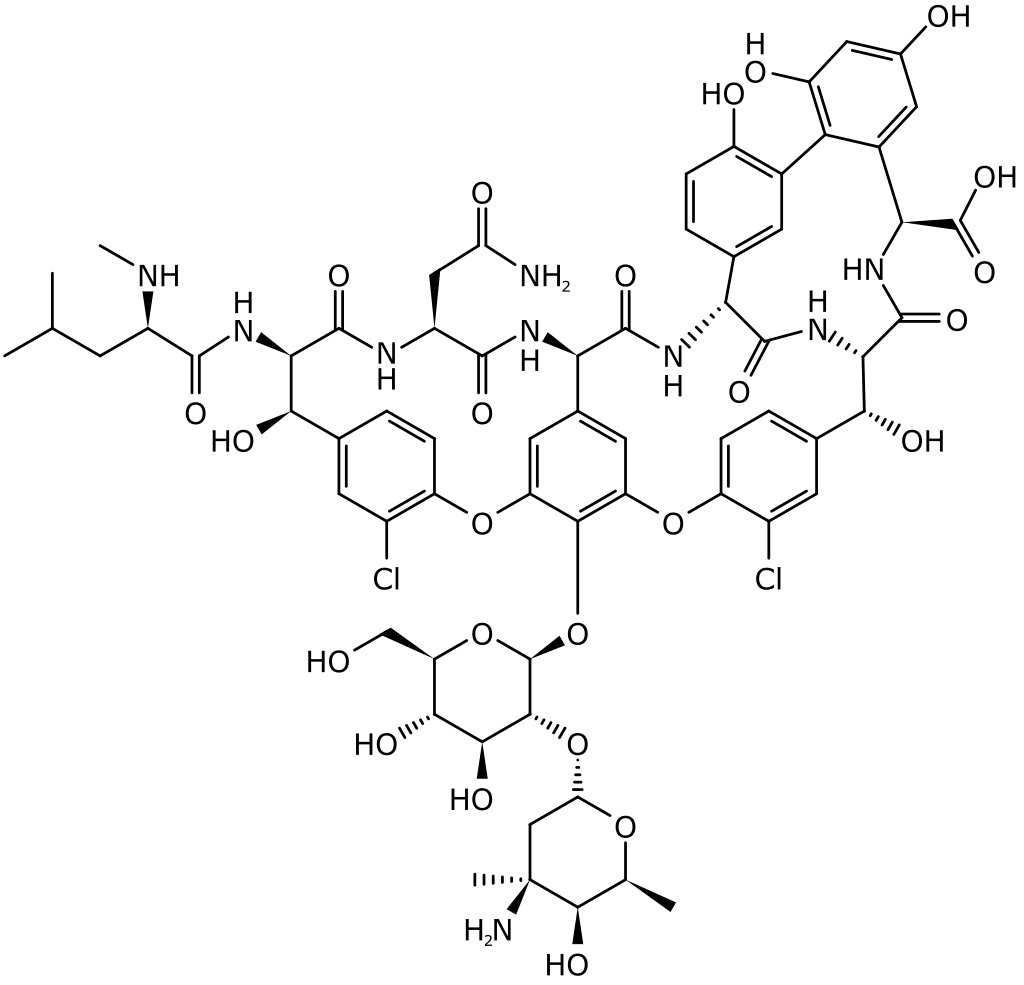
バンコマイシン
1955年グリコペプチド系抗生物質、バンコマイシン(vancomycin:VCM)が開発された。バンコマイシン (Vancomycin、VCM) は、グリコペプチド系抗生物質のひとつ。真正細菌の細胞壁合成酵素の基質であるD-アラニル-D-アラニンに結合して細胞壁合成酵素を阻害し、菌の増殖を阻止する働きがある。大部分のグラム陽性菌に殺菌作用をもち、腸球菌に対しては静菌作用がある。ペニシリン等のβ-ラクタム系抗生物質とは作用機序が異なるため、ほとんどの抗生物質が効かないメチシリン耐性黄色ブドウ球菌 (MRSA) を殺菌できる。このため、過去には最強の抗生物質といわれたこともあった。塩酸バンコマイシンは内服してもほとんど吸収されることがないため、腸などの消化管内の静菌・殺菌に有効である。内服または点滴静注で使用される。点滴静注による急速投与が原因となり、Red neck (Red man) syndromeと呼ばれる皮膚合併症や血圧低下などを来たす場合がある。腎毒性があるため、投与中は血中濃度を測定し、治療域に維持する投与量にすることが推奨される。腎機能の低下した患者に対する投与は注意が必要であり、薬物動態理論を用いた投与設計を行う。しかし、薬物動態理論を用いた投与設計を日常診療として行うには、感染制御専門薬剤師による助言が必要なことが多く、実際に投与開始時から行っている施設は少ない。一般の病院では、同系統で腎機能障害が軽いとされているテイコプラニン (TEIC) か別の系統であるリネゾリドを用いることになる。この場合には、バンコマイシン耐性の腸球菌に対しても有効なリネゾリドの使用頻度が高くなり、リネゾリド耐性菌が増加する可能性が懸念される。1956年にイーライリリー・アンド・カンパニーが開発し、メチシリン耐性黄色ブドウ球菌 (MRSA) の治療に用いられてきたが、1986年、イギリスとフランスでバンコマイシンに耐性のある腸球菌 (VRE) の存在が報告され、さらに病原性の高いバンコマイシン低度耐性黄色ブドウ球菌 (VISA) (1996年)とバンコマイシン耐性黄色ブドウ球菌 (VRSA)(2002年)の存在が報告された。薬理作用細胞壁合成阻害薬に分類される。ムレイン単体生合成を阻害する。同様にムレイン単体生合成を阻害するものにホスホマイシンがある。特徴MRSA感染が疑われる黄色ブドウ球菌菌血症患者において、ST合剤治療群ではバンコマイシン治療群に比べ、30日死亡率は1.90倍高かった。全合成キリアコス・コスタ・ニコラウらを含む複数のグループによって、全合成が達成されている。出典: フリー百科事典『ウィキペディア(Wikipedia)』ESBL産生菌・MRSA・MDRP 知って防ぐ!耐性菌 [ 矢野邦夫 ]
2021.04.19
コメント(0)
-

チアムフェニコール
1955年クロラムフェニコール系抗生物質、チアムフェニコール(tiamphenicol)が開発された。出典: フリー百科事典『ウィキペディア(Wikipedia)』【第2類医薬品】クロロマイセチン軟膏2%A 15g皮膚の薬/とびひ・めんちょう
2021.04.18
コメント(0)
-

スピラマイシン
1955年 マクロライド系抗生物質、スピラマイシン(spiramycin:SPM)が開発された。マクロライド系薬の見直しと展望 15員環マクロライドの役割と新たな可能性 [ 河野茂 ]
2021.04.17
コメント(0)
-

ベンジルペニシリン・ベンザチン
1954年ペニシリン系抗生物質、ベンジルペニシリン・ベンザチン(ベンジルペニシリン ベンザチン塩、benzathine penicillin)が開発された。出典: フリー百科事典『ウィキペディア(Wikipedia)』菌株(ペニシリン)はよみがえる【電子書籍】[ 山崎光夫 ]
2021.04.16
コメント(0)
-
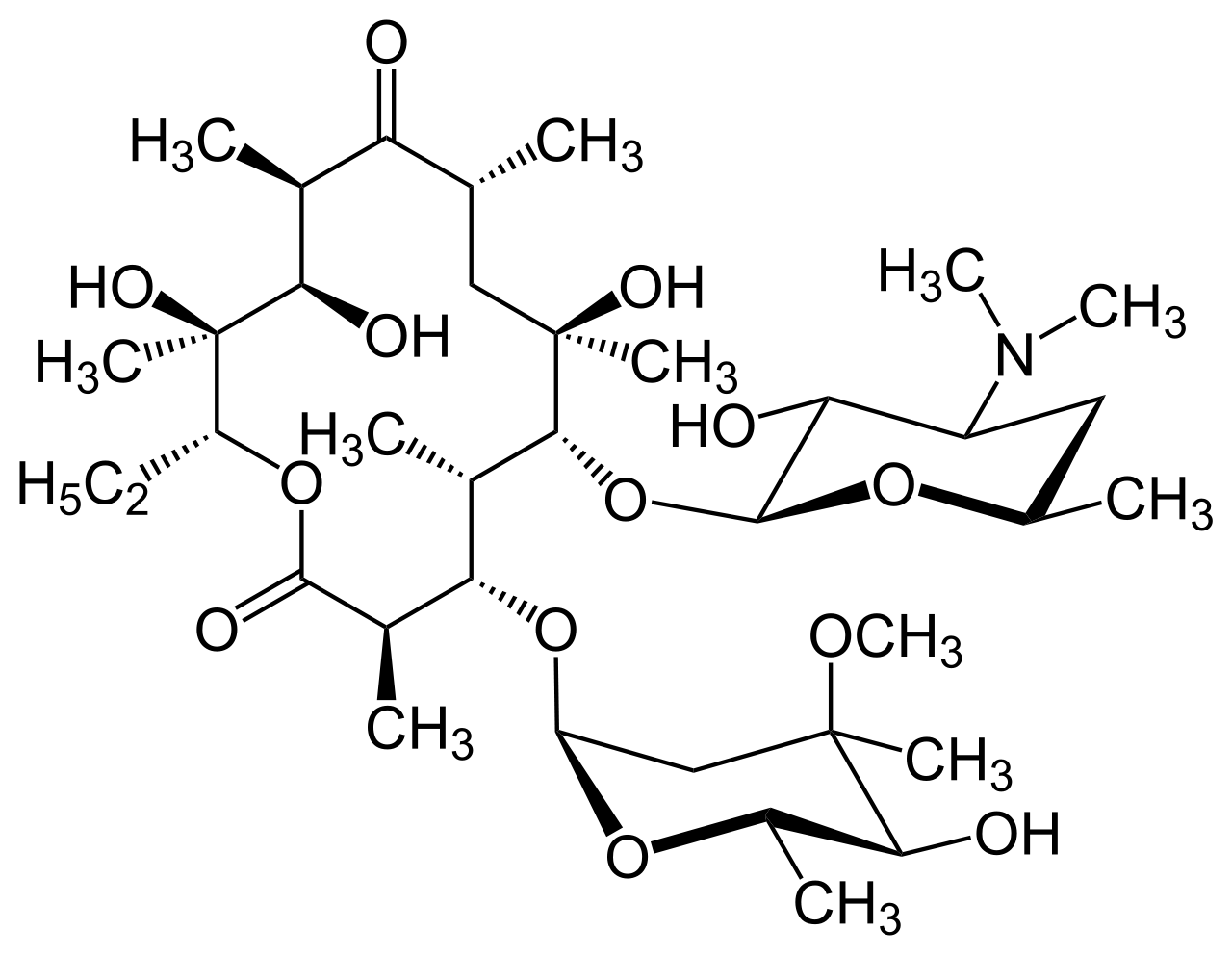
エリスロマイシン
1952年マクロライド系抗生物質、エリスロマイシン(erythromycin:EM)が開発された。エリスロマイシン (erythromycin) はマクロライド系抗生物質の1つである。製品名は「エリスロシン®」(マイランEPD合同会社製造販売)。抗菌スペクトルはペニシリンと類似するが若干幅広く、ペニシリンにアレルギーを持つ人に対してしばしば使用される。呼吸器系への感染症に関しては、マイコプラズマ・クラミドフィラなどの非定型微生物に対しても高い効果を持つが、市中肺炎の原因菌の一つであるインフルエンザ菌には抗菌活性を示さない。クラミジア、梅毒、淋病の流行に対処する場合にも用いられる。14員環ラクトン環に2つの糖(L-クラジノースとD-デソアミン)が付いた構造を持つ。10か所の不斉中心があるなど構造が複雑なため合成するのは難しいとされる化合物である。放線菌属の Saccaropolyspora erythraea (旧名 Streptomyces erythraeus)によって作り出される。歴史1949年、フィリピンの科学者アベラルド・アギュイラー (Abelardo Aguilar) は彼を雇用していたイーライリリーに、ある土のサンプルを送った。マクガイア (J. M. McGuire) が率いるイーライリリーの研究チームは、そのサンプルに含まれていた菌株 Streptomyces erythraeus の代謝産物からエリスロマイシンを単離することに成功した。サンプルが採取されたフィリピンの地名イロイロをとって商品名はイロソン Ilosone® と名付られ、1952年に上市された。イロチシン Ilotycin® とも呼ばれた。1981年、ハーバード大学の化学教授でノーベル化学賞受賞者のロバート・バーンズ・ウッドワードとその研究チームがエリスロマイシンAの最初の立体選択的不斉合成を報告した。剤形腸溶コーティング錠剤、徐放性カプセル、ドライシロップ、経口懸濁液、点眼液、軟膏、ゼリー、注射剤の形で入手可能である。(日本においては一部剤形のみ)商品名として エリスロシン, Robimycin, E-Mycin, E.E.S. Granules, E.E.S.-200, E.E.S.-400, E.E.S.-400 Filmtab, Erymax, Ery-Tab, Eryc, Erypar, EryPed, Eryped 200, Eryped 400, Erythrocin Stearate Filmtab, Erythrocot, E-Base, Ilosone, MY-E, Pediamycin, PCE Dispertab などが知られる。作用機序バクテリアのタンパク質合成を阻害することによって増殖を抑える。エリスロマイシンはバクテリアのリボソーム中で 50S サブユニットの 23s rRNA に結合し、伸張するペプチドの出口をふさぐことにより、ペプチドの転位を阻害する。薬物動態胃酸によって容易に失活するため、経口で投与する場合にはコーティングを施すか、より安定な塩やエステル体を処方する必要がある。吸収される速度は高く、ほとんどの組織や食細胞に拡散する。食細胞中での濃度が高くなりやすいためすぐに感染部位に到達し、食細胞が活動している間に高濃度のエリスロマイシンが放出される。髄液への移行はない。 バイオアベイラビリティは50%程度である。代謝大部分が肝臓で脱メチル化を受けて代謝される。主な排出経路は胆汁で、少量が尿に排出される。半減期は1.5時間である。副作用下痢、吐き気、腹痛、嘔吐などの消化器系障害がよく見られる。これらの症状はエリスロマイシンが胃で分解される際に生じるヘミケタルという物質が消化管の蠕動運動を亢進するため発生するとされる。そのため第一選択薬として処方されることはあまり無い。しかしながら、このような運動性を誘発する効果をもつことから胃不全麻痺 (gastroparesis) を処置する際には有効であるとされる。エリスロマイシンの静脈内投与が食道胃十二指腸鏡検査の際に胃の内容物を排出させるために用いられることもある。聴覚障害などのより重大な副作用はまれである。アレルギー反応は一般的ではないが、蕁麻疹やアナフィラキシーが起こることがある。胆汁鬱帯、スティーブンス・ジョンソン症候群、中毒性表皮壊死症などもまれに見られる。妊娠後期に母親がエリスロマイシンを摂取すると、子供の幽門狭窄症の可能性を増加させることが示されている。禁忌初期に突然死の例が報告されたことから大規模なコホート研究が行われ、シトクロムP450 の1つである CYP3A4 を阻害してエリスロマイシンの代謝を遅らせるベラパミルやジルチアゼムなどを同時に投与した患者におけるエリスロマイシンと頻脈や心臓性突然死の関連が明らかにされた[1]。すなわち、エリスロマイシンはそれらの薬剤やQT時間を延ばすような薬剤を使用している患者に対しての投与は避けるべきであると結論付けられた。他の例としてテルフェナジン (Seldane®, Seldane-D®)、アステミゾール (Hismanal®)、シサプリド(Propulsid®, 多くの国でQT時間を延長させる効果のため認可が取り消されている)、ピモジド (Orap®) が挙げられる。出典: フリー百科事典『ウィキペディア(Wikipedia)』マクロライド系薬の見直しと展望 15員環マクロライドの役割と新たな可能性 [ 河野茂 ]
2021.04.15
コメント(0)
-

ペニシリンG・プロカイン
1950年ペニシリン系抗生物質、ペニシリンG・プロカイン(ペニシリンG プロカイン塩、penicillin G procaine)が開発された。出典: フリー百科事典『ウィキペディア(Wikipedia)』ペニシリンはクシャミが生んだ大発見【電子書籍】[ 百島祐貴 ]
2021.04.14
コメント(0)
-
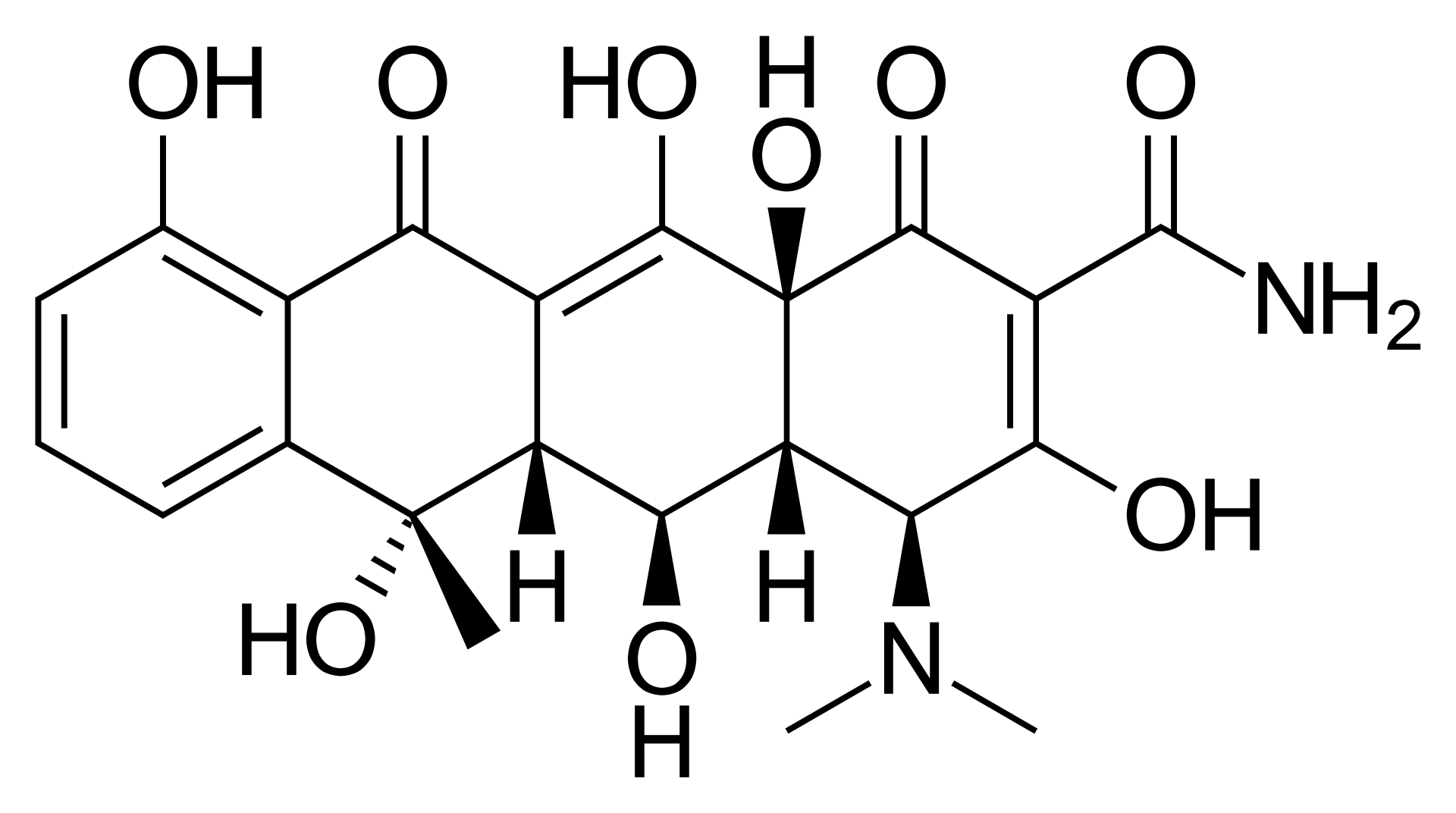
オキシテトラサイクリン
1950年テトラサイクリン系抗生物質、オキシテトラサイクリン(oxytetracycline:OTC)が開発された。オキシテトラサイクリンは、発見される抗生物質の広域スペクトルテトラサイクリン群の2番目の群であった。オキシテトラサイクリンは、必須のタンパク質を産生する細菌の能力を妨害することによって動作します。これらのタンパク質がなければ、細菌は増殖し、増殖し、数を増やすことができません。したがって、オキシテトラサイクリンは感染の広がりを止め、残りの細菌は免疫系によって殺されるか、または最終的に死ぬ。オキシテトラサイクリンは広域スペクトルの抗生物質であり、多種多様な細菌に対して活性である。しかし、細菌のいくつかの株は、感染症のいくつかのタイプを治療するための有効性を低下させ、この抗生物質に対する耐性を開発しました。オキシテトラサイクリンは、クラミジア(例えば、胸部感染性精神病、眼感染症トラコーマ、および生殖器感染性尿道炎)およびマイコプラズマ生物(例えば、肺炎)によって引き起こされる感染症を治療するためにまだ使用される。オキシテトラサイクリンは、にきびの発生に影響を与える皮膚上の細菌に対する活性のために、にきびを治療するためにも使用されます (クチバクテリウム・ アクネ).これは、慢性気管支炎の再燃を治療するために使用されます, 通常責任を負う細菌に対するその活性のために,血友病インフルエンザ.オキシテトラサイクリンは、リケッチアと呼ばれる微生物群(例えば、ロッキー山斑点熱)によって引き起こされるような他の稀な感染症を治療するためにも使用することができる。感染を引き起こす細菌がそれに影響を受けやすくするために、通常、組織サンプルは、例えば感染領域からの綿棒、または尿または血液サンプルから採取される。オキシテトラサイクリンは1949年に特許を取得し、1950年に商業的に使用されました。出典: フリー百科事典『ウィキペディア(Wikipedia)』【指定第2類医薬品】テラ・コートリル軟膏a 6G赤ニビキなどに
2021.04.13
コメント(0)
-
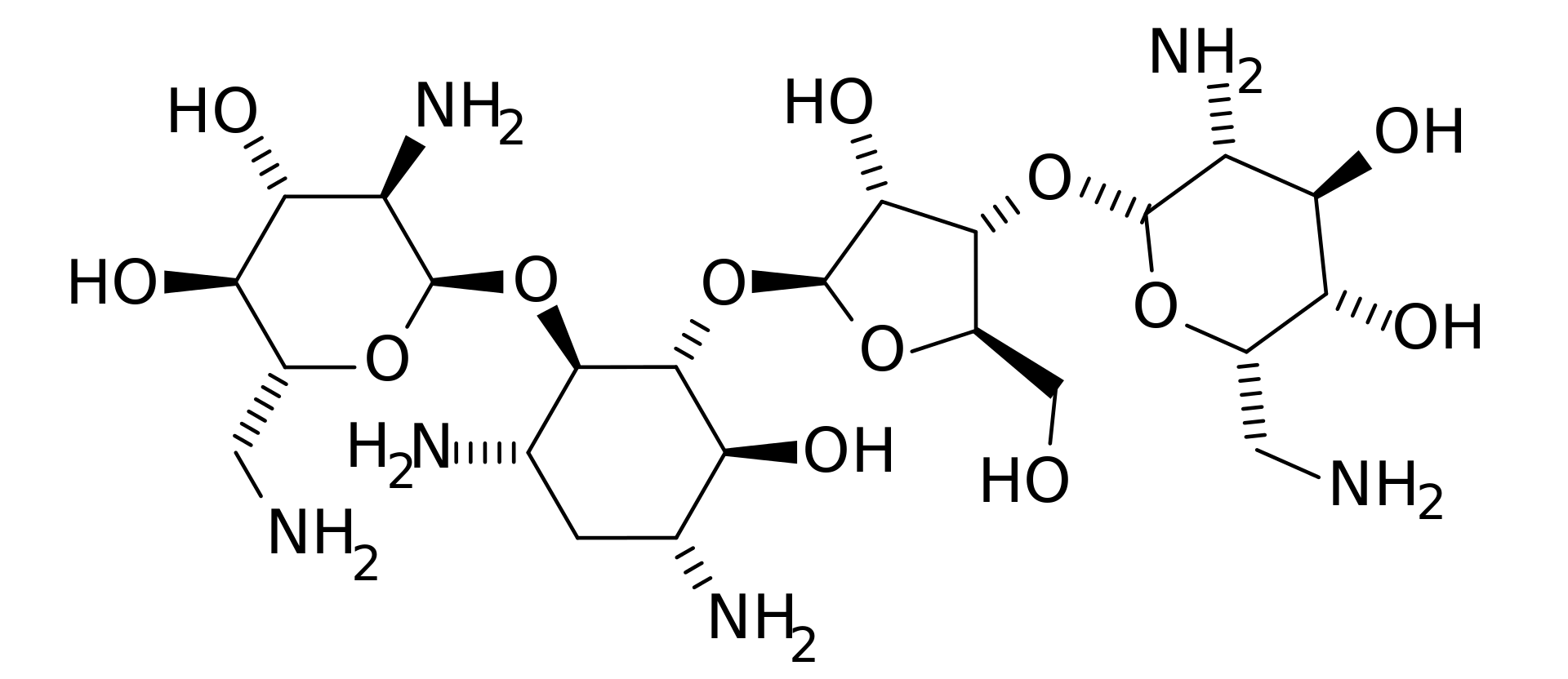
ネオマイシン
1949年アミノグリコシド系抗生物質、ネオマイシン(neomycin)が開発された。ネオマイシン(neomycin)は1948年にウクライナ出身のセルマン・ワクスマンにより発見されたアミノグリコシド系抗生物質である。分子量614.65。 放線菌の一種、Streptomyces fradiaeが生産する。そのためフラジオマイシン(fradiomycin)とも呼ばれる。日本薬局方収載医薬品としては硫酸フラジオマイシン(FRM)と呼ばれ、別名はソフラマイシン、フラミセチン。CAS登録番号は1405-10-3 (Neomycin sulfate)。作用機序ネオマイシンの作用機序はカナマイシンのそれと類似し、30Sリボソームに結合することにより細菌のタンパク質合成を阻害する。臨床応用比較的広範な抗菌スペクトルを有し、グラム陰性菌、グラム陽性菌ともに強く阻害する。副作用ネオマイシンには強い急性毒性および腎毒性が認められる。そのため、経口剤か外用剤として使用される。その他分子生物学の研究においてネオマイシン耐性遺伝子は、選択マーカーとして形質細胞の分離に利用される。出典: フリー百科事典『ウィキペディア(Wikipedia)』【第(2)類医薬品】【送料無料】ベトネベートN軟膏AS 5g しっしん、かぶれ等の皮膚の炎症にすぐれた効き目・湿疹・皮膚炎
2021.04.12
コメント(0)
-
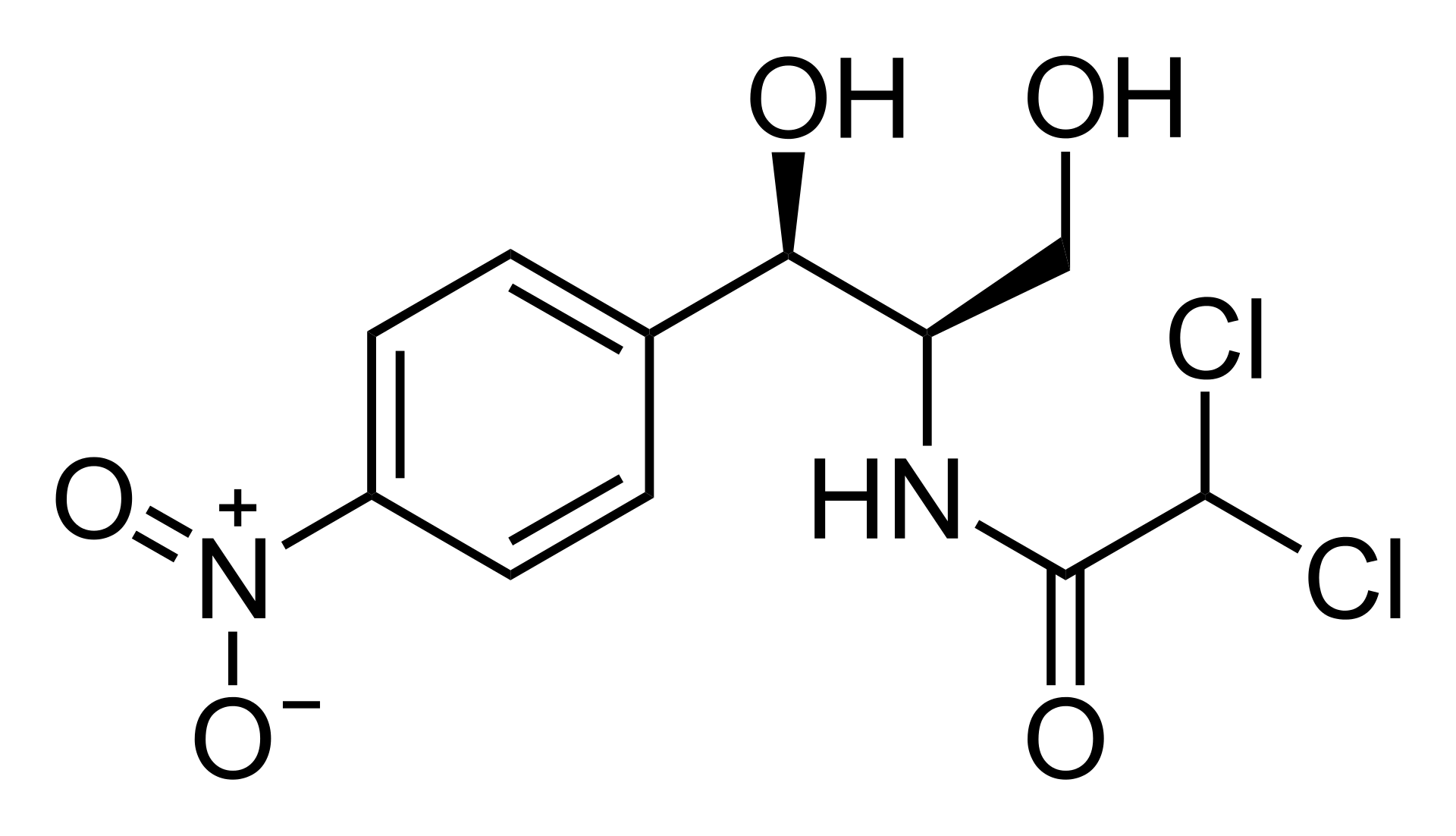
クロラムフェニコール
1949年アンフェニコール系抗生物質、クロラムフェニコール(chloramphenicol:CP)が開発された。クロラムフェニコール (Chloramphenicol) は、バクテリア Streptomyces venezuelae 由来の抗生物質であり、現在は化学合成によって作られている。化合物名は 2,2-ジクロロ-N-[(1R,2R)-2-ヒドロキシ-1-ヒドロキシメチル-2-(4-ニトロフェニル)エチル]アセトアミドである。類似化合物にフロルフェニコールがあるが、こちらは動物のみでヒトには用いられていない。概要クロラムフェニコールはStreptomyces venezuelaeから得られた抗生物質である。1947年にパーク・デイビス社(現在のファイザー社)により発見された。ペニシリン、ストレプトマイシンに次いで開発されたが、これらよりも広範な抗菌スペクトルを持ち、グラム陽性・陰性菌、レプトスピラ、リケッチア、クラミドフィラに効果を示す。クロラムフェニコールは発酵生産によって製造されていたが、発酵法では生産されたクロラムフェニコールによって生産菌自体が死滅してしまうため、現在は化学合成によって生産されている。クロラムフェニコールはグラム陽性、陰性にかかわらず、多くの微生物に対して有効であるが、再生不良性貧血を含む骨髄の損傷など人体に重大な副作用があるため、先進国においては腸チフスなど重大で生命の危機がある感染症、もしくは多剤耐性のため本剤以外に選択肢がない場合にのみ用いられる。重大な副作用はあるものの安価な代替品が存在しないため、WHOは多くの発展途上国で小児の治療に使用することを容認している。ビブリオ属細菌を殺し下痢を抑えるのでコレラの治療に用いられる。テトラサイクリン耐性ビブリオにも効果がある。日本では「クロロマイセチン」の製品名で注射剤(サクシネート静注用)、内服薬(錠50/錠250)、外用剤(軟膏2%、局所用液5%)、外耳炎や中耳炎の治療に用いる耳科用液(耳科用液0.5%)及び、細菌性膣炎の治療に用いる「クロマイ膣錠」がアルフレッサ ファーマを通じて医療用医薬品として発売されているほか、外用剤の軟膏については第一三共ヘルスケアがドラッグストアなどで購入可能な一般用の化膿性皮膚疾患用薬(第2類医薬品)として「クロロマイセチン軟膏2%A」の製品名で発売されている。米国では点眼薬や軟膏も Chlorsig の名称で一般に販売されており、細菌性結膜炎・皮膚炎・生殖器感染症などの治療に使われる。クロラムフェニコールが両生類のカエルツボカビ症の特効薬であることが最近発見された。カエルツボカビ症は両生類の致死的な真菌症であり、1980年以降に絶滅したカエル120種のうち3分の1の原因であると推定されている。機構と耐性クロラムフェニコールは原核生物である細菌の 50S リボソームに結合する。リボソーム上でのP座のペプチジルtRNAから、A座のアミノアシルtRNAへのペプチド鎖移動を司るペプチジルトランスフェラーゼ (peptidyl transferase) を阻害し、タンパク質合成を妨害することにより細菌の増殖を止める。一方、真核生物本体のリボソームは阻害しないため、真核生物への影響はバクテリアに比べれば遥かに低い。ヒトも真核生物に属すため抗生物質として使用できる。しかしながらミトコンドリアのリボソームは阻害されるため、この点が副作用の主な原因となる。なお、3ドメインの残り1つである古細菌は、細菌をターゲットとした抗生物質は効かないことが多いが、クロラムフェニコールは有効である。ただし、細菌に比べれば一般に効きにくい。腸内に存在するメタン菌であるMethanosphaera stadtmanaeの増殖は4mg/Lで阻害できるが、同様のメタン菌であるMethanobrevibacterやMethanomassiliicoccusはCATを持つことから25mg/L、SulfolobusやHalobacteriumは23S rRNAの配列の違いにより100mg/Lもの高濃度を必要とする。細菌であるクロストリジウムなどは、メタン菌からCATを獲得して耐性化した可能性がある。クロラムフェニコール耐性はCAT遺伝子により与えられる。この遺伝子は「クロラムフェニコールアセチルトランスフェラーゼ(CAT)」と呼ばれる酵素をコードする。この酵素は、アセチル-S-補酵素A(アセチルCoA)由来のアセチル基を1つまたは2つ、クロラムフェニコールのヒドロキシ基に結合させる。アセチル化されることによってクロラムフェニコールはリボソームに結合できなくなる。分子生物学では、このCAT遺伝子とプラスミド、クロラムフェニコールを用いた「CAT-assay」と呼ばれる手法がある。出典: フリー百科事典『ウィキペディア(Wikipedia)』【第2類医薬品】クロロマイセチン軟膏2%A 15g皮膚の薬/とびひ・めんちょう
2021.04.11
コメント(0)
-

クロロテトラサイクリン
1948年 テトラサイクリン系抗生物質、クロロテトラサイクリン(chlortetracycline;オーレオマイシン、aureomycin)が開発された。テトラサイクリン系抗生物質(英: Tetracycline antibiotics, Tetracycline class, Tetracyclines、略: TC系, TC類, TCs, TETs)は、一群の広域スペクトラム性抗生物質(英語版)の総称である。テトラサイクリンという名称は、四つの(tetra-)炭化水素からなる有機環(cycl-)の誘導体(-ine)という意味である。TC系の抗菌スペクトラムは、全ての抗生物質で最も広い部類に属している。抗菌作用のない化学修飾されたCMTs(Chemically Modified Tetracyclines)の研究も進んでいる。歴史1945年最初に見出されたテトラサイクリン系抗生物質であるクロルテトラサイクリンは、アメリカン・サイアナミッド(英語版)[注 1]のベンジャミン・M・ダガーによって放線菌の一種Streptomyces aureofaciensから発見された。1955年テトラサイクリンは、ファイザーに在籍していたen:Lloyd Conovarによって合成された。その後、様々な誘導体が化学合成されている。1966年ミノサイクリンは、アメリカのレダリー研究所によって天然テトラサイクリンから半合成された[2]。現在抗菌スペクトラムの若干の違いなどもあり、日本で主に内服薬として使用されているのはドキシサイクリンとミノサイクリンの2剤である。出典: フリー百科事典『ウィキペディア(Wikipedia)』毎月1日は10倍〜 いろはの日【指定第2類医薬品】テラ・コートリル軟膏a 6G赤ニビキなどに
2021.04.10
コメント(0)
-
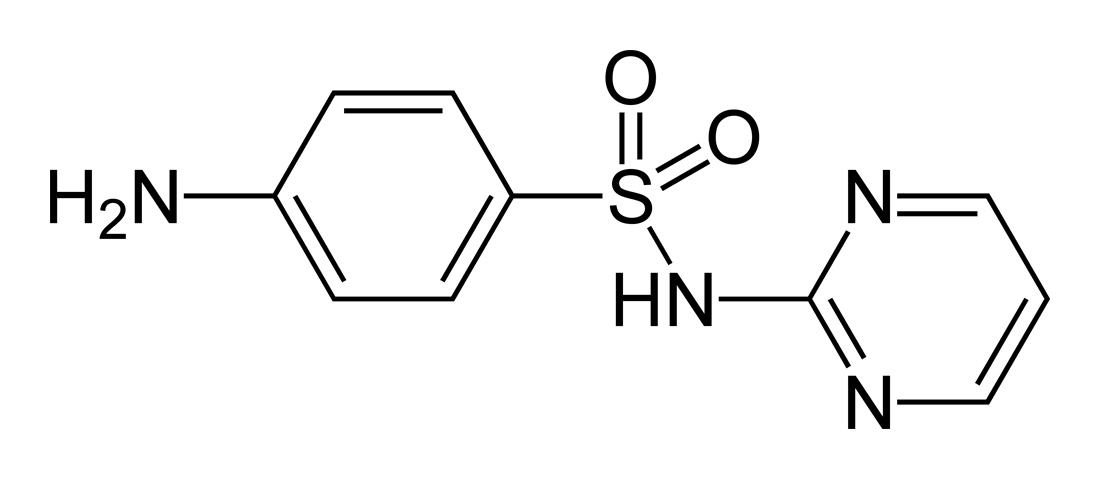
スルファジアジン
1947年 サルファ剤、スルファジアジン(sulfadiazine)が開発された。スルファジアジン(Sulfadiazine)は、サルファ薬の一つ。感染源の細菌細胞内での葉酸の合成を阻害することによって殺す効果があり、尿路感染症(UTIs)の治療に使われる。スルファジアジンとピリメタミンとの組み合わせは、トキソプラズマ(Toxoplasma gondii)が原因のトキソプラズマ症の治療に使われる。副作用については、吐き気、消化不良、拒食症、そしてめまいが報告されている。出典: フリー百科事典『ウィキペディア(Wikipedia)』サルファ剤、忘れられた奇跡 世界を変えたナチスの薬と医師ゲルハルト・ドーマクの物語/トーマス・ヘイガー/小林力【3000円以上送料無料】
2021.04.09
コメント(0)
-
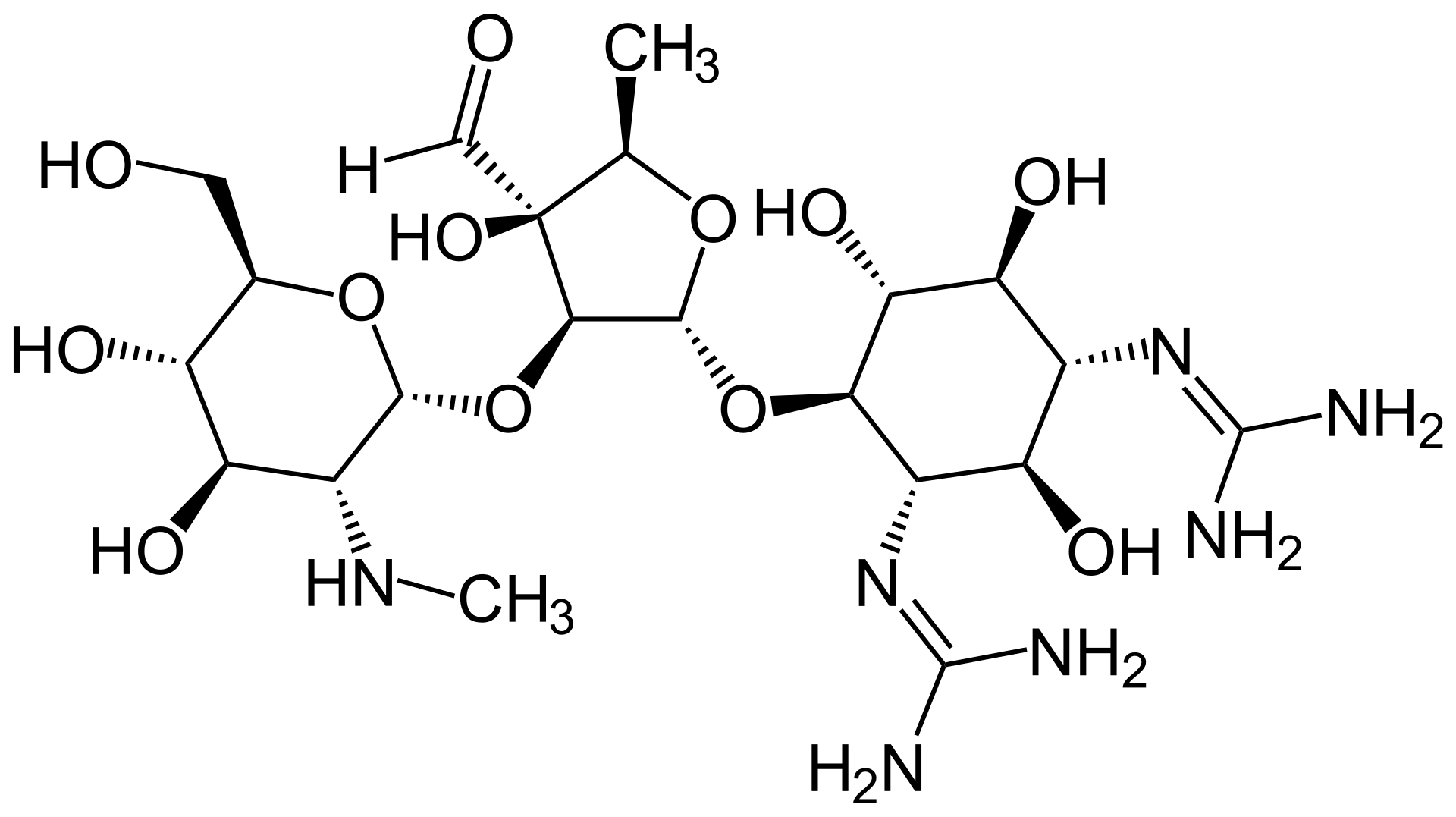
ストレプトマイシン
1944年最初のアミノグリコシド系抗生物質、ストレプトマイシン(streptomycin:SM)が開発された。ストレプトマイシン(Streptomycin)は抗生物質のひとつである。最初に発見されたアミノグリコシド類であり、結核の治療に用いられた最初の抗生物質である。略してストマイともいう。放線菌の一種 Streptomyces griseus の代謝物から発見された。真正細菌(バクテリア)型リボソームのみに選択的で、それ以外の生物、例えば古細菌には効果がない。古細菌に近い祖先をもつと考えられる真核生物本体のリボソームも阻害を受けず、真正細菌のみを選択的に殺すことができる。ただし、ミトコンドリアリボソームは進化的に真正細菌に起源があり、ある程度影響を受ける。これが副作用の原因の一つになると考えられている。なお、ストレプトマイシンは消化管からの吸収がよくないため経口では投与できず、筋肉内注射(筋注)を行わなければならない。現在では、硫酸塩および誘導体のジヒドロストレプトマイシンが農薬の一種である殺菌剤として発売されている。歴史1943年10月19日、ラトガース大学のセルマン・ワクスマンの研究室の卒業研究生、アルバート・シャッツ(Albert Schatz)によって最初に単離された。ワクスマンらはアクチノマイシン、クラバシン(clavacin)、ストレプトスリシン(streptothricin)、ストレプトマイシン、ネオマイシン、フラジシン(fradicin)、カンジシジン(candicidin)、カンジジン(candidin)など数々の抗生物質を発見している。これらのうちストレプトマイシンとネオマイシンの2つは、多くの伝染病の治療に広く適用されている。ワクスマンは抗生物質の英語 antibiotics の考案者としても知られる。日本からは東風睦之博士が当時は異例であった客員研究員として招聘され、1951年と1952年に連名で論文を発表し研究に大きく寄与した。ストレプトマイシン発見者としての詳細と名声がシャッツによって主張され、これは訴訟にまで発展した。シャッツはストレプトマイシンの発見者ではあるが、ワクスマンの指導のもとストレプトマイシンの研究を行うよう命じられていた卒業研究生にすぎず、ワクスマンの研究室の技術、装置、設備を使っていたことが論争の原因である。シャッツを1952年のノーベル賞受賞者に含めるべきという主張もあった。しかし委員会は、受賞理由はストレプトマイシン発見の功績だけでなく、発見につながった方法論や技術、および他の多くの抗生物質の発見を含めたものであるとして、この主張を退けた。この訴訟は、ワクスマンとシャッツがストレプトマイシンの共同発見者であるとみなすという公式判定が下り、和解により終息した。シャッツは1994年、74歳のときにラトガース賞を受けた。日本日本では、1950年より科学研究所(理化学研究所の前身)が生産に着手。1951年10月には30トンタンク3基を稼働させ、国内需要の1/3を生産する規模にまで拡大させた。当時の新聞広告には「結核の38度線」というキャッチコピーが用いられている[10]。適応結核感染性心内膜炎(ベンジルペニシリンまたはアンピシリンと併用の場合に限る)ペスト野兎病非結核性抗酸菌症(マイコバクテリウム・アビウムコンプレックス(MAC)症を含む)ワイル病作用機序ストレプトマイシンはタンパク質合成を阻害することによりバクテリアの成長や代謝を停止させる。具体的には、バクテリアのリボソーム上の23S rRNAに結合し、代謝を担うあらゆるタンパク質の合成、つまりリボソーム上でのポリペプチド鎖の合成の開始を阻害する。副作用他のアミノグリコシド系抗生物質と同様に内耳神経(第VIII脳神経)・腎臓に対する毒性を持つので、副作用として難聴・腎機能障害などが現れる事がある。したがって投与に際しては聴覚機能・腎機能検査の併用が必要であり、副作用の兆候が現れたら投与を中止すべきである。かつては、ストレプトマイシンによる難聴は「ストマイ難聴」と呼ばれた。母系の親族にストマイ難聴患者がいる場合特に注意が必要である。ミトコンドリアの12S rRNAにA1555G変異を持つ場合、ストレプトマイシンを含むアミノグリコシド系抗生物質への感受性が高く、少量の投与で難聴を引き起こす。上記の第VIII脳神経、腎機能障害の他に、肝障害・間質性肺炎・ショック・アナフィラキシー・中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(スティーブンス・ジョンソン症候群)・溶血性貧血・血小板減少が発生し得る。毒性マウスLD50は、静注145〜300 mg/kg、皮下注600〜1,250 mg/kgである。アメリカ食品医薬品局 (FDA) のガイダンスを参考に、マウス(静注)145 mg/kg をヒト等価用量 (HED) 換算すると、ヒト11.79 mg/kgとなる。日本人男性(成人)の平均体重65〜70kgでは766〜825 mgが相当する。同様に、マウス(皮下注)600 mg/kgをHED換算すると、ヒト48.78 mg/kg(3,170〜3,415 mg)となる。臨床用量は1日1〜2 g(筋注)である。出典: フリー百科事典『ウィキペディア(Wikipedia)』ストマイ液剤20 100ML
2021.04.08
コメント(0)
-

スルファメラジン
1943年サルファ剤、スルファメラジン(sulfamerazine)が開発された。サルファ剤、忘れられた奇跡 世界を変えたナチスの薬と医師ゲルハルト・ドーマクの物語
2021.04.07
コメント(0)
-
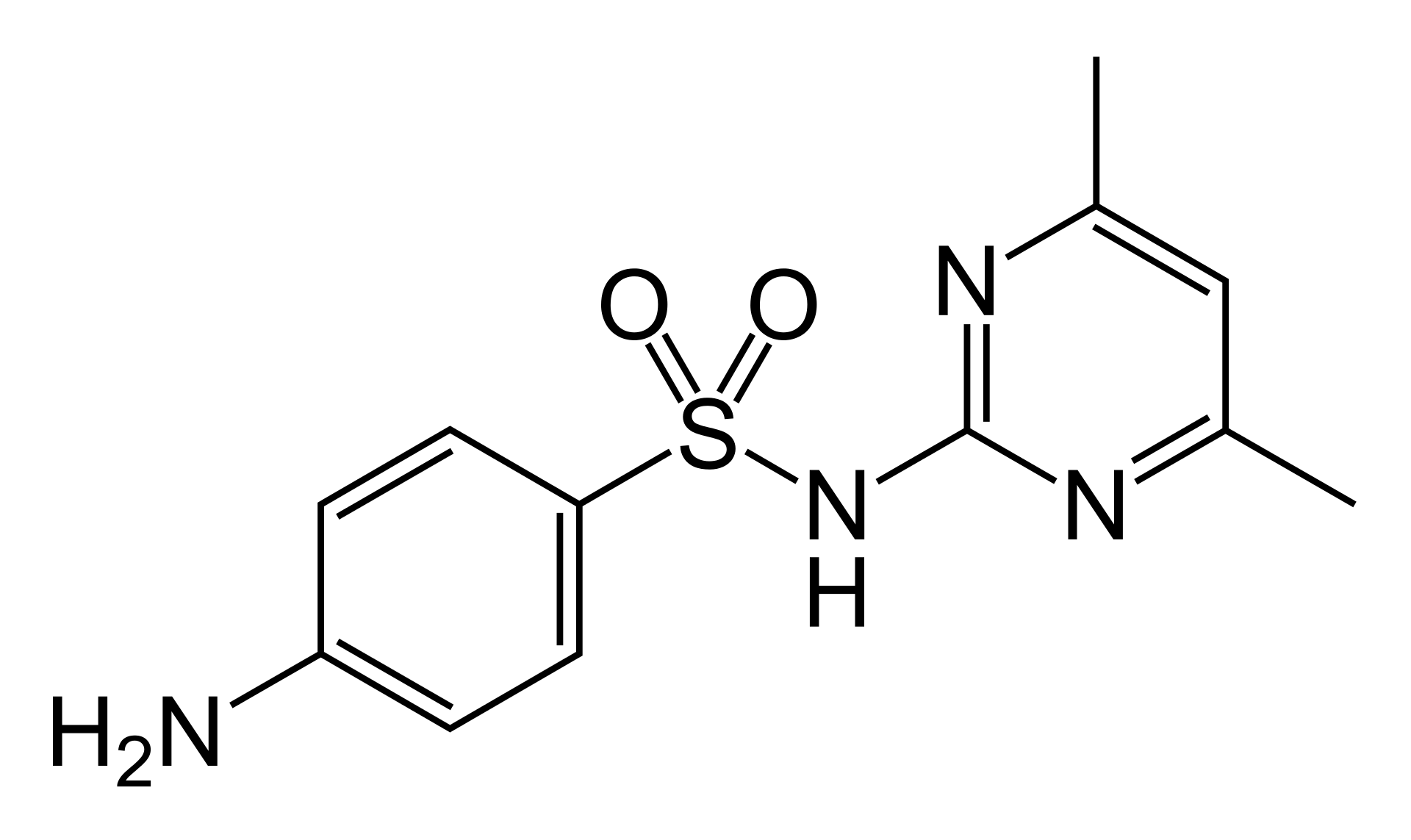
スルファジミジン
1942年サルファ剤、スルファジミジン(sulfadimidine)が開発された。出典: フリー百科事典『ウィキペディア(Wikipedia)』サルファ剤、忘れられた奇跡 世界を変えたナチスの薬と医師ゲルハルト・ドーマクの物語
2021.04.06
コメント(0)
全202件 (202件中 51-100件目)












