2018年01月の記事
全19件 (19件中 1-19件目)
1
-

生徒実験:反応に伴う熱の出入りとヘスの法則(予備実験)
反応熱を水温の上昇で測定する実験を行い、ヘスの法則を検証する生徒実験を行います。昨日はそのための予備実験を行いました。溶液の密度や比熱容量をどこまでこだわってやるのか検討しました。実験書は市販のものです。実験の写真です。発泡ポリスチレンのカップ(「サーモカップ」として教材業者から買いました)とデジタル温度計(感度0.1℃)、一番下は自作の電池式スターラー。まずは温度上昇度Δtを知るために温度変化を時間を追ってグラフにしました。検討するのは、①熱が容器から逃げ出し、温度が下がるので、グラフを書き外挿した値を使えば良いか、最高温度を使えば良いか?②水の比熱容量4.18J/(gK)の他に容器の比熱容量2.0J/(gK)と攪拌子(鉄とした)の比熱容量460J/(gK)を計算に入れるか?③この実験書では溶液の密度は全て1.00g/cm3として計算させているが、それぞれの溶液の密度を考慮する必要があるか?以上3点を計算に入れ、計算しました。それぞれの理論値よりはるかに低い溶解熱・中和熱です。原因は水酸化ナトリウム(固)が吸湿してしまったことだとおもいます。。でも、同じ水酸化ナトリウムを使えばヘスの法則は検証できるので、やってみます結果は以下です。表中最下行のヘスの法則の検証だけなら、①発泡ポリスチレンは断熱性が良いので最高温度を使い、グラフの外そうから求めなくてもよい②比熱は水と発泡ポリスチレンを使うとよい。容器は事前に質量を測らせておく③溶液の密度はこの実験条件なら、気にせず全ての溶液とも1.00g/cm3としても大差ないこんな感じです。入試などでは、温度ー時間グラフの外そうからΔtを求める問題が出ますので、実験でグラフを書かせてもいいでしょう。また、各溶液の密度を与えて、熱量を計算させてもいい勉強になります。学校の生徒の素養や意欲によって色々変えても、そこそこ5%くらいの誤差でヘスの法則の検証ができます。
2018.01.31
コメント(0)
-

生徒実験:コロイド溶液の性質(レポート)
生徒実験:コロイド溶液の性質(実施)→1/29ブログ昨日の実験のレポートが提出されました。良いものはこんな感じちょっと、誤解もあったようでうが、明日授業で解説します。そのほかのレポートの多くは気に入りません。以下に気に入らない点を記します。昨日の実験のテーマは「結果を考えて、知識を動員して実験する」です。実験にあたっては仮説を持つこと、それを超える事実が出たら研究のヒントになる。①それがレポートに現れていない生徒のレポートが多かった。②日本語が読めない・書けない 問われていることを答えていない。「色は?」と聞かれて「変化なし」と答える 主語が書いていないので、何がどうなったのか伝わってこない(どうなったかは書いてある) 文章にして書いて欲しい。単語の羅列ではわからない自然科学では、現象を相手に正確に伝えるために、記述が大切なスタートです。日本語や記述ツールの数学などかなり気を使わなければなりません。生徒は高校の実験のレポートなどやっつけ仕事でやっているのだろうと思いますが、いやしくも理系であり、これから自然科学の学徒になろうとしている生徒さんは今、ここで訓練が大切かと思います。明日は彼らにその覚悟を持ってもらえるよう伝えたいと思っています。
2018.01.30
コメント(0)
-

生徒実験:コロイド溶液の性質(実施)
生徒実験:コロイド溶液の性質(予備実験)→1/25ブログで予備実験した「コロイド溶液の性質」を生徒実験しました。説明・注意15分、実験操作・片付け35分です。計算がなく、数値記録が少ないのですが、操作自体が多く、生徒は少しバタバタしてました。この程度の実験でも(コロイドは演示して作ってあげても)35分でやっと終えました。以下は、器具です。線香・ガスマッチ・赤色レーザー光源です。秋葉原、秋月電機の赤色1mWの半導体レーザー光源を各班に用意しました。1000円以内で自作できます。また、製品も安く手に入りますので1/25のブログを参照ください。いくつか、良かったところ、気になるところを記します。①今回の実験テーマは「結果を考えて、知識を動員して実験する」です。「こうなるはずだ」と考えながら実験すること(仮説)で、そうならないときに新たな発見がある。先入観と仮説は違うことを強調しました。先週の授業で「コロイド溶液の性質」をやりましたので、忘れた生徒も少なくなかったようです。②予備実験で透析したときは微量のFe3+イオンがセルロースチューブを通過するこを確認できました(K4[Fe(CN)6]溶液で薄い青色)が、今回は確認できた班はなかったようです。③各班にレーザー光源を持たせたのは、良かったです。納得いくまで、コロイド溶液と真の溶液、煙コロイドを見てました。楽しそうです。目には当てるなとしつこく注意しました。④ゼラチンコロイドは4%にしました。寒いので朝ゲル化してましたが、少し温めてゾルにしました。部屋を暗くしてチンダル現象はしっかり見えました。水酸化鉄(Ⅲ)コロイド溶液ももちろん見えました。⑤ゼラチンコロイドは硫酸ナトリウム水溶液をいくら入れても濁りません。塩化ナトリウム固体をサジ小で4杯入れて攪拌すると濁ります。塩析です。⑥ポスカを水に解いて、ホールスライドグラスに入れ普通の顕微鏡でもブラウン運動を観察できます。色はなんでもいいのですが、今回は緑。白い光点がブルブルしているの観察できます。教卓に2台置いて、手の空いた生徒から観察させました。実験はものを見て考える訓練だとおもいます。知識があればあるほど深い見方ができて、考えも深まります。決して、知識の確認ではないと思っています。操作だけにとらわれていると意義が半減します。
2018.01.29
コメント(0)
-

生徒実験:コロイド溶液の性質(予備実験)
近く「生徒実験:コロイド溶液の性質」行います。予備実験をしたので、テキストと合わせて紹介します。テキスト抜粋です。実験1では水酸化鉄(Ⅲ)コロイドを作ります。沸騰水中に塩化鉄(Ⅲ)水溶液2mLをゆっくり滴下します。FeCl3+3H2O→Fe(OH)3+3HCl で水酸化鉄(Ⅲ)コロイドになり色は黄褐色だった滴下液が濃いワインレッドになります。これをセルロースチューブを水でほぐしてパイプ状にし、中に流し込みます。どうせ、透析するのですから、水道水でほぐしています。外は純水で洗います。ビーカーの純水中に5分程度浸します。「透析」です。コロイド粒子はチューブ内に残り、Cl =,H+、微量残ったFe3+がビーカーの純水中に拡散して出てきます。実験操作④でビーカー内の純水に硝酸銀水溶液を加える→白濁して、Cl-の確認BTB水溶液を加える→黄色に変わり、H+の確認ヘキサシアノ鉄(Ⅱ)酸カリウム水溶液(黄色)を加える→青変してFe3+の確認(微量なので、この青変には時間がかかった)次に、セルロースチューブ内のコロイド溶液をピペットで試験管にとり、他に4%ゼラチンコロイド溶液を試験管に用意します。まずは、⑥で「チンダル現象」を見ます。光源は物理科で安価に手作りしていた半導体レーザー光源を使いました。続いて、硫酸ナトリウム水溶液を加えて、水酸化鉄(Ⅲ)コロイド=疎水コロイドの「凝析」を観察します。ゼラチンコロイド=親水コロイドは硫酸ナトリウム水溶液をいくら入れても変化ありませんが、水酸化鉄(Ⅲ)コロイド=疎水コロイドは1滴で濁ります。「凝析」ですね。下の写真、左は「凝析」を起こした水酸化鉄(Ⅲ)コロイド右は「塩析」食塩を固体で大量(薬サジ小2杯くらい)に溶かし込んだゼラチンコロイドです。このくらい、食塩を入れないと濁り始めません。最後に、光学顕微鏡でポスカのインクを水にとき、「ブラウン運動」を観察します。教卓に2台用意して、手の空いた生徒から見てもらいます。スマホカメラを接眼レンズに当てて撮った写真です。点々がポスカインクのコロイドでぶるぶる動いていました。チンダル現象で使うレーザーポインターは自作でも電池こみで1000円を超えます。1台千円ちょっとで楽天から手に入ります。2349 ヤザワ レーザーポインター LPB2401BK【メール便選択可能】価格:1220円(税込、送料別) (2018/1/25時点)
2018.01.25
コメント(0)
-

銅アンモニアレーヨンの合成;予備実験
同僚が「銅アンモニアレーヨンの合成」実験を3年生用にに企画しました。これを追試・予備実験します。上記の実験書(1)(2)(3)の写真(2)では2mol/L NaOH水溶液をゆっくり5mL加えました。さらに、(4)の写真沈殿を三角フラスコにとり、濃アンモニア水を溶けるまで少しづつ加えます。濃アンモニア水は最終的に10mLまで加え、さらに水酸化ナトリウム固体を1粒加えたのが写真右。モーレツにアンモニア臭いので、ドラフトで操作し、ゴム栓して取り出します。これをシュバイツァー試薬といいます。そして、ろ紙をちぎって溶かしながら加えます。90mmのろ紙を半分溶かしました。かなり粘る液体になりました。これを注射器ですって、硫酸水溶液に押し出します。結果は上の写真右です。ひも状のものも出来ましたが、なんだか、ミミズやウーパールーパーみたいなものができてしまいました。あまりに粘りが強く、ブチュっと出てしまい、スムースに出ませんでした。アンモニアや銅は硫酸の中に出てしまいます。硫酸はだんだんと青くなってきます。銅イオンです。乾燥させた「ミミズ」はこれです。この実験の問題は①濃アンモニア水を使うのでひどく臭い。このままでは生徒には辛いかな。②セルロース源にろ紙を使うより綿を使ったほうが早く溶けそう。③溶かすセルロースの量は検討が必要。スムースに注射器から押し出せるくらいの粘度にする必要がある。以上を改善して、次の機会に生徒実験できるように掲載しますね。
2018.01.24
コメント(2)
-

チオ硫酸ナトリウムNa2S2O3・5H2Oの過飽和溶液
埼玉は大雪警報。雪の日は暖かい話題を授業で1/22ブログで過飽和溶液の再結晶が発熱反応になることを紹介しましたが、写真をのせ、やり方を説明します。左写真:左:チオ硫酸ナトリウムNa2S2O3・5H2Oの固体(一度過飽和にして再結晶させたもの)右:固体を直火で加熱して過飽和溶液にしたもの(室温まで冷やしてあります。手前はチオ硫酸ナトリウムの結晶)加熱は直火で穏やかに加熱します。私はアルコールランプ(トーチ型)で加熱しました。ガスバーナーでももちろんできます。加熱は振りながら行います。結晶水に溶けますので、水は加えません。少し濁ったような溶液になりますが、目に見える固体は溶かしきってください。溶けたら、放置して室温まで冷やします。右写真:チオ硫酸ナトリウムの結晶を投入すると、結晶を種にして発熱しながら全体に固まり、左写真の左の試験管のようになります。投入した結晶の周りに針のような結晶が生じはじめてからすぐに全体に固まります。再利用可能です。後片付け:チオ硫酸ナトリウムが固まった試験管は少し加熱すればまた溶けますので傾ければ固まりがすぐ取れます。その後水洗い、よく溶けますのですぐ落ちます。少量なら水道水の塩素などで酸化され分解されますので流してもかまわないでしょう。観賞魚の水の塩素除去に使うくらいですから…
2018.01.23
コメント(0)
-

埼玉は大雪警報。雪の日は暖かい話題を授業で
埼玉も東京も大雪警報が出ています。明日朝までに大宮で10-15cm,東京で5-10cmの積雪が予想されています。私の勤務校は3:40までに完全下校。明日は9:30から登校となりました。そんな中、授業では「反応熱」の授業第1時間目です。寒いですが、少しは暖かい話を2つ。①「昔から、雪の降る日は暖かい」と言われているがなぜ?融解熱から考えると、水が氷になるのは発熱反応。H2O(液)=H2O(固)+6KJということで、熱が出るので少しは暖かい。なんてね。「諸説があり、厚い雲で放射冷却が抑えられる」とか言われることもあります。溶解熱のカイロ。バレンタインぴったり!【大人気】プチプレゼントとしても最適★癒しのエコカイロ価格:216円(税込、送料別) (2018/1/22時点)【使い方】カイロの中の金属ボタンを軽く押し曲げます。すると透明な液体が白く結晶化し熱を発します。約40度の暖かさが約20分持続します。【再利用方法】沸騰したお湯の中に入れ、白い結晶が完全になくなるまで(約5分程度)煮てください。完全に液体に戻ったら流水等で冷やし、熱がなくなれば再利用できます。※完全に熱が冷めてからボタンを押すと再度結晶化し発熱します。チオ硫酸ナトリウムと酢酸ナトリウムの濃厚溶液を厚手PVCの袋に収めたものです。②試験管にチオ硫酸ナトリウムの結晶Na2S2O3・5H2Oを4cmほど入れて(他は何も入れず)、炎でゆっくり加熱します。結晶水によって溶液になります。そのままそっと保存し、室温まで下げても溶液のままです。溶解度をはるかに超えていますが、過飽和溶液です。授業では、教室に3本ほど持っていき過飽和状態の試験管を回覧。その後、チオ硫酸ナトリウムの結晶を落としてやると一気に結晶が析出します。その際、発熱します。これは、チオ硫酸ナトリウムの溶解熱(解けるときは吸熱反応)です。見た目でも、面白く。結晶の析出によって発熱するのは、生徒には未経験で「不思議だ」と興味深く見てもらえます。生徒は濃硫酸の溶解熱については中学校の時に印象があるようです。反応熱の種類を講義する時に使ってます。
2018.01.22
コメント(0)
-
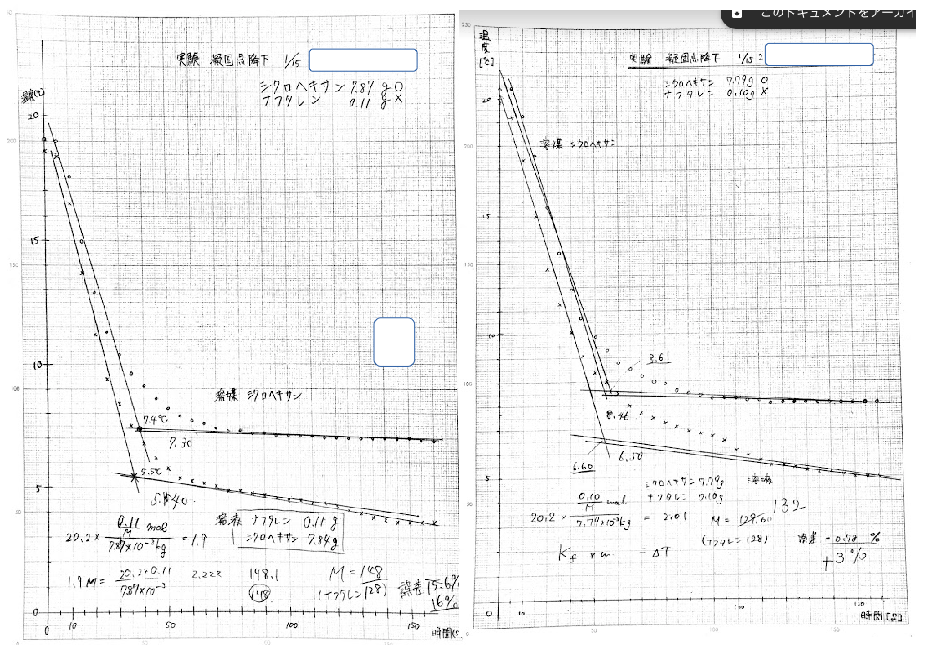
「凝固点降下で分子量を求める」⑤レポートに青ざめる
「凝固点降下で分子量を求める」④生徒実験→1/15ブログのレポートが上がって来ました。レポートからこの実験を評価したのですが、残念なことに今年のこの実験はうまくいかなかったこの実験はシクロヘキサンを溶媒とした凝固点降下から溶質ナフタレンの分子量を求めるものです。理論値、ナフタレンの分子量は128です。これまで本校で2回同じ実験をやってますがほとんどの生徒が誤差10%以内に収まっています。しかし、今回の生徒のレポートでは、誤差10%以内18%誤差30%以上67%でした。これはひどい…原因は1/15ブログでも書いたように、ナフタレンをシクロヘキサンに完全に溶かしきっていないことです。大きな誤差は全て理論値128を超えており、このことを示しています。グラフはとてもよく書けており、一生懸命レポートを書いている様子が伺えます。グラフの書き方は今後も実験を通じて教えていきますが、ご覧ください。レポートを返却して生徒への指導をしました。①グラフを使って表現することはかなり身についてきてとてもよかった。→これからも、「熱化学;ヘスの法則」「化学平衡;滴定曲線」でグラフを書く機会があるのでしっかり身につけさせたい。②実験するときは知識を総動員して、考えながら操作してほしい。→実験では生徒は授業より気を抜いたり、人任せにするような気がしします。実験操作の時こそしっかり考えて、批判的に操作して欲しい。例えば「溶液にしろ」「溶解せよ」と言われたとき、溶質を入れて溶かさずそのまま次の操作に移ったことが今回の実験の失敗に繋がります。「溶液・溶解」の言葉の意味を考えて欲しい。高校化学の実験は必ず誤差5%以内に収まるように、予備実験をして生徒に実施します。そうしないと、化学や授業への信頼感が薄れてしまいます。今回の(私の)失敗には青ざめました。来年度にリベンジします。
2018.01.19
コメント(0)
-
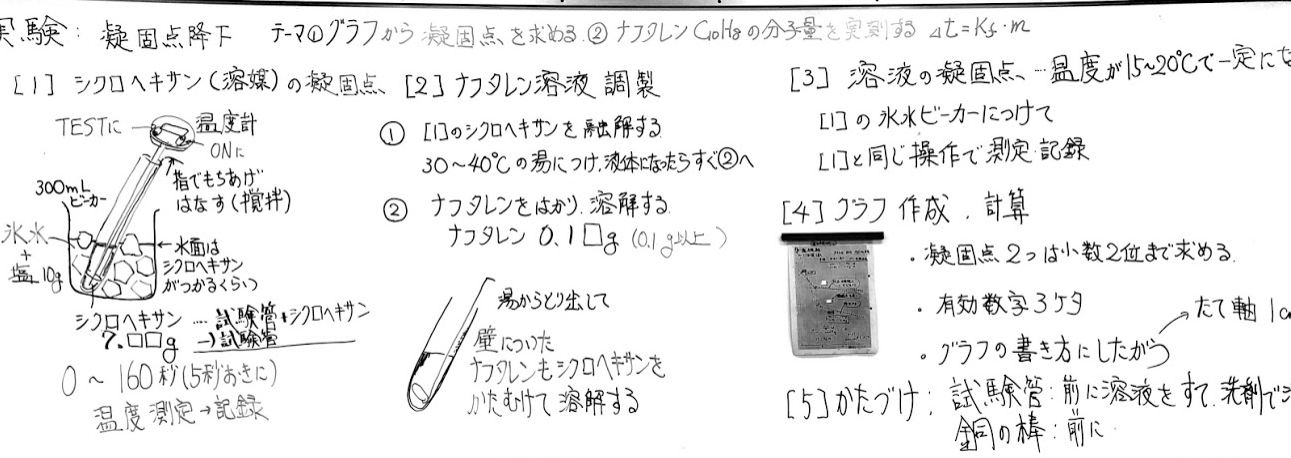
「凝固点降下で分子量を求める」④生徒実験
凝固点降下の生徒実験を行いました。2年生2クラスです。予備実験については「凝固点降下で分子量を求める」予備実験②上手く結果を出すコツ→1/11ブログ「凝固点降下で分子量を求める」予備実験①→1/11ブログです。予備実験の反省を生かして実験室白板解説・注意15分、生徒実験/片付け25分で残り10分で生徒たちはデータ整理をしました。実験上の注意点は以下です。これを怠ると、せっかく実験しても満足のいく結果が出ず、生徒の意欲が下がりそうです。①氷水の水面をシクロヘキサン面より上にして試験管をつけ、冷却する→注意を聞いておらず、水面がかなり下の実験班がありました。この班では試験管の下側のみ凝固、温度が下がり続け、上は液体の状態が続いて温度が下がり続け、凝固点が明確に出ませんでした。②ナフタレンをシクロヘキサンに完全に溶解する→「溶液にする」と注意したのですが、計ったナフタレンを試験管に投入したのち、完全に溶解しない班がいく班かありました。これは私が油断していたこともあり、廃液回収の時とけ残りのナフタレンを見つけました。事前の注意と巡回時に確認しておくべき大事なポイントでした。③グラフの書き方→測定値をグラフ用紙に打点したあと、誤差を勘案しながら直線を引くこと。→シクロヘキサンが全て固体になったあと再度温度低下があるが、凝固点を求めるグラフ作業には関係しないこと。(現象としては押さえておく必要があるが…)→生徒実験では見本のグラフと違い、液温20℃くらいから始めたので、グラフの縦軸は1℃=1cmにしないと用紙に収まらない。次の写真は、見本として生徒に配布したグラフと書方の例以上が、予備実験・生徒実験を行いながら気がついたポイントです。明後日1/17にレポート提出です。生徒の実験結果はまたあとで掲載します。
2018.01.15
コメント(0)
-

「凝固点降下で分子量を求める」予備実験③デジタル温度計の入手
「凝固点降下で分子量を求める」生徒実験を準備しています。予備実験までを昨日紹介しました。「凝固点降下で分子量を求める」予備実験②上手く結果を出すコツ→1/11ブログ「凝固点降下で分子量を求める」予備実験①→1/11ブログ今回はデジタル温度計の入手について①正確な温度を測るのでなく、温度差を見るので厳しく校正してある必要はない②感度および精度は0.1℃③生徒の実験班数そろえるので1台あたりの単価は安いものが良い以上勘案して、これを試しに注文しました。■送料無料■デジタルペンサーモ■デジタル温度計■天ぷらにも■-50〜+300℃■料理用■食品の中身の温度など、スッと差し込むだけ■ペン型■水温計★モール内何キング1位獲得★価格:470円(税込、送料無料) (2018/1/12時点)評価は届いてから後日ブログで掲載します。
2018.01.12
コメント(0)
-
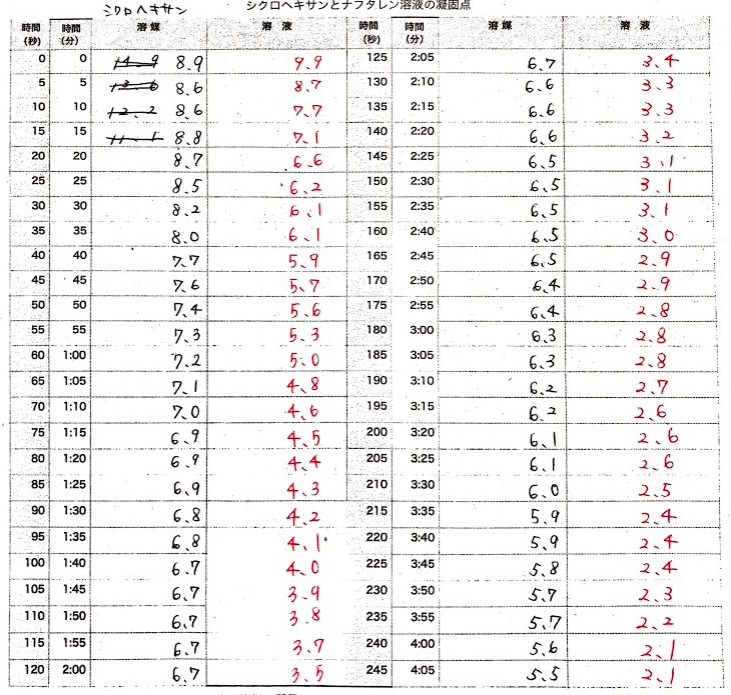
「凝固点降下で分子量を求める」予備実験②上手く結果を出すコツ
「凝固点降下で分子量を求める」予備実験①→1/11ブログで実験操作を紹介しました。さて、結果です。毎年、予備実験・生徒実験と実施しているのですっかり操作が雑になり、ひどい結果です。0秒から245秒まで5秒おきに記録しました。生徒が行う時は、温度計読み攪拌・時計・記入の係が必要で1班3人以上必要です。左黒字は溶媒のみ(純シクロヘキサン)、右赤字は溶液(シクロヘキサン+ナフタレン)です。これをグラフにすると溶媒のみのグラフでは点を直線で結んで、その交点がシクロヘキサンの融点になります。6.90℃でした⭕️A。文献値6.50℃で0.4℃の誤差があります。この実験では、差を取るのでこの誤差は引き算されて考えなくてもいいです。溶液のグラフでは変化の直線が3本引けてしまいました(ホントは綺麗に2本です)。交点は2つ⭕️B=5.25℃と⭕️C=4.40℃どちらかが溶液の凝固点です。実験の「いい加減さ」が原因です。あとでコツを紹介しますのであえてかっこ悪い結果をのせました。さて、計算です。⭕️Bと⭕️Cの値を使い2通り計算します。溶質ナフタレンC10H8の分子量は128です。Δt=⭕️Aー⭕️B=1.65=20.2X(0.12/M)/(7.55X10^-3) M=195 Δt=⭕️Aー⭕️C=2.50=20.2X(0.12/M)/(7.55X10^-3) M=128ということで、Δt=⭕️Aー⭕️Cの凝固点降下度がいい結果を導きました。これまで、何度もこの実験をやってますが大きくても+8%の誤差で収まります。最後に実験を上手く進めるヒントです。[1]今回の溶液のひどいグラフは溶液の底と液面の間の温度勾配が原因だとおもいます。①氷水の水面は試験管内のシクロヘキサンより高くする。②シクロヘキサンにナフタレンをとかす時、ゆっくり加熱(手で温めるなどして)して温度をあげすぎない。(実はお湯を使って溶かしましたので試験管と溶液の温度が平衡になっていない)③あまりに実験誤差が大きい時は直線の引き方をやり直す(今回の例のように、変な値が出た時にもいいデータが隠れていることがある)。[2]一般的なコツは①溶液を作る時にナフタレンを完全に溶解する。②試験管壁にナフタレンの粉が付着することがあるが、これも溶媒を傾けて溶かし込む。③針金の攪拌棒をゆっくり上下させるが、1cmくらいの上下でいい。凝固して動かなくなったらそのままにしておく。無理に動かさない。以上のことを、生徒に注意しながら実験していこうと思います。結果は来週おしらせします。どのくらいの誤差になるのか楽しみです。
2018.01.11
コメント(0)
-

「凝固点降下で分子量を求める」予備実験①
来週の月曜日に「凝固点降下で分子量を求める」実験を行います。実験書は次の写真です。上の実験を整理すると①シクロヘキサンC6H12を正確に計り、溶媒にして3分ほど氷(塩を加えて)で冷却しながら温度を5秒おきには仮記録します。②①で使ったシクロヘキサンにナフタレンC10H8を約0.1g(正確に質量を計ります)溶かして①と同じように冷却しながら温度を測定、記録します。③温度計はデジタル温度計(感度0.1℃)を使って計ります。④①と②の記録を縦軸温度、横軸時間でグラフ用紙にプロットします(冷却曲線)。⑤2つの冷却曲線から凝固点を求め、凝固点降下度Δtからナフタレンの分子量を求めます。上の写真のようになることが期待されますが、今回は針金の棒で試験管内を攪拌しますので「過冷却」現象は見られません。さて予備実験です。左上の丸いものがデジタル温度計の表示部。銀色の先端は試験管の中、シクロヘキサン中に入っています。針金を指先で上げ下げして、攪拌しながら温度を計ります。やがて、凝固して動かなくなりますが、その時は動かさずにそーっとしておき、温度だけ記録を続けます。測定が終わったら試験管を取りだし、温めて融解してから正確に測ったナフタレン(0.1g程度)を完全に溶かします。あとは同じように氷水に入れて冷却し温度測定を続けます。実験は以上です。操作時間は30分。50分の授業なので、実験の説明などの時間はゆとりがあります。予備実験の結果と成功させるヒントは次回です。
2018.01.11
コメント(0)
-

塩化ナトリウムNaCl結晶構造の実験;岩塩かち割り用に適当
★パキスタン/ガンダーラの岩塩クリスタルソルト結晶ブロック★1kg/貴重なクリスタル岩塩、岩塩用おろし金で擂ってお使い下さい(^^♪お漬物用としても美味しいです♪岩塩/食用塩 05P01Oct16価格:1177円(税込、送料別) (2018/1/10時点)塩化ナトリウムの結晶構造の学習実験用の岩塩の入手先について昨日問い合わせを受けました。Amazonから検索を始め、楽天で十分なサイズの岩塩を見つけました。実験の概要は以下のリンクをクリックしてください。「岩塩かち割り」と塩化ナトリウム型結晶←'17/7/29ブログ
2018.01.10
コメント(0)
-

希薄溶液の蒸気圧降下の演示と回覧
3学期始まりました。2年生最初の授業は「希薄溶液の性質=沸点上昇・凝固点降下・浸透圧」です。沸点上昇では「溶液の蒸気圧降下」から始めますが、教科書や図説に載っている写真では実感をつかめないので、実際に写真のようにU字管で接続した試験管を教室に持っていきます。左は純溶媒ベンゼン5g、右はベンゼン5gにナフタレン2.4gを溶かしてあります。しかし、室温18℃に1時間放置してもU字管内の水は同じ高さで変化がありませんでした。手でそれぞれの試験管の液部を握り30℃程度に温めたところ暖めるとすぐにU字管内の水面に変化が起き始め、上の写真のように溶媒の蒸気圧が溶液の蒸気圧より高くなり(溶液の蒸気圧が降下した)、右側のU字菅内の水面が上がりました。水面の高さを同じにして教室へ持っていき、手で温めて水面に差が出ること確認したところで、回覧しました。18℃だろうと30℃だろうと、気液平衡が起こっているわけで、水面に差が出ると思うのですが、この「暖めると変化が起きる」現象の原因は今の所わかりません。調査や研究してみたいと思います。ご存知の方、教えてください。
2018.01.10
コメント(0)
-
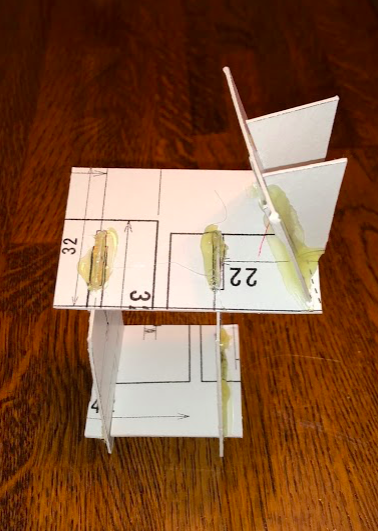
sp3用109.2°角度定規紙模型できました
メタンをはじめとする炭素正四面体に発泡スチロール球をカットする角度定規の設計図sp3炭素単結合用角度109°定規試作用図面→1/7ブログを元に厚紙で模型を作りました。球をカットし、カット面を角度定規の2面に当てて、球を4回カットすると正四面体に切ることができます。上の写真は2面を角度定規にあて、第4面を切ろうとしているところです。下の板は「2億倍分子模型定規」。カット用に穴を開けてあります。詳しくは左の[フリーページ]に載せてあります角度定規の紙モデルを眺めて使いやすく設計図を修正し、木材をカットして完成です。
2018.01.09
コメント(0)
-
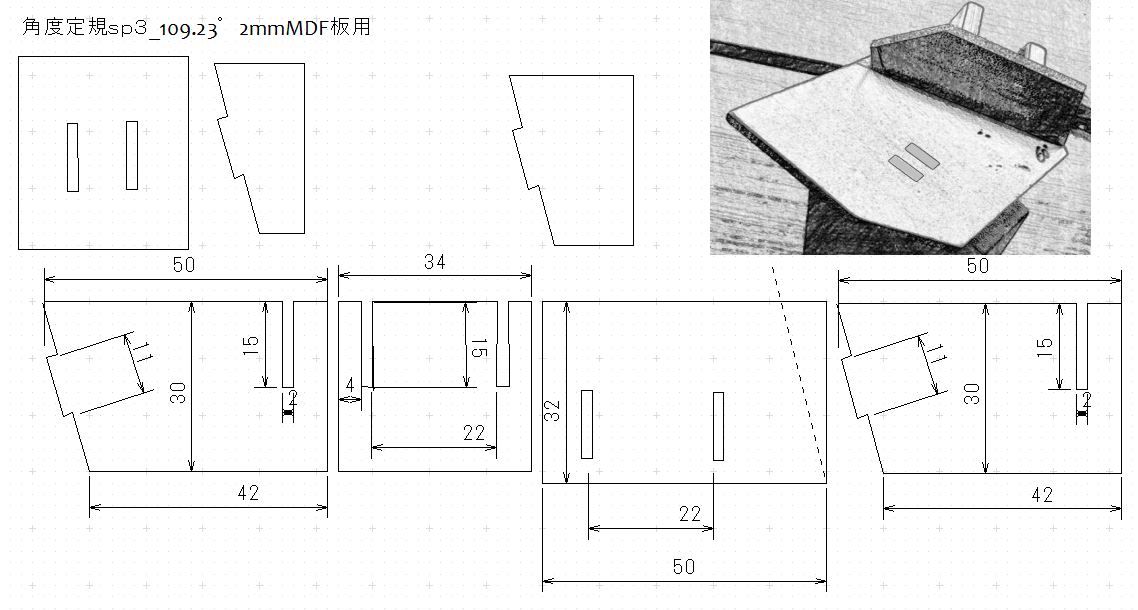
sp3炭素単結合用角度109°定規試作用図面
sp2ベンゼン用角度定規試作用図面←1/3ブログで結合角60°の角度定規の図面を紹介訂正しました。今回は「sp3炭素単結合用角度109°定規試作用図面」です109°に角度を取った板上にさらに109°の角度の板を付け、球を4面カットしたときに正四面体状になるようにします。これも、ボール紙で試作し、図面を再調整します。最終的にはMDF木材をレーザーカッティングします。
2018.01.07
コメント(0)
-

sp2ベンゼン用角度定規記事訂正
sp2ベンゼン用角度定規の紙のモデルをいじっていて気がつきました。角度面につけた60°の角度面は不要でした。写真のように60°角度面は1つで充分。よけいな羽はじゃまになります。そこで試作用図面はていせいしました。1/5ブログは削除し、sp2ベンゼン用角度定規試作用図面←1/3ブログ訂正してあります で図面を厚紙に2倍拡大コピーしてカット。 試作器の厚紙モデルを作りました。写真中では32mmとなっていますが実際は64mmです、この後、2mm(予定)のMDF材でパーツをカットし、組み上げるつもりですが、 紙で試作→図面の修正→MDF材で試作→図面の修正→完成という手順です。MDF材のカットはレーザーカッティングで行います。 作図、レーザーカッターの技術習得、カッティングパラメーターの設定など これから大変になります。
2018.01.06
コメント(0)
-
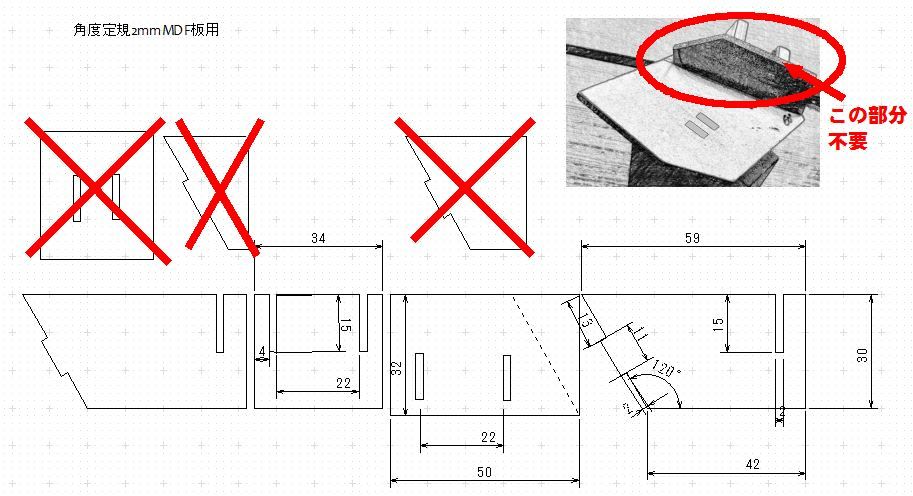
sp2ベンゼン用角度定規試作用図面
ベンゼンなど120°結合角に球を切断するための角度定規の試作図面ができました。段ボールなどの厚紙で作り、補正してから、2mm厚MDF木板での完成を目指します。
2018.01.03
コメント(0)
-
あけましておめでとうございます
あけましておめでとうございます今年の当面の目標は「分子模型カット用角度定規」を作る2mm厚のMDF木片をレーザーカッティングし、簡単に組み立てられる角度定規をめざします。こんな感じでこれは結合角60°で二つの60°かくをとってあります。球を2面・3面カットする時に簡単にできます。下のものは一面だけの角度定規です。ベンゼンなどのSP2を切るときに使いますが第3面目を切るときに平面3角形になるように球の位置を調整しなければならないので時間がかかります。2つの60°角で球を挟んでやると3面目はかんたんです。さらにSP3。メタンなど正四面体構造では109.2°で正四面体構造になるように3面目カットするとき、2つの角度(109.2°)で挟むと楽です。120°と109.2°の角度定規キットを作る予定です。しかし、試作もできていないので、これから設計とカッティング。2ヶ月はかかるかなと思います。しばしおまちください。
2018.01.01
コメント(0)
全19件 (19件中 1-19件目)
1










