[共通テスト解説] カテゴリの記事
全38件 (38件中 1-38件目)
1
-

2024共通テスト「化学基礎」解答解説速報
noteでもやってますストレートな1問1答という感じ。速やかに済ませたい。全選択の問3と、問5のケイ素からみは少し選びにくかったかも。問10のグラフ問題は、状況をつかんでグラフをうまく使うと早い。少し文章がごちゃついているので、落ち着かないと読み違えそう。第2問はサバ何とかと言っているが、要は基本事項の組み合わせ。電気分解も基本的、量的関係もうまく使えば怖くない。グラフの選び方は色々あるが、「傾きを算出」「最大値を算出」というのが基本的な戦い方。たとえば変化量などを出せばいい。適当な数値を代入してやってもOK。最後は、量的関係のからみだが、落ち着けば問題ない。全体として特に大きくひねったものはなく、比較的簡単だったと思われます。
2024.01.14
コメント(0)
-
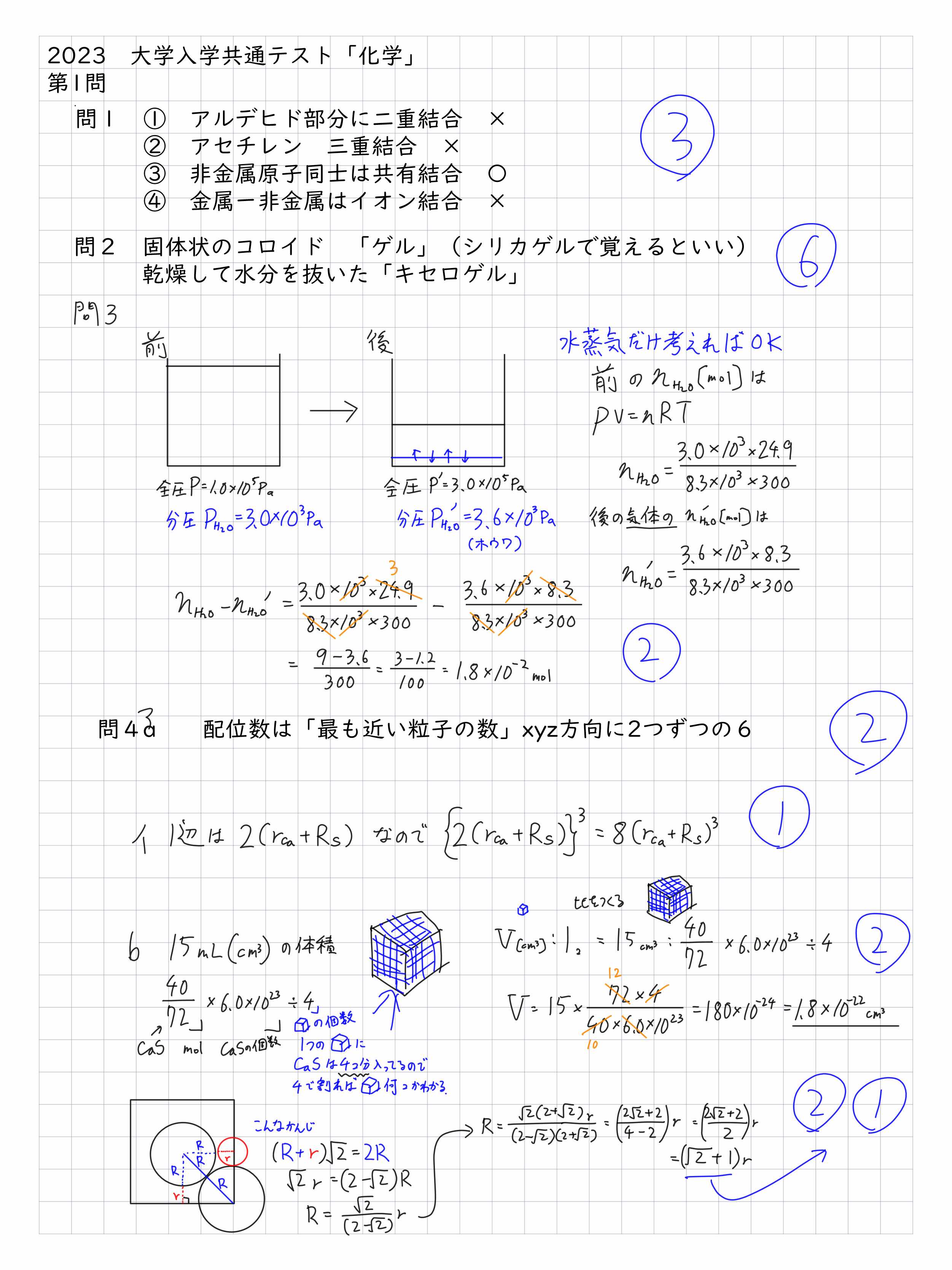
2023共通テスト「化学」解答解説速報
noteでもやってます最後のRのところ,一部訂正しました。
2023.01.15
コメント(0)
-

2023共通テスト「化学基礎」解答解説速報
noteでもやってます
2023.01.15
コメント(0)
-

2022共通テスト「化学」解答解説速報
noteでもやってます第1問 小問・ヘンリー地味に問3がやりにくい。ほとんど直感でいくか悩みどころ。時間がかかりそうなら,④⑤に絞って先に進んだほうが良かったかもしれない。5のヘンリーは基本的だが,ピストンの部分は少し読みにくい。溶解する分の気体の体積は無視してよい。というところをちゃんと読めていればスムーズだが…あと,「遊離した」を求めさせるのもちょっと意地悪。第2問 中和 反応速度 燃料電池問2は「塩酸」と「酢酸ナトリウム」でやや戸惑うが,酢酸の電離定数が成立しているというところからやっていくしかないだろう。(酢酸と,塩化ナトリウムの水溶液と考えてもいいのかもしれない。)問3もいまいちやりにくい。[A]=1は罠で,「スタート」だから,平衡時はあきらかに1ではないことに注意したい。燃料電池は頻出。覚える感じになると嫌だが,「リン酸型」で酸性のHがあるというのに注目してH⁺が電子を取りに行って…と式を立てていけば行ける。第3問 無機 アンモニアソーダ法問2は少しグラフが珍しいのでびっくりするかもだが,実はよくある問題。アンモニアソーダ法は定番なので落とせない。第4問 有機 ジカルボン酸問2の聞き方も意地悪くさい。「経由したと考えられる」なので,2,4,6のヤツしか選べない。ジカルボン酸とかいうと身構えるが,やることは同じ。異性体はちょっと数えにくいので落ち着いて取り組めたか?ただし,前半で時間を食ってしまうと,この辺焦って落としそうなところ…第5問 有機 オゾン分解 熱 反応速度問2のbは,反応熱。攻め方は色々あるかもしれないが,物質の数も多くてやりにくい。cのグラフもぱっと見いやだが,速度の求め方は基本通りやろう。dも速度式の基本的な攻め方。しかし,こんなにたくさん速度の問題が出るとは…全体として時間配分がやはり鍵か。無機有機の性質的な問題はかなり減っていて,計算や思考力を問う問題にシフトしている。平衡よりも速度がたくさん出ているのもなかなか対応しにくかったのでは…
2022.01.16
コメント(0)
-

2022共通テスト「化学基礎」解答解説速報
noteでもやってます。第1問 小問色々,中和・酸化還元しょっぱなの配位結合がひっかけ臭くて嫌ですが,選択肢的にもこれしかないので消去法で行ってもOK。問4も文章量が多いが,セッケンについて一般的に知っていればOK。某ビ〇レ「弱酸性」を売りにした石鹸があるってことは,普通は弱酸性ではないんだと覚えておけばよい。追記 イオン化エネルギーの表記が変だったので直しました問6はまともに計算すると計算量が多い。式を立てて比較する,くらいの心の余裕が欲しい。追記 問6の選択,前半は電離している酸。明らかにBの電離度が小さすぎるのでA>B 一方,中和に要する塩基の量は純粋に酸すべてのモル濃度に依存する。分母が小さいBの方が濃度が大きくなるので,A<Bだ。問9も,あまり神経質に式を追いかけると大変。文をしっかり読んで題意をつかみたい。化学基礎だと電池は若干手薄になっているかもしれない。とはいえ,丁寧に説明されているのでしっかり対応すれば問題はなさそう。第2問 熱・状態変化蒸留でまるまる1問出題してくるのはなかなか驚く。グラフなども初見だとビックリしてしまうかもしれない。特に,問3は状況が良く読めないと厳しい。第1問をいかに早く片付けて到達できたかによるだろう。bさえちゃんと計算できれば,グラフを利用してcを求めるということに気付けるはず。そういう意味では読解力・理解力をはかる良問だ。(が,実験器具の様子でもちょっと書いてもらうだけでもイメージしやすさが違ったんじゃないかな…全体として第2問が難という印象もあるが,むしろ全体的には解きやすい問題が多く易化ともいえそう。それほど大きな得点差は出ないのではないかな。
2022.01.16
コメント(0)
-
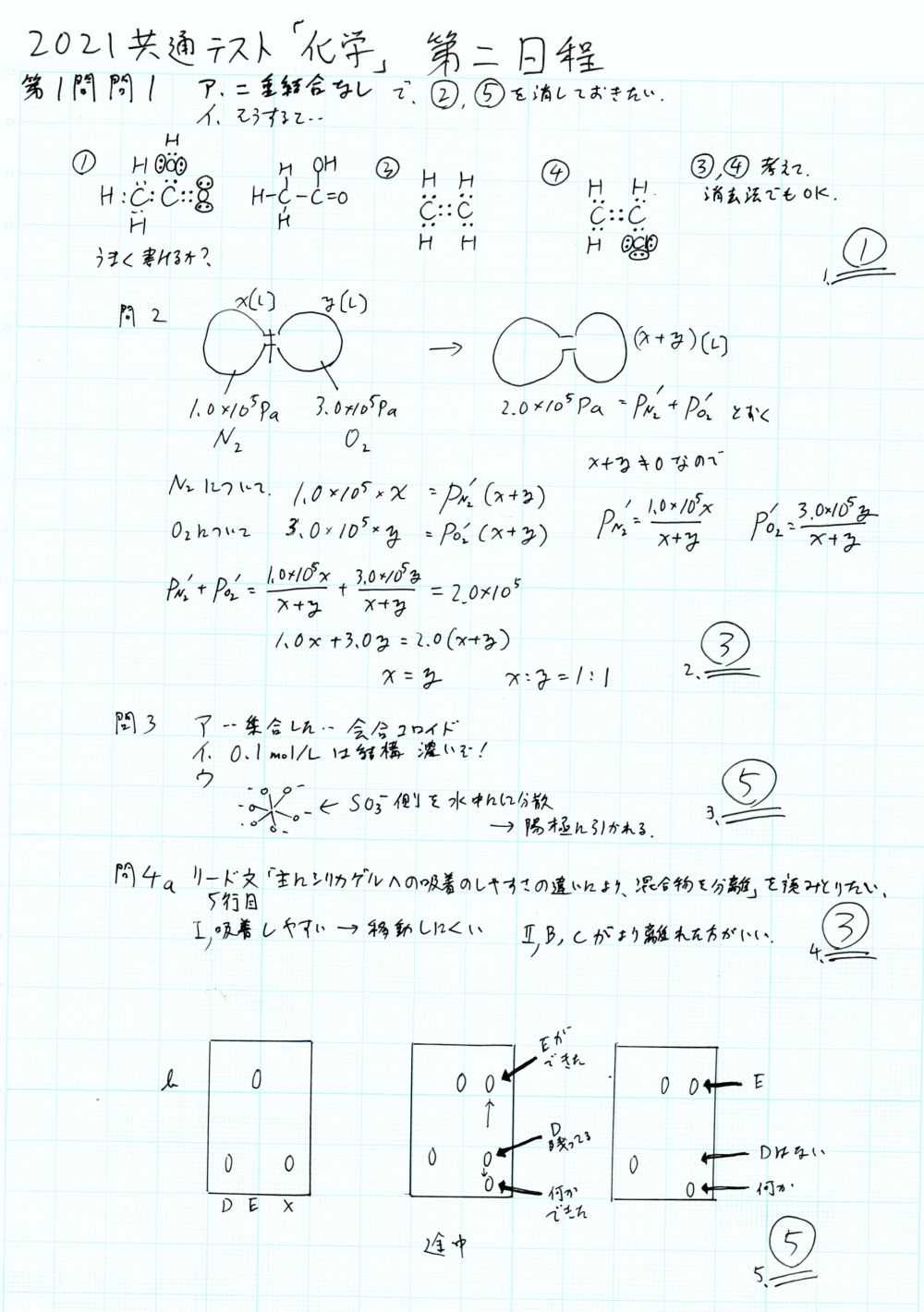
2021共通テスト第二日程「化学」解答解説
第二日程も,解説していきたいと思います。なんとなく,共通テストというよりセンター試験寄りの問題のような気もします。難易としては,第一日程の方が難しいような気もする… 問題はこちら4310-2.pdf (sankei.com) 大手の分析Microsoft Word - 4310-2.docx (kawai-juku.ac.jp) 第一問 問1の電子に関してはすぐ出てきにくいものではある。 問4のクロマトグラフィーは,類似の問題に触れていないとなかなか難しかったかも。 第二問 問1の局部電池などに関しては,ぱっと見なにやらインパクトがあるが大したことはない。 問2の緩衝液は,基本をしっかり理解していないと凡ミスがありそう。 問3の結合エネルギーは,落ち着いてエネルギー図にして整理すると良い。 問3cは,グラフがあまり見慣れないので焦るが,やっていることは普通。落ち着いて読み取ろう。どこの物質量を置いて計算するか…?というのはあるが,あとは普通に。 第三問問2のアルミの塩基への溶解は,なかなか式を覚えにくい。が,作るのも一苦労。水素発生の比は酸の場合と同じなので,そこは把握しておいても損じゃない。 問3のヨウ化銀やマンガンが絡む金属の分離はなかなかないので取り組みにくい。しかし,沈殿しやすさなどは与えてあるので落ち着いてやれば大丈夫。 問4bも,よくあるパターンだが,平衡定数の扱いに慣れていないとアイデアが出てこない。二段階電離などはよく出るので練習しておこう。 第四問問1 アセトアルデヒドの工業的製法は頻出。原子を数えて,酸素が一個付くと考えておこう。 問2 不斉を見逃さなければOK 問3aはよくあるクメン法がらみ。しかしbはやや取り組みにくい。あんまり適当にやると見落としがありそうなので,書きだしながらやっていきたい。 問4は,付加重合なので余計な原子の移動などもなく考えやすい。速やかに済ませたい問題。 第五問問1は平易。 問2はコハク酸が見慣れないが,中身は普通。特に書くこともないくらい… というわけで,第二日程の「化学」は,やや簡単なような。時間をかける場所を間違えずに,とれるところをサッととって,分離などのミスが出そうな問題を慎重に取り組むスタイルが必要かも。あとは,見慣れない題材にビビらないように,というのは共通テスト全体の傾向ですね。
2021.02.23
コメント(1)
-
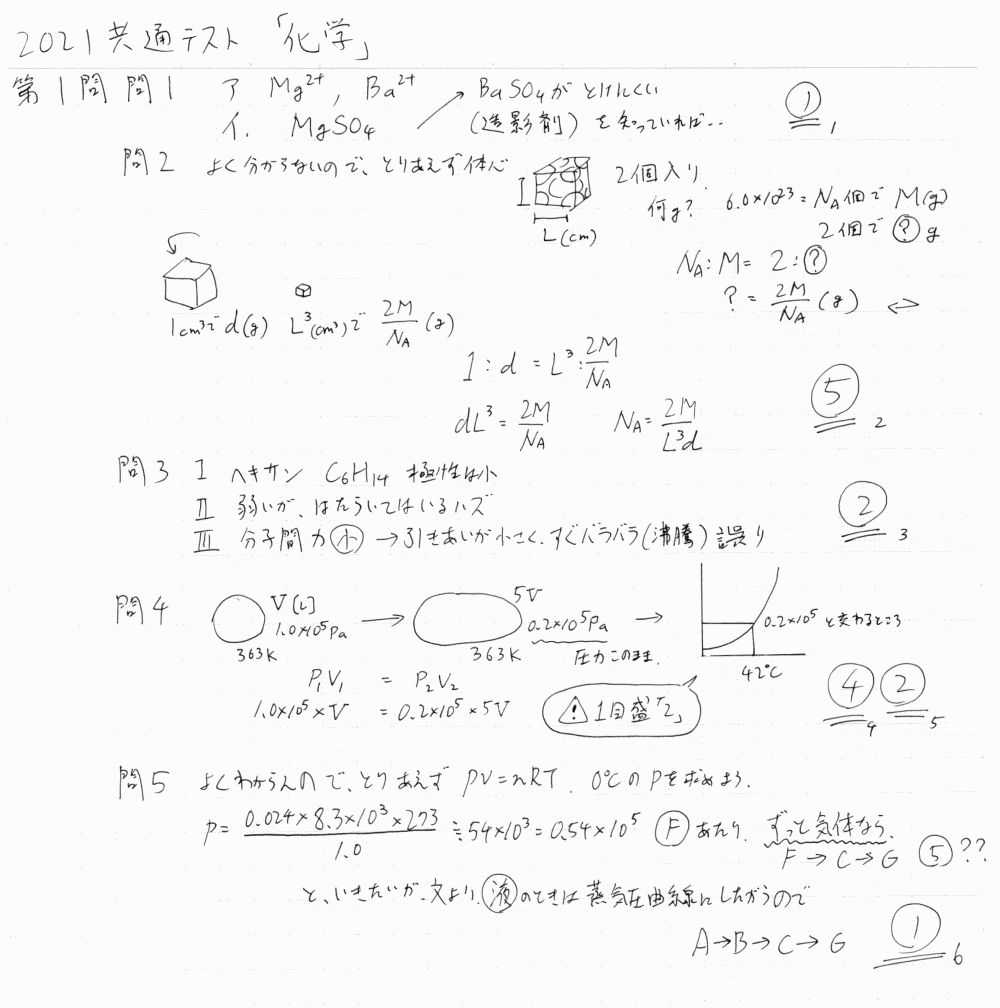
2021共通テスト「化学」解答解説速報
こちらも見ていくぞ!お疲れさまでした。 センター試験の昨年まであった後半の選択問題が消えている点は,大きな変更点といえるでしょう。 問題は公開され次第リンクを張ります。 第一問 小問・圧力など 問1のマグネシウムは少し面食らうが,落ち着いてやろう。 問2の体心立方格子はオーソドックス。 問4も落ち着いてやればいいんだけど,慌てると読み間違えそう。 問5も,聞き方がわかりにくいが,蒸気圧曲線の意味がちゃんと分かっていれば大丈夫。 第二問 電気・熱化学 問2の電気は時間を食いたくないところ。情報を読み取ってスピーディーにこなしたい。 問3はグラフや水素結合をあらかた理解している前提だ。bは特に考えにくい。問題が何を求めているか読めないとミスしそう。結局,1分子当たり何本の結合があるか,という話になる。ヘスについては,少し変わった出し方だが落ち着いて解こう。 第三問 無機・難多分,一番考えにくいのが第三問だったかもしれない。序盤は問題ないが,問3が曲者。シュウ酸の錯体という見慣れない題材。よく読まないといけない。要するに,鉄に配意しているヤツのうち,どれだけがなくなってCO₂になったか?というのをキーにしていかないといけない。中心元素のFeに注目して進める場面と,シュウ酸イオンに注目する場面とをうまく区別していかないと混乱する。1モルの鉄云々3配位が反応して,6分の1がCO₂になり,し,6分の4は鉄云々2配位になる,という。これを使っていかないと…第四問 有機特に問題ない第四問。しかし,第三問で疲弊しているとミスしそう。問5は,安易に飛びつかず,結合分を引くってのを忘れないように(私は忘れかけた)第五問 平衡・糖平衡と酸塩基はよくあるのに,糖を組み合わせてくるあたりなかなか受験生には厳しい話である。問1はちゃんと平衡定数を出していく流れを使ったほうがいいと思う。グラフは書いてもいいが,時間がもったいない気もする…糖の鎖式への変形は,ちゃんと把握しないといけない話題になってきているのかもしれない。模型で練習しましょう。問5は全体がゆるやかに連携している問題なので,総合的に糖のあたりを理解しているほど有利になった。今後はこういう出題になっていくのだろうか…?というわけで,化学の解答解説速報でした。今後の流れが見えてきそうです。追試験は,この感じで行くとえぐい問題になりそうですから,受験する人は要注意です。
2021.01.18
コメント(0)
-

2021共通テスト「化学基礎」解答解説速報
さっそく見てみましょう 問題は公開され次第リンクを張ります。こちらと同じ内容です(最近はnoteに移行しています)2021共通テスト化学基礎 解答解説速報|宮元一賢|note 第一問この辺まではケアレスミスをしなければ大丈夫そう。 問7の文字で式を表すものは考えにくいがしっかりやれば大丈夫 問8は燃料電池,話題でビックリするけど大したことはない。 第二問 陽イオン交換樹脂 陽イオン交換樹脂がとっても嫌な感じの第二問 問1が問2に関連してくるタイプというのが,共通テストの新傾向なのかもしれない。問1ができなくてもうまくいくかもしれないが,かなり厳しくなる。普通の中和滴定の問題しかやったことがないと,後半もなかなか太刀打ちできない。 というわけで,センターと比べれば普通に難化です。ただ,多分平均そのものが上がらないです。授業においても,横断的な知識や,リード文をしっかり読み込んでいろんな題材に取り組むような練習が求められそうです。
2021.01.18
コメント(0)
-

2020センター試験(追試験)「化学」解答解説
このタイミングで紛らわしいですが,2020年のセンター試験化学「追試験」の解説です。本試験はチェックしている人多いと思いますが,地味に追試験は「クセつよ問題」も多いので目を通しておくといいでしょう。なお,主なブログ記事はnoteに徐々に移行しております。宮元一賢|note 資料問題abm.php (dnc.ac.jp)正解abm.php (dnc.ac.jp) 第一問 小問 気体 溶解度など 問2が読みにくいが,ちゃんと読めば水蒸気がすぐ確定するので大丈夫。 問3はよく見るグラフ,意味を把握して読み取ろう 問4はあまり見慣れない問題化も。とにかく水減らしていって早く出そうなものを見つけよう。 問5も意味をつかみにくいが,正直酢酸からすぐ解けるし,選択肢がすくないので「あたり」をつけてやってもよい, 第二問 熱化学・化学平衡 問1の熱化学は表をちゃんと利用できれば大丈夫 問2のボルンハーバーサイクルっぽいやつは,やりなれないときつい。イオン化エネルギーなどの方向も間違えるとアウトなので,なかなかシビアな問題。 問5のグラフは教科書レベル。 問6が取り組みにくいが,硫化物イオンでの沈殿とpHの関係を前提としてしっかり押さえていればだいぶ楽。 第三問 無機問2のオキソ酸はいまいち忘れそう。 問3は,AgSCNというあまり出てこない物質だが,読めばわかるようになっている。しかし,溶解度積の意味をちゃんと把握していないとまずい。 問5も,Mg(OH)₂があまり出てこないものだが,Al側から推測できるようになっている。計算は素早くやりたい。 第四問 有機問2がちょっとびっくりするが,冷静にやればどうということはない。酸化数で計算していくこともできないこともないが,ちょっとアルデヒドの処理がやりにくいので,地道に係数を出してやるほうをお勧めしたい。 残りの問題は非常にオーソドックス。ただ,聴き方がわかりにくいものもあるので慣れた話題ほど細心の注意を払おう。 第五~七問 天然高分子・合成高分子 第五問 問2は,スクロースの変形がちゃんとわかっていないときつい。 https://youtu.be/S3UVL9q6ye8 参考にしてね。 第六問 問2はやや計算がめんどくさいが,ビビらずにやれば問題ない。 第七問 問1は少しマニアック。 問2は硫黄反応やキサントプロテイン反応で絞って,あとは分子量で済ませてしまうのが一番早い。しかし,アセチル化がちゃんとわかっていないと詰まってしまうかも…? 第六問と第七問の選択では,六のほうがやや安全かな? というわけで,化学・追試験の解説でした。 共通テストも即日解説しますので,だれか…問題を送ってくださいね!
2021.01.16
コメント(0)
-
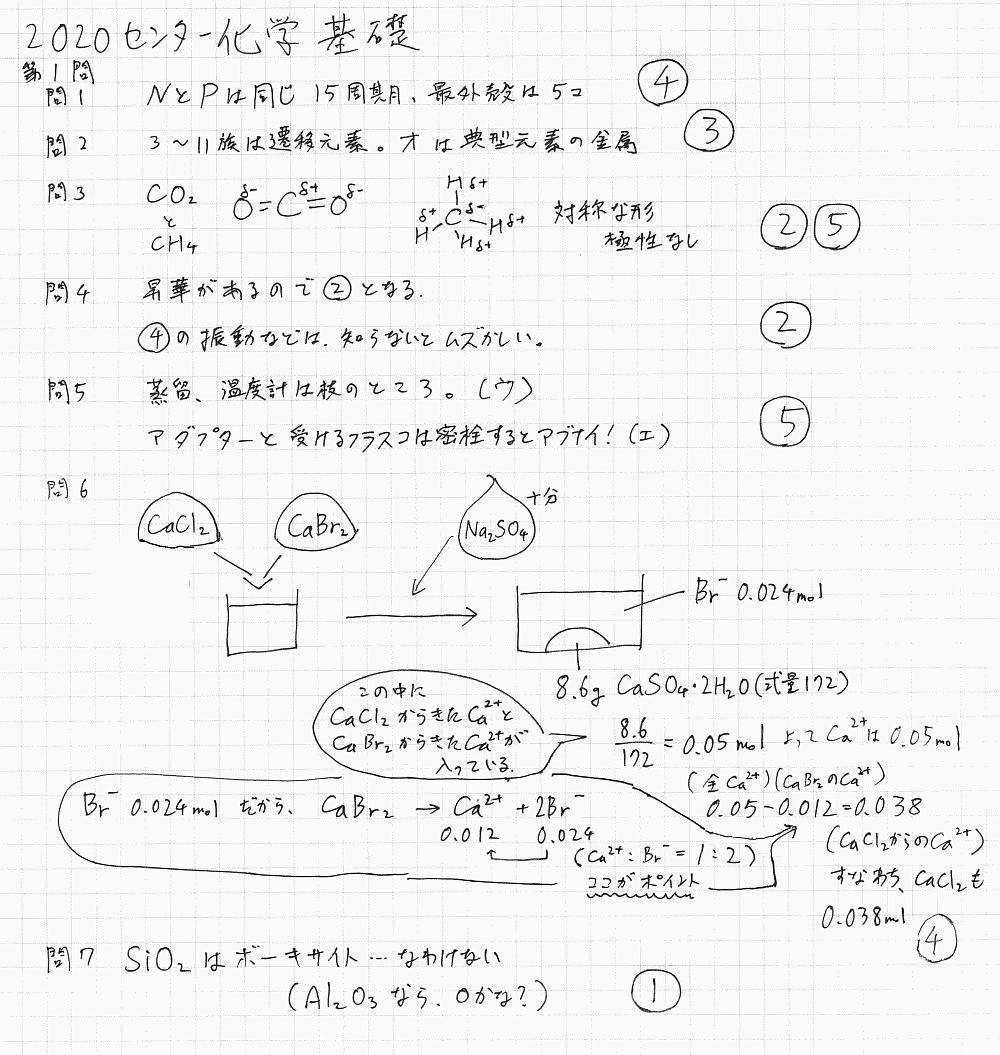
2020センター試験「化学基礎」解答解説速報
2020センター試験化学基礎の解説です問題はこちらなどを参考にしてください。【1】1~3 は基本事項4 は少し,マニアックな部分が。5 は,実験していれば大丈夫6 は,やや考えにくい。カルシウムの動きが見えているか?7 は基本的だが,考えすぎると落とし穴に落ちそう。【2】1 何を聞いているかがわかりにくい。2 これも,文章をしっかり読まないと間違えそう。3 よくあるpHジャンプだが,考える要素が意外と多くて時間がかかる。演習量で差がつくか。4 塩の性質についてはマークが薄くなりがち5 電池の酸化還元も結構盲点。確認しよう。6 イオン化傾向,さらっと通っただけだとやられそうかな…全体通して,文系選択者向けと考えるとやはりやや難化か。結構練習していないと取り組みにくいような,少し聞き方が難しい問題も増えていました。
2020.01.19
コメント(0)
-

2020センター試験「化学」(基礎じゃない方)解答解説速報
皆さんのご協力もあり,今年も某予備校よりも早く「解説」を公開できております。なにせ急ぎのもので字が乱雑だったりわかりにくい個所もあるかとは思いますが…ご意見いただければ補足訂正もしますので,よろしくお願いしますね。問題はこちらなどを参考にしてください。【1】1のハロゲン,すこし選びにくい。2の状態図は定番ではあるもののなかなかセンターでは経験不足か。3の文字式自体も定番だが,水素と窒素が同じ量,ってのをうまく処理できたかがキモ。4のトリチェリも定番だがセンターでは慌てそう。5の浸透圧も,慌てて「圧力差」を忘れてしまうとやられる。6はコロイドの知識。比較的やさしい。【2】1a 聞き方がちょっとひねっているが,中身は優しい。 bも,生成熱の定義さえ注意すれば大丈夫。2 エネルギー図でやると面倒なので,ヘスでさっと済ませたい。3 グラフが読めないときついが,読めれば即終了の問題。4 Iはルシャトリエだが,速度も考慮してグラフが読めるか。Ⅱも同様。5 聞き方が意地悪。二次の問題等で式変形などに慣れていれば早いけど…※1/26追記 Kのところを見間違えて10^-5で計算していましたが,⁻6ですね…pdfで見るとつぶれてしまって騙されていました(´;ω;`)訂正しました。【3】1 金属の性質は簡単2 酸化物の性質もそんなに難しくない。3 aは基本。bも,慌てず丁寧にやれば基本通り。4 これもカルシウムの基本事項。5 突然難しめの問題。ビビらずにファラデーに持って行けるかどうか。※2021/2/13 追記酸化物,過酸化水素の自己酸化還元でしたが,二酸化マンガンに余計な解説があったので訂正しました。ありがとうございます。【4】1 基本の選択は簡単2 ちょっとnの使い方が独特。分子量もおいてしまったほうがスムーズかと。3 芳香族の基本事項4 構造式をかいてみればよい。5 実験やったことない人が多いかも。ちゃんとイメージできているか。分液漏斗も。同位体でビックリしそうだが,聞いていることは難しくない,二次対策でそんな問題に触れていれば慌てず正解できそうだが…【5】1 合成高分子は定番,しかしゴムはマークが薄いかも…2 等電点,双性イオンなどについては押さえておきたいが,リシンの電離はちょっと難しい。【6】1 暗記というかんじ,知らないときつい。2 あわてず,3.5:1をうまく使えたか。文字を減らす流れで。【7】1 やっぱり暗記。なかなかねえ。2 あえてのマルトースでひと手間難しい。できれば【6】のほうが素早く解けたのかもしれない。というわけで,全体を通してやや難化か。計算の手間とかよりは,少し聞き方に癖がある問題が多かったようにも思うぞ。
2020.01.19
コメント(4)
-
【化学センター試験解説まとめ】2011~2019
センター試験解答へのアクセスが多いので,まとめてみました。過去問を解いて対策をする場合は,ぜひ参考にしてください。ポイントとしては,最近になるほど「テクニック」で解ける問題より二次試験的な読解や推測が必要な問題が増えているため,個人的には二次対策と並行して取り組むのがおすすめです。大学入試センターのホームページ や各予備校のホームページ,赤本などで過去問そのものは手に入れてください。2019【化学基礎】 【化学】2018 試行調査 【化学基礎】 【化学】2018【化学基礎】 【化学】2017 施行調査 【化学】2017【化学基礎】 【化学】2016【化学】2015【化学基礎】 【化学(新課程)】2014 20132012 大問1 大問2 大問3 大問32011 大問1 大問2 大問3 大問4だいたいこんな感じです。今年は最後のセンター試験、頑張りましょうね。
2019.10.09
コメント(2)
-
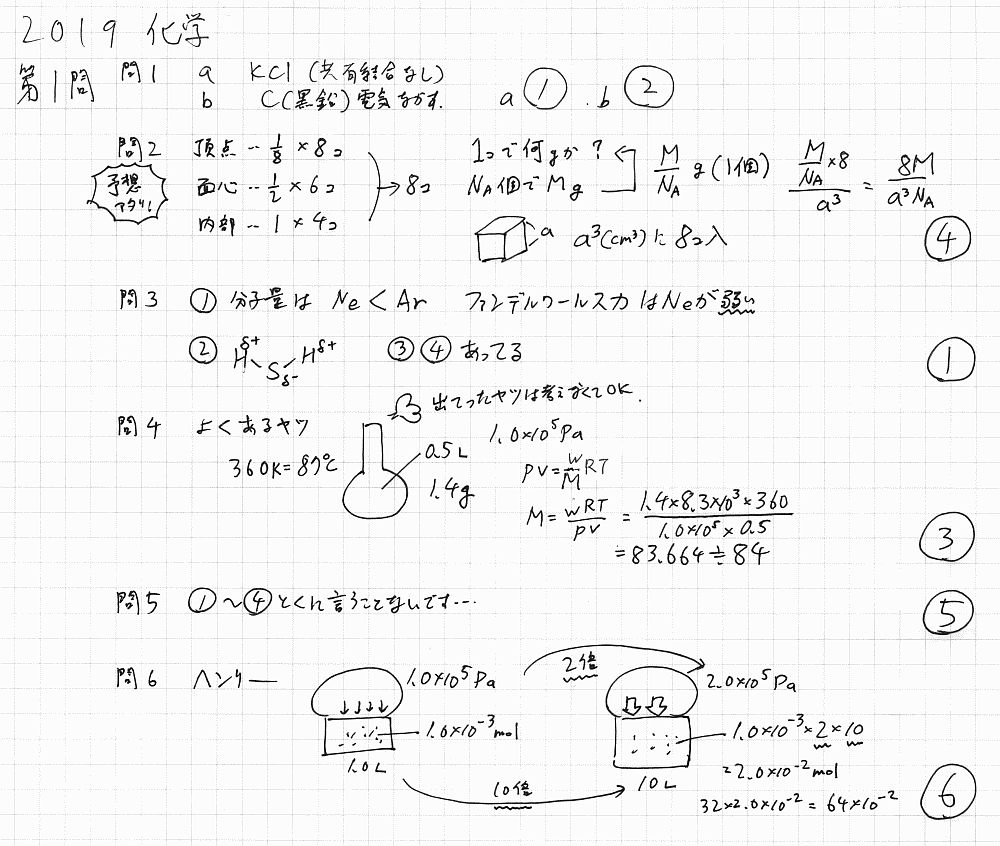
2019センター試験「化学」(基礎じゃない方)解答解説速報
遅くなりましたが、化学(基礎じゃない方)の解説です。問題は河合や東進を見て下さい。問題はここですよ!ここ!問2のダイヤモンド格子は、出るって言ってたやつです。まあやり方は普通ですが、文字式の立て方は頻出です。問4の分子量測定も定番問題。素早くやりたい。問い6のヘンリーも基本的なもの。第2問は少し時間を食いそう。問1の結合エネルギーも予想通り。中身は定番。問2の速度は、少し慣れていないと処理しにくかったかも。問3は、「同体積混合」を忘れると大変なことになりそう。慎重にやりたい。問4の電解製錬は予想通り。簡単。問5の文字の処理は面倒だから落ち着いてやろう。第3問は…妙な問題が多少。問3は、亜鉛イオンの配位の形がちゃんとわかるか、という意地悪問題。消去法でもいけるが…問5のグラフがあまり見慣れないのでやりにくい。全部求める時間はないので、幾つかに絞って計算すれば早い。第4問はだいぶイージー。しかし、問5はなかなか押さえていない人も多いかも。酢酸カルシウム…じゃない?ってことに気づけば、さすれていた人も思い出せそうだが…第5問の平均分子量は、意味が分かってれば簡単。第6問の方が、選択はしやすかったかも。ちゃんと読めば計算もそれほど難しくはない。第7問はラクトースも少し難しいし、ペプチドを元素含有量で推測、というのはなかなか難しい。というわけで、化学も、若干計算量が減ってるかな?暗記がちらほらあるが、それ故にしっかり勉強していれば解きやすく感じたかもしれない。今年は易化の傾向ではあるかもしれない。
2019.01.21
コメント(0)
-

2019センター試験「化学基礎」解答解説速報
遅くなりましたが、2019年センター試験化学基礎の解説編です。問題は河合や東進などを参考にもんだいはこちらを参照!第1問はオーソドックス。問3のニッケルは少しだけ面倒。問4の洗気びんも、実験したことがないとイメージしにくい上に文章が長め。問6の電子について、オキソニウムイオンまで押さえていたかどうかが勝負の分かれ目。問7は暗記なのでなかなか…第2問もそこまで難しくはない。問1は、特に①の意味が分からないと答えにくい。問2のグラフは一般的。問6の酸化還元は、酸化数が判断できればたいしたことない。全体的に計算量が少ないことと、選択肢が4択問題も多く、得点しやすかったと思われる。ちょっと急いで書いたから字が汚いのは勘弁ね。
2019.01.21
コメント(0)
-
2019年センター試験対策編(施行調査を基に類似傾向の問題をチェック)
2019年のセンターはどうなるんでしょうか。巷では、1 浪人して新テストへの対応ができない生徒が増えないように、易化する。 →二次試験で志望校を下げない生徒が増える。上位の競争激化、下位はチャンス。2 浪人しても問題ないよう徐々に新傾向風の問題に移行するため、実質の難化。 →二次試験で志望校が下がってくる。二次得意な生徒にはチャンス、下位層は上位が下りてくるのでピンチ。のニ説が流布しています。個人的には、センター側やそこへ加担する大学の先生方も今後の学習指導要領改訂も含めて施行調査などを進めている段階ですから、ガラッと変えるのはまだ先だとしても徐々に新傾向を導入していく方がスムーズではないかと思います。つまりは2かなーと。そういうわけで、2017、2018と実施された新テストの施行調査と類似した過去の大学入試二次問題をピックアップしました。施行調査ではそのような出題方法や題材がすでに扱われている、ということは、通常のいわゆるセンター対策も大事でしょうが、すこし違ったアプローチや題材も、仕上げにチェックしておくと良いでしょう。以降、紹介する問題は201Xに実施された○○大の問題、という形です。2015年○○大、なら、2015年に実施された2015年度入学生の選抜に使われた問題で、2016年受験用、などの問題集に掲載されています。暫定版で公開。後日、紹介できるものは予備校のリンク等を張っておきます。【化学基礎むけ】…化学基礎施行調査と似た問題・2016上智大 大問2 電気分解の液性をフェノールフタレインと組み合わせる問題・2015早大理工 大問1 ビタミンC・2016東京理大薬 大問3 ビタミンC・2014福島大 大問1 次亜塩素酸ナトリウム・2016東京医歯大 大問3 次亜塩素酸ナトリウム・2016東京理大理 大問2 中和滴定の洗浄や誤差【化学向け】…2018化学施行調査と似た問題・2017秋田大 大問2 ガスコンロ・2016中央大 大問2 ガスコンロ 会話形式・2016防衛大 大問3 アルカン1molあたりの発熱・2015学習院大 大問2 ガスタンク・2014北海道大 大問2 表とグラフで反応速度・2016北海道大 大問1 表とグラフで反応速度・2017大阪市大 大問2 表とグラフで反応速度・2015東北大 大問2 イオン半径と物性・2014立命館大 大問4 アセチレンかアセトらアルデヒド・2018同志社大 大問3 エチレンからアルデヒド 歴史・2018慶応大理工 大問3 ナフサ エチレンからアルデヒド・2014金沢大 大問4 アセトアミノフェン・2018信州大 大問3 アセトアミノフェン・2018滋賀医大 大問3 アセトアミノフェン 会話形式・2016大阪府大 大問3 有機化学実験レポート・2018和歌山県医大 大問1 炭酸の二段階電離 ヘンリーの法則・2018和歌山県医大 大問2 二酸化炭素の状態図・2017札幌医大 大問1 炭酸の二段階電離 地球環境・2018滋賀医大 大問2 炭酸の二段階電離のグラフ【余裕がある人の化学向け】…2017施行調査と似た問題・2016北海道大後期 大問2 ベンゼンとナフタレンで凝固点降下・2015東京海洋大 大問3 凝固点降下のグラフ・2015名古屋大 大問1 水酸化物の溶解度積・2016滋賀医大 大問2 溶解度とpHのグラフ・2017京都大 大問1 溶解度とpHのグラフ・2016京都大 大問3 芳香族の配向性・2016熊本大 大問3 芳香族の配向性・2015北海道大後期 大問2 COD・2015慶応大理工 大問1 COD・2014東京農工大 大問4 COD 実験手順・2017秋田大 大問3 セルロース 水素結合・2015早大理工 大問3 セルロース 水素結合
2018.12.29
コメント(0)
-

H30(2018)大学入学共通試験 試行調査(プレテスト)化学(基礎じゃない方) 解答解説
2018年11月11日に実施されたいわゆる「新テスト」の「試行調査」の解答解説です。追記2019/12/07この記事は「理科教育アドベントカレンダー」に参加させていただいております。12/25まで毎日理科関係のブログが更新されるという面白い企画です。ぜひご覧くださいね。過去記事ではありますが,高校で教科教育をするなら入試問題の研究は必須です。入試問題には「今求められている力」が隠れているからです。予備校や参考書などでも分析していることがありますが,自分でやって,授業にフィードバックしてはいかがでしょう。化学基礎の解答解説はこちら問題などはこちらから(2022・12月追記 大学入試センターのページが移動していたのでリンクを貼りなおしました。)昨年の試行調査はこちら1,2年生で今後、新テストを受験するであろう人はもちろん、3年生でもうすぐ受験の人も、同じような方針が見える可能性はあるので試行の対象校じゃなかった人も必ず解いておこう。特に3年生は「試行調査と被らない部分がセンター本番で出るかも?」という考え方も必要。おそらくほとんど同じ内容の問題、というのは直近のセンターで出ることは考えにくいからね。では見ていきましょう。第一問、ボンベはブタンだよね…というのを知らないと、ビビってしまう問題。よく表や文章を読んで対応しよう。ここで、今後のテストにあるかもしれない、まさかの「救済措置」の存在。問1を間違えたまま進んでも、計算が合っていれば得点できる、という仕組み。まさに、「思考力を見る」テストにはなっていてありがたい気もするが、自己採点の大変さが生まれそうな気もする…第一問後半、序盤の反応速度で心を折っていくスタイル、やめていただきたい。表で地道に解いていく練習できていないとつらい。問3は、グラフを書いてしまおう。問4こそ、グラフ書かなくてもわかりそうだが、念のため書くようにすれば、「比例の傾き」の凡ミスは防げるかな…分かっている人は時間かけたくない場所。さらにボリューミーな第一問は、問題稼ぎの問5同位体(謎問題)と、イオン化エネルギーの問6(定番問題)は瞬殺。問7も時間をかけたくない。「両極が銅なので、陽極は溶けるはず」というのが頭にあれば、即決できる問題ではある。そういう点では、あまり良い問題ではないかも…第二問は比較的オーソドックス。しかし、反応自体はあまり見ないものなので、慣れない人は苦戦する。弱酸の遊離と、気体発生の関係、亜硫酸と二酸化硫黄あたりをちゃんと関連付けて理解しておく必要があるか。問2の捕集装置も、ちゃんと見る訓練をしておこう。問3は、秒殺できるように、酸化還元かどうかはすぐわかってほしい。後半でまた読ませて殺すスタイルだが、負けちゃならん。というか、まともに読んでたら時間が足りない。少なくとも問4,5は流し読みで解ける。あとは、文と表をある程度理解しないと問6は解けないわけだが、下線部(c)をしっかり読んで、前後の文脈との矛盾を選べばよい…って、現代文か???第三問も題材はオーソドックス、だが、生成物じゃなく反応物を聞くあたりがクセ強め。大問としては簡単なとこなのでさっと解いてしまいたい。とはいえ、式(3)(4)あたりはあまり見ないので、周囲の文章のヒントをつかむ必要もある。第三問後半も読ませてくる。ちょっとひどいつくりじゃないですかね…アセトアミノフェン絡みなんてほとんど知らないと思うので、フェノールとアニリンあたりの知識で何とかするしかない。問4は、実験生徒の気持ちになってシミュレーションすればよい。問5の「収量」も、定番ではあるが経験がないとイメージしにくい。高校時代から、ある程度課題研究的な実験の経験があれば、ここは早いかも。座学ばっかりだと厳しい。第四問前半、よく2次試験であるようなグラフで憤死しそうになるががんばろう。ビビらずに進めば、グラフはほとんど使わない。問1のヘンリーは基本。練習しておこう。問2aの電離定数は簡単だが、bの処理は似たような問題の経験がないとつらい。グラフから、「ヒントになりそうなのはpHしかない」、という事に気づければ、右辺の邪魔な項を消すという考えに至るが…ハードルは高め?第四問後半、対数の扱いになれないと、とっつきにくい。対数表なんて、使ったことない人も多いんじゃ…?シンプルに、解答例のようにできればいいが、たとえば別解のようにやっていくこともできるけど、時間がかかる。サッと解けるようになるには、数学で対数になれておくべき。それを科学の試験でも要求するとはね…問4も対数軸なんて使って、対数押し半端ないが、問題自体は簡単。状態図の問題で慣れていればスムーズ。やっときた第五問、多分、全国の多くの皆さんが残り時間との勝負になっている。そんな時にアルギン酸がくるわけだから、いくら何でも…(人工いくらにもアルギン酸は使われます)焦らず読んで、コロイド分離にたどり着けば問1はクリア、問2は分子模型でグルコースなど作って訓練していれば早い。そうでないと間違いそう。問3はすぐできる。問4も、アミノ酸の問題を十分にやっていればすぐできるんだが…曖昧で適当に選ぶとやられてしまいそう。と、いうわけで、化学の試行調査でした。どう考えても、実際のテストがここまでの地獄のようなテストにはならないはずです。平均点が大変なことになります。何といっても読ませすぎです。おそらく実際は、もう少し読ませる部分を減らして、比較的単純な選択問題も入れるでしょう。正解が複数ある選択問題、というパターンも出てきそうです。(そうしないと、ただ問題を減らすと1問の配点がでかくなるので)また、計算も増えそうです。第一問のような、数学の問題のように四角に数字を入れるタイプになっていくかもしれません。(正確性が問われる)とりあえず、今後やっておきたい対策としては、「現代文」「対数・指数」→他教科もちゃんと頑張ろう「課題研究的実験」→授業内外で、計画→予想→実験→考察というような流れをやっておこうこのあたりがキーになりそうです。サー大変だ…
2018.11.14
コメント(0)
-

H30(2018)大学入学共通試験 試行調査(プレテスト)化学基礎 解答解説
2018年11月11日に実施されたいわゆる「新テスト」の「試行調査」の解答解説です。まずは化学基礎。「化学(基礎じゃない方)」も近日中に更新します。問題等は、こちらから閲覧できます。(2022・12月追記 大学入試センターがページを移動させていたのでリンクを貼りなおしました)1,2年生で今後、新テストを受験するであろう人はもちろん、3年生でもうすぐ受験の人も、同じような方針が見える可能性はあるので試行の対象校じゃなかった人も必ず解いておこう。特に3年生は「試行調査と被らない部分がセンター本番で出るかも?」という考え方も必要。おそらくほとんど同じ内容の問題、というのは直近のセンターで出ることは考えにくいからね。では見ていきましょう。第1問から読ませてくる問題でビビるが、あせらずやろう。中身はたいしたことなし。問3の成分表示もビビるが、日ごろからこういうものに目を光らせるのもいいかも。第2問の極性と酸化数については、授業でしっかりやってない人でも、読めばわかるようにはなっている。けど、苦手意識がある人はあきらめムードが出そう。グラフは、慌てず電子と物質量比。ビタミンC,なんてのにも惑わされずに。第3問も、いかにも新テスト感がある。一回くらい実験やってないとイメージがわきにくく、きつそう。序盤の、「おおよそどれくらいか」なんてのもイメージできないととっつきにくい。「何倍薄める」も、慣れないと処理できないかも。中和滴定そのものの計算がないのも意地悪。今後のテストでは、大幅な誤差が出たデータの処理や、実験失敗に関わる改善方法など、出題されていくのかもね。以上、難易度自体は高くないものの、文章をちゃんと読んで処理できるか、イメージできるか、というのが問われる。授業である程度「予想→実験→考察」という流れをやっていないとキツイ。また、理論の分野も、丸覚えでなく考えて理解する訓練を日ごろからしておこう。もちろん、日常の化学的事象も常に気を付けて置く癖が必要。とはいえ、実際の化学基礎新テストは、もう少し読む量を減らさないときついかな…という印象。
2018.11.12
コメント(0)
-

H29(2017)大学入試センター試験試行調査(プレテスト)化学 解答解説
忘れていてすいません。H29センター試験試行調査(いわゆるプレテスト)の解説です。問題などはここからpdfで見ることができます(2022・12月追記 大学入試センターがページを移動していたのでリンクを貼りなおしました)今後入試がある人は必ず解いておいた方がいいと思います。今からのセンターや大学が求めるような問題が盛り込まれていると思われます。全体的に、時間がかかりそうで少し難易度は高めのようです。熱化学はよくある問題ですが、ヘスもともかく、エネルギー図の考え方は押さえるようにする必要がありそう。グラフ問題のような、データ処理が必要な問題も要注意、経験がないと難しいが、教科書などのデータで練習しておくといい。凝固点降下も、水以外が溶媒、というのはちゃんと考えを理解していないときついので、しっかり理解しておこう。(正答率が低く、実際の試験では桁数の処理などがもう少しイージーになるかな?)溶解度積については、グラフがあまり見慣れないので難しい。沈殿滴定のようなケースは、二次の問題で多いから、そういうレベルまでセンター時点で仕上げるのはなかなか厳しいが…金属の分析は比較的普通のものだが、完全解答は難しい感じもある。元素分析は普通に行けそうだが、その後のステップがたどり着けなかったかも。本試験に採用するなら、元素分析、構造決定、という別得点になるかも。ビニルアルコールの不安定、は、よくあることなので外したくない。ベンゼンからの誘導は、推理力も必要で難度が高い。しかし、こういった推測からの分子合成が今後問われる可能性は高い。CODはよくあるものなので、皆訓練はある程度しているみたい。スピードよく解きたいところ。5のような有機はまだ模索感があるので、どういうものになるのかはわからない。ただ、糖類はまんべんなくいろんな問題にあたっておきたいし、繊維も、それぞれの繊維の特性を丸覚えでなく押さえておく必要はありそう。というわけで、センター試行調査です。今後のセンターの流れを決めるものですが、大学入試センターなどが求めている力が問われているとみていいと思います。これから入試がある人は一度通っておいた方がいいと思います。(来年以降入試がある人ももちろんです。)来年の試行調査も解説予定です。
2018.01.31
コメント(1)
-
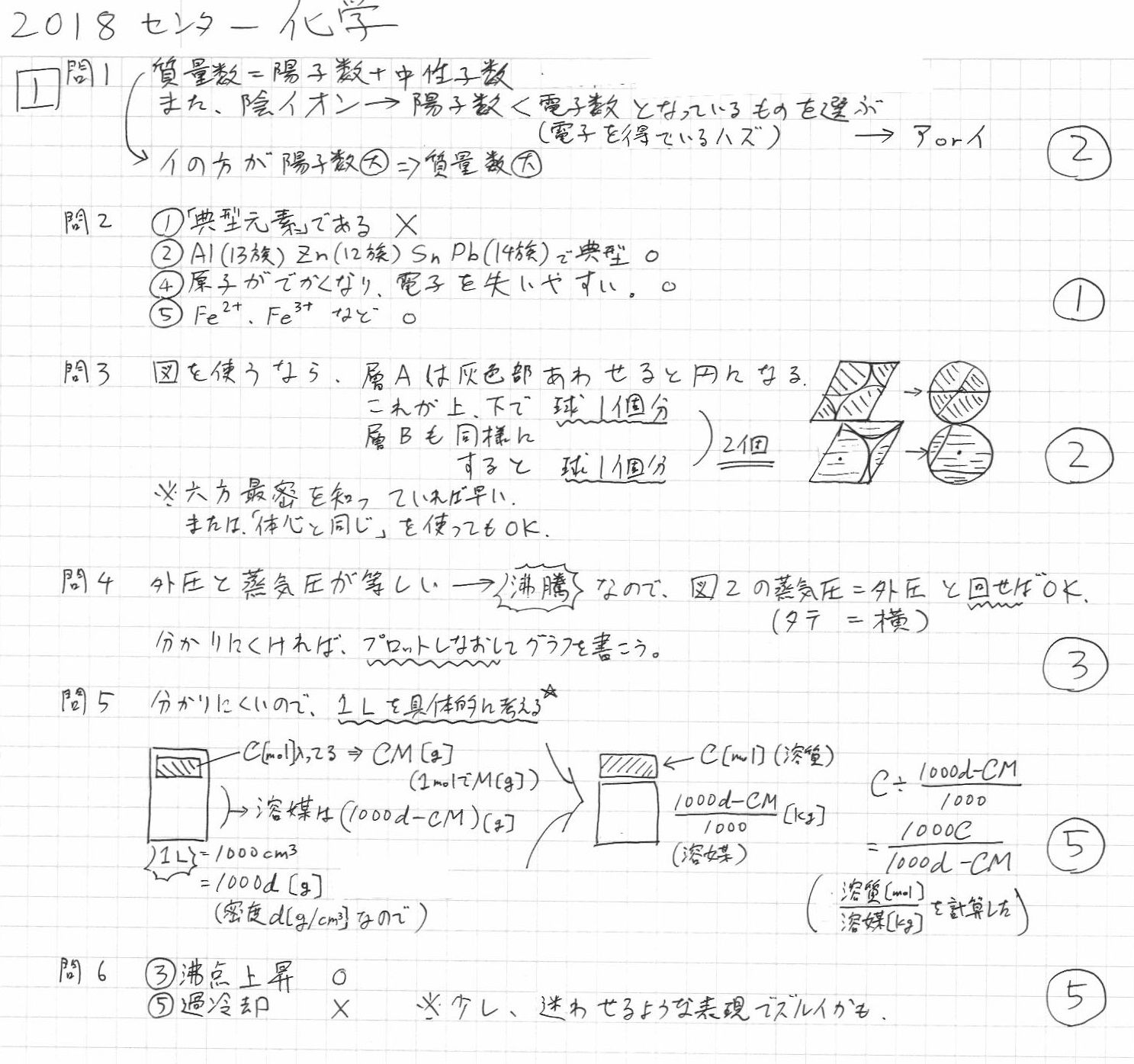
2018センター試験「化学」(基礎じゃない方)解答解説速報
2018センター化学の解答・解説速報です。それほど難易はアップしていないような。でも、時間配分に気を付けないと危険かも。選択は、7の方が早いとは思う。さあ、次は二次だ。頑張ろう。二次の解説が必要な人はリクエスト受けますよ。
2018.01.15
コメント(0)
-

2018センター試験「化学基礎」解答解説速報
2018センター試験化学基礎の解答・解説速報です。急いで書いたので微妙なところはあるかもしれませんが…少し、演習が足りないとやりにくい、クセ強めの問題もありましたが、皆が確実に撮っているような問題を落とさなければそれほど差は出ないでしょう。
2018.01.15
コメント(1)
-

2017センター試験「化学」(基礎じゃない方)解答解説速報
さー、2017基礎じゃないほう、いってみましょう。問2の結晶格子は予想どおり、というか定番。覚えていた人もいたのでは?問3の速度は、油断していなければ大丈夫。問4の状態変化は、日常の二酸化炭素をいかにイメージしてグラフに落とせたか、というところ。問5は、問題文をよく読む。全圧であることに注意。3~5は二次試験に出てもおかしくない問題だが、この辺は素早く済ませたい。問6は、凝固点降下の問題としては標準的だが、密度が苦手な人はやられたかも。第2問の問1は、よく読まないとN-H3本分というのを勘違いしそう。問2の平衡は標準的だが、問題文がわざと読みにくくなってる。問3は、グラフが二つもあり、読み取りに注意が必要。bの反応速度については練習不足だときつい。平衡定数の出題はなくて、ラッキー、かな?問3は二次試験でも頻出と思っておこう。問4は緩衝液をちゃんと理解していれば瞬殺。わかっていないと、文字式等で検討する羽目に。二次試験対策は、一歩先のpH計算までやっておこう。問5も、定番の陽イオン交換膜法とわかれば早い。問6は、桁がやや小さいから注意。第3問は基本的に無機だが、覚えこみでなく、ほかの分野の理解が必要になっている。問3の気体発生は予想通りだが、聞き方が少しだけ珍しい。実験がイメージできたか。問6は、見た目のインパクトもでかい。が、あまり気にする必要はない。黒だの白だのもあまり気にしなくていい?とにかく、電子の移動を理解できれば問題ない。焦った人はダメージを受けたか?第4問、この辺に来ると息切れしそう。しかし内容は易しい。問3は予想通りだが、ナトリウムフェノキシドあたりはよく把握していないとフェノールと間違えそう。問4の塩素置換は少し戸惑いそうだが、冷静に立式すれば問題ない。「わからなければ、置けばいいじゃない」問5も予想通りだが、喜んで「けん化!」とかいって飛びつくと罠である。第5問以降は、例年通りの問題少なさ。この辺は、いかに残された時間と余力で勝負できるかにかかっている。第5問は、思考停止していなければ余裕。第6問と第7問の選択は、自信をもって解けそうなのは6かなと。ただし、ゴムについて学習が不十分だと絞り切れないか?ポリ乳酸は、よくあるので訓練していたかもしれない。第7問のアミノ酸は、二次対策で準備していれば定番問題。それがないと、厳しい。解説例のように、丁寧にやる時間はないはず。と、いうわけで基礎じゃない方。内容的にはやや易しくなったような気もするが、現役生は二次対策を並行してやっていた人に有利な問題も多いように感じる。今後受験する人は、戦略を考えよう。二次試験も化学を使う人は、今回のセンターも比較的良問で押さえどころがいいので、ちゃんと訂正したうえで二次対策を進めよう。
2017.01.16
コメント(0)
-

2017センター試験「化学基礎」解答解説速報
今年もお疲れさまでした。センター試験の解答解説速報です。化学基礎は、例年並みという感じですが、多少見た目でびっくりする問題もありましたね。第1問は特に問題ないかと思います。スピーディーにいきたいところ。第2問の問2の単分子膜は、ちゃんとやっていないと厳しいかもしれない。飛ばす勇気も必要。問5の中和は、滴定曲線がちゃんと訓練できているかどうか問われる。問6は、比較的珍しい反応だが、酸化還元反応の式の作り方をちゃんとやっていれば大丈夫。ラストは定番の問題。ここで時間を食ってはいけない。おおよそ得点差はつかないと思いますが、やはり化学基礎は単純な練習量とスピードで差が付きそうです。
2017.01.16
コメント(0)
-

2016センター試験【化学】の解答解説速報
まず全体として難易はちょい高くなったような気もするが、傾向の変化についていけていれば実際は大して変化なさそう。ビビらずに落ち着いて解けたかどうかというところ。大問7構成で、6,7の選択も、昨年と異なり慌てたかも?それでは見てみよう。動画の予想通りの問題は☆、大体予想とに準じた問題は★優しい問題はeasy、難しめの問題はhardで示しています。格子は予想通りだが、面心というeasyなもの。蒸気圧は言及したものの、分圧・水上置換との組み合わせは少し取り組みにくそう。冷却曲線・浸透圧はなかなか手が回らなかったかもしれないが問題としては簡単。熱・ヘスは予想通りだが、「燃焼熱」なので多少扱いづらい。活性化エネルギーは基本的なもの。電離平衡も予想通りだが、慣れていないと塩酸に惑わされて憤死しそう。苦手な人は後回しにする勇気があったか?あまり見慣れない雰囲気の化学平衡のグラフだが、ちゃんと読めれば平易。酸化還元も平易な化学基礎の延長。電池・電気分解は計算など大きな出題はなかった。無機は、定番の両性元素や酸化物関係がキーになるものが多いのは確か予想通り。アンモニアソーダ法は久しぶりだが計算は定番。この辺で時間稼ぎができたかな?予想通りの分離だが、手順をほぼ完全に把握しないと厳しい。Baがせめてもの良心である。ヘキサシアニド~と、硫化物の沈殿に関しても、正確な知識が求められた。足止めを食う問題。ミョウバンは、ビビらなければたいしたことない問題。有機の出だしは基本的な問題。フェノールは予想通りだが、聞き方が珍しい。けどふつう。油脂も予想通り。ちゃんと対策さえできていれば定番の問題。異性体も予想通りだが、分子模型でイメージしていないと考えにくい。実験・気体捕集という点では予想通りのアセチレンの問題だが、臭素との量的関係まで頭が回るか、後半疲れてきていると危ない。なぜか2問だけの大問5。受験生の困惑を招く。イオン交換樹脂やゴムは多少言及したものの、ほんとに出るとは…という感じ。高吸水性樹脂は難しいので、他で答えを確定できないと苦しい。糖類は予想通りで、簡単。6,7の選択は、度胸があれば7が簡単だったか?合成ゴムも言及したが、あまり見ない出題でやりにくい。単量体を知らないと答えられない問題も、あまり勝負しにくい。メタクリル酸をあてずっぽうになった受験生も多いのでは。トリペプチドは二次対策でもよく出てくるので、まんべんなくやっていれば楽勝。DNA塩基は生物選択者でも苦しそうだが、「水素結合」というフレーズで勝負すれば答えられるスッキリ問題である。というわけで、2016化学。数年後のセンター終了→次の形式の試験という動きの準備と思われる、出題傾向もぐんぐん変化している問題でした。基礎的な知識の丸覚えではなかなか対応しにくく、「考える力」が必要という点では、やや浪人生がリードを広げたかもしれません。今後も、実験系、解答方法や手順を考える必要のある問題が出題され、新形式の試験に移行していくと考えられます。2017受験する羽目になる人たちは、そこも踏まえてちゃんと体系的に学習していこう。
2016.01.18
コメント(3)
-

2015 センター化学基礎 解答例
化学基礎の解説です。当初は基本事項、モル関係、酸塩基、酸化還元とバリエーションも多く、計算量の多さのわりに30分という時間制限、なおかつ主に文系の生徒が受験している(と思う)ので、学校での授業単位数も少な目であれば、相対的に難易度高いのではと危惧しましたが、蓋を開けてみたらびっくりです。計算量もおさえて、応用的な問題はほぼないという、非常に良心的な問題でした。【全体概況】予想通り大問は2つ。マーク数も14で、1問2分という時間配分も予想通り。正直言って難易度は低い。第一問基本事項~モル計算あたりまでを範囲とするかと思いきや、ほぼ基本事項。昨年までの化学の「第一問」の小問集合に近い。来年以降化学基礎を受験する生徒は、2014以前の大問1を練習しておこう。計算はなく、原子の構造や電子などは標準的。ただし、新分野としての極性や配位結合、状態変化などが出題。とはいえ教科書レベルでも対応できる。日常の化学も、教科書をしっかり見ておけば対応できる。第二問多少計算問題があり、モル計算から酸塩基、酸化還元まで出題。とはいえすべて標準的。今年は中和滴定がらみは出ていないが、来年以降は警戒しておくことには変わりない。以降解説プリント。
2015.01.21
コメント(0)
-
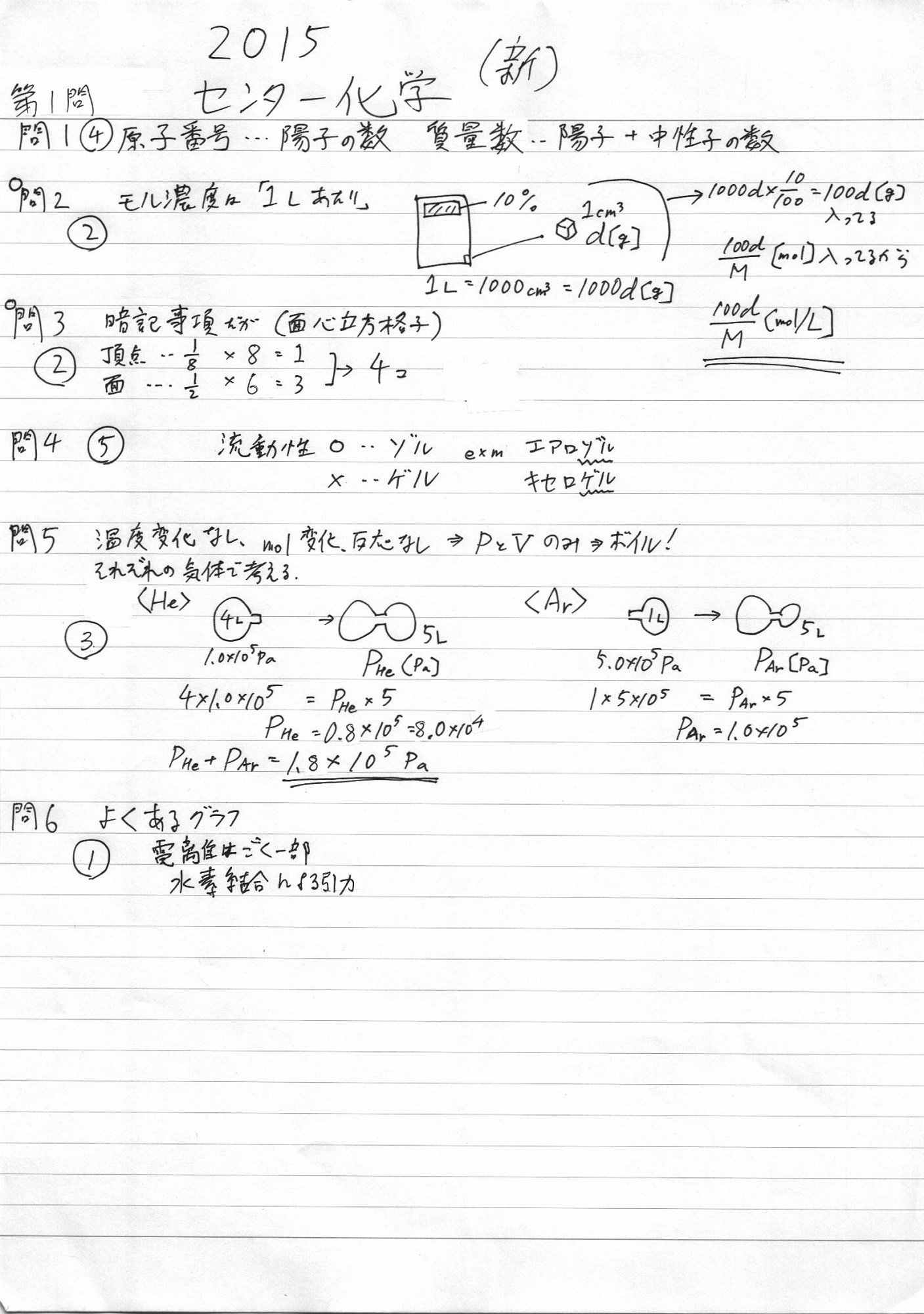
2015 センター化学(新課程) 解答例
【全体概況】懸念したほどの難化はなく、一安心。大問数が増えているので、ペース配分がちゃんとできたかが勝敗を分けたかも。選択の5,6がきて多くの受験生(や、学校)は助かったと思う。生物選択者なら迷わず6だが、ビニロンの計算はやや厄介なので、第5問を選択してしまった人は苦戦したカモ。予想通り「化学基礎で出た問題は出ない」ということで、問題のかぶりはない。(例えば電子配置や状態変化、結合の種類など)ということは、基礎科目が終わった時点で「出ていない部分を集中的に復讐する」ことで得点のブーストを図るという戦略はあながち間違いではなさそう。来年度以降の受験生は覚えておこう。【各問題】第一問オーソドックスな問題。問4が、選びにくそう。問5は、教科書レベルだし、昔のセンター試験や基礎的二次問題の過去問で対策できていれば問題なし。第二問問1は予想通りの結合エネルギー。エネルギー図のほうがはるかに早く正確に解きやすい。問2も予想通り。定番。問3の溶解度積は想定外、かつ非常に意地悪。体積変化で濃度変化を見落とすとドツボにはまる。後回しにした人が正解。問4はオーソドックスな電気分解。問5も定番。平衡定数に関する出題がないように見えるが、問3は実質的に平衡定数の問題なので来年以降は電離定数などの問題も確実に出題されそう。速度に関しては、出題されず。酸・塩基、中和に関しても、(化学基礎の履修が前提であったとしても)完全に化学基礎と棲み分けしているようだし、来年以降も化学での出題はあまりなさそう.第三問予想通り超例年通りの超得点源。ここで落としたら厳しい。とはいえ問5は少し手間がかかる。慣れてないと手こずったかも。問6は「局部電池」の問題で、知識はもちろん考える力が必要。迷ったら先に進んだほうがいい、ってくらいの問題ではあるけど、ちゃんとイオン化傾向など理解できていればできたはず。第四問第五、六問が選択になったことで、こっちは結果的にオーソドックスな形になった。問5が特殊な出題と一部ではいわれているが、化学の問題で「失敗するドジ実験者」はよく出てくる。なんのことはない、通常通り解けばいい問題。問6も、まともに計算せずに、解答例みたいに途中から適当にやろう。第五問高分子が得意な人はよかったかも。アセタール化の計算は難しい。第六問生物選択者なら有利。問1が選びにくい。問3は難しそうに見えるが、ビビらなければ楽勝。以下解答例
2015.01.20
コメント(0)
-

2015センター化学(基礎じゃない方)予想と対策
センター化学2015の概要予想と対策です。って言っても、ガラッと変わるので、要注意ポイントをあげましたという感じ。ギリギリですが、動画でも解説予定です。大雑把に、黒文字がおおよそ出そうなもので、黄色マークは要注意、青は、変化球あり?という感じ。☆は頻出、○は確実に。△は後回しでよさそう。全体的に、【1】【2】に計算が集中しそうなので、時間配分に注意。計算は後回しでいくのが吉かも。さらに、【1】【2】の化学基礎と被る部分(酸塩基、酸化還元)は、ずらしてくると考えられる(同じような問題の使いまわしはない)ので、化学基礎の試験が終了した時点で、「出なかった」部分を教科書などで直前補充しておくといいのではないかと。もしかしたら、選択問題があるかもしれないが、期待はできない。日常の化学はどの大問で出てもおかしくないので、教科書のコラムや写真を一通り見ておこう。【1】結晶・気体・溶液「基礎問はわずか!計算速度と正確さが必要!」 結晶は面心、体心の簡単な計算や密度付近まで。六方は名前くらい?充填率も、最密を覚えればOK念のため、半径の計算方法と「球の体積の公式」は確認。イオンの格子はないと思うけど… 気体は、ボイルシャルルや状態方程式はもちろん。グラフと出そう。水銀柱や蒸気圧、オーソドックスな混合気体もあり。この辺は10年以上前のセンターの問題で仕上げておくとよさそう。 溶液については、溶解度がらみの問題とは思うが、水和物が苦手な人はなんとかしておこう。ここも、グラフもあり。コロイド、浸透圧などは、もしかしたら【3】【4】あたりに流れ弾がいくかも。【2】熱・電気・速度・平衡「化学基礎との兼ね合いに注意!計算とグラフ処理!」 熱は、オーソドックスなヘスはあると思うが、結合エネルギーや活性化エネルギーがらみの可能性も。後者なら教科書の演習問題レベル以上はない。ヘスなら、問題は出尽くしてるのでやや難問カモ。 電気は普通の電気分解(グラフ・計算)はあると思うが、要注意は燃料電池。ここで酸塩基や熱(エネルギー)と複合させる工夫した問題にも対応できるように。電気がたくさんあれば酸化還元は【3】に流れるかも。こちらも滴定は注意。化学基礎との兼ね合いで。 速度は基本的な問題以上はなさそう。ただし、条件を左右するもの(触媒とか)は聞かれる。 平衡は、平衡移動についての正誤が妥当にありそう。あとは、酸塩基からKaとか、pHあたりか。酸塩基の出方は化学基礎との兼ね合いもあるが、二段階滴定や逆滴定も確認。 場合によっては圧平衡定数が【1】で出たり、ハーバーボッシュ法の平衡あたりが【3】で出たりと、他の大問に流れ弾がいくかも(流れた場合は難問にはならないだろうが)。平衡定数の単位のつけ方も念のため確認しよう。溶解度積はさすがに勘弁してほしいが、こちらも【3】に流れる危険もある。余裕があれば。【3】無機「数少ない例年に近い形。ここで得点できないと厳しい。」基本的には「例年通り」にアルカリ・アルカリ土類・ハロゲンを重点。製錬方法やイオン化傾向~分離、両性元素や鉄・銅などのイオンの色や沈殿あたり。錯イオンは要チェック。あとは、アンモニアソーダ法、接触法はもちろん、ハーバーボッシュからのオストワルトも定番。【2】からの流れ弾の平衡や酸化還元が来た場合は、得意に応じて後回しにしていいだろう。【4】有機「高分子関係の知識問題で失点を防げるかがカギ。例年通りの問題は落とせない」全体として、「異性体」「エステル」に関する問題は頻出。これは例年通りで対策しておく。前半は鎖式。からの高分子や熱の計算という展開もありそう。複雑そうな問題が来たら、時間に応じて逃げよう。後半は芳香族。定番のフェノール~サリチル酸がらみは確実に。分離やPETも頻出。計算はあまりないかも。ここに、油脂~セッケンがねじこまれそう。けん化価・ヨウ素価の計算も確認(でも、ここで計算が増えるとたぶん多くの受験生が倒れていくだろう…)。さらに、高分子の分子量計算や重合度計算もこの辺で来そうで怖い。浸透圧や、蒸気圧降下(沸点上昇・凝固点降下)などもぶっこまれる危険性もあるが、慌てず計算できるかどうかだろう。糖・たんぱく(アミノ酸)はちょびっと。イオン交換樹脂とかも、知識を余裕があれば確認。
2015.01.05
コメント(0)
-
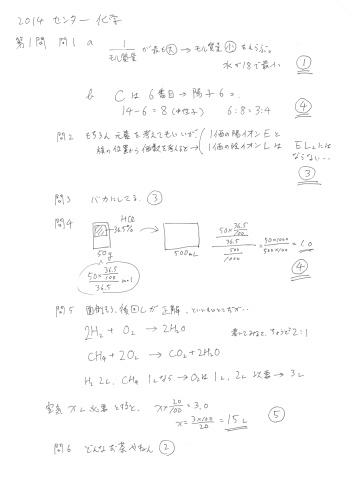
2014年センター化学 解答解説速報
2014センター化学の解答例です。難易度は低いと思っていいでしょう。二次試験も頑張りましょう。
2014.01.19
コメント(0)
-

2013センター化学解答例
2013年のセンター解答例です。キーポイントも述べていますので、見てみてくださいね。
2014.01.18
コメント(0)
-
2013 化学センター解答速報
644313231313424535212122545213533たぶんこう。詳細は後ほど!
2013.01.20
コメント(0)
-
とある化学教師のセンター解説2012 大問4
さぁオーラス行くよー,飯食ってたら遅くなった有機はイージー1 鎖式飽和→アルカンと思っていい (1)CnH2n+2だね。 × (2)極性小さいからね ○ (3)分子量大→分子間力大→沸点高い ○ (4)炭素3以下はない,と読み替えればいいね。 ○ (5)7と6でつくってみればいい。○ ということで(1)2(1)~(3) (4)不斉が無いから× (5)不斉ありのヒドロキシ酸 ○ つーことで(4)3 文より,アセチル基か,CH3CH(OH)-の構造あり→ヨードホルム陽性 あと,不飽和結合あり→臭素脱色 みたすのは(3)だけ4 付加とは,多重結合が壊裂して別な原子や原子団が付け加えられる反応。 (1)ニトロ化 置換で,ニトロベンゼン (2)付加 1,2,3,4,5,6-ヘキサクロロシクロヘキサン (3)スルホン化 置換でベンゼンスルホン酸 (4)臭素置換で2,4,6-トリブロモフェノール。ヒドロキシ基はパラ,オルト配向性 (5)無水酢酸でアセチル化。エステル結合とアセチル基ができる。 アセトフェノンとか,酢酸フェニルとか言う名前に。 つうことで(2)5 操作1でアニリンだけを水槽に出すためには,アニリンを塩にすればいい。 つまり,アニリンを中和するのは酸なのでAは塩酸しかない。この時点で (1)か(2)しかなくなる。 もしBが炭酸水素ナトリウムなら,操作2でCが水酸化ナトリウムだから 全部中和して水槽にサリチル酸もフェノールもどちらも移動してしまう。 そうなったら操作3で残ってるエーテル層にはなにもないはず。 というわけで(2)6 【ちょびっと難】 エチレンとアセチレンがあいまいになっている人は引っかかったかも。 上のラインはエチレン+水付加で,普通にエタノール。 (逆のエタノール分子内脱水を想像してもいい) 下のラインはややマニアックだがアセトアルデヒドの工業的製法。 しかし,良く分かって無くても上のラインが分かっていれば,A酸化Bですぐ出る。 寄って答えは(6)7 【計算が面倒?】 しかし,実験装置も絵だけという全く不甲斐ない。 A84mg 二酸化炭素176mg 水36mg 比だから,全部gで計算してもいい。 A84g 二酸化炭素176g 水36g それぞれmolになおして, 二酸化炭素4mol 水2mol→その中のCとHは C4mol H4mol よってC:Hは1:1 さらに,質量はC48g H4gあわせて52g よって,A中の酸素はのこり。84-52=32g よって,酸素は2mol。C:H:O=2:2:1 Oが4ってのは問題文でわかってるので, 8:8:2だから,(5)以上~。しっかり訂正して二次も使う人は頑張ろう。センターまでの人は,お疲れ様!質問があったら書いてください。
2012.01.15
コメント(2)
-
とある化学教師のセンター解説2012 大問3
では、大問3いってみるよ。1 (1)ヘキサフルオロケイ酸 になるからね ○ (2)解説するまでもなく ○ (3)エタノール→油 ってイメージもあるのかな? しかし、ヒドロキシ基があるからね。普通にナトリウムエトキシドになるから× (4)(5)も解説の必要なし ○2 【やや難】これが、5年以上超久しぶりの酸化物問題。 (1)Al単体はNaOH過剰でとける。少量ではAl(OH)3が生じて溶けにくい。 しかし、今の話は「酸化アルミニウム」。 これは、(わざわざ過剰と書いていなくても)NaOHにとける。 (既にイオン的状態になっている効果…かな?理屈は調べてませんが) 多分、両性元素付近で教科書にもにも載っていると思います。 ○ ※ ちなみに、高純度の結晶やアルミナの状態では、とけませんが、 記述がない以上こちらは例外という考えが普通でしょう。 (2)塩基性酸化物、ナトリウム自体の反応性も相まって。○ (3)酸性酸化物。「加熱すると」というのは大事だけど、まぁ、あってるからいよね。○ (4)塩基性酸化物なので、酸と中和反応に準じた反応をして塩を生じます。○ (5)これが一番厄介か。(1)~(4)がほぼ○なので これを×という方針でいいと思う。 酸化鉛(II)は両性酸化物で硫酸とも反応するが、この問題の酸化鉛(IV)は硫酸とは 反応しにくいようです。自身が酸化剤であるため、硫酸鉛(II)になるためには 何かを酸化しなければいけないわけで、じゃぁ硫酸を酸化?なんになる?と考えると 反応しにくいかなぁ~って気がします。 鉛蓄電池の正極でもありますが、負極側から電子が運ばれてくるからこそ硫酸鉛(II) になれるわけで、簡単には変わらないのでは?とかね。しかし、この選択肢単体を 推測するのはなかなか困難かも。 × っというわけで(5)です。3 結局昨年消えた窒素が復活です、 (1)解説の必要なし ○ (2)NOは酸性酸化物ではありません、COもね。 × (3)そのまま○ (4)式を立てればいいわけだけど、 選択肢が「○」と仮定して係数を入れれば確認しやすい。 (5)オストワルト法勉強していれば ○ というわけで(2)4 過酸化水素から酸素の式が 2H2O2→O2+2H2O なので過酸化水素のmolを求めに行こう。 10g×(3.4÷100)が質量。これを34で割る(分子量)。で、0.01mol 過酸化水素:酸素=2:1なので、酸素は0.005mol よって、22.4かけて (2)5 反応後を考えよう (1)酸化銀 褐色 (2)沈殿なし 青色水溶液 (3)血赤色溶液 (4)塩化鉛(II) 白 (5)硫化亜鉛 白 (塩基性or中性) で、(1) 6 アルカリ金属とマグネシウムの違い (1)(2)マグネシウムの方が水とは反応しにくい (3)硫酸塩の沈殿はアルカリ土類か鉛。マグネシウムはとける。 (4)炭酸塩はほとんど沈殿 (5)その通り。詳しいことは物理分野w というわけで(3)7 アンモニアっソーダ法もちょっと久しぶり。 (1)Aはアンモニア (2)Bは二酸化炭素 (3)塩化アンモニウムと炭酸水素ナトリウムでは、後者の方が溶解度が小さい。 (4)式立てて考えればいい。Nは1:1になってるはず。 (5)これも式立てて。炭酸カルシウムと塩化ナトリウムは2:1 よって(5)無機は標準的。かな。多少選びにくいものもあるが…
2012.01.15
コメント(2)
-
とある化学教師のセンター解説2012 大問2
ざくざくいこう。質問も指摘も受けます。大問2 グラフ問題が1個だけというふがいなさ。1 表よみきたね。しかしひねりもない。 表は「生成熱」だから、そ、アレが使える。 反応熱=生成物の生成熱‐反応物の生成熱にもっていきたい。 生成物は右辺、単体の生成熱は0だから、3CO2だけを考えて、3×394 反応物は左辺、Fe2O3と3COあわせて、824+3×111 よって反応熱=3×394-(824+3×111)=25 (4)2 キーボードで打ちたくない問題w まずは、面倒だからメタン=x〔mol〕 エチレン=y〔mol〕とおこう。 問題文より x+y=1.00 また、熱化学方程式を考えると メタンが CH4+2O2= 省略 +891kJ エチレンが C2H4+3O2= 省略 +1411kJ となる(問題解くときは右辺も考えないと解けない。ただ打つのが面倒なので省略) で、熱量は 891x+1411y=1099 連立でx=0.6 y=0.4 が出る。 メタン:酸素=1:2 エチレン:酸素=1:3 なので 酸素の物質量=2x+3y となる。後は計算。(2)3 (1)アレニウス ○ (2)ブレンステッドとローリーに殴られるレベル × (3)これもブレ・ロリ ○ (4)弱酸だしね ○ (5)pH大きいほうがより塩基性 ○ よって (2)4 まずグラフから。pHが12までしかないのが既に怪しい。14まで書き足すと一目瞭然。 (1)というわけで、グラフはこれにひっかけようとしてるね。○ (2)むろんこれは○ (3)ちょっと計算が必要そう。さらに問題のみそは「Aの価数はあるのにBの価数がない」 ことだね。なぜなら(4)の選択肢があるからよ。 まとめてかたずけることにしよう。 まず塩基からでるOH-は 1価×0.1×0.01L こんだけmolでる。 この時点で塩基の物質量は(3)で正解なわけだけど… 一方酸の価数をbとおくと、酸から出るH+は b×0.2×0.005L これらが等しいので 1×0.1×0.01=b×0.2×0.005 よってBは1価。(4)が×※ちなみに一般的に酸はAsid、塩基はBaseで頭文字も酸がA、塩基がBを使うことが多いが なんか違和感ある問題ね…5 「式中に単体があるものはほぼ酸化還元反応」を使うと、まず(1)(3)が消える。 (2)過酸化水素は一般的に酸化剤。両辺見て酸素の酸化数が変化。○ (4)過マンガン酸カリウムも酸化剤。マンガンの酸化数で判断。○ (5)見慣れない(こともない、接触法の最後の式だ)が、 酸化数全部出してみればいい。× よって(5)6 ちと面倒に見えるが…a 銅電極も銀電極も陰極→陽イオンが引かれる→イオン化傾向小さい金属析出 というわけで銀も析出する。この時点で(1)か(2)。 銅をもとに電子を求める。 Cu2++2e-→Cu より、銅:電子=1:2 銅は0.320÷64=0.005mol、よって流れた電子は0.01mol 直列回路で流れた電子量は同じだから 銀の式 Ag++e-→Ag より、電子:銀=1:1 よって銀も0.01molで(1)b それぞれ考えよう。 (1)A白金→陽極 硝酸イオンは反応しないから水反応→酸素 × (2)Aを銀にすると「陽極がPt,C以外溶ける」ので × (3)B炭素→陽極 塩化物イオンは電子出しやすい→塩素に ○ (4)Bを銅にすると(2)と同様 × よって(3)結局今年もダニエル出ず…エネルギーや環境問題もさほどからまず、滴定もオーソドックス。拍子抜けですね。
2012.01.15
コメント(0)
-
とある化学教師のセンター解説2012 大問1
ではいってみるよ。1a 単一の元素記号で表すことができるかを考えればOK。 黄銅はCuとZnの合金なので答えは(1)1b パッとやると危ないのかね?(1) H-O-O-H (2)H-S-H (3)CH3-CO-CH3 (ケトン基にC=Oの二重結合あり)(4) CH3-CH=CH2 (5)H-CHO (アルデヒド基にC=Oの二重結合あり)というわけで、(6)のO=C=Oが正解。2 同位体の定義は「陽子数が同じ(原子番号が同じ)で質量数が違う」 すなわち、違うのは中性子数。他の選択肢だと別な元素の原子になる。(3)3 質量増加分は明らかに酸素。酸素原子が何molついたかを考えよう。 1.62-1.3=0.32より、0.32÷16=0.02mol ここで、酸化の式を(必要最小限抜き出して考えると)M→MO よって、「左辺M:右辺についたO」はどうみても1:1 つまり、左辺Mも0.02mol さらに、当初の質量1.3gこれが0.02molということだから、1.3÷0.02=65 (5)4 【やや難】自分でイメージできないときつかったかも。やれば簡単。 問題文より、「どんな量のドライアイスでもこの問題が成り立たなければ出題できない」 ってことが見え見えだから、勝手に、「1gのドライアイス」とおいてみよう。 1gのドライアイスは気体になれば当然1gの二酸化炭素(気)になる。 その体積が何倍かを考えればいいね。 1gのドラの体積(密度を使う) 0.001L÷1.6g 1gの二酸化(気)(標準状態を使う) 22.4L÷44g あとは、何倍かなので 「1gのドラ体積÷1gの二酸化(気)体積」でおっけ。(4)5 やはりイオン化エネルギーと半径は来たね。 (1)(2)言わずもがな (3)同周期の陰イオンだからね。電子もらって希ガス型に。 (4)イオン化エネ→陽イオンになるために「必要な」エネルギー ネオンは「なりたくない」→エネルギーたくさん必要→× (5)そりゃ最外殻がClの方が外側だからね。 というわけで(4)が正解6 身の回りも例年通り。セッケンは久しぶり。 (1)冷凍庫使ったことないのかね?どんな固体も熱運動している限り常に 「昇華圧」が存在し、ごくわずかずつ昇華している。 (2)気→液 は凝縮だね。 (3)活性炭は表面積がでかいのです。さすがに「消◎力」は出せません(何) (4)漂白作用は「酸化還元反応」によるもの。色素を酸化還元反応によって 分解するのね。だから、塩素系or酸素系漂白剤を混ぜてはいけない。 酸化還元反応で塩素単体が発生するからね。 (5)油脂をセッケンで加水分解はできない。これは「乳化」 というわけで(5)が正解。基本法則は今年も出ず。いったいいつまで出ないのか、ずっと出ないのかなw
2012.01.15
コメント(0)
-
とある化学教師のセンター解答速報2012
というわけで、予備校に怒られそうですがwとりあえず番号だけ。もし万が一ミスってたら教えてw解答はのちほど大問ごとに行きます。大問1 1635445大問2 4224513大問3 3522135大問4 1432265
2012.01.15
コメント(0)
-
とある化学教師のセンター解説 2011 大問4
さてオーラス。大問4いってみよう。4-1 41 知ってりゃいいけど…○ まぁ、知らなくてもあからさまなのが下に。2 コレも、付加を想像すれば。○3 やや低温での分子間脱水。コレも○4 書けば分かるが、第1級アルコール→酸化したらアルデヒド、カルボン酸。×5 アルコールの性質。○4-2 5アルキンはやや珍しいけど、考えればできたはず。まず、アのシストランスできないのはC≡Cの横にHのみ、のやつ。付加したら、C=Cの1個のCにHが2個つく場所ができちゃって、対称になるもんね。この時点で2,4,5。2分子つけるってことは、完全に単結合にするってこと。書いてもいいけど、もし覚えてたら、「アルカンで不正炭素原子があるのはCが7個以上」使って絞ってもGood。2が消える。まぁ、4は左右対称すぎて、消えるってのもすぐわかるわけだけど…5番。4-3 1NaOHで切る→けん化→エステルじゃね?(ちなみに希硫酸は、けん化後カルボン酸を遊離させているわけだが、気にしなくてもとける。)銀鏡反応→還元力!しかし、エステルはカルボン+アルコールなので、還元力あるやつができるわけがない。…しかし、一人だけお決まりの彼がいるよね。ギ酸だね。つまり、カルボン酸側(COO側)がギ酸。この時点で1か2しかないじゃんw切断後のアルコールを考えると、ヨードホルム反応できるのは1番の2-プロパノールだけだね。4-4 6ハイ結局オーソドックスなクメン法…アのとこの反応は「付加」だからね、プロパンはC=Cそもそもないからむりぽ。5~8に絞る。イは、なかなか知ってるかどうかというとこだが、ウがアセトンと分かっていれば、原子の数からOが2個って分かるはず。6番。イの全体の物質はクメンヒドロペルオキシド。クメンの先にヒドロ(水素)がありペルオキシド(過酸化物=酸素が多い)になってるよ、みたいな意味ね。4-5-a 4ハイ還流~。そして、還流→エステルの製法と思っておk だったね。酢酸とエタノールだから、酢酸エチルができているはず。1,2 そのとおりです。○3 Aには酢酸と濃硫酸が残っているから、炭酸水素Naよりどちらも強酸性。Na奪う。二酸化炭素遊離。○4 ここできたか!?「スイカ(水下)」の使いどころなんだが。水層が下層(と、ほとんどの場合思っておk。例外は四塩化炭素)なので、下層は酢酸Na(操作2で酢酸はコレになってる)やエタノール、硫酸Naしかいない。油層が上。エステルは水に溶けない。アロマオイル的な。よってコレ×5 エステルの特徴ね。4-5-b 24-3と同様に、けん化。エステルだと分かれば、すぐにたどり着いたと思うが。1 けん化でエタノールと酢酸Naに戻る。コレは水溶性。○2 巨大な釣り針だが、釣られた人も多いのでは。「酢酸Na」になっているのですから、分子状の「酢酸」はほとんどありません。つまり、飛び回って鼻に入ってこないわけです。×3,4 もち○5 硫酸触媒で「加水分解」このときはエタノールと「酢酸」ができるし、においもする。○4-6 3問題文から、Aは2-ブタノールしかない。Bはエチルメチルケトン。1 書けば分かる。○2 書けば。1-ブタノール、1-メチル-2-プロパノール、そして2-メチル-2-プロパノールがある。○3 ジエチルエーテルと、メチルプロピルエーテル、そして、イソプロピルメチルエーテル(片方枝分かれ)がある。×4 ブチルアルデヒド(直鎖の端っこにCHO)、イソブチルアルデヒド(枝分かれではじっこにCHO)がある。○5 これは意地悪問題じゃないか?1-ブテンの3個目にOHがついた形の「1-ブテン-3-オール」(3個目のCが不斉)が確かにあるんだけど、高校生が考えてパッとでてくるのかい?C=O二重結合のかわりにC=C二重結合があるものを考えるというのが意地悪。まぁ、できなくても、3が明らかに×え、終わり?計算はなしか…その分少し考える系の問題が多かったね。全体的には、やや楽だと思うんだけど、知識だけでなく計算力や思考力が必要な場所が結構ある感じだね。丸覚え勝負の人にはつらかったかもしれない。まぁ、次は2次だね、頑張りましょ。※解説は、あくまで「センター向け」だったり「高校生向け」だったりで化学的に突っ込めるところはあると思いますが、そこはお察しください。
2011.01.16
コメント(3)
-
とある化学教師のセンター解説 2011 大問3
さて、疲れてきたけど、大問3いってみよう。3-1 11 空気の平均分子量28.8 22ページに「Ar=40」と答え書いてあるww ×2~4 希ガスですから ○5 一番分子量小→一番分子間力小→分子同士が引き合いにくいから、気体になりやすい。○ しかし知らなくても1が明らかに×6 Kの同位体が崩壊して… ○ って知らなくても1が(ry3-2 51,2 まぁ、そうね。○3 セッコウも、気をつけろといったけど、どうかな?○だけど、知らなくても5番がねぇ…4 熱分解。○5 中学校でもやった「ふくらし粉、カルメ焼き」水素でたら大変よ。明らかに×3-3 41 ○だけど、知らなくても…2,3 ○ JK(常識的に…もう説明したくない。4×3-4 61 「徹子に黒アリ(FeCoNiCrAl)不動態」は「濃硝酸」のとき。だから、今回は溶けるね○2 1と同様。万が一、希硝酸でも不動態と思い込んでいた人がいても、1,2両方×だから、違うって気づくはず。○3 Cuは酸化力のある酸にとける。○4 Znは水素よりイオン化傾向大なので、希酸にとける。また、両性元素なので塩基にも溶ける。○5 Agも酸化力のある酸にとける。○6 ちょwwwwww × 不動態が曖昧でもどうみてもコレ×wwww3-5 2面倒だが式を書いておこう。Fe3O4+4CO→なんたら~ コレで十分でしょうww1:4で反応とわかる。四酸化三鉄の式量が56×3+16×4=232全部kgなので、gと思い込んで解いておk。四参加なんたらのmolが4.64÷23=0.02mol。1:4だからCOは0.08molCOの分子量12+16=28 28×0.08この時点で概算10分の1で、2か3だが、丁寧にやって、2番かな。3-6 1コレも地道か…めんどいね。1 AB Cl沈はAgかPb。沈なし AC 炭酸イオンはアル金以外沈。沈ありってあれ…終わりじゃんwwww1番まー、終わりたいところだが解説と銘打っている以上…まず、AB組み合わせをざっと見ると、Cl沈はAgかPb(もしくはHg)、硝酸塩は沈殿しない、イオン化傾向小のAgは沈しやすい、あたりから沈ありは4だけとなる。AC組み合わせは、硫酸沈はアル土+Pb、炭酸沈はアル金以外、クロム酸沈はAgPbBaので、沈ありは1と4。3-7 6馬鹿にしているんでしょうか。間違い探しです。6番のアレは、「次亜塩素酸イオン」ですね。×ミョウバン知らなかった人はちょっとだけ戸惑ったでしょうか?あれ、大問3…よく読んであわてなければ、コレは簡単だったはず。
2011.01.16
コメント(0)
-
とある化学教師のセンター解説 2011 大問2
さー、大問2もどんどんやっちゃおうねぇー。2-1 2光合成とか何とかは気にせずおk。しかし、与式をみて、「右辺→左辺(逆向き)に見たら燃焼じゃね?」と分かればGood。燃焼の逆だからQは吸熱と確定し、1~3のどれかということに。あとは「反=生-反(反応=生成物の生成熱-反応物の生成熱」1273-6×(394+286) だが、下線部計算した時点で1番と3番はありえないから、2番2-2 51~3は言わずもがな。○4 水(固)を作るときは、水(液)をつくり[発熱]それが熱を放出して[発熱]凍る。一方水(気)を作るときは、水(液)をつくり[発熱]それが熱を受け取って[吸熱]気体になる。トータルの発熱(生成熱)は当然水(固)が大きい。○5 蒸発熱の定義が「吸熱」なのです。(熱を出して[冷えて]気体になるものが基本的にないからです。)つまり、「蒸発熱が××kJ」といえば、吸熱××kJで、熱化学方程式上では-××kJになります。だから、4の「水(液)をつくり[発熱]それが熱を受け取って[吸熱]気体になる。」なんだけど、そのまま「蒸発熱××kJ」で足してしまうと、まずいのは分かるよね。×【この2-2は選びにくかったかも。消去法かな?】2-3 3よし、これも出たね。「Q=mct(キューちゃんマジキュート)」まずはQを出しにいこう。メタノールの分子量は12+4+16=3264gなので64÷32=2mol1molで726kJの熱が出るので、726×2(kJ)の発熱。さらに、実際使われるのがコレの10%だから、72.6×2(kJ)あと、比熱cがJなので、1000J=1kJから、72600×2コレがQちゃん。m(質量)は1.0kg=1000gなので、72600×2=1000×4.2×t t≒35 最初の20℃を忘れず足して、3番ちなみに、選択問題だから、4.2≒4としちゃってやっても、t≒36で3番になるよね。スピードアップでこういう方法も何度か教えたけどできたかなぁ。2-4 5還元剤→自分は酸化される→酸化数増 で見ていこう。地道にね。1 Hは酸化数減、Oは変化無し ×2 酸化数減 ×3と4 Hは変化無し、Oは減 ×5 Sが+4→+6 コレが正解 ○6 S減、O変化無し ×2-5-a 3実験系も流行だよと言っていましたが、マークできてたかな?1 ホルピは使う溶液で洗う(友荒い 共洗い)コレ基本。薄まったら困るしね。 ○2 メスフラは、「どうせ薄めるんだから」水あっておk。○3 コニカルに、今から使う溶液を「量りもせずに」入れたら、先走ってるのと同じ。×4 ビュレットも共洗い。5 満たした状態で正確に測れるようになってる。しかし、コレ知らなくても3が明らかに×。2-5-b 4操作1でAを10mLとり、100mLに薄めている→濃度が10分の1になっている点に注意。Aの濃度をc(mol/L)としよう。Bの濃度は0.1cだね。おっと、当然、酢酸:NaOHだから、1:1これは確認。0.1c×10=0.110×7.50 下線部見た時点で7.5の約10分の1。4番。 2-6 6燃料電池もビンゴだね。しかし、ヒント大杉で詰まらん…「西洋のふいんき(なぜか変換できない)→正陽の負陰き」で、Aが陽、Bが陰。大まかに読んで、水素使うほど電気が流れ、陽が変化するってのは知らなくても分かるので、んで、「電気分解の陽極がC or Ptでない場合は溶ける」から、Aは減少とわかる。この時点で5番か6番。あとは、式を書いてもいいけど、とある化学教師的にいえば、「水素が1反応するとき動くのは2e-」「銅が1反応するとき動くのは2e-」これを覚えてるはずなので、水素1mol反応するとき銅も1mol反応とわかる。水素1molすなわち22.4Lをさがせば、そのとき銅はおよそ64gへって36gだったらいいので、6番。大問2は、少し時間かかるかもね。
2011.01.16
コメント(0)
-
とある化学教師のセンター解説 2011 大問1
さー、どんどんやっちゃおうねー。問題そのものは出回ってるので、見比べる有機がある人は早速見比べちゃってください。つーか、計算問がやや増えたね。我が校でやった「緑」風味というか…その辺を冷静に稼げたかが差のつきどころかな。1-1-a 3電解質=水中で電離可能なもの≒酸や塩基もしくは水溶性の塩 と考えておk。1,2アルコール 4エステル 5糖 6アルデヒド これらはみんな中性3カルボン酸 酸性。よってコレが正解。1-1-b 6地道にやるしかないよね。一番から順に数えていこう。1 2本 コレは×っぽい。2 4本 怪しいか?3 3本 この時点で1と3×4 4本 2番と被っているので答えが被ることはないから2と4両方×5 0本 この時点で6が正解。1-2 6予想通り、「典型の境目」きたね。まず、斜めの境目は「非金属-金属の境界」なので、1-4全滅wwそして、真ん中が「遷移」ですから、答え6「絶対に子供は典型的なハードゲイ(Zn Cd 典型 Hg)使わずとも…チッ1-3 2まずはそれぞれの原子を確認。電子数=原子番号なのでa 7個=N b 9個=F c 10個=Ne d 11個=Na1 まぁ○でしょ。2 窒素は三重結合。終了。答えコレ。ちなみに、3 Fは電気陰性度大 ○4 希ガスの荷電子ゼロ ○5 イオン化エネルギー小→陽イオンに簡単になれる。dはアル金なので ○1-4 4とっつきにくいが、体積→質量→モル→個数と変換しよう。1立方cmで0.91gより、0.91を水の分子量18で割るとモルが出るね。 あとは、アボをかけよう。(0.91/18)×6.0×1023= 4番1-5 1まず反応式はCH4+2O2→CO2+2H2Oなので、体積比=モル比だから、10mLのメタンと反応する酸素は1:2より20mL。最初 メタン 10 酸素 40変化 メタン-10 酸素-20 二酸化炭素+10 水(液体なので考慮しなくておk)最後 メタン 00 酸素 20 二酸化炭素 10 よって合計30mL。最初の50から20減少しているね。1番。1-6 5これもいつもの「身の回り」1 リアカーナキ…言わずもがな ○2 ジュラルミン。ラルミン。アルミン… ○3 知らないで受けた人は勇者 ○4 つまり、昇華と言いたいんです。お察しください ○5 4の時点で5番正解ですが、当然「酸化力」です。 ×大問1終了~。例年より簡単。
2011.01.16
コメント(0)
全38件 (38件中 1-38件目)
1









