[授業] カテゴリの記事
全164件 (164件中 1-50件目)
-
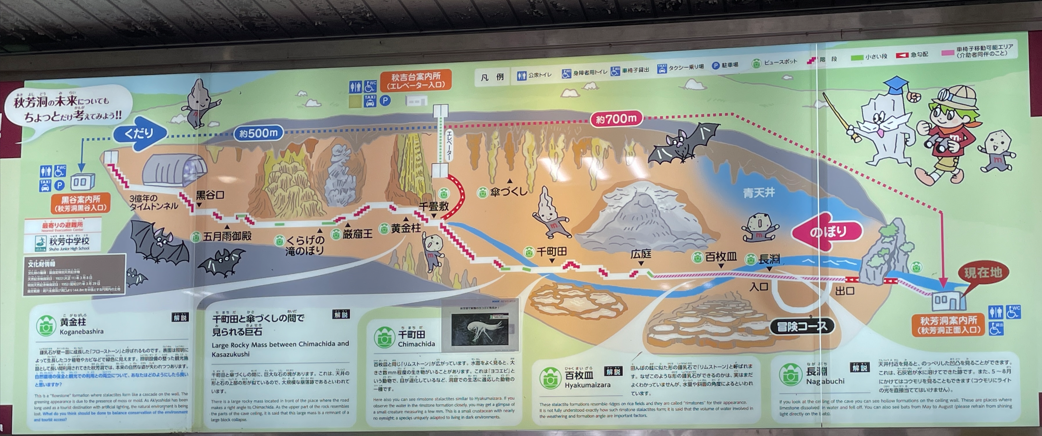
秋芳洞内の二酸化炭素濃度
40年ぶりに秋芳洞を訪ねました。(入り口の案内板)入場は会場直後の8:30(入り口)(青天井付近)(百枚皿)(すぼ柿と大松茸)(黄金柱)黄金柱付近に地上に出るエレベーターがあり、これで秋吉台に出ることができます。カルスト台地やCaCO3の溶食でできたくぼ地のドリーネをみることができます。(カルスト台地)(くぼ地;ドリーネ)鍾乳洞は石灰岩を構成する炭酸カルシウムCaCO3(水に溶けにくい)がCO2を含む水に溶け、洞内で再度CaCO3に戻ることで鍾乳石を作り出しています。上の図のように1.大気中のCO2を溶かした雨水が秋吉台などの石灰岩層にしみこむ2.石灰岩を作るCaCO3がこの雨水に溶ける、Ca(HCO3)2溶液3.石灰岩の洞窟にこの溶液が至るとCO2が放出されCaCO3が析出する4.析出したCaCO3が鍾乳石・石筍などの造形を作るということは、、洞内の二酸化炭素濃度は外より高いのではないか?実際にモニターされておりw、私が入洞したときは600ppmで大気中のCO2濃度410ppmより高い「秋芳洞内の小気候による観光客への健康影響と今後の管理方法」Kanato ANDOhttps://www.jstage.jst.go.jp/article/ajg/2022s/0/2022s_203/_pdf/-char/jaによれば、冬季の入場者数の少ないときは500ppm夏季の観光シーズン(観光中の観光客同士の距離は 0.45m 以下)では1000ppmを越えてしまうようです。
2024.06.14
コメント(0)
-
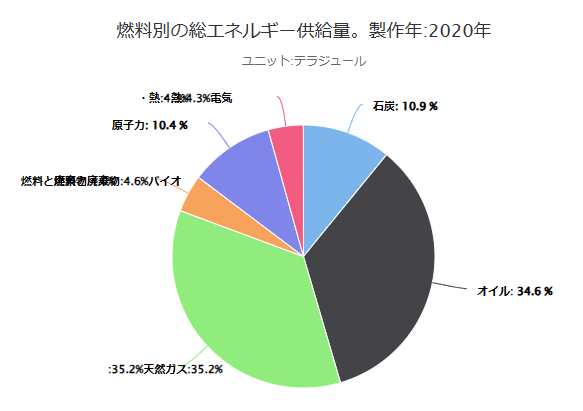
水素H2エネルギー①昨今のエネルギーを見る
自動車のEV化が話題です。世間では「温室効果ガスCO2を減らしましょ」ということでLi-ion電池中心の電気自動車(BEV)がずいぶんと推進されているようです。私は「CO2削減が気候変動に影響する」という説に懐疑的、そして寒冷期のBEVの走行距離が低下するので当分ハイブリッド車を乗り続けようと思っています。むしろ(百歩譲って)CO2を減らすなら、利便性を考えると水素H2が自動車燃料、電力生成、燃料備蓄に向いているのではと思い、水素エネルギーについて整理してみようと思います。はじめに、世界の1次エネルギーについて①世界の燃料別の総エネルギー供給量(2020年)UNSD エネルギーバランスよりhttps://unstats.un.org/unsd/energystats/dataPortal/石炭・石油・天然ガスなど化石燃料が約80%を占めています。水素H2は供給されていません。天然資源としてH2は水に溶けているものが確認されていますが、まだあまり利用されていないようです。②燃料別のエネルギー(各燃料の単位発熱量)燃料1Kg当たり、燃焼による発熱量(MJメガジュール)です。原油から水素までは液体です。液体密度をかけて質量にしています。石炭は輸入炭、国内炭、無煙炭などの平均値、重油はA~C重油の平均値です。また、LNGはメタンCH4が主成分、LPGはプロパンとブタンが中心の混合物です。③現行では水素H2は商用化されていないけど…水素H2は②で比較したようにLNG(CH4)と同じくらいの単位発熱量120MJ/Kgを持っており、技術の発展によって保存・輸送が可能になっています。電力のエネルギーミックスへの参入や自動車や列車・航空機の燃料として期待しています。今後のブログの予定は水素の作り方、輸送や保存の技術、利用の技術の発展について調べていきたいと思います。
2024.01.07
コメント(0)
-

ヘリウムの不思議な性質…超流動の動画他…「Thoisoi Japan」
おもしろい動画を見つけましたヘリウムの液体、その超流動、存在量などの動画解説ですリンク先は以下です「Thoisoi Japan」→リンクはここをクリックなかなか、実験してみることのできない画像がたくさんあります「Thoisoi Japan」ではセシウム、クロム、タングステン、イリジウム、タンタル、タリウムなどなど手に入りにくい単体の性質を動画で紹介していますどうぞ、授業で活用ください
2023.10.23
コメント(0)
-
自然科学は「見当識」の精神活動が生んだ(ノート)
救急車に収容されると、症状により、救急隊員から「見当識」の確認をされることがあります。1.「見当識」とは 自分がいる時間や場所、周囲の人や状況などを正しく認識する能力のことです。見当識は、心理学的な機能であり、注意や認知、思考、判断、記憶などの精神機能の統合が必要です。見当識が障害されると、失見当識(見当識障害)と呼ばれ、譫妄や意識障害、中毒、認知症などの原因で起こります。2.救急隊員が行う見当識の問いかけ 見当識は、時・場所・人物の3つの要素で判断されます。例えば、救急隊員はこのように問いかけることがあるのだそうです。• 時:今は何年何月何日ですか?• 場所:今どこにいますか?• 人物:私は誰だと思いますか? 3.「自然科学」 「見当識」は人間の精神活動の統合であり中核なのだと思います。人間の好奇心の根源的な表れだと思います。一方、自然科学は自然界に存在する事象や法則を観察・実験・理論化する学問です。物理学、化学、生物学、地学、天文学などが含まれます。これら自然科学が目指しているものは、物理学:物質やエネルギー、空間や時間、力や運動などを数学的手法を併用して研究し、自然現象の根源を探求し、宇宙と物質の起源と進化を解明しようとしています。根源的であるので地球や宇宙、化学、生物などの科学研究の基礎を受け持っています。 化学:物質や生物を構成する分子などの化合物、無機物質などを原子の単位で分析・合成することを研究します。また、化学反応やそのメカニズムを研究することも主要な目的です。生体内の物質や化学反応も含まれるので生物学とのかかわりが深く、岩石・鉱物の生成や結晶構造なども守備範囲です。生物学:生命の本質や多様性、進化や発展、環境との関係などを理解することです。生物学は、細胞や分子、遺伝子や生化学、生理学や発生学、生態学や行動学、進化系統学や生物工学など、多くの分野に分かれています。生命現象(生きていることって何?)を解明していきます。地学:地質学や鉱物学、古生物学、自然地理学といった分野の研究を行い、地球の歴史や惑星としての構造を解明することを目指します。また、大気や海洋の動きを知ることで気候変動や異常気象など諸問題にも取り組みます。天文学(宇宙科学):宇宙とその中にある全てのものの起源と進化とその性質、およびそこで起きるさまざまな現象を知ることを目的とする学問です。天体物理学は天体や天文現象の振る舞い・物理的性質・動力学的過程を取り扱います。天文学では、電磁波、宇宙線粒子、ニュートリノ、重力波などさまざまな観測手段を総合して研究を進めています。4.「見当識」と「自然科学」「見当識」私は何者?:①人間は生物ですが、それを作るのは原子。宇宙の始まりは水素H、Heだったが原子は109種類あり、それらができる原子進化には恒星内の核融合が必要です。人間までの進化を根源的に考えるとはじめに原子進化が必要です。物理学や天文学の知見が必要でしょう。②ここから、生物に必要なタンパク分子やDNA・RNAが必要になる。これらがどのように簡単な分子から複雑化したのかを知るためには化学や生物学、古代地球や星間物質の研究が必要になってきます。③生体分子を膜で包んで単細胞分子ができる(細胞が作られる過程も謎)が、これが多細胞化し、組織や器官を作り、統合されて最後には人間となりました。そんな生物進化の過程や分子論的なメカニズムを検討する必要があります。このあたりは、生物学や化学の範疇でしょう。「見当識」今はいつ?ここはどこ?:BIG BANG以来138億年たつと言われています。これは宇宙物理学の成果。では、BIG BANG後の恒星や星雲、宇宙の様子は?太陽系や地球はどのようにして生まれたの?その地球はどんな作り?地球や大気・海洋の動きは?自然科学全般の協働が必要になるでしょう。以上は、高校生に自然科学全般を俯瞰し整理して話してみたいと思って書いています。不完全なところもあると思います。お気づきの点がありましたら、コメントを通じてご教示ください。よろしくお願いします。
2023.07.24
コメント(0)
-

元素はどこから来たの?「PERIODIC TABLE Origin of Elements」
先日NHKの番組「コスミックフロント」でマイクロブラックホール関連の解説がありました。その中で「PERIODIC TABLE Origin of Elements」の紹介がありました。元素の核起源がおりこまれた周期表です。例えば、HやHeは青Big Bang fusion(ビッグバン初期の融合)でできた。O~Rb特に典型元素は黄Exploding massive stars(大型恒星の爆発)でできた。Reから後は紫Merging neutron stars(中性子星の衝突融合)でできたというような表現です。元素枠内の横軸は時間軸、縦軸は量を現しています。なお、灰色は人の合成によるもので、宇宙由来ではない。資料はオハイオ州立大学ジョンソン氏のデータです。これらのデータは現在もシミュレーションや観測で生成原因も書き換えられる可能性があります。NHK「コスミックフロント」では、金Auの生成は謎が多く、中性子星と小さな原始ブラックホールの衝突でできるとの仮説も紹介していました。元素はどこでできて、どこから来たのかとても壮大な話ですね。この周期表を見ていると宇宙の大きさと長い歴史に気持ちが飛躍していきます。
2023.01.29
コメント(0)
-

GoodNotes5で授業を録音…UPDATEでさらに進化
GoodNotes5は学校での授業に、コロナで休講時には在宅授業に活躍していましたが、(iPadを教室の授業で使う(まとめ)→2020/8/30ブログ)UPDATEで録音機能がついてさらに進化しました。最近はなくなりましたが休校時の在宅授業や長期休暇時の補講などで活躍できそうです。かつてコロナ休校時に生徒用在宅授業ビデオを作るときにはiPad画面の右上から下へスライドして、「録画ボタン」から動画ファイルを作成し、学校のサーバーにupしていました。ただし、音声は録画しながらつけなければならず、しくじった時にはやり直しでした。MSofficeのPowerPointなら各スライドで録音でき、動画に落とし込む機能もありましたので、それに頼っていることもありました。しかし、生徒用プリント(PDF)に直に記入したり、問題を開設するときにはやはり手書きが効率的です。GoodNotes5に録音機能があれば最強となります。また、学生の講義用のノートとして、より強力になったのではと思います。PDFに手書きで書き込み、必要に応じて画像を貼り付け、そして、講義の音声も手書きとリンクして取り込める。「私が学生の時にこんなのあればなぁ」つくづく思います。
2023.01.22
コメント(0)
-

化学のシミュレーションPhETコロラド大学
コロラド大学で研究・集約されている物理、化学、生物、地球科学、数学のオンライン無料シミュレーションがあります。これらの成果・集積物は2018年に紹介していますが、新たに加わったシミュレーションがありますので再度紹介します。コロラド大学のシミュレーション→2018/4/22ブログそのトップ画面ですリンクはこちら(HTML5…WEBブラウザーで表示できるものだけを検索)→PhET面白いと思ったものを紹介すると…「拡散」はじめはこんな画面。重心・粒子流量・容器のサイズ・ストップウォッチを表示(オプションです)質量はHe4amuとNe20AMU、温度は300K、粒子数はそれぞれ30個仕切りを取り払い、拡散を起こさせるとこの大きさ16mnx8nmの容器では重心の位置が中央になるのは31psかかりました。(あくまでシミュレーションの結果ですが)シミュレーションが作りやすい「気体」関係が充実しています。他に濃度やpH、原子核の安定性もあります。授業にも使えそうです。ぜひ、WEBを訪ねてみてください。
2022.12.20
コメント(0)
-

iPadを使う授業;AnyCastの不具合を対策する
2020年の7月2日に2代目のAnyCastに変更し使っています。授業用プロジェクター画面ミラーリングAnyCast換えました→2020/7/2ブログケーブルレス(WiFi)でつながっているので、机間巡視しながら黒板にプリントや写真を表示でき、さらに、手書きにも対応しています。今年10月に入ってから、①Padとのリンクが切れる②再接続すると表示されるが、5分も使っているとまた表示できない(リンクが切れる)講義に差支えが出てきましたので、原因を見つけて対応しました。以下対応です。これで不具合は解消されています。①コネクタの接触不良本体とアンテナ、電源をつなぐUSB2.0Micro-Bの接触不良がよくあります。上の写真の赤↑部分。接続させたままカバンにれると、コネクタに無理な力がかかりやすい。これにより、接触不良が起こります。コネクタを抜いてエタノールで洗い、乾かして刺しなおしました。接点復活剤を少量吹くのも効果的です。②iPad-OSのupdateで睡眠モードなどが追加iPadやiPhone のOSが大きくupdateしました。これにより私の場合、何かのはずみで授業中に「睡眠モード」になってしまっていました。これを「仕事」モードに変えます。③「画面自動off」を「常時」に「設定」の「画面表示と明るさ」で「画面自動off」が5分や10分になっていると設定した時間で画面が消えます。AnyCastとのリンクが切れることもありました。そこで、「画面自動off」を「常時」にしています。④USB電源を大容量に以前はiPhoneのUSB電源5Wを使っていましたが、パワー不足でリンクが切れる原因になっていました。以降Daisoの15W電源に変えて快適に使っていましたが、2年も使っているとヘタッテきたようです。1時間くらい使うとリンクが切れます。別の15W電源に変えて使い始めました。anycastとのリンクが切れることがなくなりました。もし、anycastをお使いの方で、頻繁にリンクがきれる方は上の①~④を試してください。anycastは安くて、手軽、便利なHDMI出力機器です。うまく使いながら授業に役立ててください。リンクをたどってもらうか、ブログ内の検索で「AnyCast」と検索していただければ、たくさん記事をアップしています。
2022.11.11
コメント(0)
-
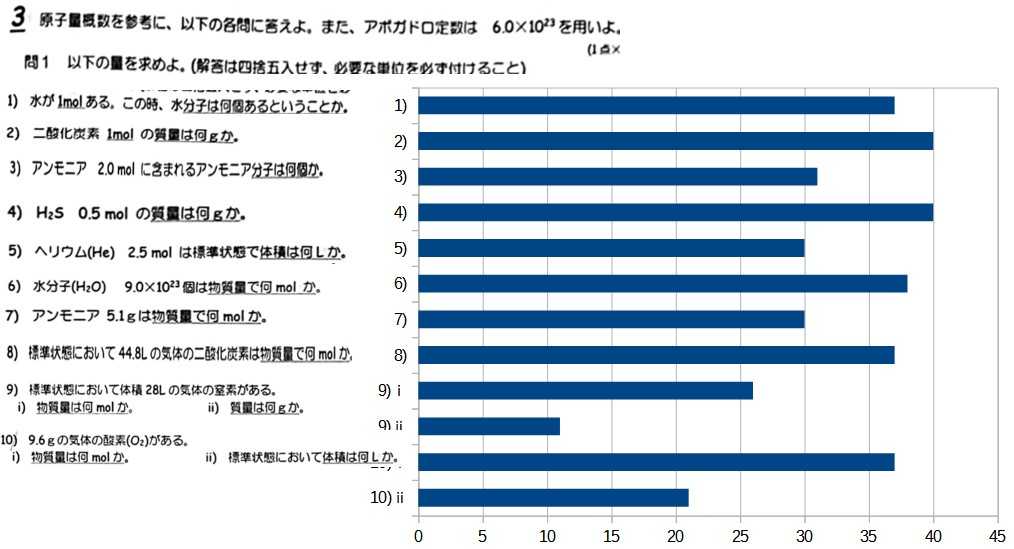
物質量と粒子数・質量・気体の体積をつなぐ計算ができない
前回に引き続き、2学期中間試験の結果です。大問3は物質量(mol)と諸量の関係を計算する問題です。横軸は正解者人数(受験者数は56名)です。①9)10)2段階で計算する問題はできない:ⅰ)の正解者数がⅱ)で半減します。問題が分割していて、順に解いていけばいいのですが、ⅱ)でmol→gまたはLにするところで息切れます。他の問題mol→g(小問2,3,4)ではできていた。複数の計算がからむと混乱するのかな?②1)3)指数がからむと混乱する:高校1年生は数学で指数計算をならってませんが、1年で化学を授業するときは必須なので演習して身につけさせます。しかし、生徒さんにとっては新しい表記なので、理解も計算も難しいのでしょう。物質の種類に関係ない、個数の問題です。物質が水、アンモニアと異なるので混乱したのかな?この試験を行うにあたって次のようなまとめをしています。物質量(mol)を中心に粒子数、質量、気体の体積、モル濃度を配置し、「上から下へ変換するには割り算、下から上に変換するには掛け算」この図をイメージして問題に取り組めば、物質量の計算など簡単です。裏付けは比例計算なので、比例計算を使っても構いませんが、問題で与えられた量(例えば質量g)から求める量(例えば気体の体積L)を算出するには質量[g]を分子量(モル質量)で割って物質量[mol]にして22.4[L/mol]をかける。こういった回答への道筋が明確です。どうすればいいんでしょう。これから、化学反応式・量論へとすすみます。新しい考え方をなかなか吸収できない生徒がいます。ドリルの日々なんでしょうかねぇ、、、
2022.10.24
コメント(0)
-
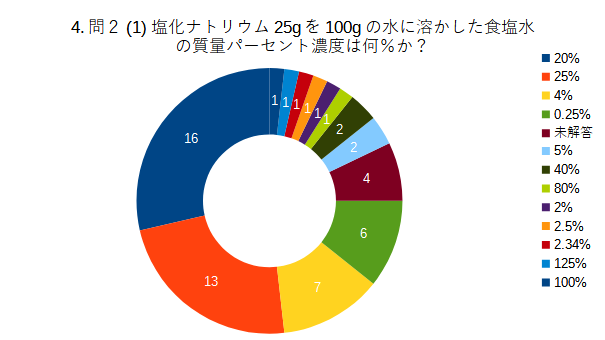
%計算に苦労する高校生(;^ω^)
非常勤講師をしています。いわゆる「進学校」、「中堅校」、それほどでもない高校に勤務しています。毎年、学校が変わりますが、それぞれの学校で化学科の先生方に助けていただいてなんとかこなしています。ことしは「それほどでもない高校」で化学基礎を1年生2クラスに教えています。さて、中間試験が終わりました。今回の出題範囲は「原子量、分子量、物質量(mol)、モル濃度」です。高校化学では、生徒さんに最も負担を強いる内容ですが、これを越さないと化学反応の量的面白みが伝わらないとても基礎的な部分です。「質量パーセント濃度」中間試験の中で、生徒の行く末も含めて心配になったのが「質量パーセント濃度」の問題の正解率が低いことです。問題と生徒の解答を上の写真に載せました。「20%]と正しく解答できたのは56人中16人で28.6%でした。「質量パーセント濃度」は中学校1年「理科」で学ぶのですが、定着していないので高校の授業でも復習、練習もします。多い誤答について①25%:25g塩化ナトリウム/100g水で計算したのですね。この間違いはよくある(中堅校でも)。②4%:100水/25塩化ナトリウム=4で算出したのでしょう。びっくりなのですが、生徒に「2割る4は?」と聞くと、2と即座に答える生徒が少なからずいます。自分が答えやすいように、分子と分母を脳内で入れ替えてしまうのでしょう。「おしい!もう一度、考えて」ゆっくり考えさせると0.5と答える生徒がほとんどです。5%:同じく分子分母の脳内入れ違いです。125/25=5で5%。⓷0.25%:これは%にするのに100をかけ忘れましたね。でも、正答へはまだまだなんですけど...生徒は小数と分数が嫌い生徒は、割り算して小数が答えになるような問題を解きたがりません。小学校5年生までに小数や分数を定着させるべく小学校でたくさんドリルをしているようですが、このドリルを避けてしまうとあとでどり戻せなくなります。その、典型的な例がこの問題や物質量の計算に表れているのでしょう。また、分数も生徒は使いたがりません。約分を使うと簡単な計算もヒーヒー言いながら筆算しています。今回の中間試験は四則演算能力を必要とする分野ばかりでしたから。でもパーセントのセンスは社会人には必要だよ私は彼らには「化学のエキスパート」になることを期待しません。しかし、「市民としての化学の素養」は授業を通して学んでいってほしい。その一つが「パーセント」と「パーセント濃度」です。成分表示の見分け、「どちらが成分濃度が大きいの?」くらいはイメージできてほしい。さらには「100円の商品に5割引きと5%引き。元の値段はどちらが高い?」くらいの判断はつけてほしい。中間試験の得点分布です試験の得点は予想した通り2極化しています。原子量、分子量、物質量、モル濃度、基礎的な問題をたくさん出したのですが、量をこなせる生徒が増えてきたなと思っています。(試験内容については次のブログで)しかし、計算となるとすくんでしまう生徒も多くいます。ドリルを通して自信をつけ、やる気を起こしてもらわなければと思っています。
2022.10.23
コメント(0)
-
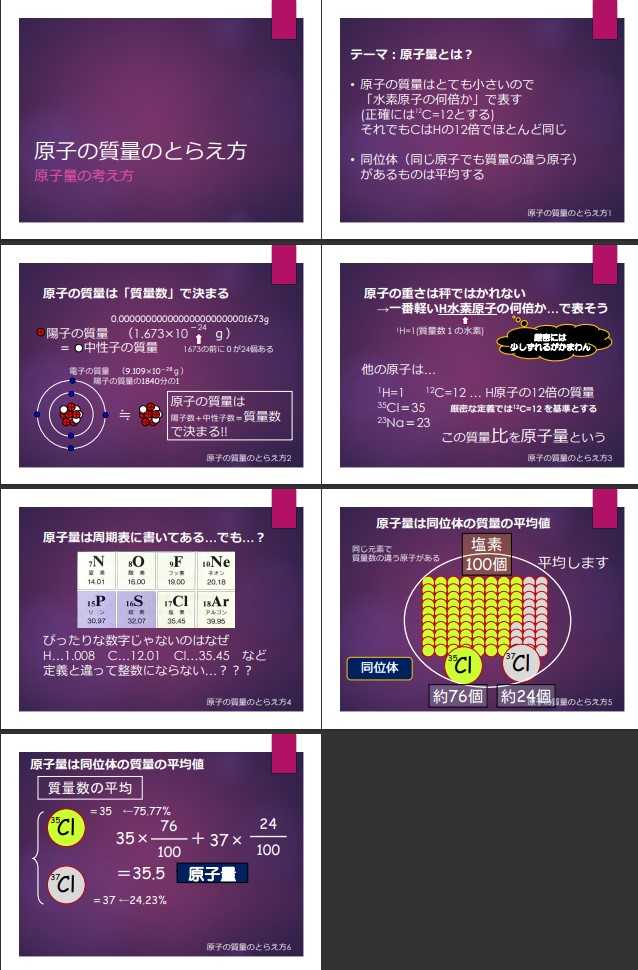
「原子量」の授業…まったく定着しない生徒のためにごまかします
2学期の授業がはじまります。9月は「原子量」「分子量」「物質量」の授業です。ここは、現任校の生徒の定着がひどく悪い。できるだけ、本質をおさえながら、ごまかします。まずは「原子量」。パワポ資料です。1.「質量数12の炭素原子=12」とする定義はほとんどふれません 比例計算の直感的なイメージがない生徒はここで大きくつまずく、そこで2.最も軽いH原子の何倍の重さかを表現したのが原子量(ご批判受けるのは承知です)3.「質量数が原子量になる」おおざっぱですが…これも付記しておきましたパワポ資料を見ていただければ授業の流れはわかっていただけると思います。なにせ、現任校の生徒は算数の素養があまりないものですから、いよいよ量論に入ろうとする教える側は不安でしかありません。
2022.09.02
コメント(0)
-
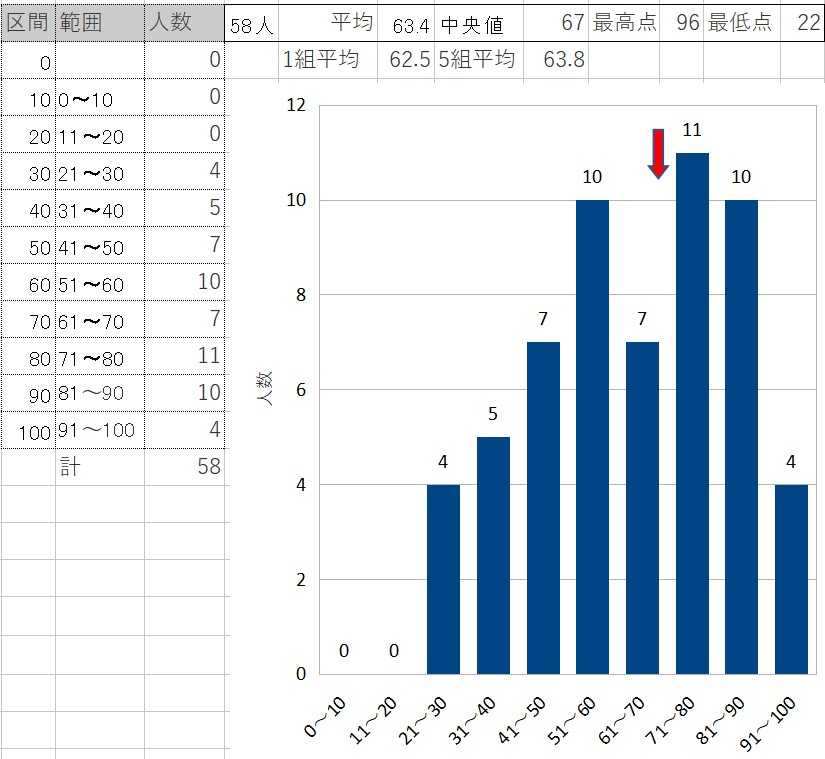
早くも二極化する生徒たち;中間試験と生徒実験2回目
今年度は化学基礎1年2単位50分で偏差値45の高校で講師をしています。5月中間試験は元素、炎色反応、原子の作り、原子核(原子番号と質量数)、同位体、電子配置、周期表、イオン式、実験基本操作 です。得点ヒストグラムは以下です。早くも70点を境に2極化しています。中学校まであんまり勉強する習慣のなかった生徒が得点下位に甘んじたようです。とても素直でかわいい子たちなので大好きです。だからこそ1学期中間試験は点を取りやすいので平均80点をとらせて、自信を付けさせたかったのですが残念です。さて、生徒実験の1回目は「基本操作・基本実験」で器具とガスバーナーの扱い方です。ヨウ素デンプン反応と炎色反応を行いました。生徒実験 炎色反応;色の表記について→2022/5/13ブログ生徒実験2回目です。タイトルは「アルカリ金属・アルカリ土類金属の単体と化合物の性質」目標は① アルカリ金属であるナトリウムの性質を調べ、理解することができる。② アルカリ土類金属であるカルシウムの性質を調べ、理解することができる。《実験1》水酸化ナトリウム粒(アルカリ金属) (1) 時計皿に水酸化ナトリウム粒を1個取りしばらく放置し粒の変化を観察する →水酸化ナトリウムの色や形、潮解性を見る《実験2》ナトリウム(アルカリ金属) (1)灯油中のナトリウムを乾いたピンセットでとり、ろ紙で灯油をよくふきとる。米粒位にナイフで二分する、すぐに切断面の色と光沢を観察する。(2)試験管に水を5mL程度とり、ここへ(1)で切りとった一方の金属ナトリウム粒をピンセットではさんで水中に落とし別の試験管で蓋をする。水と反応する様子を観察する。反応終了後、蓋の試験管にたまった気体にマッチの火を近づけ点火する。次に、ナトリウムが溶けた溶液にフェノールフタレイン溶液を2~3滴加える。(3)ビーカーにろ紙を敷き、水で濡らしそのろ紙上に残りの金属ナトリウム粒を落とし、時計皿でふたをする。 →発生する水素、水面上で反応する金属ナトリウム、ろ紙上で発火したナトリウムの炎色反応などを観察記録する《実験3》カルシウム(アルカリ土類金属)(1)カルシウムCaの粒を観察する。(2)試験管に水を5mL程度とり、カルシウムCaの粒をいれる。水との反応の様子を観察する。その溶液にフェノールフタレイン溶液を加える。→発生する水素、水面下で反応する金属ナトリウム、生じた水酸化カルシウムによる白濁などを観察記録する《考察》(1)実験1のような変化を「潮解性」と呼ぶ、なぜこのようなことが起きるのか調べよ。(2)実験2(2)で発生した気体は何か?(3)実験2(2)でナトリウムと反応した後の水溶液、実験3(1)でカルシウムと反応した後の水溶液はどのような性質か?(観察5、観察9より)(4)ナトリウムは「灯油中」に保存するのはなぜだろうか?理由を考えよ。生徒たちは、好奇心旺盛でなかなかよく実験していました。実験中はいいのですが、レポートをまとめるとなると、またもや2極化。いいレポート書いてくる生徒が4割くらいそのほかは、気に入りません。それは、①提出日を守れない実験の翌日が提出日です。授業の最初に集めます。遅れて提出する生徒が多いです。(遅れた場合は大幅減点です)実験の印象はすぐ薄れます。だから、すぐにまとめることが大切です。また、どんなに長いまとめの期間をおいても、前日(または提出日の朝)にしか記入にかかりませんから翌日提出しても同じことです。②考察を書いてこない考察を書いてこない生徒が意外に多かった。一番大切な部分です。化学実験は料理の時間ではありません。これも、翌日提出のせいかもしれませんね。とはいえ、あきらめるつもりもなく、今後の指導にかけてみます。
2022.06.17
コメント(0)
-
GoodNotesのテンプレート機能を授業で使う
新学期から化学基礎を教えることになりました相変わらず授業ではiPadとGoodNotesでプロジェクターを使っていきますこれまでの利用方法は「キーワードサーチ」で検索して下さい新しい試みとして、GoodNotesのテンプレート機能を使ってより効果的な授業を目指します①組成式の指導に利用イオン式モデルを表示し、動かしながら授業で使います。GoodNotesでの登録と利用について以下の動画をご覧ください。②共有結合、分子の構造式の指導に利用テンプレートを使って構造式を簡単に作ります。以下の動画をご覧ください。新学期が始まります。頑張りましょう。
2022.04.05
コメント(0)
-
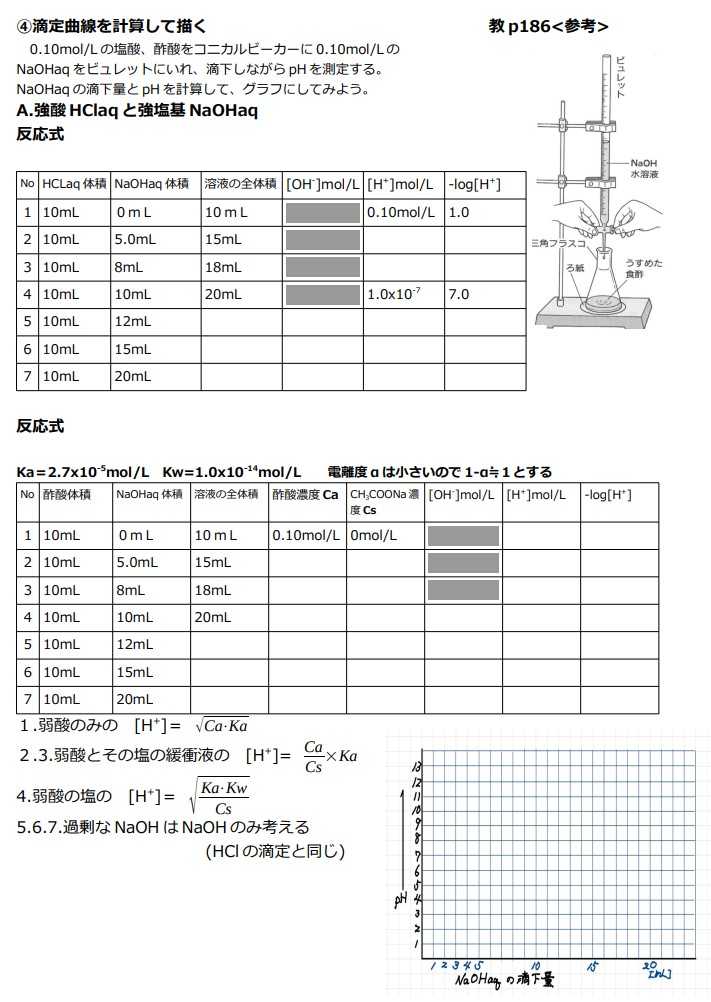
滴定曲線のシミュレーションを生徒に書かせました-グラフ指導
「電離平衡」において弱酸・強塩基の混合、緩衝液、塩のpHの計算生徒がなかなか身に着けられない分野です。そこで、高校入試期間、休講中に『「酢酸・塩酸と水酸化ナトリウムの滴定曲線」をグラフにして提出しなさい』という課題を与えました【目的】①この分野の計算ドリルを行う②グラフの書き方を学ぶ【指導のプリント】①計算方法Henderson–Hasselbalch の式やVan Slyke の式などを使わず、近似式を使って計算させました。②グラフの書き方A4グラフ用紙を生徒に配布し以下の注意をしました。この他、曲線を用いる、グラフ用紙は横に使ってもよい1mL間隔で計算、ただし、変曲点ではNaOHaq9.5mL、9.7mL、9.9mL、10.0mL、10.5mLも計算することなど注意を与えました。【よく書けた生徒のレポート】表計算ソフトをつかって提出した生徒は全体の1/5もいて驚いています。グラフ用紙に手書きのほうが楽かなと思っていました。がんばりましたね。いい経験になったと思います。【失敗した生徒のレポート】左は縦軸にNaOHaqの体積、横軸にpHを書いたもの右は、目盛幅が1ml=7~5mmとグタグタになったものこの他、目盛がふってない、折れ線で変化を書く、打点が明確でない凡例がない、タイトルがないなど後ほど指導が必要なグラフもおおくありました。以前実験が頻繁にできたころ、pHを測定し滴定曲線を提出させました。生徒実験:「酸・塩基の滴定曲線」生徒のレポート→2018/9/29ブログ予備実験:「酸・塩基の滴定曲線」を描く→2018/9/22ブログ「生徒にはいい体験をさせたなぁ」と勝手に思っています(笑)
2022.03.10
コメント(2)
-
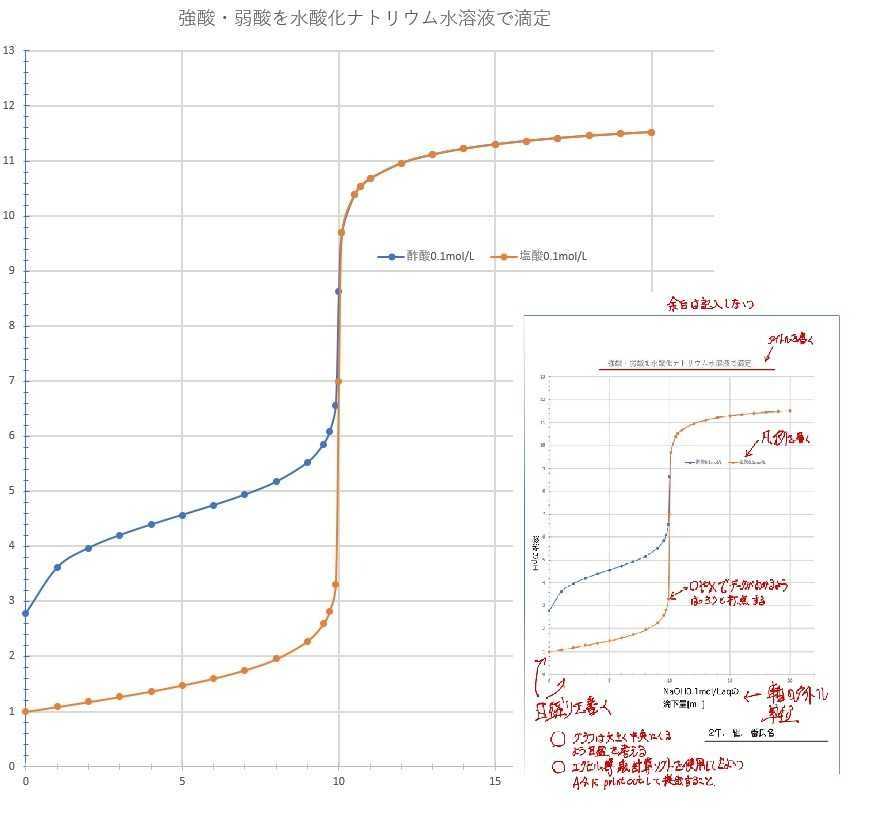
電離平衡のまとめに「滴定曲線」計算-グラフ化
酢酸0.1mol/Lと水酸化ナトリウム水溶液0.1mol/L塩酸0.1mol/Lと水酸化ナトリウム水溶液0.1mol/Lの混合によるpHの変化を生徒に計算させ、グラフに書かせてみます。計算手順のプリントとグラフ用紙を配布し、レポートとして提出してもらいます。目的は1.「電離平衡」弱酸とその塩、緩衝液のpHの授業の復習2.グラフの書き方3.化学基礎ー滴定曲線の復習上の図は、見本です。右下にグラフの書き方(グラフ用紙の使い方)を付けました。計算手順のプリントは以下です。生徒はたくさん計算しなければならないのですが、反復ドリルです。濃度計算とpH計算を身に着けてほしい。なお、コロナがなければ滴定曲線を測定する実験もやるはずでした。予備実験:「酸・塩基の滴定曲線」を描く→2018/09/22ブログ生徒実験:「酸・塩基の滴定曲線」を描く→2018/09/26ブログ生徒実験:「酸・塩基の滴定曲線」生徒のレポート→2018/09/29ブログ
2022.02.19
コメント(0)
-
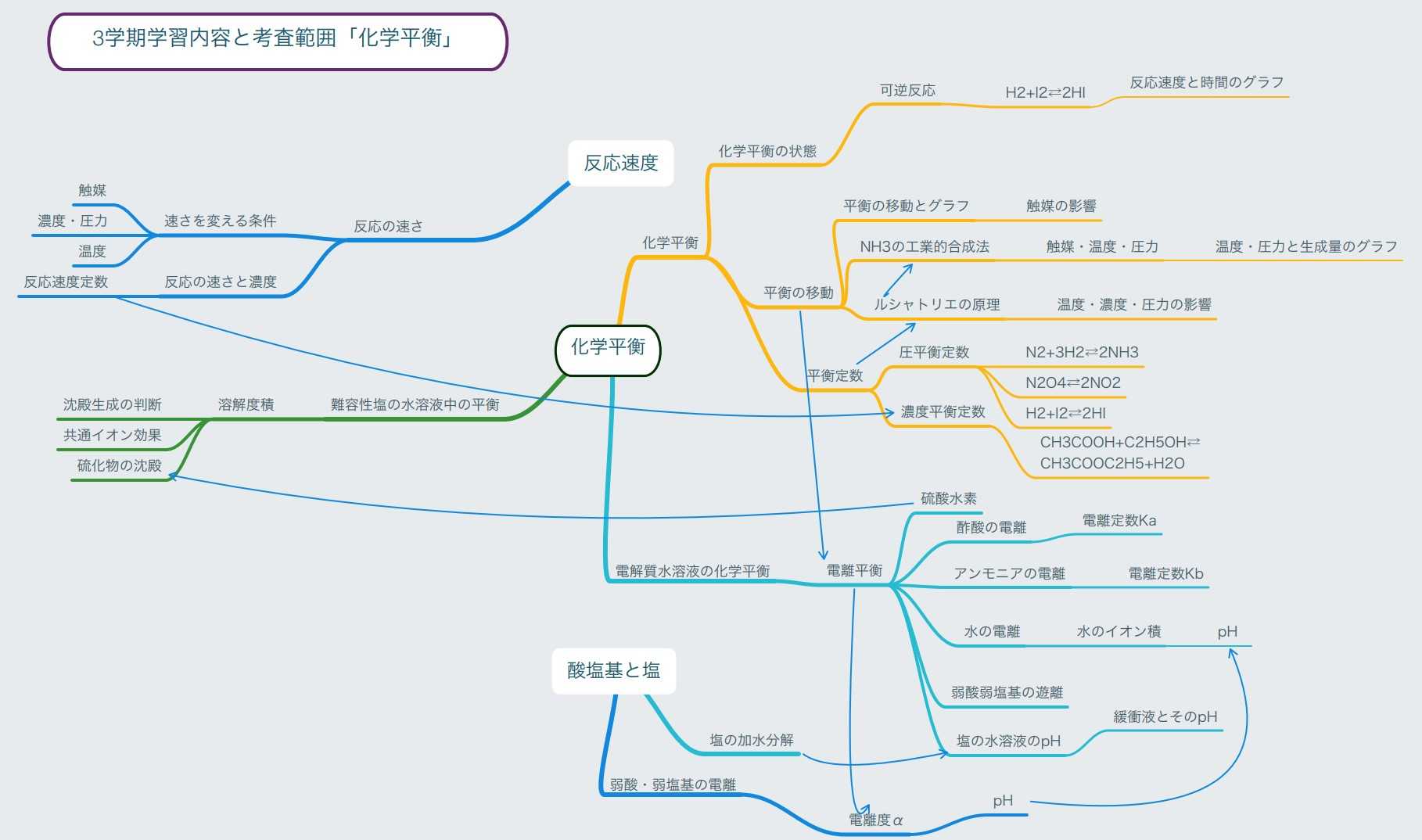
3学期学習内容-マインドマップ風
昨日、共通テストがありました。あいかわらずグラフが問題に取り入れられています。授業ではかなり意識してグラフを扱っていこうと思っています。物質の変化の実態ー分子原子の動きのイメージーグラフ3つを一体的にとらえる力を経験(授業)を通じて養ってほしい。
2022.01.17
コメント(0)
-
リットルℓとL:なぜ”L”表記になったのか
なんか、知らんうちに体積リットルの単位表記がℓからLへなってまして、なんとなく”L”を使ってました。プリント作るのに「リットル」を変換して「ℓ」とするより「L」としたほうが便利だったりしましたから。日本では2010年まで、初等教育では「ℓ」「mℓ」でしたが、2011年には国際的表記である「L」「mL」表記に変更になりました。世界史では1793年:フランスの法案で公定単位としてリットルが定められる「1リットルを(0.1m)^3 =1dm^3とする」1879年:リットルを「l」で表す…1と混同してしまう問題1964年:国際度量衡総会で「標準大気圧の下にある1kgの純水(最大密度)の体積」が削除され(キログラム原器が本来の定義より重くできてしまったため削除)「1リットルを(0.1m)^3 とする」が確認された1979年:第16回国際度量衡総会で「l」も「L」も特例として認める 注)大文字単位(Nニュートン、Paパスカルなど)は 科学者の名前の頭文字であるがLは対応する科学者はいない リットルという偉人をでっち上げよう(エイプリルフールのネタがはじまり)とまでした現在では誤認を防ぐために大文字「L」が使われることが多くなったので、日本もそれに沿うように導入したのが流れのようです出典・参考:Wikipedia「リットル」より
2022.01.12
コメント(0)
-

コロイド溶液の生徒実験レポート=生徒に求めること
コロイド溶液の生徒実験→2021/11/11ブログ以下は、レポートの期待値で、私が書きました。コロイド溶液の生徒実験レポートが提出されました。授業で返却し、次の点について指導しました。①実験前の準備 1時間の実験には1時間の準備と1時間以上のレポート作成。生徒は合わせて3時間以上の時間がかかることを覚悟してほしい。何もわからぬまま実験室にやってきて。いわれた通り(書かれた通り)溶液を混ぜ混ぜして、「あら赤くなった、青くなった!」と騒いで終わりにするのは、小学校の実験ごっこです。◎実験前に操作をイメージトレーニングして、操作ごとにどんな変化が起こるか予想してほしい。 予想することで何を観察し、どう表現するか明らかになります。これは、実験まえに生徒にくれぐれも準備するように伝えたことです。しかし、、、<生徒の結果の記録>ここでは、チンダル現象に注目してほしいのに、「通ったか・通らないか」の視点でみている<生徒の結果の記録>3.(4)では、「色が薄くなること」ではなく、「沈殿が生じないこと」が重要な視点です。実際に研究し、結果を出すには、すぐれた仮説→それを証明する的確な実験計画が大切です。結果について予断をもって実験せよというわけではないが、「こうなるはず」という仮説をもつことは大切です。仮説と違う結果がでたら、それこそ、新たな発見への糸口になり、そこから研究が始まる。これが、生徒実験の意義だと思います。②色の表現 <生徒の結果の記録>アクエリアス色、グレープフルーツ色、オレンジ色、レモン色などは”文学”における色の表現で、科学的ではありません。常に、訂正が必要です。③丁寧な記述 レポートをつくり、他人に読んでもらうには丁寧な記述とまともな日本語がどうしても必要で、当たり前です。論理がわからない、いやそれ以前に文字が読めないレポートも少なからずあり、それは評価できません。いやはや、なかなか実験できない=なかなかレポート指導ができないので恥ずかしい内容になりました。たくさん訓練したいのですが、、、
2021.11.18
コメント(0)
-

ディーゼルエンジンンと尿素水
韓国では「尿素水(水溶液)」不足のため、ディーゼルエンジントラックの運行ができず、物流に支障をきたしているというニュースがありました。韓国ではこれまで安価な「尿素水」のほとんどを中国から輸入しており、これが滞ったためにあらゆるディーゼルエンジン車の走行ができなくなっています。現在、韓国には輸入尿素に駆逐され、尿素の製造工場はない模様です。<尿素合成過程>合成法は、アンモニアと二酸化炭素を原料とし、120℃、150気圧前後に加熱加圧して化合させ、製造するのが一般的です。2NH3 + CO2 → (NH2)2CO + H2O尿素はディーゼルエンジン車の排出ガス中に含まれる窒素酸化物(NOx)を低減する為に用いられます。これを使用しないと、排気ガス中の窒素酸化物(NOx)濃度が増加し、大気汚染の原因となります。日本では三井ケミカルがAdBlueという名称で合成、販売しています。「尿素水」はタンクにためられてエンジン排気ガスに添加、アンモニアによりNOxを窒素に還元します。貼り付け元 <https://jp.mitsuichemicals.com/jp/service/basic_materials/industrial/adblue/index.htm>尿素自体は合成が簡単で昔からたくさん作られてきましたが、安価な中国製品にたよってしまうと、国内産業の縮小をまねきます。日本では、工場が生産を続けていること、ディーゼル車が少ないことで、韓国のようなトラブルは起きていないようです。(「経済安全保障」なんていう言葉もでてきましたね)尿素自体はこの他に、肥料・保湿用クリーム・接着剤原料・メラミン原料等として使用されています。
2021.11.14
コメント(0)
-
息子が「理学部化学」に進学したいがアドバイス欲しい…
かつて化学を教え、卒業していった学生も歳をかさねて、その子供たちが高校生となり受験の季節がやってきました。その方から、メールをいただきました。「(略)…今度、3男が受験生となり、まさかの化学希望と言い出しており、相談にのっていただければと思います。応用化学とかではなく、化学がやりたいとのことです。…(略)」ということでお返事しましたが、この機会に私の大学・受験感を記しておこうと思います。私は、大学からの学問について次のように考えています。①たのしいか?私は自然科学を勉強していて今でも楽しいです。自然科学にはたくさんの分野があります。私の場合はもちろん化学です。研究者としてとりたてて大きな成果をあげられませんでしたが、それでも楽しい。高校時代は生物学が好きでした(今もですが)ので生物部に入って「研究もどき」のことをしていました。大学は理学部化学科にたまたま(ほんとにたまたまです)入り、「化学も面白いなぁ」と思うようになりました。「面白いから勉強する」そういうものに出会えたのは幸せです。大学で勉強するのにはお金がかかります。「面白い勉強」をお金を出して買っている。映画を見たり、フェスに金を払って出かけるようなものです。勉強のコスパを上げるのは「面白さ」です。ただし、自然科学は何をやっても面白い、私の人生ではたまたまの化学です。当初の「生物学が面白い」から化学に面白さを見いだせたのは私の性格(こだわらない才能(笑))のせいかも知れません。でも、研究手法は根元のところで同じですから、何をやっても面白いと思えるのでしょう。②苦しいか?それも素養化学にはさらに広い分野がありますが、どの分野であろうとも、国語、数学、英語…おおよそ高校までで学習するすべてのものは、化学の研究の下支えになります。私は、高校時代まで理科以外の科目を勉強するのがつらかった。勉強していて苦しかったです。怠けたものです。しかし、今はそれらの科目から逃げたこと(特に数学)を後悔しています。しっかり、センスを磨いておけばよかったと思います。「化学」の勉強や研究をしていても、大きな壁にぶつかることはしょっちゅうです。苦しいです。そこを乗り越えるかどうかで、さらなる楽しさに出会える。学問をすることは「楽しいですが、同時に苦しいです」でも、全体には楽しいです。あなたが、「化学の勉強をしたい」と思ったことは、とてもうれしいですが、面白いと思える自然科学なら何でもいいのです。楽しいと思える学問に進んでください。あとは、英数国などの勉強は面倒だがとても大切です。③息子の受験と大学生活息子は理学部化学を受験しました。関東圏で受験先を選びました。国立大学は千葉大、埼玉大。私立は立教、学習院を受験しました。私立大学で理学部があるところはとても少ないので選びようがありません。センター試験を受け、比較的高得点だったので、国立二次は千葉大で、かなり厳しい挑戦です。私立大学で立教(3パターン、3回受験)・学習院を押さえておいて最終的に千葉大に入りました。学部と博士課程前期課程を修了しました。そこで出会った友人にたいしては「すげー!頭良すぎる」と尊敬してました。大学の先生より友人に育ててもらったと思っています4年・博士課程前期課程では研究室で社畜のような生活を送りました。目立つような研究成果は上げられなかったようですが、研究する根性は養われたようです。しかし、研究に対する考え方や研究そのものの戦略は指導されてないのではないかと思われます。「どのように仮説を立てて、それを証明する実験を計画する」ことは、あまりに忙しい研究生活の中では指導しにくいので、多くの研究室では研究者として独り立ちするような指導は行われないのかなぁと思います。作業し、先生と研究の中身を議論する中で、身に着けるような徒弟制度みたいなものが、いまだにあるんですね(私もそうでした)。④結論1)理学部化学を設置している大学は少ないので、簡単に受験校を決めることができます。 どこを受験するかは、テクニカルな問題で学校の担任、予備校、もしデータを見るといいでしょう。2)企業とのリレーションはあんまり考えなくてもいいかと思う。未来の見通しのきかない世相ですし、大学入試も就職もご縁です。3)やはり、大学は偏差値が高いほうがいい。これは、学友との議論や会話からもっとも学ぶことがおおい。教授には優秀な人はいるが、教育力という点で期待できないこともある。4)大学で「研究手法」を教えてくれるところがあれば、最高です。 そこは調査してほしい。私は調べようがないので大学説明会などで個別に聞いてみるといい5)面白いと思える(直感でいいかな)ところはどんなにマイナーな研究室でもいいと思う。学習・研究の原動力となる。せっかくお金かけて大学行くなら、先のことを考えずに楽しむ=情熱持って勉強する大学を選ぶべきかと思います。受験生の皆さん、親御さんがんばってくださいね。
2021.11.06
コメント(3)
-

2年生2学期期末試験までの授業…マインドマップ風
中間試験が終わり、2学期後半の授業です。テーマは「反応熱」と「反応速度」。コロナも一段落し、これまでできなかった生徒実験がたくさんできそう。楽しみですが、他の学年も怒涛の実験が入り実験室がいっぱいです。
2021.10.23
コメント(0)
-

「化学反応と熱」導入のための演示実験
「化学反応と熱」の初めに演示実験を見せています。これまで、溶解や化学反応式の量論が中心でしたが、変化には熱の出入りがあることを知ってもらうことが目的です。上記のプリントに記入しながら進めます。発泡ポリスチレンカップとなっていますが、中が見えるようにビーカーを使っています。発熱量の計算もあわせて練習してもらいます。ここで使われているスターラーは電池式で小型スターラー回転数可変型を作る→2017/10/17ブログで作成したものです。最初に入れた電池はまだ使えてます。
2021.10.20
コメント(0)
-

溶解熱の演示…チオ硫酸ナトリウムの過飽和溶液
詳しくは、こちらをクリックして、解説に飛んでください反応熱の演示実験:チオ硫酸ナトリウムの溶解熱→2019/1/29ブログ
2021.10.13
コメント(0)
-

気体の溶解度…生徒は生活に知識をどこまで投影できるか?
化学の授業では、化学で学習した知識を日常生活のモノ・コトに関連付けて話をします。先日「気体の溶解度」の導入で炭酸水を教室に持ち込んで授業しました。次のように演示し、生徒の意見を聞きました。①未開封のペットボトルを見せて「炭酸水ペットボトルのすきまに何の気体が入っていますか?」 生徒→二酸化炭素半数、空気半数の人数が手をあげましたさすがに、たじろぎましたが、知らん顔して次の質問②ペットボトルの蓋を取ります。「プシュッ」といって気体が抜け、炭酸水から泡が出ました。 「プシュッ」と音がしたのはなぜ?生徒→「気体が逃げた」私→「そうだね。この気体は二酸化炭素なんだ」「ところでこの気体はもともと何気圧で入っていたと思う?」生徒→「1気圧くらい…?」私→「ぐぬぬー…」「みんなはどう思う?1気圧?1気圧以上?」 生徒→1気圧の生徒は2割くらい。1気圧以上は8割。ちなみに、JAS規格によるとペットボトル内の炭酸圧力は4気圧までだそうです。珍解答として:「ふたを取ると、炭酸水中の二酸化炭素が泡となって出て、ペットボトル内の気体の量が増え、圧力が高くなる」ちょっと、順番が違うよなぁこのあと、炭酸水のペットボトルの発問の答えを言って、気体の溶解度と圧力の授業を進めるのです。生徒たちは、問題もよく解けますし、教科書の文字内容については正しく答えます。しかし、化学は日常生活と関係が深いから身近な現象を分析し説明できるようになってほしい生徒たちはコーラなど炭酸水をよく飲みます。しかし、そこで起きている現象には全く無関心、注意をはらいません。わかる気がしますが、日常生活や世界に学んだことを投影してほしいものです。気体の溶解度と温度の関係についても、生徒に見せます。生徒が「これほど現象に目を向けないのかぁ」とよくわかったからです。お湯はステンレス保温ボトルに入れて教室に持っていきます。上の写真は、室温27℃と湯温80℃につけた結果です。(少し時間が経ったので、湯のほうの泡の出方が最初ほど強くない)泡は、高温のほうがたくさん出ます。香港では、「熱可楽」と呼ばれるコーラを温めて風邪の時に飲むという習慣があるそうです。中には、レモンやショウガを入れるそうです。なんだか効きそう。「この飲み物、シュワシュワと泡が出てるかな?」などと聞いたりします。身近なものを徹底して見せたい。ただし、問題意識を持って見せないと、生徒には印象に残らないだろうなぁ。
2021.09.21
コメント(0)
-
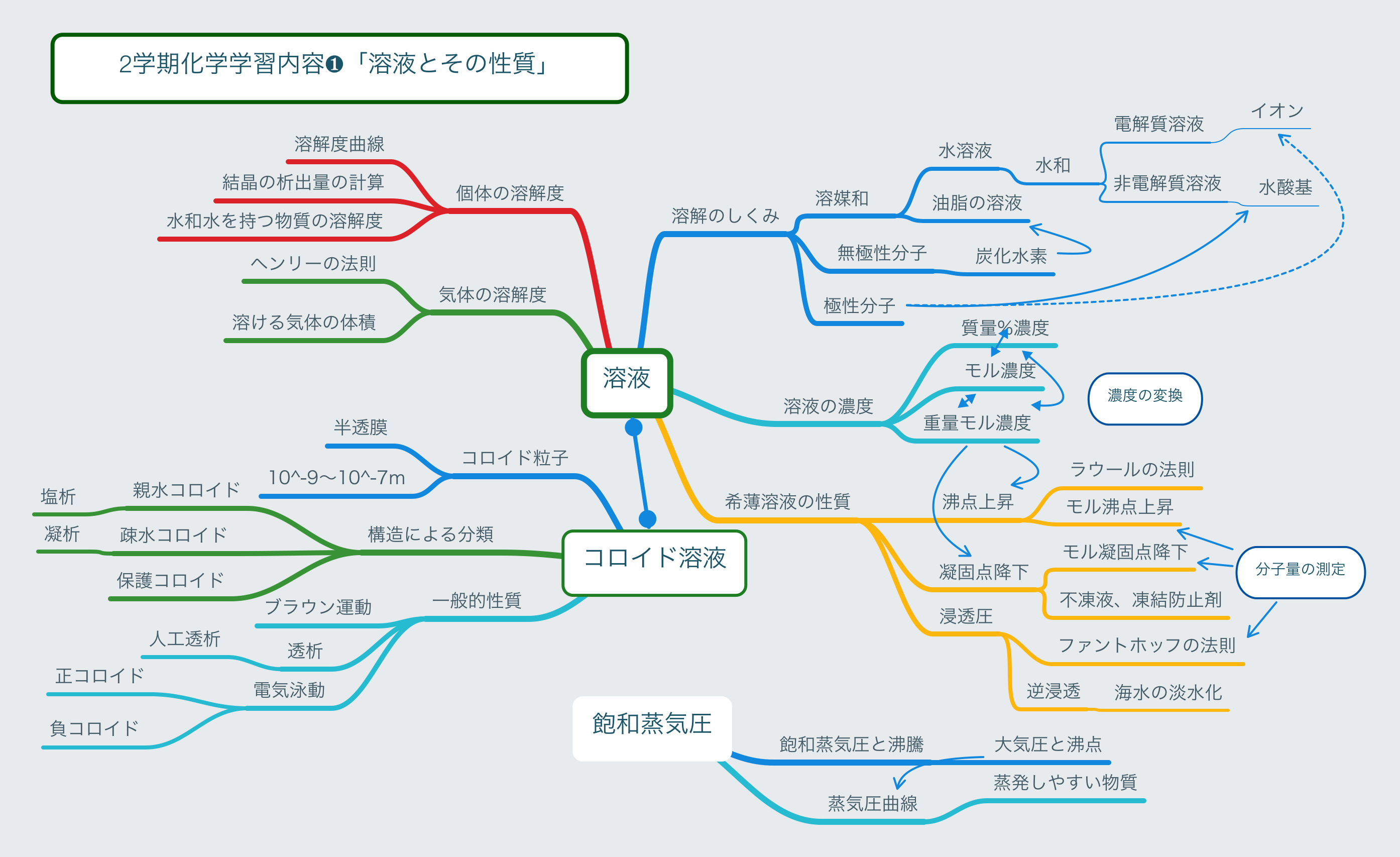
2学期授業計画❶「溶液とその性質」MM風
コロナ下、2学期当初の授業形態は今週中に決まるようです。WEB授業にするか、クラスの半数ずつの登校・授業にするか今日のところはわかりません。ともあれ、2学期当初は「溶液とその性質」から始めます。いずれの授業形態になっても、生徒実験はむずかしいと思っています。これまでは、演示実験に加えて、「凝固点降下」「コロイド溶液」の生徒実験を行っていました。対面授業なら演示実験で実物を見せられるでしょうが、WEB授業なら動画で見せることになります。どちらにしても、とても残念ですが、しばしガマンですね。ご健康で。8/27追記9月から、授業時間5分短縮+クラス半数登校(残りは家庭でwebで授業視聴)となりました。生徒実験はきびしいかな?
2021.08.26
コメント(0)
-

銅の精錬と利用③現代の銅精錬
足尾銅山に行ってきました→2021/7/11ブログ銅の精錬と利用 ①古代; 自然銅→2021/7/13ブログ銅の精錬と利用 ②江戸時代の銅精錬→2021/7/19ブログ銅精錬の歴史を調べています。これまで、①古代の銅精錬②江戸時代の銅精錬でした。今回は現代の銅精錬です。PAN PACIFIC COPPER 銅ができるまで上の資料を参考にしました。[1]銅鉱石の輸入原料となる鉱石はほとんど海外からの輸入。2015年度の銅精鉱の輸入は492万トン(銅分約30%)です。チリ(全体の44%)、ペルー(12%)、インドネシア(12%)、カナダ(12%)オ-ストラリア(10%)、などから輸入されています。これを設定された品位に調合「銅精鉱」され、自溶炉に送られます。この鉱石は日本国内で精錬され、国内消費は95万トン。59万トンが輸出されています(2015年)。[2]自溶炉銅精鉱は珪砂SiO2、常温高酸素空気とともに自溶炉に吹き込まれます。CuFeS2 + SiO2 + O2 → Cu2S・FeS + 2FeO・SiO2 + SO2+反応熱この反応は発熱反応で、炉内で瞬時に酸化反応し、鉱石自身の酸化熱により反応が進みます。Cu2S・FeSは溶融した鉱石に浮かんで銅品位65%の「マット」とFeO・SiO2などからなる「スラグ」になり、下に沈みます。溶融した「マット」を炉内上層から取り出して転炉に送ります。[3]転炉転炉では炉内に酸素を付加した空気を吹き込み、さらにマットを酸化させます。Cu2S・FeS + SiO2 + O2 → Cu + 2FeO・SiO2 + SO2+反応熱転炉では銅品位約99%の粗銅を作ります。粗銅は精製炉に送り、さらに純度を高めます。自溶炉・転炉で発生したSO2は硫酸工場に送られ、硫酸をつくります。[4]精製炉粗銅には酸素が含まれているので、ブタンガスを吹き込んで除去します。これにより純度が99.5%まで上がります。[5]アノード鋳造精製粗銅は鋳型で電解精錬用の陽極版(アノード)に鋳造されます。アノードの大きさは約1m×1m×0.05m、重量は約380kgです。上の写真は足尾銅山の展示室で撮りました。[6]電解精錬硫酸銅(Ⅱ)水溶液を入れた電気分解槽槽に粗銅アノード(陽極)とステンレスのカソード(陰極)を交互に漬けます。約10日間通電して、最終製品の純銅(99.99%)をステンレス板からはぎとります。この純銅は重さ80kgあります。電解精錬で沈殿した陽極泥から、金・銀・テルルを取り出しています。かつては、カソードに純銅を使っていましたが、今はステンレス板を使っています。以上です。
2021.07.22
コメント(0)
-
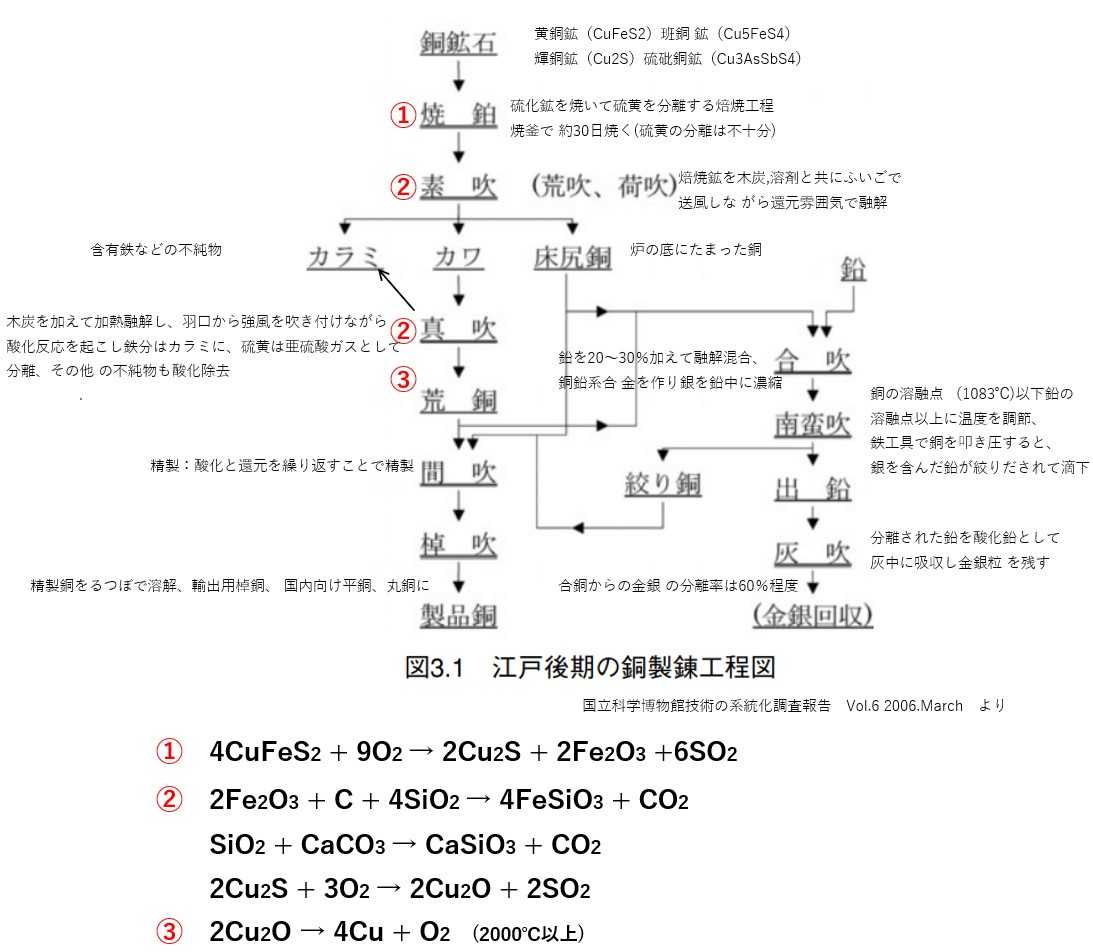
銅の精錬と利用 ②江戸時代の銅精錬
足尾銅山に行ってきました→2021/7/11足尾銅山で銅鉱石の採掘と精錬について興味を書きたてられたので銅精錬の歴史を調べています。前回は古代の銅精錬でした。銅の精錬と利用 ①古代; 自然銅→2021/7/13今回は江戸時代の銅精錬です。1697年(元禄10年)の銅の生産高は世界一の約6000トンで、長崎貿易の輸出量はその半分にも達する状況でした。このころはまだ新大陸の鉱山が発見されておらず、生産量は世界一でした。「国立科学博物館技術の系統化調査報告 Vol.6 2006.March」を中心に述べていきますが、その文献には化学反応式が記載されていないので、反応式については20世紀の銅精錬(Wikipedia)から推理しました。当時の精錬はこの段階を追わず、②~③の繰り返しを「真吹」「間吹」で行ったと私は推理しています。先日見た「孫氏兵法」という中国のTVドラマで、呉国の青銅剣製造の際、強い剣を作るために水晶を加えると強い剣ができる場面があり、銅の純化にSiO2を加える意味をうかがわせています。足尾銅山の資料館には、精錬銅を使った天保通貨の展示がありました。
2021.07.19
コメント(0)
-
銅の精錬と利用 ①古代; 自然銅
足尾銅山を見学してきて、銅利用の歴史に興味を持ちました。銅は人間が初めて扱った金属です。足尾銅山に行ってきました→2021/7/11ブログ今回は自然銅の利用と精錬銅です。「銅製錬技術の系統化調査」 酒匂 幸男 国立科学博物館 技術の系統化調査報告 第6集 より以降の記述はこの「銅製錬技術の系統化調査」を参考にしています。古代文明は石器時代→銅器時代→青銅器時代へと変遷しています。初めての銅は銅石器自然。自然銅を叩いたり伸ばしたりして利用していました。貼り付け元 <http://copper-brass.gr.jp/copper-and-brass/copper/history> 精錬銅は酸化銅鉱を700~800℃で加熱してスポンジ状と したものから銅を得ていました。赤銅鉱Cu2Oでは 2Cu2O + C → 4Cu + CO2 木材を燃料に生活していた時の炉壁などから銅が遊離することで銅が鉱石から得られることを知ったと考えられています。その後、エジプトでは前5,000年頃の墓から副葬品として銅製の武器や用具が出土されています。前3,800年頃、シナイ半島においてはスネフル王によって銅鉱石が採掘されたという記録や、当時のるつぼも発見されており、 鉱石からの銅精錬技術があったことを示しています。前2,750年頃のエジプトのアプシル神殿には、銅で作った給水管が使用された事実があり、これは銅を薄い板にたたき出して、管にまるめて用いたものです。銅の歴史 日本伸銅協会←参考にしました日本の銅製錬の始まり 原料は自然銅や酸化銅で平安時代には精錬の難しい硫化銅へと変化しました。しかし、平安末期になると国内産が不足し宋銭を輸入して利用するようになりました。おもに、貨幣として利用されています。富本銭(貨幣):飛鳥池遺跡から出土。鋳造年代が700年以前和同開珎(貨幣):708年奈良大仏(総重量380t):奈良時代、500tの胴が使用皇朝十二銭(貨幣):平安時代鎌倉大仏:1252年~ 中国銭が大量に使われる室町時代の終わりには天下は乱れ群雄割拠した武将は軍資金として の金、銀、銅の需要が増大し鉱山開発が盛んになったようです。次回は江戸時代・中世における鉱石(主原料は黄銅鉱)の精錬です。
2021.07.13
コメント(0)
-
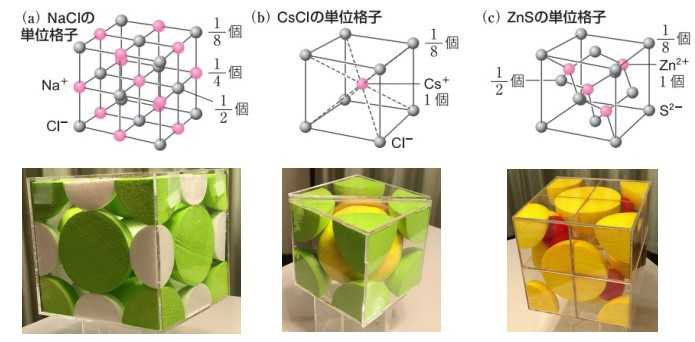
問題意識を持たせず模型を回覧しても意味がなかった
2年生化学の授業は結晶構造「イオン結晶」に入っています。毎年のように、3種類の結晶模型を回覧して見てもらっています。「単位格子内の陽イオンと陰イオンの数、配位数を確認してごらん」と問題提起して回覧します。しかし、生徒は「ふーん」「きれい」などと楽しそうに見て回覧しますが、教科書などの図(写真上)と比較して、どのイオンが模型のどの玉に対応するかを確認することはしません(なんと残念)。2次元の表現と3次元の表現を一致させたいがためにこの作業を行いますが、それがどこまで伝わっているのか…そこで、第一学習社セミナー化学問題集を解かしてみました。これで、やっと生徒は問題意識をもって模型を観察することを始めました。(3)は模型を見ると陽イオンと陰イオンの接触の様子が簡単にわかります。 生徒は「きれい」だけではない模型の意義を認めます。 「√3=1.73」の意味も伝わります。(3)CsClでは写真「1」に相当する長さが0.412nmですから (Cl-の半径:0.167nm)x2+(Cs+の半径) x2 =0.412x√3 nm NaClでは一辺上にNa+とCl-が接触して並んでいるので (Cl-の半径:0.167nm)x2+(Na+の半径) x2 =0.0.564 nmこうして、毎年ボンヤリと模型を眺める生徒に模型を確認する意義を伝えています
2021.06.01
コメント(0)
-

ダニエル電池の電極間距離を離すとモーターは遅くなる=電圧降下
先日の講義実験でダニエル電池を実験しているとき素焼き容器中の銅板をそのまま動かさず、ビーカー中の亜鉛板を遠ざけるとモーターの回転が遅くなり、亜鉛板を素焼き容器に近づけるとモーターの回転が速くなりました。モーターを外して、起電力をテスターではかると亜鉛板を動かしても起電力は変わりません。しかし、モーターをつなぐと起電力に変化が出ます。どうしたことでしょう!?<電流が大きくなると電池は電圧が低下する>起電力(理論上の電圧) 2V のある電池に、5.0Ω の抵抗器をつなげると 0.2A の電流しか流れなかったりします。オームの法則 V = RI から考えると (2V ÷ 5Ω =) 0.4A の電流が流れるはず。0.2A しか流れてないのでこの電池の実質的な電圧は (0.2A × 5Ω =) 1V になっています。<原因は電池の内部抵抗>この電池の性能低下は、電池の内部に抵抗がある、とみなすと説明ができます。この抵抗を内部抵抗といいます。<ダニエル電池で極板を離すと内部抵抗は大きくなる>電池の極板は電解質溶液で隔てられています。電解質溶液の抵抗値は極板間の距離が離れると大きくなります。V(測定電圧地)=E(起電力)-r(内部抵抗)xI(電流) を考えると極板間の距離が離れるとr(内部抵抗)が増える。したがって、電圧降下rIの値が増えます。こんなことからどんな電池でも、正極・負極の電極間距離を短くする工夫がなされています。
2021.04.26
コメント(0)
-
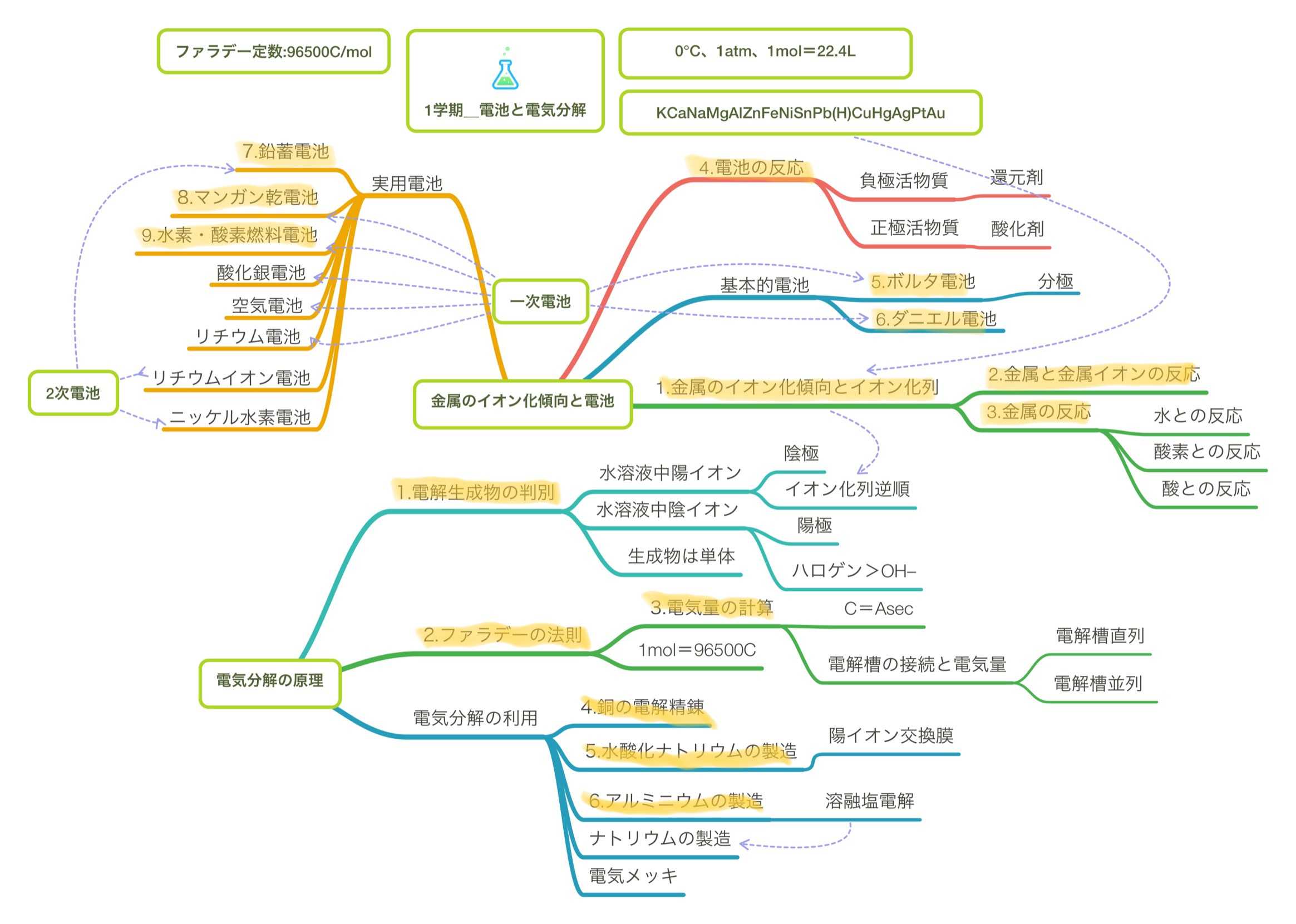
2年理系一学期授業内容ーマインドマップ風
そろそろ新学期が始まります。1学期の授業内容を考えましたので、マインドマップ風にまとめました。暫定的な予定です。最初の授業で、「学習の進め方」とともに生徒に配布しようと思います。
2021.04.03
コメント(0)
-

エネルギー源としてのアンモニア④アンモニア低エネルギー合成
Ru[C12A7:e-エレクトライド]エネルギーキャリアとしてのアンモニアが保存運搬にすぐれていても、水素H2と窒素N2からアンモニアNH3を合成するのに高温高圧が必要です。そのために、エネルギーを使ってしまっては無意味です。低温低圧下で働くハーバーボッシュ法の新しい触媒の開発が行われています。東工大と東大が多く新触媒を発表しています。ざっと検索した表を下に示します。上は、Ru[C12A7:e-エレクトライド]触媒の図です。さらに、窒素と水から常温常圧でアンモニアを合成することも試みられています。具体化しているのは、上表2列目の味の素・三菱が出資した実験プラントです。これまでの、鉄系触媒に比べて低温低圧で合成でき、ゼオライト膜により効率よく取り出すことができます。水素H2は化学工業の様々なところで副生成物として得られ、炭化水素の改質や水の電気分解によっても得ることができます。水素の合成も重要な要素なので下の図にまとめておきます。エネルギー源としてのアンモニアの話はこれで終わりです。下に、これまでの話のリンクを貼っておきます。関連した記事エネルギー源としてのアンモニア①人類を再び救うか →2021/2/28ブログエネルギー源としてのアンモニア②アンモニア発電→2021/3/1ブログエネルギー源としてのアンモニア③アンモニアの貯蔵と輸送→2021/3/2ブログ
2021.03.04
コメント(0)
-

エネルギー源としてのアンモニア③アンモニアの貯蔵と輸送
(1)電力の貯蔵技術発電所で作られた電力は作りっぱなしで、電力網で各地へ調節(大電力が必要な地域には多く)されて送られています。ついでのはなしですが、各家庭には40Aとか60Aのブレーカーがありますが、これは電力会社と契約すると「この電流まで発電し、保証しますよ」という契約を結んでいるのです。いくら家庭で節電しても、電力会社は契約分発電しているので、社会全体のエネルギー消費量はかわりません。そうはいっても、発電しても社会で使われなかった電力を貯める方法があれば無駄になりません。NIES環境展望台:電力貯蔵技術 一度発電した電力をムダにせず、必要なときに効率的に利用できるように、充電・放電を繰り返す工夫が電力貯蔵技術です。 上の図は夜間に電力消費が少ないとき、電力を貯めておいて、昼間の需要が多いときに送り出そうという考えです。 現在、実際に使われているのは「揚水発電※」ですが、その他にも研究が進んでいます。主な用途の「負荷平準化」が上のグラフの「エネルギーの貯蔵」「放出」にあたります。※揚水発電揚水発電の仕組(2)アンモニアの貯蔵と輸送 CO2フリー(二酸化炭素を排出しない)水素の生産は可能になりつつあります。しかし、 水素H2の沸点はー253℃で貯蔵や輸送に困難、さらに金蔵容器では水素脆化(水素により金属がもろくなる)が起こります。一方、 アンモニアNH3は、常圧(1atm)でー33℃、20℃では8.5atmで液化します。すでに、アンモニアは世界中で2億トンも作られていて、貯蔵と輸送技術は蓄積があります。そこで、エネルギーの貯蔵・輸送にアンモニアを使うことが研究されています。(水素やその他のエネルギーキャリアとあわせて研究されている) さて、後はエネルギーをできるだけ使わずにアンモニアを合成するかが問題です。ハーバーボッシュ法では500℃、200atm(Fe系触媒)です。これでは、原料の水素H2が得られても合成だけでエネルギーを使ってしまいます。このアンモニアの合成法については次回の記事で紹介します。関連した記事エネルギー源としてのアンモニア①人類を再び救うか →2021/2/28ブログエネルギー源としてのアンモニア②アンモニア発電→2021/3/1ブログ
2021.03.02
コメント(0)
-

エネルギー源としてのアンモニア②アンモニア発電
アンモニアは燃えます。NH3+3/4O2=1/2N2+3/2H2O+380kJこの時発生する熱エネルギーを発電に利用(火力発電)したり、燃料電池として電力を取り出したりすることができます。今日のテーマは経産省資源エネルギー庁の資料を中心に「アンモニア発電」を見ていきます。(1)CO2削減のために火力発電への混焼 石炭火力発電のボイラーへアンモニアを混ぜて燃焼します。メリットは①アンモニアの製造・輸送・貯蔵に既存のインフラを使って整備できる②石炭との混焼ボイラーはバーナーなどを変えるだけで対応できる③CO2排出削減量 石炭火力発電所を20%アンモニア混焼にすると1基で約100万トン、国内の大手電力会社の保有するすべての石炭火力発電所では約4000万トンになると試算されています。 2021年度から、愛知県碧南火力発電所(100万kW)で、20%混焼の実証試験を実施する予定※混焼により、窒素酸化物NOxが発生する恐れがありますが、アンモニアを20%混焼しても、石炭だけの時と同じ程度で環境基準を満たすそうです。(2)ガスタービン発電 ガスタービンとは液化天然ガス(LNG)などの燃料を燃やした際に発生する高温・高圧ガスでタービンを回し、電気をつくります。(下図:川崎重工HPより)①LNGとの混焼LNGなどの燃料とアンモニアを混焼して使う方法も考えられており、現在は50~2,000kW級の中⼩規模ガスタービンで研究開発がなされています。また、燃料アンモニアだけを燃やして発電する専焼技術についても研究開発が始まっています。②灯油との混焼実験(産総研TODAY)https://www.aist.go.jp/Portals/0/resource_images/aist_j/aistinfo/aist_today/vol15_02/vol15_02_p12.pdf③アンモニアだけを直接燃焼させる 数10万kW級の大型ガスタービンでは、液体アンモニアをガスタービンの排熱で水素と窒素に分解し、ガスタービンで燃焼して発電するという研究開発も進んでいます。もし大型ガスタービンでのアンモニア燃焼の研究が進み、55万kW級のガスタービンでアンモニアを燃料として発電することに成功すれば、一基につき年間で110万トンのCO2排出削減効果があるとされています。(3)アンモニア燃料電池 IHIより負極:2NH3→N2+6H++6e-正極:3O2+12e- → 6O2-燃料電池では燃料としてH2を用います。メタンCH4などの家庭用燃料電池では、改質して水素を取り出して利用しますが、この電池はアンモニアを直接利用します。2018年3月に,1kW級の発電に成功したそうです。https://www.ihi.co.jp/ihi/all_news/2018/technology/1190443_1624.htmlエネルギー源としてのアンモニア①の続編です。リンクは以下エネルギー源としてのアンモニア①人類を再び救うか →2021/2/28ブログ
2021.03.01
コメント(0)
-

エネルギー源としてのアンモニア①人類を再び救うか
「化学平衡」の授業で大きく取り上げる「ハーバー・ボッシュ法」1906年鉄を主体とした触媒上で水素と窒素を 400–600 °C、200–1000 atmの超臨界流体状態で直接反応させる。N2+3H3⇄2NH3この方法で2019年に全世界で約2億トン作られているそうです。多くは肥料に使われて、農地の単位面積当たりの生産量を高めています。下のグラフは「ハーバー・ボッシュ法」以降の世界人口の伸びです。穀物・食肉生産の飛躍的な伸びはアンモニア生産量に支えられ、人口の増加も急激な伸びを示しています。アンモニア合成は多くの人類を飢餓から救いました。「脱CO2」が騒がれるようになって久しいです。私は「地球温暖化はCO2濃度の増加が原因である」という説には組しないのですが、化石燃料を無節操に使い続けることには、資源維持の面から反対です。できれば、再生可能エネルギーや原子力エネルギーをつかって水素H2を作って利用することに期待しています。さて、テーマです。エネルギーキャリア(H2エネルギーを運ぶもの)としてのアンモニアに注目していきます。3点について(1)エネルギーとしてのアンモニアNH3: アンモニアは燃えます。 NH3+3/4O2=1/2N2+3/2H2O+380kJ (ちなみに、CH4+2O2=CO2+2H2O+888kJ) 酸素と混合して火を付ければ炎を上げて燃えます。 アンモニアを燃やしても二酸化炭素CO2はでません。 既存の施設では「石炭火力発電所」で石炭と混焼して利用することが試みられています。 詳しくは、別立てでアンモニアを使ってエネルギーを得るお話をしたいと思います。(2)保管と輸送: 水素H2の沸点は-259℃です。 液化して運ぶためには極低温まで冷やし、高圧にしなければなりません。 さらに、金属容器だと水素脆性で、壊れやすくなります。 ガラス強化プラスチックタンクに‐253℃で水素を詰めて輸送する川崎重工のプロジェクトがある。 それにしても、水素を保管し、運搬するだけでエネルギーが必要となる。 一方、アンモニアは沸点―33℃。 常温でも圧力をかけると容易に液化する。 かつては、冷蔵庫の冷媒に使われていたので、取扱には経験の蓄積があります。 保管や輸送するにも、水素より圧倒的に簡単です。 エネルギーキャリアとして注目されているのはこのためです。(3)アンモニア合成: 「ハーバー・ボッシュ法」は高圧高温が必要で、アンモニア合成に使うエネルギーは莫大です。 より低圧・低温でアンモニア合成を行えるよう研究が進んでいます。 以上、(1)~(3)について、今後のブログで詳しく見ていこうと思います。 以上の話はここでご覧ください。SIP エネルギーキャリア アンモニア合成システム開発
2021.02.28
コメント(0)
-

酢酸の[H+]=√(cKa)どの濃度まで通用するか
酢酸の電離平衡を授業でやっていて生徒の質問にあったのが、「近似値[H+]=√(cKa)はどの濃度で使えるか?」・濃度cが高いこと・電離定数Kaが小さいこと(酢酸くらい)と答えましたが、実際にはどうだろう?計算し、比較しました。酢酸水溶液の[H+]を√(cKa)で表すことができるよ、とふれました。ここでは、平衡時の酢酸濃度をc(1-α)として、さらに1-α≒1と近似します。近似なしで、ちゃんと計算してみます。このようにやはり少し違いが出ます。特に酢酸濃度が小さくなると、違いが大きくなります。比較した表を下にのせます。酸の電離定数が大きくなる=電離度が大きくなっても違いが大きい。酢酸水溶液では酢酸濃度が0.030mol/L以上で違いが少なくなり、近似値を使った式②[H+]=√(c・Ka)をつかえます。
2021.01.28
コメント(0)
-

時計反応を授業で演示
時計反応を授業で演示。この反応は亜硫酸水素ナトリウムのモル濃度に比例する一次反応v=k[HSO3-]になります。無色の溶液が紫黒色に変化するので生徒の人気が高い。22℃教室で[HSO3-]初期濃度で12.5秒で変色、[HSO3-]濃度を1/2にすると24.5秒で変色しました。お湯58℃につけて[HSO3-]初期濃度で8.5秒でした。濃度と反応速度の関係はよくわかってもらえたと思います。温度は傾向だけとらえてもらいました。いつもは生徒実験で楽しんでもらえるのですが、今年は演示実験だけです。それでも、生徒へのインパクトは大きい。実験方法など関連は以下にリンクを貼ります。生徒実験:化学反応の速さ(生徒実験)→2018/2/9ブログ生徒実験:化学反応の速さ(レポート)→2018/2/11ブログ生徒実験「化学反応の速さ」③生徒のレポート→2019/2/13ブログ時計反応がうまくいかないときの対処法→2020/11/12ブログ
2020.11.18
コメント(0)
-

コロナ下、クラス半分でやっと実験…「コロイド溶液」
実験が制限されています。これまで40人1クラスで実験を行ってきましたが、4人/実験台で対面になるためにできませんでした。そこで、クラスを半分に分け20人(2人/実験台)で実験します。残りの20人は講義室で自習です。6クラス(40人5クラス・20人1クラス)で合計11回の実験になります。実験テーマは「水酸化鉄(Ⅲ)コロイドを作り、性質を調べる」です。[1]水酸化鉄(Ⅲ)コロイド溶液をつくるはじめにFeCl3溶液を沸騰水に加えて色の違いを比較します。FeCl3溶液を加えた試験管に残っているFeCl3溶液に純水を加え、色を比較します。[2]透析セロファンで透析します。5分間、純水中に付けておきますが、待っている間演示用に用意してあるチンダル現象、電気泳動、煙のブラウン運動を観察します。チンダル現象;左はK2Cr2O7aq、右はFe(OH)3コロイドです。電気泳動;140Vの電圧をかけています。1,2分で陰極に動いている様子です。生徒が観察終えたら、逆に電圧をかけて元に戻し、次の実験にそなえます。[3]透析した純水中のイオンの確認Cl-、Fe3+,H+を確認します。左から、硝酸銀aqでCl-イオンの確認、K4[Fe(CN)6]aqで未反応のFe3+の確認メチルオレンジで酸性確認→H+の確認です[4]精製した水酸化鉄(Ⅲ)コロイドの凝析と保護コロイド左からNaClaq、Na2SO4aq、を加えたもの保護コロイドとしてゼラチン溶液を加えたのちNa2SO4aq、を加えたもの[結果・考察]以上です。今年から、学校をかわりました。生徒は、よく勉強する、素直な生徒たちです。私の実験後の感想①セロファンを糸で結べない生徒がいました。生活体験が不足しているなとおもいます。②色を表現できない生徒が多いです。機会を見つけて色のお勉強が必要かな?③沈殿が起こったり、色が変わったりする意味を考えて実験していないようです。 授業ではよくわかっていそうな生徒に、どのイオンがこれらの変化を起こしているか?と試験管を前に質問しても回答できません。 物質を前にして、変化を起こすイオンを考えられない。座学だけではだめだと強く実験の意義をかんじます。関連です。かつて他校で行った「コロイド溶液の性質」の実験です。生徒実験:コロイド溶液の性質(実施)→2018/1/29ブログ生徒実験:コロイド溶液の性質(レポート)→2018/1/30ブログ
2020.10.07
コメント(0)
-

画像を「Googleレンズ」でテキスト化→GoodNotesで活用
今日の話題は「Googleレンズ」です。撮影した文章映像や手書き文字をテキスト化してくれるソフトです。教科書の例題などを解説するために、スマホのカメラを使うスキャナーアプリ※1でとりこみ、画像のままGoodNotesに読み込んで使っていました。教室においてプロジェクターで映すと視認性が今ひとつだったり、数値を変えて演習したりできないので、テキスト化できないかなと思っていました。そこで、「Googleレンズ」です。私は、「Googleフォト」に画像を一元管理しています。そこに、スキャナーアプリで撮った写真、教科書などの文章画像を取り込んでおきます。iPadではGoogleフォト内に「Googleレンズ」の機能が内蔵されています。では、画像を「Googleレンズ」でテキスト化→GoodNotesで活用する方法①Googleフォトを立ち上げるとその下部に「Googleレンズ」のアイコンがあります。上の写真は撮影した例題のjpeg画像です。ペン先のアイコンが「Googleレンズ」です。これをタップします。②必要な部分を指先で反転させたのち(画像では青色の帯)コピーをタップします。同じGoogleアカウントをもつ他のパソコンにコピーしたいときは「パソコンにコピー」をタップすれば、Windowsパソコンにもコピーしたテキストを送ることができ、Wordなどにもペーストすることができます。③GoodNotesを立ち上げて、ペーストします。こんな感じでペーストできました。元の画像と比べてみてください。テキスト化の精度がいいでしょ。ただし、改行が余計に入る、変換ミスが1か所ある、下付き・上付き文字を変換してくれない、など、欠点がありますが、キーボードから入力するより圧倒的に早い。④あとは、改行を削除して形を整えると出来上がりです。上は、テキスト形式でペーストし、整えた結果です。※1 私はiPhoneでReaddle「Scanner Pro」というスキャナーアプリをつかっています。 カメラで撮るようにスキャンします。JpegやPDF形式で書きだすことができます。
2020.10.02
コメント(0)
-

凝固点降下のデータ処理・グラフのレポート
凝固点降下の実験を毎年行っています。今年は残念ながら、実験できません。そこで、凝固点降下のデータ処理・グラフ…実験できないので→2020/8/20ブログデータを与えてグラフを書くレポートを出しました。提出されたレポートから典型的なものを紹介します。①使ったデータ②生徒のグラフ(典型的なもの)凝固点降下のデータ処理・グラフ…実験できないので→2020/8/20ブログで指示した書き方をよく守ってくれて書いてくれいるんだけどナフタレン―シクロヘキサン溶液の外挿線のと書き方が惜しかった。大体190秒以降は温度一定で、ここは「共晶」領域※1になると考えられる。(上の図で楕円の部分)「共晶」については、授業で説明したが、実際のデータにあたってみないと認識するのは難しいのだと思う。したがって、外挿を引くときにこのデータを入れてはならない。※1「共晶」溶液部分の濃度が高まり、飽和溶液になるので、シクロヘキサンとナフタレンが共に結晶化する。このため、濃度は一定。したがって、温度は一定となる。③グラフを書かせて、期待すること(1)縦軸―横軸の単位をしっかり意識してグラフを見ることができるようになること(2)グラフの変化と実際の現象を関連させることができるようになること以上のことを特に期待して、返却・指導していきたいと思います。
2020.09.12
コメント(0)
-

iPadを教室の授業で使う(動画)
iPadを授業で活用しています。プロジェクターで黒板面に投影して、使っています。その方法を紹介します。GoodNotesというアップルペンを使うソフトが講義の中心になります。詳しいまとめはこちらをご覧ください。iPadを教室の授業で使う(まとめ)→2020/8/30ブログ
2020.08.31
コメント(0)
-
iPadを教室の授業で使う(まとめ)
iPadを教室での授業で使い始めて2年以上になります。板書のみの授業に比べて、圧倒的に効果的・能率的になりました。これまで、このブログで紹介してきた内容をまとめてみました。《授業準備と授業プレゼン編》①iPad、ApplePenを使い授業プリントPDFをGoodNoteで表示・書き込む方法新世代iPadとPencil購入、授業テキスト支援システムできました→2018/4/16ブログ②プロジェクターを使いiPadの出力をHDMIケーブルレスで黒板に映す教室にプロジェクターを背負っていってます→18/4/27ブログ③演示実験提示用のパーツ…拡大して実物提示ができますiPadを授業に使う②実物映像提示パーツ→18/5/24ブログ④iPadに授業用プリントを連携、さらに演示実験提示、ビデオ・写真画像も提示1学期のまとめ「教材作成・提示編」→18/7/13⑤Goodnotesのプレゼン機能が強化されました。また、MyScriptCalculater=applePenで書いた数式がフォントになり計算してくれますGoodNotes5がVerUp + MyScriptCalculaterで授業が快適に→19/9/4ブログ⑥Goodnotesは画像をApplePenで自在に切り取ってトリミングできるGoodNotes5を授業に使う:画像トリミングツール→19/11/24ブログ⑦Windowsで作ったファイルをiPadに送る方法、その他公立高校の環境(会計など)でiPadを授業に使う方法→19/2/11ブログ《WEB授業用動画教材作成編》⑧iPadのプレゼンソフトKeyNoteを使い、これをiPad上で再生しながらナレーションを付けます。この時、画面キャプチャして動画をつくります。iPadだけで簡単にWEB授業用教材を作る (1)→20/5/8ブログ⑨学習支援にZoomを使ってみたが、セキュリティが心配だったので止めました学習支援にZoomを検討する①→20/4/10ブログ、「検討する」②、③で検討結果あります
2020.08.30
コメント(0)
-

「蒸気圧降下」の演示…地味な演示ですが
東京書籍「ビジュアルワイド図説化学」より蒸気圧降下はどの資料にもこんな感じの写真が載っています。生徒実験ができないこの時節ですので、教室ではできるだけ、演示実験をしてみてもらっています。今日の演示実験は「蒸気圧降下」です。とても、地味な実験ですが、溶媒をヘキサン、溶質をナフタレンで行うと中央のU字管の圧力差がみるみる変化するのでわかりやすい。実験装置です。U字管には水を入れてあります。赤のゴムの試験管は溶媒(ヘキサン)のみ、黒のゴムの試験管は溶液(ナフタレン-ヘキサン溶液)です。ナフタレンは飽和まで入れてあります(試験管底の白い沈殿)。演示では上のピンチコックを開けてゴム栓をして、U字管の水面を合わせ、ピンチコックを閉じます。教室の温度は30℃弱(エアコンつけて窓は開けています)でした。みるみる溶媒だけの圧があがってきます。経験上ですが、始める前にゴム栓を取って、フッと息を吹きこみ、試験管内のヘキサン蒸気を逃がしたほうがU字管内を水が移動する様子を見ることができます。教卓で行いますが、後ろの生徒のために、教室のプロジェクターに大きく映して見てもらいます。iPadを授業に使う②実物映像提示パーツ→2018/5/24ブログ実に地味な演示実験ですが、授業ではできるだけ現象やモノを見せたいと思っています。
2020.08.26
コメント(0)
-

凝固点降下のデータ処理・グラフ…実験できないので
実験室は対面になり、生徒同士が近接するので生徒実験がゆるされていません。クラスを2分して、20人ずつ実験するのは可能なのですが残りの生徒の対応ができなくなるので難しいです。そこで、しばらくは実験の様子を写真・ビデオでみせて、データ処理だけでも生徒にやってもらおうと思っています。今回は「凝固点降下」の実験です。実験プリントとグラフ処理についての解説プリントです。①実験「凝固点降下」プリントナフタレン(溶質)・シクロヘキサン(溶媒)溶液の凝固点降下をはかります。【実験1】ではシクロヘキサンの凝固点を調べるために5秒おきに温度を調べ記録します。【実験2】ではシクロヘキサンにナフタレンを溶解し凝固点を調べます。【考察】ではグラフを描き、凝固点降下度を求めます。そこからナフタレンの分子量を求めます。②実験データデータと要求するレポート内容です。③グラフ用紙の使い方とグラフの描き方過去に行った生徒実験のレポートをつかって解説しています。①余白は使わない方針で指導します。②実験タイトルと日付は後で見たときに書いた本人すら何のグラフかわからなくなるのでタイトルを書くことは重要です。④データの記入や考察は別紙が正しいが、一枚で書いておくと後で見たときに一目で全体がわかるので書いてもらいます。⑤-⑦グラフ用紙の中央に大きくグラフが書けるように目盛を工夫させたい。⑧⑨凝固点を求める処理です。どのように線を引くかが生徒の考察のポイントです。以上です。のちほど、生徒のレポートが提出されたら報告します。
2020.08.20
コメント(0)
-

「エアロゲル」コロイド溶液の授業で見せたい
高校化学で「コロイド溶液」の分野をまもなく授業します。コロイド粒子の利用についていろいろ探っていたところ高い断熱効果のある「エアロゲル」がありました。手に入れて生徒にみせたいと思っています。ネタ元はNIMSのYouTube動画です。未来の科学者たちへ #13 「エアロゲル断熱材」半透明の軽いSiO2構造のコロイド粒子を集めたものです。多孔質で内部の微細な穴に空気が入っています。写真上はエアロゲル上に置いた枯葉をアルコールランプで加熱しても焦げたり燃えたりしない。写真下は粉末状のエアロゲルをまぶした水滴を熱したフライパンに落としても「ジュ―」っといって蒸発しない。今はコロナウイルスの感染を心配して生徒実験ができないので派手な演示で生徒を引き付けようと思います。断熱粒素ヒートカットパウダー300ml(NASA断熱塗料1Lに相当)価格:5803円(税込、送料別) (2020/7/18時点)楽天で購入
2020.07.18
コメント(0)
-

授業用プロジェクター画面ミラーリングAnyCast換えました
1学期のまとめ「教材作成・提示編」→2018/7/13ブログここで、使っている授業の中核はiPad-ApplePenです(ソフトはGoodNote)プロジェクターとAnyCast(HDMI出力の画面ミラーリングドングル、下の写真)です。1.安価である。(2000円程度)2.AppleのAirplayで画面をそのままプロジェクションできる Windowsやandroidにも対応しています。3.HDMIケーブルがいらず、無線=Wi-Fiで画像を送れるので、教室を回りながらプレゼンできる。 スマホの画面も送ることができるので、プレゼンも手軽です。4.小さい。ほぼ、プロジェクターと一体化します。この「AnyCast」は2年2ヶ月使ってきましたが、本体とUSB接続部に接触不良が時々起こるようになりました(下の写真の赤矢印)。同僚に話をきくとやはり1年ぐらいで接触不良が起こったとのこと。私のはよくもったほうだと思います。2000円程度で購入できますので、修理に時間かけるより、新しいものを購入しました。2020年版のAnyCast M100 にアップグレード購入です。4K対応版をうたっていますが、それだけCPUが速くなったことを期待しての購入です。表示された画面ディレイも以前より少なくなり、満足して使っています。形状、大きさはM9と同じ。Wi-Fiアンテナの形が少し違ってました。以前なかった取扱説明書(日本語)もついていました。これで、しばらくは授業に支障をきたすことはないでしょう。4K Anycast ドングルレシーバー モード切替え不要 簡単接続 大画面 4K高画質動画転送 ミラーキャストレシーバー ワイヤレス 無線 HDMIアダプター ANYGOLD価格:2150円(税込、送料無料) (2020/7/4時点)楽天で購入ところで、7月になりましたが、勤務校では7月21日から1週間ほど期末試験です。中間試験がなくて試験範囲が広い上に前半ネット授業できっと定着が悪いだろうなぁ生徒の健闘を祈るばかりです。
2020.07.02
コメント(0)
-

気体の状態方程式:演示で熱気球
今年は生徒実験ができません。感染予防のため実験机での対面着席が許されません。出来るだけ教室に教材を持っていくのですが手と手を介する、生徒の閲覧もはばかられます。今は、写真とビデオをを中心にモノを見せています。しかし、つまらんなぁ。授業は気体の状態方程式に入りました。現象をたくさん見せたいので、今年も熱気球を上げます。より軽く手抜きしてー熱気球演示実験→PV=nRT2018/11/30ブログ上は2018年の11月の熱気球こちらは、2020年7月1日に予備実験を行ったもの。支えの細いピアノ線で作った輪は同じですが、ほそい工作用アルミ線を中央に1本わたし、軽量化をはかりました。アルミ線の中心に綿をつけ、メタノールをしみこませ、軽く絞って点火するとすぎに浮きます。ダイソーの20Lポリ袋(下写真)は軽くていいのですが、やはり熱に弱い。1回の飛行(30秒くらいかな)でちりめん状に溶けてしまい、毎回取り換えなければなりません。ピアノ線の4か所にセロテープで袋の口を貼り付けているので、取り換えじたいは簡単です。生徒は毎度、面白がりますが、これを気体の状態方程式にこじつけます(笑)。この演示を見てもらって、浮力の説明をし、PV=nRTを使って、何グラムまで持ち上げられるかをレポートで提出してもらいます。
2020.07.01
コメント(0)
-

箱にボールを詰め込む…細密充填
結晶の授業をしています。教材の都合で金属結晶が最後になりました。細密充填構造である「面心立方構造」、「六方細密構造」と「体心立方構造」を勉強します。「どっちの詰め方がたくさん箱に入る?」野球のボールで聞いてみます。これは、野球部の生徒さんが得意です。部活後の片づけで自然に身についています。
2020.06.20
コメント(0)
-
これまで試した授業用教材ビデオ作製
来週から、変則的に対面の授業が始まります。授業時間を短くして、クラス人数を半分の20人に分けて授業します。これまで、授業用ビデオを15本UPしてきました。オンライン授業は行ってません。生徒は学校のHPかにリンクされたビデオとプリントPDFを使って自学自習をします。様々な授業用ビデオの作り方をしてきましたので、記録として残しておきます。① Windows10 Microsoft Office PowerPoint 利用 Microsoft Store ダウンロード版office2019 \29791 とても高価ですがこれが一番使いやすい *.MP4の動画ファイルで記録されます。詳しくは以下にMicrosoftのリンクを張りますのでご覧ください。プレゼンテーションをビデオに変換する② Windows10 PowerPoint 互換プレゼンsoft 利用 Libre Office Impress 無料、King Soft WPS Officeダウンロード版 \5988 Windowsのソフトの動作をキャプチャーしてビデオに変換する(1)ソフトを動かし、キャプチャーします Windowsキーを押しながらgを押す(WIN+g)と、キャプチャーモードになります プレゼン画面の上に三つのwindowが開きます左上windowのキャプチャーの左から3番目◎印(マイクのアイコンの隣)を押すと録画が始まります。この時、プレゼンソフトは全画面でうごいているはずです。そのまま、プレゼンしながらマイクに向かって話します。(マイクのアイコンに"/"が入っているとマイクoffですのでクリックして外しておいて)終わったら、[ESC]を押すとプレゼンも動画キャプチャーも終わります。(2)編集する余計な部分をカットして完成版にします。キャプチャーしたファイルはもう一度"WIN+g"を押すと記録された*.MP4ファイルのありかが表示されます。それを編集ソフトにかけます。上の写真では「撮ったスクリーンショットとゲームクリップはここに表示されます」画面の下に出ています。一般的には「ユーザー>ユーザー名>ビデオ>キャプチャ」にあります。この動画ファイルをWindowsのフォトアプリで編集します。「フォト」アプリで、撮った写真やビデオの整理や編集、共有に→Microsoft私は細かい動画編集ができるAviUtilをつかっています。③ Apple iPad プレゼンsoft KeyNote 利用 iPad 添付のソフトをつかいます。 詳しくは以下でiPadだけで簡単にWEB授業用教材を作る→2020/5/8ブログ結局のところ、私は②の方法に落ち着きました。シミュレーションソフトを動かしてキャプチャーできるので、プレゼンソフト以外も自由に使えます。
2020.06.04
コメント(0)
-

硫酸銅(Ⅱ)水溶液の電気分解によりファラデー定数を求める動画
硫酸銅(Ⅱ)水溶液の電気分解-銅電極によりファラデー定数96500Cを求める実験の動画を作りました。無音です。実験書から、実験手順、データの処理まで6分の動画に編集してあります。途中で止めて、ご覧ください。今回の実験では、陰極の増加と陽極の減少が、たまたま同じになりました。何度も実験していますが、こんなことはありませんでした。したがって、実験書では陰極増加量と陽極減少量からファラデー定数を求めるようになっていますが、ここでの計算は一回だけです。今回の実験では、ファラデー定数として93900Cが得られました。誤差は-2.69%でした。いつも、この程度の誤差です。関連して以下のブログをご覧ください。実験:ファラデー定数を求める→2017/9/8ブログ生徒実験「ファラデー定数を求める」実施しました→2017/11/1ブログその他、本ブログ内の検索窓から「ファラデー定数」で検索いただければ、詳細な実験準備と実験結果をご覧いただけます。
2020.05.15
コメント(0)
全164件 (164件中 1-50件目)











