この広告は30日以上更新がないブログに表示されております。
新規記事の投稿を行うことで、非表示にすることが可能です。
広告
posted by fanblog
2020年04月23日
アメリカで新型コロナウイルス抗体検査始まる
アメリカで新型コロナウイルス抗体検査始まる
PCR検査を受けたことのない市民の1/3に抗体(+)、かつ無症状
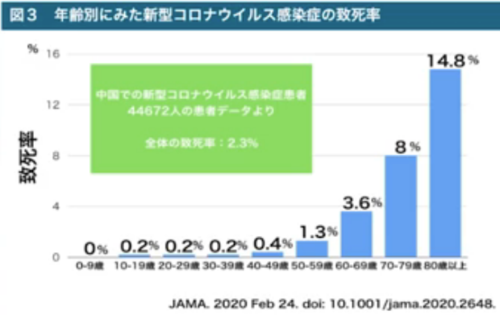
感染力は強いが、50歳以下には致死率が低いので、60歳以上の高齢者、あるいは基礎疾患(高血圧、糖尿病、悪性疾患、膠原病、喫煙 歴のある人)およびその家族だけが、神経質にならなければならない感染症と証明される結果となりました。
当然医療関係者も含まれます。
>コロナ抗体検査、NYで始動 1日2000件に市民殺到
2020/4/22 4:37 (2020/4/22 11:14更新)
抗体検査は、指などから少量の血液を採取してウイルスへの抗体があるかどうかを調べる(カリフォルニア州で実施された抗体検査の様子)=ロイター
【ニューヨーク=野村優子】
米国で人がこれまでに新型コロナウイルスに感染していたかを調べる「抗体検査」が本格化する。
ニューヨーク州は20日から、1日2000件と全米最大規模の抗体検査を始めた。
客観的なデータを蓄積し経済活動の再開時期を探るが、十分な量の検査キットの確保や精度の向上などが課題になる。
■抗体検査とは 血液採取し免疫判定
感染の有無を調べるPCR検査に対して、「抗体検査」は既に感染を経て体にウイルスに対する免疫が備わったかを診る。
人間は感染症にかかると、次に同じウイルスが侵入した際、素早く防御するよう特殊な抗体を体内につくる。
抗体検査とはこの抗体を調べるもの。
検査方法は喉や鼻を拭ってウイルスの有無を調べるPCR検査と異なり、指などから少量の血液を採取してウイルスの抗体を調べる。
自身の感染やウイルスの拡散リスクが低い免疫保持者を特定できる可能性があるため、経済活動の再開に向けた判断材料の一つとして注目されている。
■「免疫持つか知りたい」スーパーに市民が列
感染者数が全米最多となるニューヨーク州。
北部バファローにある大手スーパー、ウェグマンズには長蛇の列ができていた。
客の目的は買い物ではない。
抗体検査の実施場所は公表されていないが、ここで検査を受けられるとの噂を聞きつけた人が、自分が新型コロナの免疫を持つかどうかを知りたいと殺到したのだ。
ニューヨーク州のクオモ知事は19日、1日2000人、週1万4000人のペースで抗体検査を始めると表明した。
全米では最大規模ではあるものの、同州の感染者は判明しているだけで25万人に達する。
検査キットは圧倒的に足りないのが現状で、ニューヨーク州は無作為に選んだ人を対象に州内の約20のスーパーで検査を始めた。
クオモ知事は「経済活動の再開はデータに基づいて判断すべきだ。抗体検査がカギとなる」と指摘する。
抗体を持つ人を医学的に絞り込んだうえで外出制限を緩めれば、再び感染が広がるリスクを抑えながら経済活動を再開できるとみる。
先駆けて抗体検査を実施した州では、実際には従来の検査結果を大きく上回る感染者がいるとの見方も出ている。
21日にトランプ大統領と会談したクオモ知事は新型コロナの大規模な抗体検査の実施へトランプ氏と合意したと明らかにした。
新型コロナウイルスの抗体検査は世界で注目されている(ドイツの研究所)=AP
■精度向上課題、未認可の中国製も
米スタンフォード大学などの研究チームはカリフォルニア州サンタクララ郡の保健当局と連携し、ドライブスルー方式の検査場を設けて抗体検査を実施。
4月上旬に約3300人を対象に実施した抗体検査の結果、同郡で新型コロナに感染した人は従来の検査で感染が確認された人数の50〜85倍にのぼる可能性があるとしている。
マサチューセッツ州の病院でも、従来の検査を受けたことがない200人を対象に抗体検査を行った結果、3分の1で抗体が確認された。
無自覚で感染した人を効率的に抽出できれば、経済活動の再開を後押しする可能性がある。
今後、検査キットの量産と精度の向上が課題になる。
米食品医薬品局(FDA)が4月以降に承認した抗体検査キットのメーカーは4社にとどまる。さらに承認を受けていない中国製の検査キットが一部で流通。
米国公衆衛生協会のスコット・ベッカー会長は、「質の悪い検査が流通しており、その多くが中国製で無法地帯のようになっている」と指摘した。
抗体検査キットを巡っては非営利団体の米国立科学アカデミーもホワイトハウスに書簡を送付。
検査の抽出手法にばらつきがあることや、一般的な風邪の原因となる他のコロナウイルスへの抗体への誤認が見られることなどを挙げ、検査の有用性について「さらなる検証が必要」と注意喚起した。
米国立衛生研究所(NIH)は全米の1万人を対象に、抗体検査の正確性を調べる研究に着手している。
世界保健機関(WHO)は4月中旬、新型コロナ感染者が回復後に再び陽性になるケースが出ていると報告した。
新型コロナは科学的に不明な点が多く、今後、抗体の有効性も含めた調査、研究が重要になる。
https://www.nikkei.com/article/DGXMZO58339750S0A420C2000000/?n_cid=NMAIL007_20200422_H
A8からのメルマガ希望
2020年04月17日
新型コロナに対する特効薬がアビガン!
新型コロナに対する特効薬がアビガン!
催奇形性だけが、問題点だが、高齢者には関係ない。
>アビガンを共同研究してきた富山大学の白木公康名誉教授(千里金蘭大学副学長)は、開発者という立場上、「自ら発信することにはためらいがある」と話しながらも、中国の論文報告などをもとに、「発症6日までにアビガンを開始すれば、ウイルスの早期消失、咳嗽(せき)の軽減、肺炎の進行や重症化が阻止され、死亡率は激減するはずだ。
ウイルス量がピークを過ぎるころから治療を始めても大きな効果は期待できない」と述べる。
アビガンに期待する人が押さえておきたい裏側
坂口 直 : 医薬経済社編集部 記者2020年04月08日
新型コロナ感染症の治療薬候補として世界各国の注目を集める「アビガン」

新型コロナウイルス感染症(COVID-19)が世界中で蔓延するなか、富士フイルム富山化学が開発した抗インフルエンザウイルス薬「アビガン」が注目を浴びている。
安倍晋三首相が記者会見で名指ししてアピールした薬剤で、新型コロナウイルスへの治療薬として期待が高まっている。
だが開発の経緯を子細にたどると、実際の治療で使われるためには、越えなければならない高いハードルがある。
菅官房長官は4月3日の記者会見で、アビガンを希望する各国に無償提供する方針を明らかにした。
現時点で約30カ国から提供要請があるという。
アビガンが注目されたきっかけは、実際に新型コロナに感染した患者に使用した中国の試験で、効果がみられたからだ。
新型コロナウイルスの発生源とされる武漢市の武漢大学中南病院では、患者を「アビガン(中国では後発品のファビピラビル)」を投与したグループ(116人)と、ウイルスの侵入を阻害する薬剤である「アルビドールを投与したグループ(120人)の2つに分け、効果を比較した。
その結果、回復率はアビガン投与群が「71.4%」、アルビドール投与群は「55.9%」と差がみられた。
さらに、深?第三人民病院では、アビガンを投与したグループ(35人)と、新型コロナにも効き目があるとみられている抗HIV薬の「カレトラ」を投与したグループ(45人)に分けて比較したところ、新型コロナウイルスが消失した期間は、アビガン投与群が「4日」、カレトラ群「11日」だった。
胸部画像による改善率では、アビガン群「91.4%」、カレトラ群「62.2%」と、アビガンが効果を示した。
2つの試験は3月に論文として公表されたが、後者は今月に入って取り下げられたことがわかっている。
その理由は不明だ。
効果が確認されればコロナ治療薬になりうる
いまだ有望な治療薬もワクチンも見つかっていないなかで、もし効果が確認されれば、貴重な薬剤となる。
日本でも臨床試験が始まったが、中国でもさらなる臨床試験が行われている。
安倍首相は2月29日の記者会見で、「アビガンを含む3つの薬について、新型コロナウイルスに有効性があるかどうかを見極めるため、観察研究としての患者への投与をすでにスタートしている」と述べ、3月28日の記者会見では国産であることをアピールするかのように「アビガンは海外の多くの国から関心が寄せられ、臨床研究を拡大するとともに、増産をスタートする」と語った。
ここで、アビガンの開発にさかのぼってみよう。
アビガンはもともと富士フイルムホールディングスに買収された旧富山化学が1990年代後半から開発してきた薬剤だ。
抗菌薬、炎症性疾患、神経系疾患の領域を対象に、新薬のタネを探していたところ、たまたまインフルエンザに活性のある(インフルエンザウイルスに作用する)化合物を見つけた。
それが開発コード「T−705」、のちのアビガンだ。
T−705は当初から大きな期待を背負っていた。
代表的な抗インフルエンザ薬「タミフル」が細胞内で増殖したウイルスを外へ出なくさせる作用機序(作用メカニズム)を持つのに対して、アビガンは「RNAポリメラーゼ」という酵素を阻害することでウイルスの増殖そのものを防ぐ、今までにない作用機序であるためだ。
原理上は、遺伝子変異が起きず、耐性ウイルスを生じないといわれている。
2000年にカナダで開催された国際会議では、アビガンがインフルエンザのほか、既存の抗インフルエンザ薬の耐性ウイルスにも有効性があったことを示した。
T−705が発表されてしばらくの間、この新薬候補は将来の売り上げが1000億円を超す大型製品になると目されていた。ところが開発がストップしてしまう。
開発資金の不足とタミフルの先行
理由の1つには開発資金の不足があった。
当時、富山化学が販売していた脳梗塞後遺症治療薬「サープル」の有効性が否定され、全品が回収に追い込まれていた。
2つ目の理由として、ライバル薬として1999年にアメリカで承認されたタミフルがすでに世界中で使われ始めていた。
T−705はヒトを対象とした試験がまだであり、薬剤として世に出るには数年先になってしまう。
その間にタミフルが市場シェアを押さえてしまえば、挽回するのは容易ではなかった。
さらには、動物実験段階で「催奇形性」の副作用のリスクがあった。
催奇形性とは、妊婦のお腹の中にいる胎児に障害が出る、薬剤にとっては致命的な副作用だ。
抗がん剤などの中には催奇形性のある薬剤があり、妊娠の可能性のある世代には厳重な管理が求められている。
それでなくとも「催奇形性」というだけで敬遠されがちだ。
複合的な理由が重なり、開発は中止された。
だが、しばらくして転機が訪れた。
2004年ごろから、鳥インフルエンザウイルスがヒトに感染して死亡する事例が世界的に多発したのだ。
世界保健機関(WHO)も、事態を受けて「ヒトへの感染が広がり続けると、新型のインフルエンザウイルスが出現し、世界的な感染爆発に発展する可能性が高まる」との警告を始めた。
日本でも病原性の高い鳥インフルエンザウイルスが新型インフルエンザウイルスに変異した場合、致死率は高くなるのではないかとの一部の専門家の指摘をもとに厚労省がはじき出した被害想定では、死亡者数を「17万〜64万人」と推計した。
そこで再びT−705に注目が集まる。
タミフルとは作用機序が異なるため、パンデミック(世界的大流行)時に、タミフルでは効かない患者に投与する薬剤としての価値が見いだされたようだ。
2004年にアメリカの国立アレルギー感染症研究所は、富山化学から提供されたT−705が高病原性の鳥インフルエンザに効果があることを突き止めた。
これが契機となって、催奇形性の副作用はあるものの、富山化学は「経営上の判断」(富山化学関係者)によって、2007年にヒトを対象とした臨床試験を開始し、2011年には国に薬剤としての認可を求める申請にまで漕ぎつけた。
しかし、やはりここで壁にぶち当たった。
薬剤の有効性や安全性について審査する日本の医薬品医療機器総合機構(PMDA)が、T−705の催奇形性の副作用リスクを問題視したのだ。
動物実験で胎児の催奇形性が認められたことから、ヒトへの影響が強く懸念されるため、慎重に審査されることになった。
審査に3年を要しても承認に突き進んだ
当時の富山化学が催奇形性のリスクがわかっていながら承認申請に突き進んだ理由は謎だが、結局、アビガンが承認されたのは2014年だった。
通常だと1年程度で済む審査期間が3年もかかっている。
さらに、当初は通常の季節性インフルエンザに使用できる薬剤をめざしていたが、結局は新型インフルエンザにのみ使用が認められた。
通常のインフルエンザに使われないよう徹底した管理を求められ、その後、パンデミックに備えて、200万人を目標に備蓄されることになった。
資金難や催奇形性の紆余曲折を経て、いわば「首の皮一枚」でつながったアビガンが、今、新型コロナの「切り札」として注目を集めている。
なぜ抗インフルエンザウイルス薬が新型コロナウイルスに効果をもたらす可能性があるのかは未解明だが、共通点はインフルエンザも新型コロナも同じ「RNAウイルス」であることだ。
2013年末に西アフリカで起きた「エボラ出血熱」のアウトブレイク(突発的発生)でも、アビガンが使われ、死亡率を「3分の2」に引き下げる効果があったとされている。
このエボラウイルスも同じRNAウイルスだ。
アビガンを共同研究してきた富山大学の白木公康名誉教授(千里金蘭大学副学長)は、開発者という立場上、「自ら発信することにはためらいがある」と話しながらも、中国の論文報告などをもとに、「発症6日までにアビガンを開始すれば、ウイルスの早期消失、咳嗽(せき)の軽減、肺炎の進行や重症化が阻止され、死亡率は激減するはずだ。
ウイルス量がピークを過ぎるころから治療を始めても大きな効果は期待できない」と述べる。
白木名誉教授は、「外来の時点で、胸部CTで肺炎を確認して、アビガンを使用して(肺炎の進行を)止めるべきではないか」との考えを示す。
さらに、「アビガンの早期使用は死亡率を下げる効果だけでなく、若い患者が、間質性肺炎による肺の線維化(スポンジのようになり機能しなくなること)や瘢痕化(炎症によって傷跡が残ること)などの後遺症を残さないことにも意味がある」とする。
また、「高齢者が急激な悪化を防ぐためにもアビガンは有用」とみている。
催奇形性の影響受ける世代には慎重な投与必要
これだけ聞くとアビガンの早期承認が待たれるが、実際の医療現場で使うとなるには大きな課題がある。
白木氏は、早期の段階(無症状や症状の軽い段階)から使えば効果が期待できるとするが、とくに催奇形性の影響を受けやすい世代には、事前に説明して承諾を得なければならない。
それは、致死的な症状に陥るかわからない段階で、催奇形性のある薬剤の投与を勧めることを意味する。
男性に投与した場合、精液へ移行することがわかっている。
それに備蓄薬としては承認されたが、実際に使われた実績がなく、広く使われた場合にどんな副作用が生じるかは不明だ。
承認を得る段階での試験では患者数が限られており、広範囲に使われたときに持病や特異な体質をもつ人にどんな副作用が起きるかは想像がつかない。
アビガンが新型コロナウイルスの救世主になる可能性はあるかもしれない。
その一方で、副作用を踏まえたうえでインフォームドコンセントをどうするか、どんな患者にどのように使用するかなど、クリアしなければならない課題は大きい。
https://toyokeizai.net/articles/-/342917?fbclid=IwAR1w-sL_cOIL1Kng_dfHwJ5j7ksBSutCJm5PaoLYeT_8S3w23cfaEcFboZw








