公費 0
[薬の話] カテゴリの記事
全386件 (386件中 1-50件目)
-
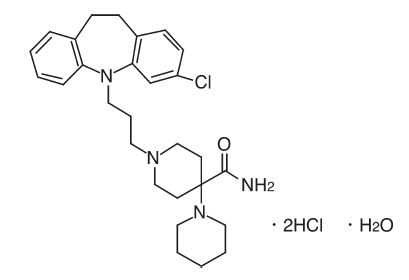
その他の抗精神病薬:クロカプラミン塩酸塩水和物(クロフェクトン)
承認年1973年開発の経緯クロカプラミン塩酸塩水和物は,当社研究所において開発された三環イミノジベンジル系抗精神病薬で,カルピプラミン塩酸塩水和物(販売名:デフェクトン,2013 年発売中止)のイミノジベンジル核3 位にCl 基を導入した化合物である。錠剤(10,25mg)及び顆粒剤は1973 年1 月に承認を取得し,1974 年2 月に発売を開始した。その後,1986 年2 月には50mg 錠の承認を取得,1987 年10 月に発売を開始した。また,錠剤(10,25mg)は2001 年2 月に,顆粒剤は2002 年2 月に販売名変更に伴う再承認を受け,それぞれ2001 年7 月及び2002 年7 月に変更銘柄名で薬価収載された。製品の治療学的特性・製剤学的特性(1)クロカプラミン塩酸塩水和物は抗精神病薬の抗精神病作用と相関が高いといわれている中枢性抗ドパミン作用を有する。(2)本剤は,臨床的には統合失調症の抑うつ気分,無為,自閉,感情鈍麻等に対して気分高揚,発動性促進的に働き,疎通性の改善,接触性の拡大をもたらすとともに,幻覚や妄想等の異常体験に対しても効果を示す。(3)総症例数4,565 例中1,174 例(25.72%)1,854 件の副作用が報告されている。(承認時~1977 年1 月までの調査及び文献調査等に基づき集計)重大な副作用として,Syndrome malin(悪性症候群),無顆粒球症,白血球減少,遅発性ジスキネジア,麻痺性イレウス,抗利尿ホルモン不適合分泌症候群(SIADH),肺塞栓症,深部静脈血栓症があらわれることがある。また,類似化合物のブチロフェノン系化合物(ハロペリドール)で心室頻拍(Torsades de Pointes を含む)が,フェノチアジン系化合物及びブチロフェノン系化合物の長期又は大量連用により眼障害があらわれることが報告されている。販売名和 名クロフェクトン錠10mg、クロフェクトン錠25mg、クロフェクトン錠50mg、クロフェクトン顆粒10%洋 名CLOFEKTON TABLETS 10mg,CLOFEKTON TABLETS 25mg,CLOFEKTON TABLETS 50mg,CLOFEKTON GRANULES 10%名称の由来カルピプラミン塩酸塩水和物(販売名:デフェクトン,2013 年発売中止)にクロル(Cl)基がついたことに由来する。一般名和 名(命名法)クロカプラミン塩酸塩水和物(JAN)洋 名(命名法)Clocapramine Hydrochloride Hydrate(JAN)、Clocapramine(INN)ステムイミプラミン系物質(飽和三環系化合物):- pramine抜粋:クロフェクトン・インタビューフォーム臨床精神薬理(Vol.23 No.3(Mar) 特集:新規抗精神病薬blonanserinテープ製剤とは
2022.10.31
コメント(0)
-

ブチロフェノン系抗精神病薬:スピペロン(スピロピタン)
承認年1971年開発の経緯ブチロフェノン系化合物はJanssen研究所で合成されたものであるが、その出発点は合成麻薬性鎮痛剤のメペリジンとされている。メペリジンからブチロフェノン系薬剤のプロトタイプといわれているハロペリドールが合成されて以来、約5000 の誘導体が作られ、その中の19 の化合物につき臨床試験が行われた。スピロピタン錠の有効成分であるスピペロンは9 番目のものである。本薬は1962 年にJanssen 研究所で合成され、薬理学的スクリーニングが行われたもので、動物のカタレプシー惹起作用は他の抗精神病薬に比べて非常に強く、特徴として、作用発現までの時間も長いが作用の持続時間が長く、ハロペリドールタイプの薬剤に分類される。当社では、スピロピタン錠(0.25mg)を1969 年2 月に販売を開始し、1971 年2 月にスピロピタン錠1mgの販売を開始した。スピロピタン錠(0.25mg)については、医療事故防止対策に伴ない販売名が変更されスピロピタン錠0.25mgとして2001 年7 月に製造承認され、現在に至っている。製品の治療学的特性・製剤学的特性スピロピタン錠の有効成分であるスピペロンは、ブチロフェノン系化合物で、強力な抗精神病薬に位置づけられており、精神抑制作用と賦活作用の二面性を持つスペクトルの広い薬剤である。精神運動興奮、幻覚・妄想などに速やかな抑制効果を発揮し、また自発性減退、感情鈍麻など陳旧性統合失調症の中核症状に対しても奏効することが報告されている。販売名和 名スピロピタン® 錠0.25mg、スピロピタン® 錠1mg洋 名Spiropitan® Tablets 0.25mg、Spiropitan® Tablets 1mg名称の由来開発当時の一般名Spiroperidol の「Spiro」と、弊社の向精神薬Propitan と同系統の化合物という意味から「pitan」をとり、Spiropitan とした。一般名和 名(命名法)スピペロン(JAN、INN)洋 名(命名法)Spiperone(JAN、INN)ステムトランキライザー、神経遮断薬、4′⊖フルオロ⊖4⊖ピペリジノブチロフェノン誘導体:⊖perone抜粋:スピロピタン・インタビューフォーム臨床精神薬理(Vol.23 No.3(Mar) 特集:新規抗精神病薬blonanserinテープ製剤とは
2022.10.30
コメント(0)
-
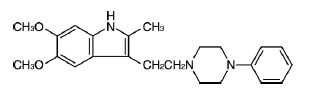
その他の抗精神病薬:オキシペルチン(ホーリット)
承認年1970年開発の経緯オキシペルチン(Oxypertine)は1962年、米国のウインスロップ社(現:サノフィ社)において開発された、フェノチアジン系、ブチロフェノン系あるいはレセルピン系などの向精神薬とは異なる構造をもつ脳内生体アミン類似の抗精神病薬である。1972年に販売名「ホーリット錠20mg」、「ホーリット錠40mg」及び「ホーリット散」として発売された。また、医療事故防止対策として「ホーリット散」から「ホーリット散10%」に販売名の変更を申請し、2008年3月承認された。製品の治療学的特性・製剤学的特性(1)有効性自発性減退、感情鈍麻等の情動表出障害を改善し、疎通性、対人接触、感情表出を高める。(2)安全性承認前及び承認後における調査1,761例中報告された主な副作用は不眠13.3%(234件)、錐体外路症状[手指振戦11.6%(204件)、アカシジア5.6%(99件)、筋強剛3.1%(54件)]、不安・焦燥3.0%(53件)、低血圧3.2%(57件)、食欲不振3.1%(55件)、けん怠感3.3%(58件)であった。(再審査対象外)重大な副作用として頻度不明であるが、Syndrome malin(悪性症候群)、麻痺性イレウス、無顆粒球症、白血球減少が報告されており、抗精神病薬において、肺塞栓症、深部静脈血栓症が報告されている。(3)製 剤錠20mgは白色、錠40mgはうすいだいだい色であり、両者の識別が可能である。また、錠40mgは漸次増量時以降に使用する。(4)治 療統合失調症患者において自発性減退、感情鈍麻等の情動表出障害を改善し、疎通性、対人接触、感情表出を高める。また、治療の初期に、一過性に興奮、衝動行為、不安、焦燥、多幸等の随伴症状がみられることがあるが、これは症状の悪化ではなく、むしろ、情動表出障害の改善への“ゆさぶり”で、本剤の賦活効果のあらわれと考えられる。上記賦活効果のほか、精神運動興奮、衝動性等に対し、鎮静的効果が認められている。(5)薬理学ノルアドレナリン系のみならず、ドパミン系、セロトニン系など各種神経系に影響を及ぼす。また、シナプス前膜及びシナプス後膜の両方に作用する。(6)その他オキシペルチンは化学的には中枢作用の予想されるインドールアルキル体と抗アドレナリン作用をもつフェニールピペラジンを結合させることより、中枢での抗アドレナリン作用を期待して合成された薬剤で、フェノチアジン系、ブチロフェノン系あるいはレセルピン系などの薬剤とは異なる構造をもつ抗精神病薬である。販売名和 名ホーリットⓇ錠20mg、ホーリットⓇ錠40mg、ホーリットⓇ散10%洋 名FORIT® Tablets 20mg、FORIT® Tablets 40mg、FORIT® Powder 10%名称の由来「for it(そのために)」に由来する一般名和 名(命名法)オキシペルチン(JAN)洋 名(命名法)Oxypertine(JAN)ステム不明抜粋:ホーリット・インタビューフォーム臨床精神薬理(Vol.23 No.3(Mar) 特集:新規抗精神病薬blonanserinテープ製剤とは
2022.10.29
コメント(0)
-
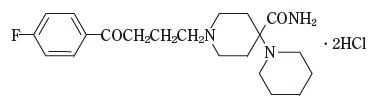
ブチロフェノン系抗精神病薬:ピパンペロン塩酸塩(プロピタン)
承認年1965年開発の経緯ブチロフェノン系化合物はJanssen研究所で合成されたものであるが、その出発点は合成麻薬性鎮痛剤のメペリジンとされている。メペリジンからブチロフェノン系薬剤のプロトタイプといわれているハロペリドールがPaul A. J.Janssen により合成されて以来、約5000 の誘導体が作られ、その中の十数種の化合物につき臨床試験が行われた。プロピタンの有効成分であるピパンペロンは6 番目に開発されたもので、外国ではDipiperonの名で商品化されている。日本においては、プロピタン錠は1965 年3 月、プロピタン散は1967 年1 月に販売が開始された。その後医療事故防止対策のため、販売名が変更され、プロピタン散はプロピタン散10%として2001 年7月、プロピタン錠はプロピタン錠50mgとして2007 年8 月に製造販売承認され、現在に至っている。製品の治療学的特性・製剤学的特性プロピタンの有効成分であるピパンペロンは、ブチロフェノン系薬剤で、急性・慢性統合失調症の幻覚・妄想など異常体験を早期に消退させ、不安、緊張、興奮などの症状にも抑制作用を示す。販売名和 名プロピタン® 錠50mg、プロピタン® 散10%洋 名Propitan® Tablets 50mg、Propitan® Powder 10%名称の由来精神症状の寛解という意味でpropitiate(やわらげる、なだめる)の「propi」に接尾語の「tan」をつけてPropitan とした。一般名和 名(命名法)ピパンペロン塩酸塩(JAN)洋 名(命名法)Pipamperone Hydrochloride(JAN)ステムトランキライザー、神経遮断薬、4′‒フルオロ‒4‒ピペリジノブチロフェノン誘導体:‒perone抜粋:プロピタン・インタビューフォーム臨床精神薬理(Vol.23 No.3(Mar) 特集:新規抗精神病薬blonanserinテープ製剤とは
2022.10.27
コメント(0)
-
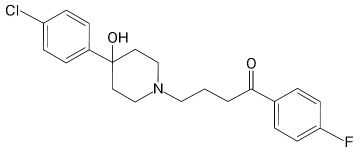
ブチロフェノン系抗精神病薬:ハロペリドール(セレネース)
承認年1964年開発の経緯ハロペリドールは、1958年ベルギーのヤンセン社研究所で合成されたブチロフェノン系抗精神病薬である。ハロペリドールは、動物実験によって薬理作用、毒性などの検討が行われた後、臨床試験に供された。最初の臨床試験は1958年、Liege大学精神科のDivryらの手で行なわれた。その後ヨーロッパ各地(ベルギー、フランス、ドイツ、デンマークなど)の施設で経口、非経口投与による臨床試験がなされ、精神運動興奮、幻覚、妄想、躁状態、舞踏病、チック、精神病質の攻撃性、不安、不眠、悪心・嘔吐、急性、慢性のせん妄、うつ病の不安など(注:本邦における効能又は効果、用法及び用量は、外国での承認状況とは異なる。)の症状軽減に有用であることが明らかにされた。ハロペリドールの製剤は、日本では1964年から市販されている。製品の治療学的特性・製剤学的特性(1) 経口投与による臨床試験において、統合失調症と躁病に有効性が認められた。(2) 重大な副作用として、悪性症候群(Syndrome malin)、心室細動、心室頻拍、麻痺性イレウス、遅 発性ジスキネジア、抗利尿ホルモン不適合分泌症候群(SIADH)、無顆粒球症、白血球減少、血小板減少、横紋筋融解症、肺塞栓症、深部静脈血栓症、肝機能障害、黄疸が報告されている。販売名和 名セレネース錠0.75mg、セレネース錠1mg、セレネース錠1.5mg、セレネース錠3mg、セレネース細粒1%、セレネース内服液0.2%洋 名Serenace Tablets, Fine Granules、Serenace Oral Solution名称の由来Serene(静かな、穏やかな)+ace(優秀な)で、すぐれた鎮静・静穏化剤の意味をもつ。一般名和 名(命名法)ハロペリドール(JAN)洋 名(命名法)Haloperidol(JAN、INN)ステム抗精神病薬、ハロペリドール誘導体:-peridol抜粋:セレネース・インタビューフォーム臨床精神薬理(Vol.23 No.3(Mar) 特集:新規抗精神病薬blonanserinテープ製剤とは
2022.10.26
コメント(0)
-
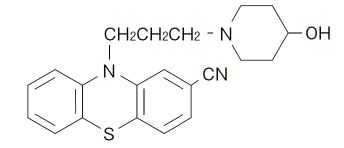
フェノチアジン系抗精神病薬(ピペリジン側鎖):プロプレシアジン(ニューレプチル)
承認年1964年開発の経緯プロペリシアジンは、フランスで合成、開発されたピペリジン系のフェノチアジン誘導体である。ピペジン系フェノチアジン誘導体は、ジメチルアミノプロピル系よりも鎮静催眠作用が、ピペラジン系よりも錐体外路症状が弱い。1964年4月、塩野義製薬が承認を受け、同年8月、我が国で最初に発売された。2012年8月、塩野義製薬株式会社から高田製薬株式会社に承継した。製品の治療学的特性・製剤学的特性(1)統合失調症の不安、緊張、抑うつ気分、幻覚、妄想、作為体験、精神運動興奮、自閉、自発性減退等の各種症状に効果を示す。(2)本剤は使用成績調査等の副作用発現頻度が明確となる調査を実施していないため、発現頻度については文献、自発報告等を参考に集計した。主な副作用は、過敏症状、光線過敏症、白血球減少症、顆粒球減少症、血小板減少性紫斑病、肝障害、血圧降下等であった。(3)重大な副作用:悪性症候群(Syndrome malin)、突然死、再生不良性貧血、無顆粒球症、白血球減少、麻痺性イレウス、遅発性ジスキネジア、抗利尿ホルモン不適合分泌症候群(SIADH)、眼障害、SLE様症状、肺塞栓症、深部静脈血栓症があらわれることがある。販売名和 名ニューレプチル錠5mg、ニューレプチル錠10mg、ニューレプチル錠25mg、ニューレプチル細粒10%、ニューレプチル内服液1%洋 名Neuleptil名称の由来neuroleptics(神経弛緩剤)に由来する。一般名和 名(命名法)プロペリシアジン(JAN)洋 名(命名法)Propericiazine(JAN), Periciazine(INN)ステム抜粋:ニューレプチル・インタビューフォーム臨床精神薬理(Vol.23 No.3(Mar) 特集:新規抗精神病薬blonanserinテープ製剤とは
2022.10.25
コメント(0)
-
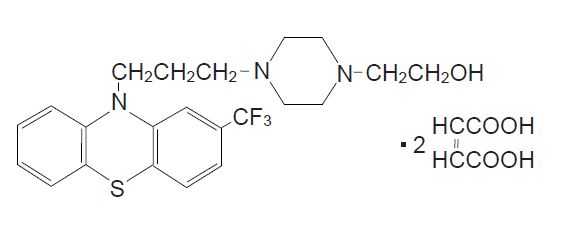
フェノチアジン系抗精神病薬(ピペラジン側鎖):フルフェナジンマレイン酸塩(フルメジン)
承認年1960年開発の経緯最初は色素の合成染料として合成されたフェノチアジンの誘導体が抗ヒスタミン薬として使用された。その後より強力な催眠・鎮痛・降温効果を持つ中枢性の自律神経安定剤として,フランスのローヌ・プーラン社(現サノフィ・アベンティス社)によりフェノチアジン誘導体のクロルプロマジンが合成され,精神神経安定剤として使用されるようになった。更に研究が進み,側鎖のピペラジン化と置換基のハロゲン化により錐体外路系副作用は起こしやすいものの,催眠・自律神経系副作用は弱く,用量力価が高い鋭利型薬物としてフルフェナジンが登場し,1958 年以降臨床に応用されるようになった。本剤は1960 年10 月に承認され,1960 年10 月に糖衣錠(0.25,0.5,1)の販売を開始し,1961年4 月に散0.2%の販売を開始した。その後1973 年11 月21 日に医薬品再評価結果その1 において「有用性が認められるもの」と判定された。また,1997 年6 月5 日の神経症に対する有効性についての再評価結果に基づき効能・効果の一部を変更した。製品の治療学的特性・製剤学的特性(1)フルメジンはフェノチアジン系の精神神経安定剤で,統合失調症に用いられる。(2)重大な副作用としてSyndrome malin(悪性症候群),無顆粒球症,白血球減少,麻痺性イレウス,抗利尿ホルモン不適合分泌症候群(SIADH),遅発性ジスキネジア,眼障害,肺塞栓症,深部静脈血栓症があらわれることがある。また,類薬の重大な副作用として突然死,再生不良性貧血,SLE 様症状があらわれることが報告されている。販売名和 名フルメジン糖衣錠(0.25)、フルメジン糖衣錠(0.5)、フルメジン糖衣錠(1)、フルメジン散0.2%洋 名FLUMEZIN SUGAR-COATED TABLETS & POWDER 0.2%名称の由来一般名から一般名和 名(命名法)フルフェナジンマレイン酸塩(JAN)洋 名(命名法)Fluphenazine Maleate(JAN)ステム不明抜粋:フルメジン・インタビューフォームSWNS-J手引き 抗精神病薬治療下主観的ウェルビーイング評価尺度短縮 [ 下平美智代 ]
2022.10.19
コメント(0)
-
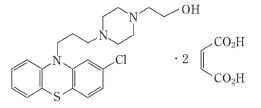
フェノチアジン系抗精神病薬(ピペラジン側鎖):ペルフェナジン(ピーゼットシー)
承認年1959年開発の経緯フランスのローヌ・プーラン社(現:サノフィ・アベンティス社)が開発したクロルプロマジンが1953 年以来,向精神薬として臨床に用いられるようになった。その後主としてフェノチアジンの2 位の置換基と10 位の側鎖の構造変換の研究が進められ,1956 年Cusic によりペルフェナジンが合成された。当社ではピーゼットシーの商標名で1958 年に糖衣錠,1960 年に散の販売を開始し,1973 年11 月21 日医薬品再評価結果その1 にて再評価結果通知を受け,現在に至る。散は2002 年3月に,糖衣錠は2003 年2 月に販売名変更に伴う再承認を受け,散は2002 年7 月に変更銘柄名にて,糖衣錠は2003 年7 月に新販売名にて薬価収載された。製品の治療学的特性・製剤学的特性ピーゼットシーはフェノチアジン系の精神神経安定剤で,統合失調症,術前・術後の悪心・嘔吐,メニエル症候群(眩暈,耳鳴)に用いられる。重大な副作用として,Syndrome malin(悪性症候群),突然死,無顆粒球症,白血球減少,麻痺性イレウス,遅発性ジスキネジア,眼障害,SLE 様症状,肺塞栓症,深部静脈血栓症があらわれることがある。また,類薬の重大な副作用として抗利尿ホルモン不適合分泌症候群(SIADH),再生不良性貧血があらわれることが報告されている。販売名和 名ピーゼットシー糖衣錠2mg、ピーゼットシー糖衣錠4mg、ピーゼットシー糖衣錠8mg、ピーゼットシー散1%洋 名糖衣錠:PZC SUGAR-COATED TABLETS散:PZC POWDER 1 %名称の由来一般名(Perphenazine)より一般名和 名(命名法)糖衣錠:ペルフェナジンマレイン酸塩(JAN)散:ペルフェナジンフェンジゾ酸塩(JAN)洋 名(命名法)糖衣錠:Perphenazine Maleate(JAN)散:Perphenazine Fendizoate(JAN)ステム不明ペルフェナジンマレイン酸塩ペルフェナジンフェンジゾ酸塩抜粋:ピーゼットシー・インタビューフォームココロピルブック 抗精神病薬・抗うつ薬・抗不安薬・睡眠薬・気分安定薬 [ 相田くひを ]
2022.10.12
コメント(0)
-
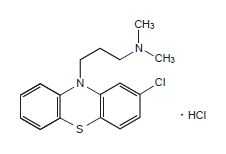
フェノチアジン系抗精神病薬(プロピル側鎖):クロルプロマジン塩酸塩(コントミン)
承認年1955年開発の経緯フランスのローヌ・プーラン社(現:サノフィ・アベンティス社)の一連のフェノチアジン系化合物の研究の結果得られた薬品で,1950 年Charpentier により合成された。同社では,初め抗ヒスタミン作用を示すエチレンジアミン系の10-dimethylaminoethylphenothiazine を合成し,10 位の側鎖を延長してpropylamino 基を導入することにより精神安定作用を有することが分かり,更に同族体の探求の結果,クロルプロマジンが発見されるに至った。本品の薬理作用は4560R.P.として研究され,1952 年Largactil として発売,第7 改正日本薬局方から収載されている1。当社では,コントミンの商標名で1955 年より販売を開始し,1973 年11 月21 日に医薬品再評価結果その1 において「有用性が認められるもの」と判定された。また,1997 年6 月5 日の神経症に対する有効性についての再評価結果に基づき効能・効果の一部を変更した。また,「医療事故を防止するための医薬品の表示事項及び販売名の取扱いについて」(2000 年9 月19 日医薬発第935 号)に基づき,2002 年2 月に販売名を現販売名に変更した。製品の治療学的特性・製剤学的特性(1)コントミンはフェノチアジン系の精神神経安定剤で,統合失調症,躁病,神経症における不安・緊張・抑うつ,悪心・嘔吐,吃逆,破傷風に伴う痙攣,麻酔前投薬,人工冬眠,催眠・鎮静・鎮痛剤の効力増強に用いられる。(2)重大な副作用として,Syndrome malin(悪性症候群),突然死,心室頻拍,再生不良性貧血,溶血性貧血,無顆粒球症,白血球減少,麻痺性イレウス,遅発性ジスキネジア,遅発性ジストニア,抗利尿ホルモン不適合分泌症候群(SIADH),眼障害,SLE 様症状,肝機能障害,黄疸,横紋筋融解症,肺塞栓症,深部静脈血栓症があらわれることがある。販売名和 名コントミン糖衣錠12.5mg、コントミン糖衣錠25mg、コントミン糖衣錠50mg、コントミン糖衣錠100mg洋 名CONTOMIN SUGAR-COATED TABLETS12.5mg,25mg,50mg,100mg名称の由来コンコンと眠る、TOMIN→ヨシトミのアミン一般名和 名(命名法)クロルプロマジン塩酸塩(JAN)洋 名(命名法)Chlorpromazine Hydrochloride(JAN)、Chlorpromazine(INN)ステム不明抜粋:コントミン・インタビューフォーム予測して防ぐ抗精神病薬の「身体副作用」 Beyond dopamine antagonis [ 長嶺敬彦 ]
2022.10.05
コメント(0)
-
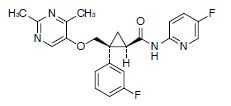
オレキシン受容体拮抗薬:レンボレキサント(デエビゴ)
承認年2020年開発の経緯デエビゴ錠(一般名:レンボレキサント)は、エーザイ株式会社が創製した新規化合物であり、オレキシン受容体の2種のサブタイプ(オレキシン1受容体[OX1R]、オレキシン2受容体[OX2R])に対してオレキシンと競合的に拮抗するアンタゴニスト(dual orexin receptor antagonist:DORA)である。オレキシン作動性神経は、覚醒維持にかかわる神経系に広く投射しており、睡眠・覚醒の主要な調節因子と考えられるオレキシンがオレキシン受容体と結合することにより活性化すると考えられ。オレキシン受容体にはOX1RとOX2Rの2種のサブタイプが存在し、近年の基礎研究では、OX2Rの方が睡眠・覚醒リズムの調節や覚醒からREM睡眠、non-REM睡眠への移行に、より重要な役割を担っていることが示唆されているが、生理的には両方の受容体が睡眠・覚醒の制御に関与しているとされている。本剤は、OX1R及びOX2Rの両者への結合を競合的かつ可逆的に阻害することで、不眠症患者の覚醒を抑制し正常な睡眠を促すものと期待され、不眠症治療薬として開発された。本剤の臨床開発は、不眠症患者を対象とした海外第Ⅱ相プラセボ対照比較試験(用量反応試験)[外国201試験]及び2つの海外第Ⅲ相試験(国際共同第Ⅲ相プラセボ対照比較試験[国際共同303試験]、海外第Ⅲ相プラセボ/ ゾルピデムER対照比較試験[外国304試験])の成績に基づき有効性及び安全性が検討された。これらの試験成績に基づき、本剤は2020年1月に「不眠症」を効能又は効果として、デエビゴ錠2.5mg、5mg、10mgの製造販売承認を取得した。製品の治療学的特性・製剤学的特性(1) 2種のオレキシン受容体サブタイプ(OX1R及びOX2R)の両者に対し、競合的かつ可逆的拮抗作用を有するオレキシン受容体拮抗剤である。OX1R:オレキシン1受容体、OX2R:オレキシン2受容体(2) OX1R及びOX2Rの両者に親和性を示し、結合及び解離を示した(in vitro )。(3) 不眠症患者に対するレンボレキサント投与により、主観的評価及び客観的評価による睡眠潜時及び中途覚醒時間の短縮が認められた。国際共同第Ⅲ相プラセボ対照比較試験[国際共同303試験]海外第Ⅲ相プラセボ/ゾルピデムER対照比較試験[外国304試験](4) 不眠症患者に対するレンボレキサント投与により、客観的評価による夜間後半部分の中途覚醒時間の短縮が認められた。海外第Ⅲ相プラセボ/ゾルピデムER対照比較試験[外国304試験](5) 不眠症患者を対象とした国際共同第Ⅲ相試験において、本剤が投与された884例(日本人155例を含む)中249例(28.2%)に副作用が認められた。主な副作用は、傾眠95例(10.7%)、頭痛37例(4.2%)、倦怠感27例(3.1%)等であった。(承認時)販売名和 名デエビゴ錠 2.5mg、5mg、10mg洋 名Dayvigo Tablets 2.5mg,5mg,10mg名称の由来Day(日中)+Vigor(活力)+Go(ready to go)が名称の由来である。一般名和 名(命名法)レンボレキサント(JAN)洋 名(命名法)Lemborexant(JAN)lemborexant(INN)ステムオレキシン受容体拮抗薬:-orexant抜粋:デエビゴ・インタビューフォーム不眠症のための睡眠薬と精神安定剤 (2) [睡眠薬編] 市販薬を含む睡眠薬との適切な付き合いかた【電子書籍】[ 福西勇夫 ]
2022.09.28
コメント(0)
-
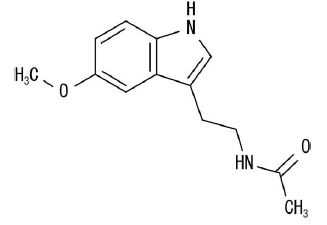
メラトニン製剤:メラトニン(メラトベル)
承認年2020年開発の経緯メラトベル®顆粒小児用 0.2 %%(本剤)は 、 日本で初めて、 内因性 ホルモンと 同一の化学構造式を持つ メラトニンを有効成分と した 入眠改善剤 である。内因性メラトニンは、トリプトファンからセロトニンを経て合成され、 2 つのメラトニン受容体 サブタイプ MT 1 及び MT 2 によって睡眠に対する作用を発揮していることが知られてい る。 MT 1 受容体の活性化は催眠に関与し、 MT 2 受容体の活性化は視床下部の視交叉上核によって制御される 睡眠・覚醒を含む概日リズム の維持・調整に 関与 する 。神経発達症は、知的能力障害群、コミュニケーション症群、自閉スペクトラム症、注意欠如・多動症、限局性学習症、運動症群及び他の神経発達症群の 7 つの診断分類で構成され 、しばしば併発する。神経発達症に伴う睡眠障害の臨床において特に注意すべき点は、慢性的な睡眠不足と不規則な睡眠覚醒リズムの問題である。睡眠不足がある場合、小児では多動や過活動、興奮症状を示すことが多く、また、睡眠の問題は神経発達症の特性を強め、困りごとを大きくすることがある。さらにそのことによって、また睡眠の問題が悪化するという悪循環を伴う 3 。以 上のように、神経発達症と睡眠障害は双方向の関係にあり、神経発達症の特性が睡眠障害を発症・増悪させている場合は神経発達症の治療を優先し、睡眠障害が神経発達症の症状を悪化させている場合は睡眠障害の状態に応じた治療を優先するというのが、基本的な治療方針となっている。しかしながら 、国内に「小児期の神経発達症に伴う睡眠障害 」 に対する医薬品は承認・販売されていないことから、本剤の開発が進められた。2013年より臨床試験を開始し、 2016 年には神経発達症のうち自閉スペクトラム症を有する睡眠障害の小児を対象とした国内第 相試験( NPC 15 5 試験)及び神経発達症を有する睡眠障害の小児を対象とした 26 週間投与の国内第相試験( NPC 15 6 試験)を実施し 、有効性と安全性が 検証された 。なお、2019 年 1 月には日本小児神経学会より厚生労働大臣宛に、「神経発達症に伴う睡眠障害に対するメラトニンの早期承認」についての要望書が提出された。これらの臨床試験の結果を踏まえてノーベルファーマ株式会社が 2019 年 4 月に製造販売承認申請を行い、 本剤が2020 年 3 月に「小児期の神経発達症に伴う入眠困難 の改善 」の効能又は効果で承認された。製品の治療学的特性・製剤学的特性(1) メラトベル®顆粒小児用0.2%は、日本で初めて、内因性ホルモンと同一の化学構造式を持つメラトニンを有効成分とした入眠改善剤である。(2) 本剤は、主に視交叉上核によって制御される睡眠・覚醒を含む概日リズムの維持・調整に関与することにより、入眠潜時(入床から入眠するまでの時間)を短縮する。(3) 本剤は、「小児期の神経発達症に伴う入眠困難の改善」の効能又は効果を有する医薬品として有効性と安全性が示された。(4) 本剤の承認された用法及び用量は、「通常、小児にはメラトニンとして1日1回1mgを就寝前に経口投与する。なお、症状により適宜増減するが、1日1回4mgを超えないこと。」である。(5) 本剤の投与対象となる睡眠障害の分類は、DSM-5における「不眠障害の入眠困難」及び「概日リズム睡眠‒覚醒障害群の睡眠相後退型」、 又は、ICSD-3における「不眠症の慢性不眠障害における入眠困難」及び「概日リズム睡眠・覚醒障害群の睡眠・覚醒相後退障害」である。(6) 国内臨床試験における主な副作用(発現率1.0%以上)は、傾眠4.2%(13/308例)、頭痛2.6%(8/308例)及び肝機能検査値上昇1.3%(4/308例)であった。 副作用については、添付文書の副作用の項及び臨床成績の項の安全性の結果を参照すること。販売名和 名メラトベル®顆粒小児用 0.2洋 名Melatobel® granules 0.2 for pediatric名称の由来メラトニンとノー ベル ファーマを組み合わせたものである。一般名和 名(命名法)メラトニン(JAN)洋 名(命名法)Melatonin(JAN)ステム不明抜粋:メラトベル・インタビューフォーム不眠症のための睡眠薬と精神安定剤 (1) [不眠症解説編] ストレス、うつ病など不眠の原因と症状、改善法【電子書籍】[ 福西勇夫 ]
2022.09.21
コメント(0)
-

オレキシン受容体拮抗薬:スポレキサント(ベルソムラ)
承認年2014年開発の経緯1998 年に櫻井 武ら、及びde Lecea L らによりほぼ同時に同定されたオレキシン1)2)は覚醒/睡眠を調整する重要な神経伝達物質である。3)オレキシン産生ニューロンの細胞体は視床下部に局在し、その軸索を脳内の覚醒系神経核に密に投射し、活性化させることで覚醒を維持している。3)また、動物実験では、摂食行動、報酬系、情動及び自律神経系の制御等、様々な機能への関与も示唆されている。3)Merck Sharp & Dohme Corp., a subsidiary of Merck & Co., Inc., Whitehouse Station, N.J., U.S.A.では、High Throughput Screening(HTS)により、2 種のオレキシン受容体(OX1R 及びOX2R)に拮抗作用を持つジアゼパン誘導体を2005 年に見出した。この誘導体をリード化合物として、代謝安定性に優れ、オレキシン受容体に対し高い選択性及び結合親和性を持つスボレキサントを合成した。従来の睡眠薬はGABAA 受容体又はメラトニン受容体に作用するのに対し、本剤は、OX1R 及びOX2R の選択的拮抗薬として作用し、オレキシンニューロンの神経支配を受けている覚醒神経核を抑制することで睡眠を誘導する。その後、国内外でランダム化比較試験を含む臨床試験が実施された。本剤は2014 年9 月に不眠症に対する有用性が認められわが国で承認を取得した、世界初のオレキシン受容体拮抗薬である。本邦においては、スボレキサントの臨床用量を成人には1 日1 回20 mg、高齢者には1 日1 回15mg として2014 年9 月にベルソムラ®錠15 mg 及びベルソムラ®錠20 mg の不眠症に対する適応を取得した。一方で、本剤と中等度のCYP3A 阻害剤(ジルチアゼム、ベラパミル、フルコナゾール等)との併用時には本剤の減量が必要な場合が想定されることを踏まえ、10 mg 錠の開発を行い、ベルソムラ®錠10 mg が2016 年9 月に承認された。製品の治療学的特性・製剤学的特性(1) 治療学的特性1.覚醒を促進するオレキシンの受容体への結合を阻害する、世界初のオレキシン受容体拮抗薬である(in vitro)。2.脳を覚醒から睡眠へ移行させ、生理的なプロセスによる睡眠をもたらす(ラット、イヌ、サル)。3.投与1 週時、1 ヵ月時、3 ヵ月時の時点において、入眠障害、中途覚醒に対して効果が認められている。4.主な副作用は、傾眠、頭痛、疲労であった。(2) 製剤学的特性楕円形(15 mg)、円形(10 mg 及び20 mg)のフィルムコーティング錠である。販売名和 名ベルソムラ®錠10 mg、ベルソムラ®錠15 mg、ベルソムラ®錠20 mg洋 名Belsomra® Tablets 10 mg、Belsomra® Tablets 15 mg、Belsomra® Tablets 20 mg名称の由来一般名和 名(命名法)スボレキサント(JAN)洋 名(命名法)Suvorexant(JAN)、suvorexant(INN)ステムオレキシン受容体拮抗薬:-orexant抜粋:ベルソムラ・インタビューフォーム 内科医のための睡眠薬の使い方 [ 松浦雅人 ]
2022.09.14
コメント(0)
-
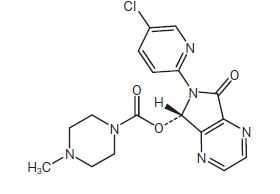
非ベンゾジアゼピン系睡眠薬(超短期型):エスゾピクロン(ルネスタ)
承認年2012年開発の経緯ルネスタⓇ錠(一般名:エスゾピクロン)は、ラセミ体であるゾピクロンを光学分割して得られたS体のエスゾピクロンの製剤であり、セプラコール社(現サノビオン社)により開発されたイオンチャネル型γ⊖アミノ酪酸(Gamma Amino Butyric Acid:GABA)受容体作動薬である。エスゾピクロンは、非臨床試験から、GABAA受容体への結合を介した催眠作用、鎮静作用及び抗不安作用を有すること、加えてゾピクロンの薬理活性の大部分を有することが明らかになった。外国では、種々の不眠症を対象とした臨床試験が実施され、原発性と併発性のいずれの不眠症に対しても、入眠障害及び中途覚醒に有効であることが示された。また、投与期間に関わらず臨床的に問題となる副作用(依存性、持ち越し効果等)は認められなかった。長期投与による耐性の形成、投与離脱時の退薬症候や反跳性不眠も認められなかったことから、米国では睡眠薬として初めて投与期間に関する制限なしで承認された(2004年12月承認取得、販売名「LUNESTAⓇ」として、2005年から販売)。このように、本剤は様々な不眠症の入眠障害及び中途覚醒に有効で、長期に投与した場合でも注意すべき副作用のリスクが少ない睡眠薬と考えられた。本剤は、これらの特徴を有する非ベンゾジアゼピン系睡眠薬として期待され、国内で開発するに至り、2012年1月ルネスタ錠1mg、錠2mg、錠3mgとして、「不眠症」の効能・効果で製造販売承認を取得した。製品の治療学的特性・製剤学的特性(1) 中枢神経系のGABAA受容体複合体に結合し、GABAの効果を増強して催眠作用および鎮静作用を発揮する不眠症治療薬である。(2)ゾピクロンを光学分割して得られた、ゾピクロンの薬理活性の大部分を有するS体である。(3) 不眠症の主症状である入眠障害と中途覚醒のいずれにも有効である。(4) 原発性と併発性のいずれの不眠症にも有効である。(5) 承認時までに、国内並行群間比較試験において認められた主な副作用は、味覚異常、傾眠であった。また、外国並行群間比較試験において認められた主な副作用は、味覚異常、頭痛、傾眠、浮動性めまいであった。なお、重大な副作用として、ショック、アナフィラキシー、依存性、呼吸抑制、肝機能障害、精神症状、意識障害、一過性前向性健忘及びもうろう状態がある。販売名和 名ルネスタⓇ錠1mg、ルネスタⓇ錠2mg、ルネスタⓇ錠3mg洋 名LunestaⓇTablets 1mg、LunestaⓇTablets 2mg、LunestaⓇTablets 3mg名称の由来米国で‘LUNESTAⓇ’の製品名で販売されていることから、国内の販売名を「ルネスタⓇ」とした。なお、Luna(=月)+Star(=星)が、米国の販売名Lunestaの由来となっている。一般名和 名(命名法)エスゾピクロン(JAN)洋 名(命名法)Eszopiclone(JAN)ステム催眠鎮静剤:-clone抜粋:ルネスタ・インタビューフォーム ココロピルブック 抗精神病薬・抗うつ薬・抗不安薬・睡眠薬・気分安定薬 [ 相田くひを ]
2022.09.07
コメント(0)
-
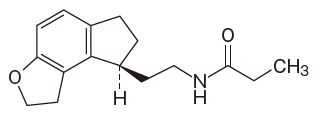
メラトニン受容体作動薬:ラメルテオン(ロゼレム)
承認年2000年開発の経緯メラトニンは睡眠覚醒リズムに関与するメラトニン受容体1 型(MT1 受容体)及びメラトニン受容体2 型(MT2 受容体)に作用し、睡眠中枢を優位に導くことで睡眠を誘発し、副交感神経を優位に保つことにより自律神経を抑制する。このように、メラトニンによる催眠作用は覚醒中枢の抑制によるものではなく、視交叉上核を介して間接的に睡眠中枢を賦活、すなわち、覚醒中枢と睡眠中枢の優位性を変化させることによるものであると考えられている。当社研究所では、メラトニン受容体作動薬の開発に着手し、動物試験において、MT1 及びMT2 受容体に選択的に作用し、睡眠誘発作用を示す新規メラトニン受容体作動薬ラメルテオンを見出した。以後、国内外で二重盲検比較試験を含む臨床試験を実施し、米国で2005 年7 月にROZEREM tablets として「入眠困難の特徴を有する不眠症」の効能・効果で承認を得た。国内において、「向精神薬」「注意−習慣性あり」に該当しない医薬品として「不眠症における入眠困難の改善」の効能・効果で2010 年4 月に製造販売承認を得た。2019 年6 月に再審査結果が公表され、有用性が再確認された。製品の治療学的特性・製剤学的特性(1) 新しいメカニズムの不眠症における入眠困難の改善薬。メラトニン受容体アゴニストである。(in vitro )(2)睡眠−覚醒リズムに働きかけ、鎮静作用や抗不安作用によらない睡眠をもたらす。(3)優れた睡眠導入効果が認められ、全睡眠時間の改善が認められている。(4) 本剤単剤で実施された国内の長期投与試験で、反跳性不眠の指標となる投与終了後の自覚的睡眠潜時は延長せず、退薬症候の指標となるベンゾジアゼピン退薬症候質問票(BWSQ)のスコアの悪化はみられなかった。(5) 承認時までのわが国での臨床試験では1 日1 回ラメルテオンとして4mg、8mg、16mg 又は32mg が投与された1,864 例中の194 例(10.4%)に臨床検査値の異常を含む副作用が認められた(承認用量は8mg である)。主な副作用は傾眠(3.4%)、頭痛(1.0%)、倦怠感(0.5%)、浮動性めまい(0.5%)であった。製造販売後の調査では1 日1 回ラメルテオンとして8mg が投与された3,223 例中の109例(3.4%)に副作用が認められた。主な副作用は傾眠(1.2%)、浮動性めまい(0.7%)、倦怠感(0.3%)であった。うち、精神疾患の既往又は合併のある患者では727 例中の40 例(5.5%)に、精神疾患の既往及び合併のない患者では2,361 例中の64 例(2.7%)に副作用が認められた。精神疾患の既往又は合併のある患者での主な副作用は傾眠(2.2%)、浮動性めまい(1.1%)であり、精神疾患の既往及び合併のない患者での主な副作用は傾眠(0.9%)、浮動性めまい(0.4%)であった。なお、重大な副作用としてアナフィラキシー(蕁麻疹、血管浮腫等)※があらわれることがある。販売名和 名ロゼレム® 錠8mg洋 名ROZEREM® Tablets 8mg.名称の由来「健やかな眠りを取り戻し、ばら色の夢を見ましょう」との願いをこめてRose REM から名づけられた。一般名和 名(命名法)ラメルテオン(JAN)洋 名(命名法)Ramelteon(JAN)、ramelteon(INN)ステムメラトニン受容体アゴニスト:− melteon抜粋:ロゼレム・インタビューフォーム 不眠症のための睡眠薬と精神安定剤 (1) [不眠症解説編] ストレス、うつ病など不眠の原因と症状、改善法【電子書籍】[ 福西勇夫 ]
2022.08.31
コメント(0)
-

非ベンゾジアゼピン系睡眠薬(超短期型):ゾルピデム酒石酸塩(マイスリー)
承認年2000年開発の経緯中枢神経系にはベンゾジアゼピン(以下、BZD と略す)に高い親和性を示す部位が存在し、BZD 受容体と命名された。しかし、その後の研究でBZD 受容体には、BZD 以外の構造を持つ化合物の中にも高い親和性を示すものもあることが判明したため、“BZD”と化学構造で規定する名称は好ましくないとして、1988 年Langer and Arbilla は、オメガ(ω)受容体に改称することを提唱した。中枢のω 受容体には2 つのサブタイプが存在し、それぞれω1、ω2 受容体と呼ばれる。ω1、ω2 受容体の脳内分布は異なり、ω1 受容体が小脳、嗅球、淡蒼球、大脳皮質第4 層等に多いのに対して、ω2 受容体は筋緊張に関与する脊髄や記憶に関与する海馬に多く、したがって関与する生理的機能も異なるとされている。BZD 系睡眠薬は一般にω1、ω2 受容体に対する選択性が低いため、催眠鎮静作用、抗痙攣作用、抗不安作用及び筋弛緩作用の間の分離が悪いと考えられ、ω1ないしω2受容体に選択的な親和性を有する化合物は、これら作用の間の分離ができる可能性が考えられ、ω 受容体サブタイプに選択的に作用する薬剤の開発が待たれていた。フランスのSynthelabo 社(現 Sanofi)では、ω 受容体のサブタイプに選択的に作用する薬剤を開発するために、BZD 構造とは異なるイミダゾピリジンをプロトタイプとして1979 年より研究を開始し、1980 年ゾルピデムを発見した。ゾルピデムはω1 に特異性が高く、動物実験で選択的な催眠鎮静作用を示すことから、催眠鎮静剤として、BZD 系睡眠薬の欠点が改良される可能性が示唆され、1982 年より臨床試験が開始された。その結果、BZD 系睡眠薬とは異なる特徴及び有用性が確認され、フランスでは1987 年6 月に承認された。我が国では、1987 年5 月より開発が始められ、不眠症(統合失調症及び躁うつ病に伴う不眠症は除く)に対する有用性が認められ、2000 年9 月承認を取得した。その後、平成19 年8 月6 日付薬食審査発第0806001 号「我が国における一般的名称の変更について(その1)」に基づき、一般的名称を酒石酸ゾルピデムから、「ゾルピデム酒石酸塩」に変更した。2011 年4 月に、ゾルピデム酒石酸塩錠として第16 改正日本薬局方(2011)より収載された。2015 年6 月現在、フランス、米国をはじめ100 ヵ国以上で承認されている。製品の治療学的特性・製剤学的特性(1)ゾルピデムは非ベンゾジアゼピン構造を有し、ω1 受容体に選択的に作用する。(2)速効性の超短時間型睡眠薬である。(3)選択的な催眠鎮静作用を有し、しかも生理的睡眠パターンに近い睡眠をもたらす。(4)入眠障害、熟眠障害のみならず、作用持続時間が短いにもかかわらず途中覚醒、早朝覚醒にも効果を示し、翌朝までの持ち越し効果が少ない。また、反復投与しても耐薬性、依存性が形成されにくく、増量なしで長期間安定した作用を示す。(5)重大な副作用として、依存性、離脱症状、精神症状、意識障害、一過性前向性健忘、もうろう状態、睡眠随伴症状(夢遊症状等)、呼吸抑制、肝機能障害、黄疸があらわれることがある。販売名和 名マイスリー錠5mg、マイスリー錠10mg洋 名Myslee Tablets 5mg・10mg名称の由来MY SLEEP の下線部をとってMyslee と命名した。一般名和 名(命名法)ゾルピデム酒石酸塩 (JAN)洋 名(命名法)Zolpidem Tartrate (JAN) Zolpidem (INN)ステムゾルピデム誘導体、催眠鎮静剤:-pidem抜粋:マイスリー・インタビューフォーム 精神科の薬-抗精神病薬・抗うつ薬・睡眠薬・抗認知症薬…-はや調べノート これだけは押さえておきたい 薬がわかる!ケアにいかせる!/杉田尚子/諏訪太朗/村井俊哉【3000円以上送料無料】
2022.08.24
コメント(0)
-
ベンゾジアゼピン系睡眠薬(長時間型):クアゼパム(ドラール)
承認年1999年開発の経緯クアゼパムは,米国シェリング・プラウ社で1971年に合成された1位にトリフルオロエチル基を有するベンゾジアゼピン系薬物で,中・長時間型薬剤に分類される睡眠障害改善剤である。米国をはじめとした諸外国で実施された臨床試験で不眠症に対する有効性が認められており,本邦では,エスエス製薬で1986年から第Ⅰ相試験が開始され,1987年に第Ⅱ相試験,1988年に第Ⅲ相試験が順次行われ,1999年6月16日に承認を取得し発売するに至った。なお,本剤は2005年4月1日に久光製薬がエスエス製薬から製造販売承認を承継している。また,発売後3,925例の使用成績調査,303例の長期使用調査(特定使用成績調査)を実施し,2005年9月に再審査申請を行った。その結果,2008年10月に薬事法第14条第2項第3号イからハまで(承認拒否事由)のいずれにも該当しないとの再審査結果を得られ,「効能又は効果」並びに「用法及び用量」は承認事項のとおり変更はない旨通知された(2008年10月)。製品の治療学的特性・製剤学的特性(1)ベンゾジアゼピン1受容体へ選択的に作用する(ラット)。(2)睡眠障害の各種症状(熟眠障害,中途覚醒,早朝覚醒,入眠障害)に効果を示す。(3)麻酔前投薬(手術前夜睡眠)に効果を示す。(4)血中濃度半減期が36.6時間で、中・長時間作用型に分類される。(5)臨床試験の安全性評価対象症例495 例中,副作用が報告されたのは52例(10.5%)で,その主なものは眠気・傾眠30件(6.1%),ふらつき18件(3.6%),頭重感7件(1.4%),倦怠感5件(1.0%)等であった。(承認時)製造販売後調査の安全性評価対象症例3,925例中,副作用が報告されたのは140例(3.6%)で,その主なものは傾眠50件(1.3%),浮動性めまい46件(1.2%),悪心8件(0.2%),倦怠感8件(0.2%)等であった。(再審査終了時)重大な副作用として,依存性,刺激興奮,錯乱,呼吸抑制,炭酸ガスナルコーシス,精神症状(幻覚,妄想等),意識障害,思考異常,勃〇障害,興奮,運動失調,運動機能低下,協調異常,言語障害,振戦,一過性前向性健忘,もうろう状態があらわれることがある。販売名和 名ドラール®錠15、ドラール®錠20洋 名DORAL® TABLETS名称の由来該当資料なし一般名和 名(命名法)クアゼパム(JAN)洋 名(命名法)Quazepam(JAN,INN)ステム抜粋:ドラール・インタビューフォーム 不眠症のための睡眠薬と精神安定剤 (2) [睡眠薬編] 市販薬を含む睡眠薬との適切な付き合いかた【電子書籍】[ 福西勇夫 ]
2022.08.17
コメント(0)
-

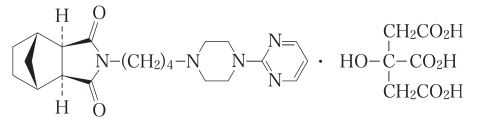
セロトニン1A部分作動薬:タンドスピロンクエン酸塩(セディール)
承認年1996年開発の経緯セディールは、非ベンゾジアゼピン系の抗不安薬で、セロトニン神経系に選択的に作用する。当社は、アザピロン誘導体の作用特性について検討を行い、合成と薬理学的研究により、1980 年、D2 受容体やα1 受容体に感受性が弱く同時に5-HT1A 受容体に選択性の高い (1R*, 2S*, 3R*, 4S*)-N-[4-[4-(2-pyrimidinyl)-1-piperazinyl] butyl]-2, 3-bicyclo[2.2.1]heptanedicarboximide dihydrogen citrate(タンドスピロンクエン酸塩)を得た。本剤は心身症(自律神経失調症、本態性高血圧症、消化性潰瘍)における身体症候ならびに抑うつ、不安、焦躁、睡眠障害及び神経症における抑うつ、恐怖に対して臨床上有用であることが認められ、1996 年にアザピロン誘導体としては本邦で初めて承認された。市販後に5132 例の使用成績調査を実施し、2002 年10 月に再審査申請を行った結果、2005 年3 月に事法第14 条第2 号各号(承認拒否事由)のいずれにも該当しないとの再審査結果を得た。また、2006 年9 月には「セディール錠20mg」の販売を開始した。なお、「セディール錠5」、「セディール錠10」は、医療事故防止対策の一環として、2007 年2 月にそれぞれ、「セディール錠5mg」、「セディール錠10mg」に名称変更した。製品の治療学的特性・製剤学的特性(1)タンドスピロンはセロトニン神経系に選択的に作用し、従来のベンゾジアゼピン系誘導体とは異なった作用機序により抗不安作用及び抗うつ作用を示す。(2)動物実験における薬物依存性の検討において精神依存性及び身体依存性があることを示唆する結果は認められなかった。さらにバルビタールあるいはジアゼパムとの交差依存性も認められなかった。(3)α1 受容体やD2 受容体に対する親和性が弱いことがin vitro で認められている。(4)重大な副作用として、肝機能障害、黄疸、セロトニン症候群、悪性症候群が報告されている。販売名和 名セディール錠5mg、セディール錠10mg、セディール錠20mg洋 名Sediel名称の由来ラテン語で「安静」の意味。一般名和 名(命名法)タンドスピロンクエン酸塩(JAN)洋 名(命名法)Tandospirone Citrate(JAN)、Tandospirone(INN)ステム-spirone anxiolytics, buspirone derivatives抜粋:セディール・インタビューフォーム 睡眠医療(Vol.14 No.2(202) 睡眠医学・医療専門誌 特集:睡眠薬・抗不安薬を安全に使いこなす,効果的に減薬する
2022.08.10
コメント(0)
-
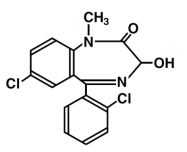
ベンゾジアゼピン系睡眠薬(短時間型):ロルメタゾラム(エバミール)
承認年1990年開発の経緯エバミール錠 1.0 は米国ワイス社(現ファイザー社)で合成されたベンゾジアゼピン系睡眠薬であり,強い鎮静作用,抗不安作用,睡眠増強作用および抗けいれん作用と比較的弱い筋弛緩作用を示し,約 10 時間の消失半減期を有する.本剤は,1975 年にドイツ連邦共和国においてシエーリングAG(現バイエル社)とワイス社との共同開発が開始され,各種臨床試験を経て,1980 年に承認された.本邦においては,1980 年より前臨床試験を,1981 年より臨床試験を開始した.その結果,本剤の睡眠導入剤としての有効性と安全性が認められ,1990年に承認を得て発売に至った.製品の治療学的特性・製剤学的特性 (1) 健常者を対照とした第Ⅰ相試験の終夜睡眠ポリグラフィーによる各睡眠段階を科学的に検討した結果,本剤はレム睡眠,ノンレム睡眠への影響が少なく生理的に自然な睡眠パターンを導入した.(2) 不眠症患者を対象とした精神科,神経科,心療内科・内科領域の第Ⅲ相二重盲検試験の結果,本剤は従来使用されている製剤と同様,優れた睡眠改善効果が認められた.また,本剤は各種不眠症(入眠障害,熟眠障害,中途・早朝覚醒)に対しても有効性が認められた.国内で実施された不眠症患者を対象とした本剤の臨床試験(990 例)の改善率は 83%であった.(やや改善を含む)(P.10~11 参照)(3) 本剤は製剤学的特性としてω1 受容体への選択性が高く,筋弛緩作用が弱い.(ラット,マウス)(4) 本剤は肝の代謝過程においてグルクロン抱合化が行われ,肝薬物代謝酵素による代謝を受けないベンゾジアゼピン系睡眠剤である.販売名和 名エバミールⓇ錠 1.0洋 名EvamylⓇ名称の由来なし一般名和 名(命名法)ロルメタゼパム(JAN)洋 名(命名法)Lormetazepam(JAN,INN)ステムジアゼパム誘導体:-azepam抜粋:エバミール・インタビューフォーム 【送料無料】精神科の薬−抗精神病薬・抗うつ薬・睡眠薬・抗認知症薬…−はや調べノート これだけは押さえておきたい 薬がわかる!ケアにいかせる!/杉田尚子/諏訪太朗/村井俊哉
2022.08.03
コメント(0)
-
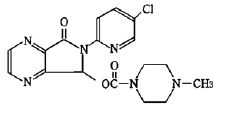
非ベンゾジアゼピン系睡眠薬(超短期型):ゾピクロン(アモバン)
承認年1989年開発の経緯臨床の場で睡眠導入剤として汎用されているベンゾジアゼピン系化合物は、臨床上入眠作用、熟眠作用有し、比較的副作用が少ないとされている。しかし、血漿中半減期の長いものが多く、排泄が比較的遅いめ昼間への持ち越し効果(ハングオーバー)をもたらし、また筋弛緩作用を有するため脱力、けん怠感など症状を伴うことがある。フランス ローヌ・プーラン社(現 サノフィ社)は、従来のベンゾジアゼピン系化合物とは異なる構造式をし、持ち越し効果や筋弛緩作用が少なく、かつ不眠症患者にみられる乱れた睡眠パターンを改善し、自然な睡眠をもたらす薬剤として、シクロピロロン系誘導体の一つであるゾピクロンを開発した。日本では1989年3月に承認を得て発売に至り、1998年3月に再審査が終了している。製品の治療学的特性・製剤学的特性1.超短時間作用型の睡眠障害改善剤2.不眠の各種症状(入眠障害、熟眠障害、中途覚醒、早朝覚醒)に優れた効果を示した。3.睡眠段階への作用深い眠り(徐波睡眠:ステージ3・4)を増加させ、レム睡眠に対する影響は少なかった。4.総症例11,677例中、831例(7.12%)、1,026件に副作用が認められた。主な副作用は、にがみ488件(4.18%)、ふらつき104件(0.89%)、眠気60件(0.51%)、口渇56件(0.48%)、けん怠感48件(0.41%)、頭重26件(0.22%)、頭痛22件(0.19%)、嘔気22件(0.19%)、不快感15件(0.13%)、めまい14件(0.12%)等であった。(再審査終了時) 重大な副作用として依存性、呼吸抑制、肝機能障害、精神症状、意識障害、一過性前向性健忘、もうろう状態、アナフィラキシーがあらわれることがある。販売名和 名アモバン®錠 7.5、アモバン®錠 10洋 名AMOBAN®Tablet 7.5、AMOBAN®Tablet 10名称の由来特になし一般名和 名(命名法)ゾピクロン(JAN)洋 名(命名法)Zopiclone(JAN, INN)ステムなし抜粋:アモバン・インタビューフォーム 内科医のための睡眠薬の使い方 [ 松浦雅人 ]
2022.07.27
コメント(0)
-
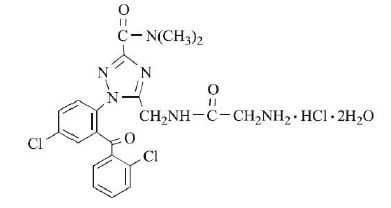
ベンゾジアゼピン系睡眠薬(短時間型)リルマザホン塩酸塩水和物(リスミー)
承認年1989年開発の経緯リルマザホン塩酸塩水和物は1974 年に塩野義製薬研究所で創製されたベンゾジアゼピン系の睡眠誘導剤であり,多数の1,4-ベンゾジアゼピン開環誘導体の中から催眠作用と筋弛緩作用の乖離度が大きく,徐波睡眠やREM 睡眠に対する影響が少ない等の特徴から選出されたものである。また本剤は,生体内で活性体である4 種の新規ベンゾジアゼピン誘導体(代謝物のM-1,M-2,M-A,M-3)となって薬理作用をあらわすプロドラッグである。1981 年から臨床試験を開始し,不眠症と麻酔前投薬において有効性及び安全性が確認され,1989 年3 月31 日に製造承認された。1989 年3 月31 日から11956 例の使用成績調査を実施し,1995 年6 月30 日に再審査申請を行った結果,1999 年3 月3 日に薬事法第14 条第2 項各号(承認拒否事由)のいずれにも該当しないとの再審査結果を得た。2016 年12 月,塩野義製薬株式会社から共和薬品工業株式会社に販売を移管した。2018 年4 月,塩野義製薬株式会社から共和薬品工業株式会社に製造販売承認が承継された。製品の治療学的特性・製剤学的特性(1) 不眠症:承認時における一般臨床試験での有効性評価対象例は224 例であり,有効率は59.8%(134 例)であった。麻酔前投薬:ニトラゼパムを対照薬とし、手術前夜及び麻酔前投薬を対象とした二重盲検比較試験において、本剤の有用性が確認された。(2) 承認時における安全性評価対象例1277 例中,副作用は319 例(24.98%)に認められた。再審査終了時における安全性評価対象例12618 例中,副作用は135 例(1.07%)に認められた。(3) 重大な副作用:呼吸抑制,刺激興奮,錯乱,一過性前向性健忘,もうろう状態があらわれることがある。炭酸ガスナルコーシスを起こすことがある。依存性を生じることがある。販売名和 名リスミー®錠1mg、リスミー®錠2mg洋 名Rhythmy®名称の由来自然の睡眠リズム(Rhythm)に近い眠りをもたらすことから,リスミー(Rhythmy)と命名された。一般名和 名(命名法)リルマザホン塩酸塩水和物(JAN)洋 名(命名法)Rilmazafone Hydrochloride Hydrate(JAN)ステムアロザフォン誘導体:-zafone抜粋:リスミー・インタビューフォーム ココロピルブック 抗精神病薬・抗うつ薬・抗不安薬・睡眠薬・気分安定薬 [ 相田くひを ]
2022.07.20
コメント(0)
-
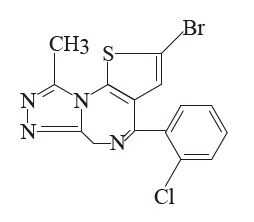
ベンゾジアゼピン系睡眠薬(短時間型)ブロチゾラム(レンドルミン)
承認年1988年開発の経緯臨床の場では睡眠導入剤として,入眠作用と熟眠作用を有し,比較的副作用の少ないベンゾジアゼピン系化合物が繁用されている。しかし,これらの薬剤のうち,排泄の遅いものは翌日に持ち越し効果 (ハングオーバー) をもたらし,逆に排泄の速いものは熟眠障害や早朝覚醒に対する効果が不十分である。ドイツベーリンガーインゲルハイム社は,持ち越し効果が少なく,かつ生理的睡眠をもたらす薬剤として,2-ブロモ-チエノトリアゾロジアゼピン誘導体であるブロチゾラムを開発した。レンドルミン錠について日本においては外国での試験成績を検討し,1980 年から開発に着手,臨床試験を実施した。その結果,不眠症治療及び麻酔前投薬に有用性が認められた。また,効果発現は速やかで、作用持続時間は生理的睡眠時間に近く,徐波睡眠,レム睡眠に対する影響はほとんど認められず,自然に近い睡眠をもたらし,覚醒時の気分は良好で翌朝への持ち越し効果が少ないことが確認された。その結果,レンドルミン錠は1988 年6 月に承認され,同年9 月に発売された。レンドルミンD錠0.25mg についてはコンプライアンスの向上を目的に口腔内崩壊錠として開発が進められ,レンドルミン錠との生物学的同等性試験が実施された結果,同等性が確認された。その結果,レンドルミンD錠0.25mg は2002 年3 月に承認され,同年7 月に発売された。その後,「医薬品関連医療事故防止対策の強化・徹底について」(平成16 年6 月2 日付 薬食発第0602009 号) による事故防止対策の観点から,レンドルミン錠については2006 年8 月に名称変更品(レンドルミン錠0.25mg) が新たに承認され,同年12 月に薬価基準に収載された。製品の治療学的特性・製剤学的特性(1) 徐波睡眠やレム睡眠への影響が少なく,熟眠感が得られます。(2) 本剤投与翌朝の視覚運動協調能力の抑制はプラセボと同等でした。(3) 不眠症の各種症状 (入眠障害,中途覚醒,早朝覚醒,熟眠障害) に優れた効果を示します。(4) 水なしでも服用できる口腔内崩壊錠が加わりました。(5) 副作用の発現率は3.91% (256 例/6,548 例) でした。レンドルミン錠 (普通錠) について,臨床試験及び再審査終了時の調査症例数6,548 例中,副作用が報告されたのは256 例 (3.91%) でした。主な副作用は,残眠感・眠気144 件 (2.20%) ,ふらつき66 件 (1.01%) ,頭重感50 件 (0.76%) ,だるさ48 件 (0.73%) ,めまい25 件 (0.38%) ,頭痛8 件 (0.12%) ,倦怠感7 件 (0.11%) 等でした。また,臨床検査値においては特に一定の傾向を示す変動は認められていません (承認時及び再審査終了時の合算集計) 。なお,重大な副作用として,肝機能障害,黄疸,一過性前向性健忘,もうろう状態,依存性が,また,類薬で呼吸抑制が報告されています。販売名和 名レンドルミン®錠0.25mg、レンドルミン®D錠0.25mg洋 名Lendormin® Tablets 0.25mg、Lendormin® D Tablets 0.25mg名称の由来眠りにつくことを意味するフランス語l’endormir に由来する。一般名和 名(命名法)ブロチゾラム (日局,JAN)洋 名(命名法)Brotizolam (日局,JAN)ステムジアゼパム誘導体(-azepam)の関連物質:-izolam抜粋:ブロチゾラム・インタビューフォーム 不眠症のための睡眠薬と精神安定剤 (1) [不眠症解説編] ストレス、うつ病など不眠の原因と症状、改善法【電子書籍】[ 福西勇夫 ]
2022.07.13
コメント(0)
-
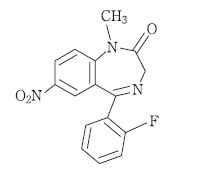
ベンゾジアゼピン系睡眠薬(中間型)フルニトラゼパム(サイレース)
承認年1983年開発の経緯フルニトラゼパムは、F. Hoffmann⊖La Roche 社で合成された一連のベンゾジアゼピン系誘導体のひとつで、薬理作用はニトラゼパムに比べ約5 倍強く、特に鎮痛剤の作用を著明に増強するという特徴が認められ、1968 年前半より西欧諸国を中心に臨床試験が開始された。以来多くの臨床成績から優れた催眠・鎮静効果が認められ、経口剤は催眠剤として、注射剤は麻酔前投薬、麻酔導入剤及び局所麻酔時の鎮静剤として、1973 年フランスにて承認・発売されてから、日本を含む世界各国で許可又は発売された。その後、サイレース錠は2014 年6 月に悪用防止を目的に青色色素を添加した処方変更を主目的とした承認事項一部変更承認申請を行い、2015 年7 月に承認された。製品の治療学的特性・製剤学的特性サイレース錠はF. Hoffmann⊖La Roche 社が開発したベンゾジアゼピン系化合物に属するフルニトラゼパム製剤で、強力な催眠・鎮静作用を有し、入眠障害、熟眠障害及び早朝覚醒などの不眠症に有効である。さらに、麻酔前投薬としても有効性が確認されている。販売名和 名サイレースⓇ 錠1mg、サイレースⓇ 錠2mg洋 名SileceⓇ Tablets 1mg、SileceⓇ Tablets 2mg名称の由来Silent(静か、鎮静)のace(達人)からサイレースと命名した。一般名和 名(命名法)フルニトラゼパム(JAN)洋 名(命名法)Flunitrazepam(JAN、INN)ステムジアゼパム誘導体:azepam抜粋:サイレース・インタビューフォーム 不眠症のための睡眠薬と精神安定剤 (2) [睡眠薬編] 市販薬を含む睡眠薬との適切な付き合いかた【電子書籍】[ 福西勇夫 ]
2022.07.06
コメント(0)
-
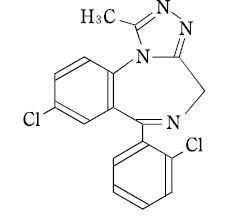
ベンゾジアゼピン系睡眠薬(超短時間型):トリアゾラム(ハルシオン)
承認年1982年開発の経緯馴化作用、鎮静作用、睡眠誘発・増強作用、抗痙攣作用及び筋弛緩作用等を示すベンゾジアゼピン系化合物は、1960 年にクロルジアゼポキサイドが、続いてジアゼパムが開発されて以来、より優れた抗不安剤及び睡眠剤を求めて、新しい置換基を持つ1,4 ベンゾジアゼピン誘導体の合成並びにスクリーニングが広くかつ精力的に行われた。その結果、ニトラゼパム、オキサゾラム、エスタゾラム、ニメタゼパム、フルラゼパム等の各種製剤が相次いで医療に供されている。睡眠剤として広く使用されているニトラゼパムは1965 年Randall らによって発表されたが、その作用は従来のバルビツレートと異なり大脳辺縁系、視床下部及び中脳網様体に作用し、不眠の原因となる過剰な刺激伝達を抑え、情動活動を低下させて睡眠導入効果を示す。しかし、ニトラゼパムはハングオーバー様の症状と考えられる覚醒時の脱力感や残眠感等、改善されるべき点を残していた。本ベンゾジアゼピン化合物、一般名トリアゾラム(triazolam)は、米国ファイザー社(旧米国アップジョン社)における一連のベンゾジアゼピン系薬剤研究開発中に発見された化合物群、トリアゾロベンゾジアゼピンの一つである。薬理作用のスペクトルはニトラゼパムに近似しているが、活性はニトラゼパム及び他のベンゾジアゼピン系化合物より強い。しかし、臨床的に問題となる宿酔感はニトラゼパム等より弱く、吸収・排泄が速いため、より自然に近い睡眠をもたらすことが臨床薬理学的に確認されている。日本においては日本アップジョン株式会社と住友化学工業株式会社の2 社共同で開発を行った。1975 年6 月より臨床試験を開始し、昭和57 年(1982 年)12 月15 日製造承認を得、1983 年4 月11日より発売を開始した。12,027 例の市販後調査を実施し、再審査申請を行った結果、1990 年9 月薬事法第14 条第2 項各号(承認拒否事由)のいずれにも該当しないとの再審査結果を得た。製品の治療学的特性・製剤学的特性(1)半減期は2.9 時間と短く、吸収・分布・代謝から排泄までの時間が速い。(2)0.125mg~0.25mg 投与で、速やかな入眠、熟眠効果が得られる。(3)副作用の発現率は2.61%(338 例/12,930 例)調査症例数12,930 例中、副作用発現症例は338 例(2.61%)であり、副作用発現件数は延べ700 件であった。その主なものは、めまい・ふらつき164 件(1.27%)、眠気155 件(1.20%)、倦怠感100 件(0.77%)、頭痛・頭重91 件(0.70%)等であった。(承認時までの調査及び市販後の使用成績調査の集計)重大な副作用として、薬物依存、離脱症状、精神症状、呼吸抑制、一過性前向性健忘、もうろう状態、肝炎、肝機能障害、黄疸、ショック、アナフィラキシーが報告されている。販売名和 名ハルシオン®0.125mg 錠、ハルシオン®0.25mg 錠洋 名Halcion® Tablets 0.125mg、Halcion® Tablets 0.25mg名称の由来風と波を静め、穏やかな海にする不思議な力を持つ古代ギリシャの伝説の鳥、Halcyon に由来している。一般名和 名(命名法)トリアゾラム(JAN)洋 名(命名法)triazolam(JAN、INN)ステム抜粋:ハルシオン・インタビューフォーム 内科医のための睡眠薬の使い方 [ 松浦雅人 ]
2022.06.29
コメント(0)
-
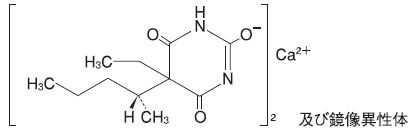
バルビツール酸系睡眠薬:ペントバルビタールカルシウム(ラボナ)
承認年1982年開発の経緯ペントバルビタールカルシウムは、1916 年Bayer 社の特許にすでに記載されているが、193年Volwiler らによりその効果が再認識され広く用いられるようになった。アメリカのAbbott 社により催眠薬としての効力が認められ、そのNa 塩が催眠、麻酔などの注射薬として開発された。一方、Ca 塩は催眠、鎮静に内服用として用いられる。製品の治療学的特性・製剤学的特性(1)バルビツール酸誘導体としての共通の作用機序により鎮静、催眠作用を現す。すなわち、GABAA 受容体のサブユニットに存在するバルビツール酸誘導体結合部位に結合することにより、抑制性伝達物質GABA の受容体親和性をたかめ、Cl-チャネル開口作用を増強して神経機能抑制作用を促進する。バルビツール酸誘導体はその作用時間によって分類されるが、本薬は短時間作用型に属する。(2)重大な副作用として、皮膚粘膜眼症候群(Stevens-Johnson Syndrome)、依存性があらわれることがある。販売名和 名ラボナ錠 50mg洋 名RAVONA Tablets 50mg名称の由来不明一般名和 名(命名法)ペントバルビタールカルシウム(JAN)洋 名(命名法)Pentobarbital Calcium(JAN)ステム催眠剤、バルビツール酸誘導体:-barb-抜粋:ラボナ・インタビューフォーム 精神科の薬−抗精神病薬・抗うつ薬・睡眠薬・抗認知症薬…−はや調べノート これだけは押さえておきたい 薬がわかる!ケアにいかせる!/杉田尚子/諏訪太朗/村井俊哉【3000円以上送料無料】
2022.06.22
コメント(0)
-
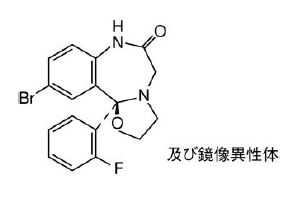
ベンゾジアゼピン系睡眠薬(長時間型):ハロキサゾラム(ソメリン)
承認年1980年開発の経緯本剤は、三共株式会社(現:第一三共株式会社)が開発した薬剤で、ベンゾジアゼピノオキサゾール誘導体の中から、睡眠導入剤の開発を意図してスクリーニングし、運動機能の抑制が少なく、また、REM 睡眠の抑制が少ない薬剤である。本剤は、基礎試験成績からはニトラゼパムと同等の睡眠導入作用を有し、かつ安全性はより高いものと考えられ、また、健康男性を対象とした第Ⅰ相試験、一般臨床試験、ニトラゼパムとの二重盲検試験などから、各科領域において有効性と安全性が確認され、1980 年6 月に「ソメリン細粒」「ソメリン錠5mg」及び「ソメリン錠10mg」として製造承認取得に至った。1987 年4 月に、薬事法第14 条第2 項各号のいずれにも該当しない、との再審査結果を得た。なお、医療事故防止対策として、「ソメリン細粒」から「ソメリン細粒1%」に販売名の変更を申請し、2008年3 月承認された。製品の治療学的特性・製剤学的特性(1) ベンゾジアゼピン系化合物・ハロキサゾラムの製剤で、長期作用型催眠剤に属する。(2) 自然に近い睡眠が得られる。(3) すぐれた入眠効果を示す。(4) 延べ2,178 施設、総症例22,798 例中、副作用が報告されたのは1,055 例(4.63%)で、そのうち主なものは、眠気(1.83%)、ふらつき(1.57%)、頭重感(0.55%)などの精神神経症状のほか、けん怠感(0.52%)、脱力感(0.32%)であった。〔新医薬品等の副作用のまとめ(その76)〕重大な副作用としては、呼吸抑制(頻度不明)、炭酸ガスナルコーシス(頻度不明)、依存性(0.01%未満)があらわれることがある。類薬での重大な副作用は、一過性前向性健忘、もうろう状態が報告されている。販売名和 名ソメリン®細粒1%、ソメリン®錠5mg、ソメリン®錠10mg洋 名SOMELIN® Fine Granules 1%、SOMELIN® Tablets 5mg、SOMELIN® Tablets 10mg名称の由来フランス語で「睡眠」を表わす「Sommeil(ソメイユ:ローマ神話のSomnus“眠りの神”による)」を基本とし、Benzodiazepine 系化合物であることを示す語尾を接続させて「SOMELIN(ソメリン)」と命名された。一般名和 名(命名法)ハロキサゾラム(JAN)洋 名(命名法)Haloxazolam(JAN)ステムジアゼパム誘導体:-azolam(関連ステム:-azepam)抜粋:ソメリン・インタビューフォーム 不眠症診療&マネジメントマニュアル 「眠れません…」を解決する 7つの主訴でわかる!10の問診でわかる!睡眠薬の使いどき・やめどきがわかる![本/雑誌] (単行本・ムック) / 内山真/著
2022.06.15
コメント(0)
-
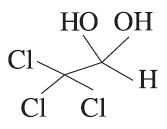
その他睡眠薬:抱水クロラール(エスクレ)
承認年1979年開発の経緯抱水クロラールは、1832 年 Liebig により合成され、1869 年 Liebreich により催眠作用が認められて以来、吸収および効果の発現が速やかであり、ほとんど発揚期がみられず、また治療量では呼吸や血圧に与える影響が自然睡眠の場合とほぼ変わらないこと等から、催眠・鎮静・抗けいれん剤として広く用いられてきた。しかし、抱水クロラールは不快な臭いがあり、胃の粘膜を刺激するなど、経口投与しにくく、一方、注腸では水溶液が不安定なため用時調製しなければならない等の問題があった。エスクレ®坐剤は安定性の高い抱水クロラール製剤(レクタルカプセル)で、使用が簡便、かつ経口投与や注腸と同等の効果が得られ、1979 年 3 月 13 日に承認を得ている。製品の治療学的特性・製剤学的特性①抱水クロラール製剤(レクタルカプセル)である。②理学検査時の催眠や抗けいれんの効果が認められている。③1499 例中副作用が報告されたのは 6 例(0.40%)で、その症状は、下痢 5 件(0.33%)、食欲不振 1 件(0.07%)、徐脈・呼吸緩徐 1 件(0.07%)であった。(承認時及び承認時以降の副作用調査時)また、重大な副作用として、無呼吸、呼吸抑制(頻度不明)、ショック(頻度不明)、依存性(頻度不明)があらわれることがある。販売名和 名エスクレ®坐剤「250」、エスクレ®坐剤「500」洋 名ESCRE® SUPPOSITORIES「250」、ESCRE® SUPPOSITORIES「500」名称の由来特になし一般名和 名(命名法)抱水クロラール (JAN) 洋 名(命名法)Chloral hydrate (JAN、INN) ステム抜粋:エスクレ・インタビューフォーム 精神科の薬−抗精神病薬・抗うつ薬・睡眠薬・抗認知症薬…−はや調べノート これだけは押さえておきたい 薬がわかる!ケアにいかせる!/杉田尚子/諏訪太朗/村井俊哉【3000円以上送料無料】
2022.06.08
コメント(0)
-
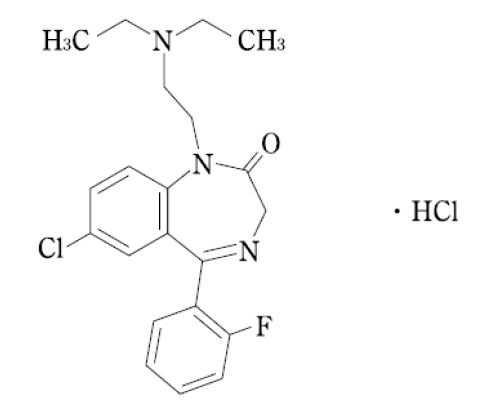
ベンゾジアゼピン系睡眠薬(長時間型):フルラゼパム塩酸塩(ダルメート)
承認年1975年開発の経緯フルラゼパム塩酸塩は、昭和37 年にHoffmann-La Roche 社によって合成されたベンゾジアゼピン化合物の一つであるが昭和46 年住友化学㈱ではインドール誘導体の環拡大による合成法を開発した。本剤はREM 睡眠への影響が少なく、筋弛緩作用が弱い。本邦においては、昭和50 年に日本ロシュ株式会社(現 中外製薬株式会社)がダルメートの商品名で発売した。 共和薬品工業株式会社は平成14 年1 月に、日本ロシュ株式会社が製造販売していたダルメートカプセル15 の承認を承継し、同年2 月に同一商品名で製造販売することとなった。製品の治療学的特性・製剤学的特性(1) 長時間作用型のベンゾジアゼピン系睡眠薬である。(2) 入眠障害、熟眠障害および早朝覚醒などいずれのタイプの不眠症にも有効である(3) ベンゾジアゼピン系薬物としての共通の作用機序により鎮静、抗不安、催眠、などの作用を現す。(4) 副作用として、昼間の眠気、ふらつき、倦怠感、頭重、口渇等が報告されている。(5) 重大な副作用として、依存性、呼吸抑制、炭酸ガスナルコーシスが、また、類薬で一過性前向性健忘、もうろう状態があらわれることがある。販売名和 名ダルメート®カプセル15洋 名DALMATE® Cap.15名称の由来特になし一般名和 名(命名法)フルラゼパム塩酸塩洋 名(命名法)Flurazepam Hydrochloride(USP)、Flurazepam(INN)ステム抜粋:ダルメート・インタビューフォーム 精神科の薬−抗精神病薬・抗うつ薬・睡眠薬・抗認知症薬…−はや調べノート これだけは押さえておきたい 薬がわかる!ケアにいかせる!/杉田尚子/諏訪太朗/村井俊哉【3000円以上送料無料】
2022.06.01
コメント(0)
-

ベンゾジアゼピン系睡眠薬(中間型):エスタゾラム(ユーロジン)
薬価収載年1975年開発の経緯製品の治療学的特性・製剤学的特性販売名和 名ユーロジン1mg錠、2mg錠、散1%洋 名EURODIN名称の由来一般名和 名(命名法)エスタゾラム洋 名(命名法)Estazolamステム抜粋:ユーロジン・添付文書精神科の薬−抗精神病薬・抗うつ薬・睡眠薬・抗認知症薬…−はや調べノート これだけは押さえておきたい 薬がわかる!ケアにいかせる!/杉田尚子/諏訪太朗/村井俊哉【3000円以上送料無料】
2022.05.25
コメント(0)
-

ベンゾジアゼピン系睡眠薬(中間型):ニトラゼパム(ベンザリン)
承認年1967年開発の経緯本剤は,スイス,F・ホフマン・ラ・ロシュのRieder とSternbach によって1963 年に合成された,ベンゾジアゼピン誘導体に属するニトラゼパム製剤であり,睡眠誘導剤・抗痙攣剤として開発された。日本では最初のベンゾジアゼピン系睡眠誘導剤として1967 年3 月に販売開始した。また,抗てんかん剤としてはエピベンザリンの名称で1969 年4 月に発売し,その後1971 年8 月にベンザリンに移行させ統一した。2016 年12 月,塩野義製薬株式会社から共和薬品工業株式会社に販売を移管した。2019 年10 月,塩野義製薬株式会社から共和薬品工業株式会社に製造販売承認が承継された。製品の治療学的特性・製剤学的特性(1) ニトラゼパムの催眠作用(睡眠誘導作用)は,不安,緊張,興奮等の情動障害を抑制し,生理的な自然に近い睡眠をもたらすとされている。(2) 血中半減期は中間型に属する。(3) 入眠障害,熟眠障害,早朝覚醒に効果が認められた。(4) 手術前夜,麻酔前の投与により,手術に対する不安・緊張を和らげ,入眠及び麻酔導入をスムーズにする。(5) 異型小発作群,焦点性発作等のてんかん発作に効果が認められている。(6) 承認時における安全性評価対象例553 例中,副作用は41 件であった。 再評価結果(1997 年6 月)における安全性評価対象例3294 例中,副作用は664 件であった。(7) 重大な副作用:呼吸抑制,刺激興奮,錯乱,肝機能障害,黄疸があらわれることがある。炭酸ガスナルコーシスを起こすことがある。依存性を生じることがある。また,類薬(他の不眠症治療薬)において,一過性前向性健忘,もうろう状態があらわれることがある。販売名和 名ベンザリン®錠2、ベンザリン®錠5、ベンザリン®錠10、ベンザリン®細粒1%洋 名Benzalin®名称の由来Benzalin(benzodiazepin + l [中間語呂調整])一般名和 名(命名法)ニトラゼパム(JAN)[日局]洋 名(命名法)Nitrazepam(JAN,INN)ステムジアゼパム誘導体:-azepam抜粋:ベンザリン・インタビューフォーム 内科医のための睡眠薬の使い方 [ 松浦雅人 ]
2022.05.23
コメント(0)
-
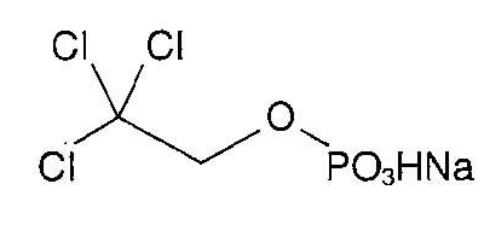
その他睡眠薬:トリクロホスナトリウム(トリクロリール)
承認年1965年開発の経緯クロラールは抱水クロラールとして古くから用いられてきた催眠薬であるが、その味とにおい及び製剤化に難点があった。抱水クロラールは肝で代謝されてトリクロロエタノールとなり、これが催眠作用を呈することからイギリスのGlaxo社でトリクロロエタノールをリン酸でエステル化したナトリウム塩を開発した。本剤は、1965年11月に承認を得て上市し、2007年8月に医療事故防止対策に基づき、販売名をトリクロリールシロップからトリクロリールシロップ10%に変更した。製品の治療学的特性・製剤学的特性(1) 脳波や心電図検査時の入眠鎮静剤として幅広く使用でき、かつ小児に服用しやすいバニリン様のにおいを有するシロップである。(2) トリクロリールシロップと抱水クロラールとの比較試験において、同等の効果(睡眠導入時間)が認められている。1)(3) 重大な副作用として、無呼吸、呼吸抑制、ショック、アナフィラキシー、依存性(いずれも頻度不明)が報告されている。販売名和 名トリクロリールⓇシロップ 10%洋 名TRICLORYLⓇ Syrup 10%名称の由来特になし一般名和 名(命名法)トリクロホスナトリウム(JAN)洋 名(命名法)Triclofos Sodium(JAN)ステム抜粋:トリクロリール・インタビューフォーム 三省堂書店オンデマンド法研 あなたに合う睡眠薬と精神安定剤
2022.05.22
コメント(0)
-
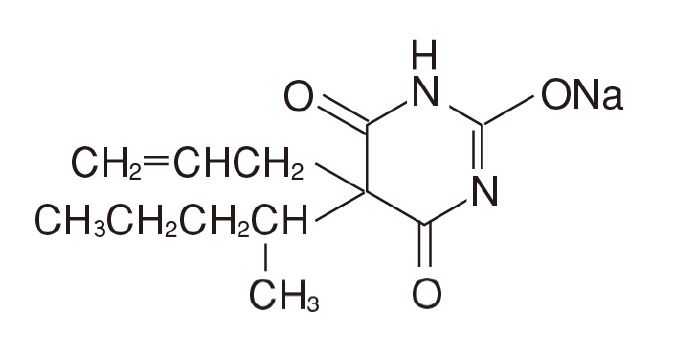
バルビツール酸系睡眠薬:セコバルビタールナトリウム(アイオナール・ナトリウム)
承認年1961年開発の経緯セコバルビタールは1938年Watersによりその経口投与が,また,1948年Stoeltingにより静注が試みられた。三菱ウェルファーマ(旧吉富製薬)が「注射用アイオナール・ナトリウム(0.2)」の規格及び試験方法を設定,安定性試験等を実施し,1961年9月29日に承認を取得,1962年4月12日に販売を開始した。1995年9月7日,再評価(薬効の再評価)の結果,薬事法第14条第2項各号(承認拒否事由)のいずれにも該当しないとの再評価結果を得た。2004年10月5日,日医工株式会社は,「注射用アイオナール・ナトリウム(0.2)」の製造販売承認を三菱ウェルファーマ株式会社より承継し,2005年6月1日に販売を開始した。その後,2006年2月10日,粉末充填アンプルから凍結乾燥バイアルに剤形変更の承認を取得し,2006年7月7日に薬価収載し,販売を開始した。製品の治療学的特性・製剤学的特性(1)本剤は,セコバルビタールナトリウムを成分とする催眠鎮静剤である。(2)セコバルビタールは短時間作用性のバルビツレートである。(3)医療事故防止に配慮し,バイアルのラベルを二層ラベルにしている。(4)総症例数945例中73件(7.72%)の副作用が報告されている。主な副作用は眠気10件(1.06%),頭重感8件(0.85%),脈拍異常4件(0.42%)等であった。(再評価結果)重大な副作用として,皮膚粘膜眼症候群(Stevens‐Johnson症候群)(頻度不明),チアノーゼ,呼吸抑制(0.1~5%未満),薬物依存(頻度不明)が報告されている。販売名和 名注射用アイオナール®・ナトリウム(0.2)洋 名IONAL® SODIUM FOR INJECTION名称の由来特になし一般名和 名(命名法)セコバルビタールナトリウム(JAN)洋 名(命名法)Secobarbital Sodium(JAN)ステムバルビツール酸系催眠薬:(-)barb-抜粋:アイオナール・インタビューフォーム 精神科の薬−抗精神病薬・抗うつ薬・睡眠薬・抗認知症薬…−はや調べノート これだけは押さえておきたい 薬がわかる!ケアにいかせる!/杉田尚子/諏訪太朗/村井俊哉【3000円以上送料無料】
2022.05.21
コメント(0)
-
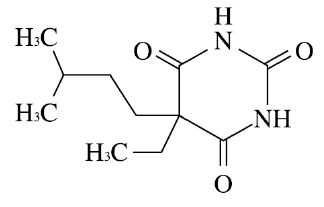
バルビツール酸系睡眠薬:アモバルビタール(イソミタール)
承認年1950年開発の経緯アモバルビタールは、1923年 Shonleらによって合成され、アメリカのLilly社よりAmytalとして発売れた。国内では1950年2月より発売されている。2007年9月に医療事故防止対策のため、販売名を「イソミタール」から「イソミタール原末」に変更した。製品の治療学的特性・製剤学的特性アモバルビタールは作用の持続時間が中程度の中間型に属するバルビツール酸誘導体であり、服用後約30分で入眠し、4~6時間熟眠が得られる。販売名和 名イソミタール原末洋 名Isomytal名称の由来不明一般名和 名(命名法)アモバルビタール(JAN)洋 名(命名法)Amobarbital(INN)ステム-barb:催眠剤、バルビツール酸誘導体抜粋:イソミタール・インタビューフォーム 内科医のための睡眠薬の使い方 [ 松浦雅人 ]
2022.05.20
コメント(0)
-
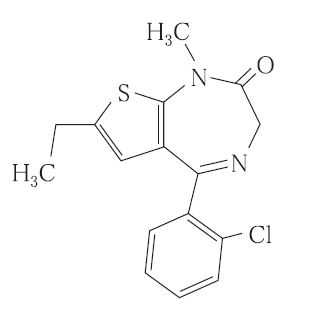
クロチアゼパム(リーゼ)
承認年1998年開発の経緯リーゼ(一般名:クロチアゼパム)は,当社研究所で開発された心身安定剤で,従来のベンゾジアゼピン系化合物と化学構造上異なるチエノジアゼピン化合物である。本剤は心身症(消化器疾患,循環器疾患)における身体症候並びに不安・緊張・心気・抑うつ・睡眠障害,自律神経失調症に伴うめまい・肩こり・食欲不振を改善させる。また,麻酔前投薬としても用いられる。1969 年よりクロチアゼパム製剤の前臨床試験を開始し,その後の臨床試験により本剤の有効性,安全性並びに有用性が確認され,1978 年5 月に承認を取得しリーゼ糖衣錠(5mg・10mg)並びにリーゼ顆粒を発売するに至った。その後,1988 年5 月31 日に「自律神経失調症」の効能追加の一部変更承認を受け,更に1989 年3 月1 日には再評価結果その31 にて結果通知された。1998 年1 月には糖衣錠からフィルムコーティング錠に処方変更したリーゼ錠5mg 並びにリーゼ錠10mg の代替新規承認を取得,1998 年7 月より販売を開始し現在に至っている。製品の治療学的特性・製剤学的特性(1)リーゼは優れた抗不安作用を示し,催眠鎮静作用,筋弛緩作用は弱いことが認められている。(2)総症例数14,032 例(糖衣錠,顆粒)中692 例(4.93%)883 件の副作用が報告されている。主な副作用は眠気390 件(2.78%),ふらつき109 件(0.78%),倦怠感57 件(0.41%)等であった。(国内文献及び効能追加申請資料〔自律神経失調症〕等の集計-再審査対象外)なお,重大な副作用としては依存性,肝機能障害,黄疸が報告されている。販売名和 名リーゼ錠5mg、リーゼ錠10mg、リーゼ顆粒10%洋 名RIZE TABLETS、RIZE GRANULES 10%名称の由来lyze(分解する)→不安をとる,Rise(上る)→気分高揚,RIESE(独)巨人一般名和 名(命名法)クロチアゼパム(JAN)洋 名(命名法)Clotiazepam(JAN)ステム抜粋:メイラックス・インタビューフォーム 内科医のための抗不安薬・抗うつ薬の使い方 [ 松浦雅人 ]
2022.05.19
コメント(0)
-
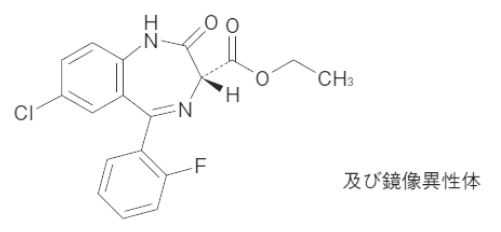
ロフラゼプ酸エチル(メイラックス)
承認年1988年開発の経緯ロフラゼプ酸エチルは、1975年にフランスのSanofi社(現 SANOFI-AVENTIS FRANCE)Clin-Midy研究所のH.DEMARNE及びA.HALLOTによって合成された新規なベンゾジアゼピン系抗不安薬である。クロラゼプ酸二カリウムの後継品としての一連の研究から新たに抗不安作用が選択的に強く、鎮静作用や筋弛緩作用が弱く安全性の高い薬物として開発された。本薬は、3位にエトキシカルボニル基を有することを化学構造上の特徴とし、生体内ではその活性代謝物が薬効を発現する。国内では1979年4月から非臨床試験を実施し、1980年8月から、メイラックス錠1㎎・2㎎について一般臨床試験を実施するとともに二重盲検比較試験を実施した。その結果、各種の神経症及び心身症に対し治療効果を示し、また安全性も高いベンゾジアゼピン系抗不安薬であることが確認され、1988年9月20日に承認された。更に1998年1月8日にメイラックス細粒が承認された。なお、メイラックス錠1㎎・2㎎とメイラックス細粒とは生物学的同等性が確認されている。メイラックス細粒は2008年12月19日付厚生労働省告示第550号にて医療事故防止に係わる販売名変更品として、新たに「メイラックス細粒1%」の販売名で薬価基準収載され、2009年1月に発売となった。「ロフラエプ酸エチル」及び「ロフラゼプ酸エチル錠」は2021年6月に第十八改正日本薬局方に収載された。製品の治療学的特性・製剤学的特性(1)本薬はベンゾジアゼピン系の持続性心身安定剤である。(2)動物実験において、試験を実施したベンゾジアゼピン系化合物の中では抗不安作用が強く、筋弛緩作用や協調運動抑制作用の弱いことが確認された。(3)臨床試験において、1日1回もしくは2回投与により、神経症及び心身症(胃・十二指腸潰瘍、慢性胃炎、過敏性腸症候群、自律神経失調症)における不安・緊張・抑うつ・睡眠障害に対し治療効果を示した。(4)市販後使用成績調査の結果、副作用発現症例は14,522例中545例(3.75%)676件であった(錠剤、再審査終了時)。一般臨床試験において副作用が認められた症例は55例中10例(18.18%)15件であった(細粒、承認時)。(5)重大な副作用として、薬物依存、離脱症状、刺激興奮、錯乱、幻覚、呼吸抑制があらわれることがある。販売名和 名メイラックス®錠1㎎、メイラックス®錠2㎎、メイラックス®細粒1%洋 名MEILAX® TABLETS 1mg、MEILAX® TABLETS 2mg、MEILAX® FINE GRANULES 1%名称の由来Meiji Relax一般名和 名(命名法)ロフラゼプ酸エチル(JAN)洋 名(命名法)Ethyl Loflazepate(JAN,INN)ステムdiazepam derivatives:-azepam抜粋:メイラックス・インタビューフォーム 抗不安薬プラクティカルガイド 今だから知っておきたい正しい使い方 [ 松永寿人 ]
2022.05.18
コメント(0)
-
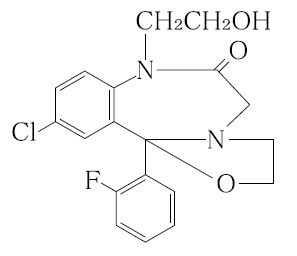
フルタゾラム(コレミナール)
承認年1987年開発の経緯コレミナール錠4mg/細粒1%は,フルタゾラムを含有する消化管機能安定剤である。スイス国F.Hoffmann-La Roche & Co. が1959 年に1,4-ベンゾジアゼピン骨格を有するクロルジアゼポキシドを抗不安剤として開発して以来,世界各国で新規な置換基を有する誘導体あるいはその母核に異項環を縮合させた化合物が合成され,現在ではジアゼパムを初めとして多数の1,4-ベンゾジアゼピン誘導体がそれぞれの特徴に基づいて臨床で使用されている。三井製薬工業(株)(現:バイエル薬品株式会社)は,F.Hoffmann-La Roche & Co. が1970~71 年に合成および抗不安剤としてのスクリーニングを行った一連の新規のオキサゾロ-1,4-ベンゾジアゼピン誘導体について研究していることを知り,同社にデータの開示を申し入れるとともに,1971 年10 月より同社との間でフルタゾラムの導入交渉を行い,1972 年9 月に技術導入契約を締結した。これにより,三井製薬工業(株)が我が国においてフルタゾラムの研究開発を進めるに至った。発売後,10,024 例の使用成績調査を実施し,再審査申請を行った結果,1992 年6 月に薬事法第14 条第2 項各号(承認拒否事由)のいずれにも該当しないとの再審査結果を得た。なお,本剤は2005 年10 月に沢井製薬(株)が日本シエーリング(株)(現:バイエル薬品(株))から製造販売承認を取得している。その後,2008 年3 月に販売名変更に伴う再承認を受け,2008年6 月に変更銘柄名で薬価収載された。製品の治療学的特性・製剤学的特性1)ベンゾジアゼピン系消化管機能安定剤である。2)過敏性腸症候群,慢性胃炎,胃・十二指腸潰瘍などの消化器系心身症に対して優れた効果がある。精神症状とともに消化器症状を改善する。3)承認時及び市販後使用成績調査において11,011 例中,副作用が報告されたのは179 例(1.63%)で,主な副作用は眠気88 件(0.80%),口渇31 件(0.28%),めまい・ふらつき・たちくらみ18 件(0.16%)等であった(再審査終了時)。なお,重大な副作用として,依存症が報告されている。また,類薬の重大な副作用として,刺激興奮・錯乱が報告されている。販売名和 名コレミナール錠4mg、コレミナール細粒1%洋 名COREMINAL tablets 4mg、COREMINAL fine gramules 1%名称の由来胃腸症状を調整(CORRECT)するminor tranquilizer であることから命名した。一般名和 名(命名法)フルタゾラム(JAN)洋 名(命名法)Flutazolam(JAN,INN)ステム-azepam:diazepam 系のトランキライザー,催眠鎮静剤抜粋:コレミナール・インタビューフォーム ココロピルブック 抗精神病薬・抗うつ薬・抗不安薬・睡眠薬・気分安定薬 [ 相田くひを ]
2022.05.17
コメント(0)
-
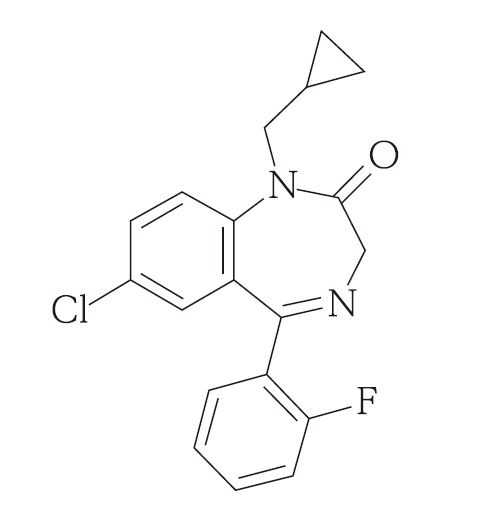
フルプラゼパム(レスタス)
承認年1986年開発の経緯フルトプラゼパムは鐘紡株式会社(現 クラシエ製薬株式会社)により開発された持続性心身安定剤である。本剤は従来のベンゾジアゼピン系化合物の中でも強い抗不安作用と作用持続性を有しており、神経症、心身症における不安・緊張・抑うつ・睡眠障害等に対して改善効果を示す。医療事故防止を目的として、「レスタス錠」から「レスタス錠2mg」へ販売名変更の申請を行い、2007 年3 月1 日に承認を受け、2007 年6 月15 日に薬価基準収載された。2016 年10 月にMSD 株式会社より製造販売承認を承継し、販売を移管した。製品の治療学的特性・製剤学的特性(1)神経症、心身症における不安・緊張・抑うつ・易疲労性・睡眠障害に対し、ジアゼパムより優れた症状改善効果を示す。(2)消化管からの吸収は極めて良好であり、組織への移行および代謝は速やかで、尿中および腸肝循環を経て糞中へ排泄される(動物データ)。ヒトにおける代謝物のデスアルキル体の血中半減期は約190 時間である。(3)抗不安作用を示唆する作用と、運動機能を抑制する作用との分離が大きく、安全域の広い薬剤である。(4)総症例10,794 例中558 例(5.2%)に副作用が認められた。その主なものは眠気(3.5%)、ふらつき(0.9%)、易疲労感・倦怠感(0.4%)、めまい感(0.3%)等であった。販売名和 名レスタスⓇ 錠2mg洋 名RestasⓇ Tablets 2mg名称の由来休息(REST)という名の持続性心身安定剤としてRESTAS と名付けた。一般名和 名(命名法)フルトプラゼパム(JAN)洋 名(命名法)Flutoprazepam(JAN、INN)ステムジアゼパム誘導体:-azepam抜粋:レスタス・インタビューフォーム抗不安薬プラクティカルガイド 今だから知っておきたい正しい使い方 [ 松永寿人 ]
2022.05.16
コメント(0)
-
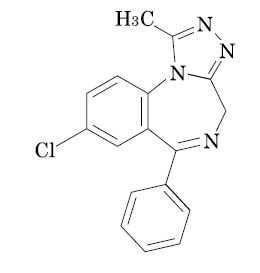
アルプラゾラム(ソラナックス)
承認年1984年開発の経緯武田薬品と米国アップジョンで、それぞれ独自にベンゾジアゼピン系化合物の基礎研究を進めていたが、研究対象に選んだ一連の化合物(トリアゾロベンゾジアゼピン系)が偶然にも一致していることが特許出願の段階であきらかになった。以後研究開発を効率的に行うために共同開発に関する基本契約を締結し(1972 年)、両社ともこれらの化合物の中からアルプラゾラムを選択し開発することにした。国内においては、武田薬品、日本アップジョンに加え、日本アップジョンが輸入した製剤バルクを小分け製造する住友化学の3 社で共同開発することになった(1976 年)。その後、基礎的及び臨床的検討によりアルプラゾラムは心身症(胃・十二指腸潰瘍、過敏性大腸症候群)及び自律神経失調症における不安・緊張・抑うつ及び睡眠障害に有用性が認められ、1984 年2 月15 日に製造承認を得た。8,459 例の使用成績調査を実施し、1990 年2 月に再審査申請を行った。再審査結果通知の際、効能・効果の表現を抗不安薬の臨床評価方法に関するガイドラインを踏まえ「心身症(胃・十二指腸潰瘍、過敏性腸症候群、自律神経失調症)における身体症候並びに不安・緊張・抑うつ・睡眠障害」と改められた。2021 年9 月、ファイザー株式会社からヴィアトリス製薬株式会社へ製造販売移管された。製品の治療学的特性・製剤学的特性(1) アルプラゾラムはトリアゾロベンゾジアゼピン系化合物に属し、薬効スペクトラムはジアゼパムに類似するが、動物実験においてジアゼパムの2~7 倍の効力を示し、臨床試験においてもジアゼパム錠の1/7 の用量で同等の効果を示す効力の強い抗不安薬である。(2) アルプラゾラム錠(1.2~2.4mg/日)は、比較試験により心身症に対し、ジアゼパム錠(9~18mg/日)及びロラゼパム錠(1.5~3.0mg/日)とほぼ同等の有用性を有する。(3) アルプラゾラム錠はロラゼパム錠と比較して心身症の精神症状、とくに緊張、焦燥、抑うつ、攻撃性(易怒性)並びに肩・首のこりなどの改善でよりすぐれており、また、これらの差は投与後の早い時期に認められたことから、効果発現がより早いことが示された。(4) アルプラゾラム錠はジアゼパム錠と比較して心身症のめまい・ふらつき感の改善ですぐれていた。(5) 心身症の代表疾患のひとつである胃・十二指腸潰瘍において、アルプラゾラム錠とゲファルナートとの併用投与はそれぞれの単独投与に比し高い潰瘍治癒率を示しアルプラゾラム錠とゲファルナートとを併用投与することの意義が示唆された。(6) アルプラゾラム錠の概括的な安全性はジアゼパム錠及びロラゼパム錠とほぼ同等であった。販売名和 名ソラナックス®0.4mg 錠、ソラナックス®0.8mg 錠洋 名Solanax® Tablets 0.4mg、Solanax® Tablets 0.8mg名称の由来米国の販売名Xanax はすでに国内で他剤が類似した名前を使用していたためSolanax(ソラナックス)とした。一般名和 名(命名法)アルプラゾラム(JAN)洋 名(命名法)Alprazolam(JAN、INN)ステム抜粋:ソラナックス・インタビューフォーム各科領域における抗不安薬の選び方・使い方
2022.05.15
コメント(0)
-
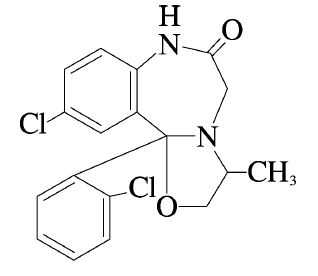
メキサゾラム(メレックス)
承認年1983年開発の経緯本剤は、向精神薬のオキサゾロベンゾジアゼピン誘導体の中から、より抗不安作用が強く、運動機能系に及ぼす影響が少ない化合物として三共株式会社(現、第一三共株式会社)がスクリーニングしたものである。1971 年から基礎試験を開始した結果、薬理学的には抗不安薬の指標とされる条件付けラットの葛藤改善作用及びマウスのメジマイドに対する抗痙攣作用等の成績から、より強力な作用を有する反面、毒性は低く、筋弛緩、歩行失調等の随伴症状は比較的弱いことが認められた。一方、臨床試験は二重盲検比較試験を含めた総症例921 例を対象に実施され、このうち対象疾患(神経症・心身症・自律神経失調症)で効果判定が行われたのは783 例であった。その結果、全般改善率(著名改善+改善例数/判定例数)は70.5%(552/783)に認められ、特に神経症に対する効果は、不安神経症では有効率75.1%(127/169)、抑うつ神経症では75.9%(60/79)を示し、また心身症についても慢性胃炎、高血圧症、心臓神経症に対する有効率はそれぞれ85.7%(42/49)、75.0%(63/84)、72.7%(24/33)とすぐれた効果が認められた。さらに、神経領域におけるジアゼパム及びプラセボを対照とした二重盲検比較試験の結果、強迫症状に対し有意差が認められ、また内科領域におけるオキサゾラムを対照とした二重盲検比較試験においても緊張、強迫症状、睡眠障害などに有意差が認められたことから、1983 年9 月「メレックス錠0.5mg」「メレックス錠1mg」及び「メレックス細粒」として製造販売承認取得に至った。1992 年6 月、再審査結果公示の際に、「抗不安薬の臨床評価方法に関するガイドライン」を踏まえ、効能・効果の表現方法が現行に改められた。なお、医療事故防止対策として、「メレックス細粒」から「メレックス細粒0.1%」に販売名の変更を申請し、2008 年3 月承認された。製品の治療学的特性・製剤学的特性(1)有効性ベンゾジアゼピン系抗不安剤で、長期作用型(24 時間以上)に属する。1) 神経症では、強迫、恐怖で改善率が得られた。2) 胃・十二指腸潰瘍による各種愁訴に改善が見られた。3) 頭痛、頭重、肩こり、めまい等の自律神経症状に改善がみられた。(2)安全性重大な副作用としては、依存性、刺激興奮、錯乱があらわれることがある。販売名和 名メレックス®錠0.5mg、メレックス®錠1mg、メレックス®細粒0.1%洋 名MELEX® Tablets 0.5mg、MELEX® Tablets 1mg、MELEX® Fine Granules 0.1%名称の由来一般名 Mexazolam のm、e、x、l を組み合わせ、語呂の良いMELEX と命名された。一般名和 名(命名法)メキサゾラム(JAN)洋 名(命名法)Mexazolam(JAN)ステム-azolam:ジアゼパム誘導体 (関連ステム:-azepam)抜粋:メレックス・インタビューフォーム精神科の薬−抗精神病薬・抗うつ薬・睡眠薬・抗認知症薬…−はや調べノート これだけは押さえておきたい 薬がわかる!ケアにいかせる!/杉田尚子/諏訪太朗/村井俊哉【3000円以上送料無料】
2022.05.14
コメント(0)
-
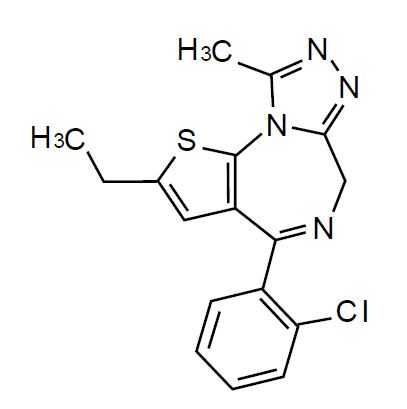
エチゾラム(デパス)
承認年1983年開発の経緯デパス(一般名:エチゾラム)は,当社研究所における一連のチエノジアゼピン系化合物に関する研究により,“心身安定剤リーゼ”についで創製された精神安定剤である。チエノジアゼピン環にトリアゾール環を縮合したデパスは,全般に薬理活性の強化が認められ,強力な抗不安作用とともに優れた鎮静・催眠作用,抗うつ作用,筋緊張緩解作用を示す。1971 年よりエチゾラム製剤の前臨床試験を開始し,その後の臨床試験により本剤の有効性,安全性並びに有用性が確認され,1983 年9 月に承認を取得し発売するに至った(錠0.5mg・1mg,細粒1%)。発売後,10,720 例の使用成績調査を実施し,1989 年12 月に再審査申請を行った。その結果,1992 年6 月に「製造(輸入)承認事項の一部を変更すれば薬事法第14 条第2 項各号のいずれにも該当しない」旨再審査結果通知され(1992 年6 月3 日付厚生省薬務局長通知),効能・効果及び用法・用量の表現を改めた。また,細粒剤は2002 年2 月に販売名変更に伴う再承認を受け,2002 年7 月に変更銘柄名で薬価収載された。さらに,医療現場では,エチゾラム製剤が処方される患者のうち,50%以上を65 歳以上の高齢者が占めており,1 日投与量では0.5mg/day が最も多くなっているが,高齢者には0.5mg 錠では効果が強すぎるため,さらなる低用量製剤が望まれていた。この要望に応えるため,0.25mg錠の開発に着手し,加速試験,生物学的同等性試験を実施して2012 年2 月に承認を取得,2012年7 月に販売を開始した。製品の治療学的特性・製剤学的特性(1)神経症における不安・緊張・抑うつ・神経衰弱症状に対して改善効果を示す。(2)うつ病における不安・緊張に対して改善効果を示す。(3)心身症(高血圧症,胃・十二指腸潰瘍)における身体症候並びに不安・緊張・抑うつに対して改善効果を示す。(4)頸椎症,腰痛症,筋収縮性頭痛における不安・緊張・抑うつ及び筋緊張に対して改善効果を示す。(5)神経症,うつ病,心身症(高血圧症,胃・十二指腸潰瘍),統合失調症における睡眠障害に対して改善効果を示す。(6)総症例数12,328 例中866 例(7.02%)1,133 件の副作用が報告されている。主な副作用は眠気444 件(3.60%),ふらつき241 件(1.95%),倦怠感77 件(0.62%),脱力感46件(0.37%)等であった。(再審査終了時)重大な副作用として,依存性,呼吸抑制,炭酸ガスナルコーシス,悪性症候群,横紋筋融解症,間質性肺炎,肝機能障害,黄疸があらわれることがある。販売名和 名デパス錠0.25mg、デパス錠0.5mg、デパス錠1mg、デパス細粒1%洋 名DEPAS TABLETS、DEPAS FINE GRANULES 1%名称の由来(病的状態から)離れ= De 通り過ぎる= Pas一般名和 名(命名法)エチゾラム(JAN)洋 名(命名法)Etizolam(JAN)ステムジアゼパム誘導体(-azepam)の同類薬として分類されている。:‐tizolam抜粋:デパス・インタビューフォーム抗精神病薬完全マスター (精神科臨床エキスパート) [ 中村純 ]
2022.05.13
コメント(0)
-
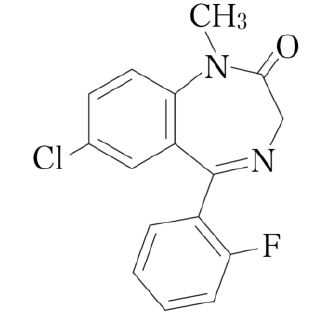
フルジアゼパム(エリスパン)
承認年1980年開発の経緯エリスパンは、当社開発の製法技術により合成された約250 種に及ぶベンゾジアゼピン系薬剤のスクリーニングから、不安・緊張除去作用が強く、ねむけ・脱力感と関連する作用が弱いという特性を有することから選択された。製品の治療学的特性・製剤学的特性(1)ジアゼパムに比べ不安・緊張除去作用が強い。(マウス、ラット)(2)ジアゼパムに比べ、自発運動抑制作用が弱い。(マウス)(3)重大な副作用として、依存性、刺激興奮、錯乱等が報告されている。販売名和 名エリスパン錠0.25mg洋 名Erispan名称の由来特になし一般名和 名(命名法)フルジアゼパム(JAN)洋 名(命名法)Fludiazepam(JAN、INN)ステムジアゼパム系の薬剤:-azepam抜粋:エリスパン・インタビューフォーム抗精神病薬をシンプルに使いこなすためのExercise [ 長嶺 敬彦 ]
2022.05.12
コメント(0)
-
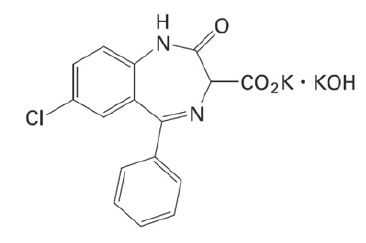
クロラゼプ酸二カリウム(メンドン)
承認年1979年開発の経緯1964 年フランスにおいて,クロラゼプ酸二カリウムが水溶性ベンゾジアゼピンとして合成された.1965~1966 年において毒性,臨床試験などが実施され,1969 年1 月フランスにおいて,Tranxene の商品名で発売された.国内においては,1970 年より物理化学,毒性,薬理などの基礎的研究が開始され,その後臨床試験が実施され,国外の成績とほぼ同じ結果が報告された.本剤は,活性代謝物を有し,血中半減期が長く,過度の鎮静作用や催眠作用,筋弛緩作用が比較的弱いマイナートランキライザーとして,期待されている.神経症における不安・緊張・焦躁・抑うつに有効である.メンドンは1979 年3 月13 日に承認され,同年12 月より発売された.なお,医療事故防止対策に基づき,2009 年6 月に販売名を「メンドン7.5 ㎎」から「メンドンカプセル7.5 ㎎」に変更した.製品の治療学的特性・製剤学的特性・神経症における不安・緊張・焦躁・抑うつに有効である.・抗不安作用が中等度で,長時間作用型のマイナートランキライザーに位置づけられる.・副作用として,承認までの臨床試験1,223 例及び市販後の調査10,110 例の合計11,333 例中796 例(7.0%)に副作用がみられた.主なものは眠気(4.0%),めまい・ふらつき(1.7%),易疲労感・脱力感・倦怠感(1.2%)等であった.(新開発医薬品の副作用の頻度に関する調査終了時)重大な副作用として依存性,刺激興奮,錯乱があらわれることがあると報告されている.販売名和 名メンドンカプセル7.5 ㎎洋 名Mendon Capsules 7.5 ㎎名称の由来Mental(心)+ don(指導者)→ 心の疾患に使用される薬の指導的存在一般名和 名(命名法)クロラゼプ酸二カリウム(JAN)洋 名(命名法)Clorazepate Dipotassium(JAN,INN)ステム抗精神病薬受容体の発見ものがたり 精神病の究明を目指して [ ニール・シーマン ]
2022.05.11
コメント(0)
-
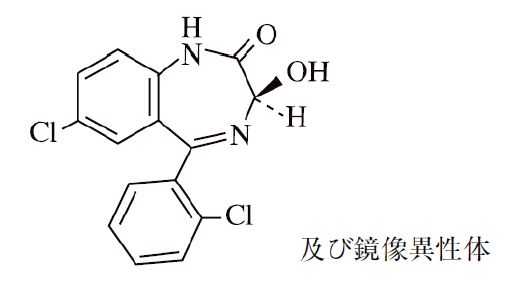
ロラゼパム(ワイパックス)
承認年1977年開発の経緯Wyeth Laboratories Inc(アメリカ)では、抗不安作用、抗痙攣作用が強く、副作用の少ないminor tranquilizer の開発を意図して3 位にOH 基を有する各種のベンゾジアゼピン誘導体を合成し、1964年には、オキサゼパムを開発した。更に研究を続けて1968 年に一連の化合物の中からロラゼパムの開発に成功した。本邦での開発は、1970 年、実験動物中央研究所において各種の毒性試験、効力試験の結果、抗不安効果の効力が強く、安全性の高い薬剤である事が確認された。1977 年に日本ワイス株式会社(現 ファイザー株式会社)がロラゼパムの初回の輸入承認を取得し、1978 年薬価収載、同年山之内製薬株式会社から発売された。1997 年6 月に再評価の結果「カテゴリーⅡ」(効能・効果の表現の変更)として公示された。更に2002 年4 月より武田薬品工業株式会社からの販売に至ったが、2013 年1 月よりファイザー株式会社へ販売会社が変更となった。製品の治療学的特性・製剤学的特性ロラゼパムは不安緊張症状、抑うつ症状にジアゼパムより優れている販売名和 名ワイパックス®錠0.5、ワイパックス®錠1.0洋 名WYPAX® TABLETS 0.5、WYPAX® TABLETS 1.0名称の由来該当資料なし一般名和 名(命名法)ロラゼパム(JAN)洋 名(命名法)Lorazepam(JAN)ステムジアゼパム誘導体:−azepam抜粋:ワイパックス・インタビューフォーム抗不安薬プラクティカルガイド 今だから知っておきたい正しい使い方 [ 松永寿人 ]
2022.05.10
コメント(0)
-
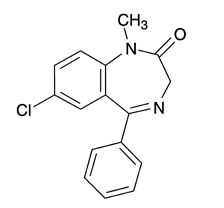
ブロマゼパム(レキソタン)
承認年1976年開発の経緯レキソタンは、F. Hoffmann−La Roche社(ロシュ社)が開発した一連のベンゾジアゼピン系化合物であるブロマゼパムを含有する精神神経用剤である。本剤は強力な静穏・抗不安作用を有し、臨床上、不安・緊張・抑うつ及び睡眠障害に加え、強迫・恐怖症状にも有効な薬剤である。国内においては、錠2mg、錠5mg及び細粒を1977年5月に発売し、1981年9月には、錠1mgを剤形追加している。なお、医療事故防止対策に伴い販売名が変更され、レキソタン細粒はレキソタン細粒1%として2007年3月に製造販売承認された。2020年9月に製造販売承認がアスペンジャパン株式会社(現サンドファーマ株式会社)に承継された。製品の治療学的特性・製剤学的特性レキソタンの有効成分であるブロマゼパムは、1960年Sternbachらにより合成された一連のベンゾジアゼピン誘導体の一つである。1960年以来、ロシュ社において薬理学的な検討が加えられ、ブロマゼパムはクロルジアゼポキシド、ジアゼパムと比較し、静穏作用、抗不安作用、筋弛緩作用、抗痙攣作用が強力であるというすぐれた薬理学的特徴が明らかにされた。販売名和 名レキソタンⓇ 錠1、レキソタンⓇ 錠2、レキソタンⓇ 錠5、レキソタンⓇ 細粒1%洋 名LexotanⓇ Tablets 1、LexotanⓇ Tablets 2、LexotanⓇ Tablets 5、LexotanⓇ Fine Granules 1%名称の由来該当資料なし一般名和 名(命名法)ブロマゼパム(JAN)洋 名(命名法)Bromazepam(JAN、INN)ステムジアゼパム誘導体:−azepam抜粋:レキソタン・インタビューフォーム内科医のための抗不安薬・抗うつ薬の使い方 [ 松浦雅人 ]
2022.05.09
コメント(0)
-
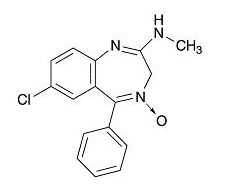
クロキサゾラム(セパゾン)
承認年1973年開発の経緯1967年、国産初のベンゾジアゼピン系マイナートランキライザーであるオキサゾラム(販売名:セレナール)が三共株式会社(現:第一三共株式会社)により合成されたが、このオキサゾラム誘導体の中から更に一層強力な馴化作用と抗痙攣作用を有する本剤クロキサゾラムが1969年に見出された。臨床的には、各種神経症(不安神経症、強迫神経症、心気症、抑うつ反応など)を始めとして、各科領域での心身症又は自律神経症失調症における不安・緊張・焦燥・抑うつ・易疲労性などの情動障害、自律神経症状及び睡眠障害、あるいは術後の不安除去に効果が認められ、1973年、製造販売承認を取得した。1989年3月の再評価において「抗不安薬の臨床評価方法に関するガイドライン」に基づいた有効性に関する評価が行われ、効能・効果の表現方法が改められた結果、抗不安薬の効能が神経症と心身症の領域に分類された。製品の治療学的特性・製剤学的特性セパゾンはマイナートランキライザー・クロキサゾラムの製剤で、長期作用型(24時間以上)・中力価型ベンゾジアゼピン系薬剤に属する。(1) 抗不安効果のみでなく、強迫神経症・恐怖症、抑うつ反応などにも効果を発揮する。(2) 自律神経調節効果を示し、自律神経失調に基づく症状を改善する。(3) 睡眠障害や術前の不安除去に適している。(4) 総症例11,701例中、副作用が報告されたのは1,261例(10.78%)であり、そのうち主なものは、眠気(6.35%)、ふらつき(4.16%)、けん怠感(1.38%)、口渇(1.13%)、めまい(0.85%)、悪心・嘔吐(0.86%)、脱力感(0.85%)であった。なお、重大な副作用として依存性(頻度不明)、刺激興奮(0.31%)が報告されている。販売名和 名セパゾン®錠1、セパゾン®錠2、セパゾン®散1%洋 名SEPAZON® Tablets 1、SEPAZON® Tablets 2、SEPAZON® Powder 1%名称の由来当社セレナール(SERENAL)の姉妹品であることのイメージを考えたセ(SE-)、あるいはSEPA(Sankyo’s Extensive Powerful Anxiolytica)に-ZONを付した。一般名和 名(命名法)クロキサゾラム(JAN)洋 名(命名法)Cloxazolam(JAN)、cloxazolam(INN)ステムジアゼパム誘導体:-azolam(関連ステム:-azepam)抜粋:セパゾン・インタビューフォーム【送料無料】 抗不安薬プラクティカルガイド 今だから知っておきたい正しい使い方 / 松永寿人 【本】
2022.05.08
コメント(0)
-
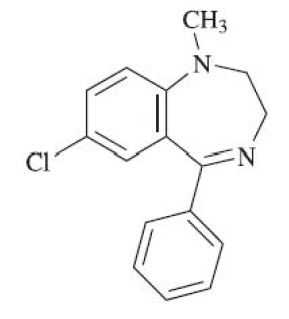
メダゼパム(レスミット)
承認年1971年開発の経緯F・ホフマン・ラ・ロシュ社において合成された一連のベンゾジアゼピン系化合物のうちの一つで,鎮静・催眠作用,筋弛緩作用の弱い抗不安剤として開発された。日本では1971 年5月に承認を得た。2016 年12 月,塩野義製薬株式会社から共和薬品工業株式会社に販売を移管した。2021 年4 月,塩野義製薬株式会社から共和薬品工業株式会社に製造販売承認が承継された。製品の治療学的特性・製剤学的特性(1) 本剤は,ジアゼパム等と同じベンゾジアゼピン系に属する抗不安剤である。(2) 神経症における不安・緊張・抑うつ,心身症(消化器疾患,循環器疾患,内分泌系疾患,自律神経失調症)における身体症候並びに不安・緊張・抑うつに適応を有する。(3) 臨床的に抗不安作用と関係が深いと考えられる抗コンフリクト作用,馴化作用,条件反射抑制作用,抗ペンテトラゾール痙攣作用はジアゼパムと同等かやや弱い。〔ラット,マウス〕 (4) 承認時における安全性評価対象例779 例中,副作用の発現件数は224 件であった。 再評価結果における安全性評価対象例12563 例中,副作用の発現件数は1558 件であった。(5) 重大な副作用:依存性を生じることがある。刺激興奮,錯乱があらわれることがある。販売名和 名レスミット®錠2、レスミット®錠5洋 名Resmit®名称の由来rest (安心・休息)+ mit(語尾調整)一般名和 名(命名法)メダゼパム(JAN)[日局]洋 名(命名法)Medazepam (JAN,INN)ステムジアゼパム誘導体:-azepam抜粋:レスミット・インタビューフォーム各科領域における抗不安薬の選び方・使い方
2022.05.07
コメント(0)
-
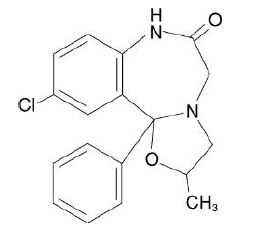
オキサゾラム(セレナール)
承認年1970年開発の経緯1967年、三共株式会社(現:第一三共株式会社)によりBenzodiazepino oxazol誘導体の一種であるオキサゾラムが創製され、国産初のベンゾジアゼピン系マイナートランキライザーとなった。オキサゾラムは前臨床試験成績から、従来のベンゾジアゼピン誘導体に比しはるかに低毒性であり、かつ催眠作用、筋弛緩作用、運動失調の発現、耐性の獲得などが明らかに弱く、クロルジアゼポキシド、ジアゼパムなどより安全域が広い特性を有することが確認された。臨床試験の結果から、眠気、ふらつき、けん怠感などの副作用が極めて少なく、正常の日常生活活動にほとんど影響を与えることなく、より選択的な静穏作用を発揮するという利点を有し、各種神経症をはじめ、器官神経症、心身症、うつ病などにおける不安、緊張、抑うつ、易疲労性などの情動障害を速やかに除去し、各種の神経症症状、自律神経症状、睡眠障害の改善にすぐれた効果をもたらすことが示された。1970年、本剤の製造販売承認を取得し、発売した。1989年3月の再評価において「抗不安薬の臨床評価方法に関するガイドライン」に基づいた有効性に関する評価が行われ、効能・効果の表現方法が改められた結果、抗不安薬の効能が神経症と心身症の領域に分類された。また、1997年6月には麻酔前投与に係る用法・用量がより適切な表現に改められた。製品の治療学的特性・製剤学的特性(6) 総症例10,603例中、副作用が報告されたのは延べ796件(7.51%)であった。そのうち主なものは、眠気(2.88%)、けん怠感(0.78%)、ふらつき(0.77%)等であった。 重大な副作用として、頻度不明であるが、依存性が報告されている。(1) 国産初のマイナートランキライザー・オキサゾラムの製剤で長期作用型のベンゾジアゼピン系薬剤に属し、クロルジアゼポキシド、ジアゼパムと類似の薬理学的性質を有する。(2) 不安・緊張・焦燥・抑うつ・意欲減退・易疲労性等の情動障害、神経症症状を解消する。(3) 自律神経失調に基づく諸種の身体症状を改善する。(4) 効果発現が早い。排泄が早く、蓄積傾向はみられない。(5) 間代性痙攣を少量で明らかに抑制する(マウス、ラット)。(6) 総症例10,603例中、副作用が報告されたのは延べ796件(7.51%)であった。そのうち主なものは、眠気(2.88%)、けん怠感(0.78%)、ふらつき(0.77%)等であった。 〔新開発医薬品の副作用のまとめ(その18)1)〕 重大な副作用として、頻度不明であるが、依存性が報告されている。販売名和 名セレナールⓇ錠5、セレナールⓇ錠10、セレナールⓇ散10%洋 名SERENALⓇ Tablets 5、SERENALⓇ Tablets 10、SERENALⓇ Powder 10%名称の由来SERENE(穏やかな、平和な)に語感の良いALを付与した。一般名和 名(命名法)オキサゾラム(JAN)洋 名(命名法)Oxazolam(JAN)、Oxazolam(INN)ステムジアゼパム誘導体:-azolam(関連ステム:-azepam)抜粋:セレナール・インタビューフォーム【送料無料】 抗不安薬プラクティカルガイド 今だから知っておきたい正しい使い方 / 松永寿人 【本】
2022.05.06
コメント(0)
-
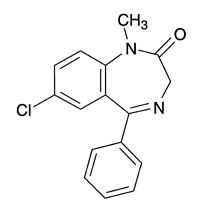
ジアゼパム(セルシン)
販売開始年1964年開発の経緯製品の治療学的特性・製剤学的特性販売名和 名2mgセルシン錠、5mgセルシン錠、10mgセルシン錠、セルシン散1%洋 名CERCINE TABLETS名称の由来一般名和 名(命名法)ジアゼパム洋 名(命名法)Diazepamステム抜粋:セルシン・添付文書各科領域における抗不安薬の選び方・使い方
2022.05.05
コメント(0)
-
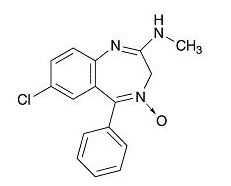
クロルジアゼポキシド(コントール)
薬価収載年1961年開発の経緯製品の治療学的特性・製剤学的特性販売名和 名5mgコントール錠、10mgコントール錠洋 名5mg. CONTOL TABLETS, 10mg. CONTOL TABLETS名称の由来一般名和 名(命名法)クロルジアゼポキシド洋 名(命名法)Chlordiazepoxideステム抜粋:クロルジアゼポキシド・添付文書ココロピルブック 抗精神病薬・抗うつ薬・抗不安薬・睡眠薬・気分安定薬 [ 相田くひを ]
2022.05.04
コメント(0)
-
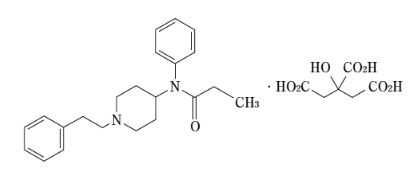
フェンタニルクエン酸塩(フェントス)
薬価収載年2018年開発の経緯製品の治療学的特性・製剤学的特性販売名和 名フェントステープ0.5mg、1mg、2mg、4mg、6mg、8mg洋 名FENTOS Tapes名称の由来一般名和 名(命名法)フェンタニルクエン酸塩 洋 名(命名法)ステム抜粋:フェントス・添付文書オピオイド乱用・依存を回避するために 臨床医のためのガイド
2022.05.03
コメント(0)
-
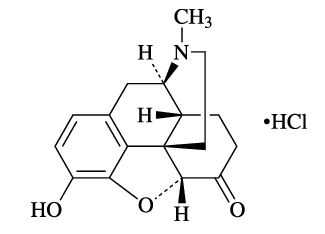
ヒドロモルフォン塩酸塩徐放錠(ナルサス)
販売開始年2017年開発の経緯製品の治療学的特性・製剤学的特性販売名和 名ナルサス錠2mg、6mg、12mg、24mg洋 名NARUSUS TABLETS名称の由来一般名和 名(命名法)ヒドロモルフォン塩酸塩徐放錠洋 名(命名法)ステム抜粋:ナルサス・添付文書【送料無料】 オピオイド 基礎を知って臨床で使いこなす / 垣花学 【本】
2022.05.02
コメント(0)
全386件 (386件中 1-50件目)








