全て
| カテゴリ未分類
| プレスリリース
| ドライアイ
| 文献発表
| 厚生労働省通知
| 妄想
| 新聞報道
| お勉強
| 前立腺がん
| 医療費
| 原発
| 制がん剤
| 政治
| 自閉症
| 子宮頸がんワクチン
| 哲学
| 宣伝
| 憲法
| 医療用医薬品
カテゴリ: プレスリリース
- フルタミド錠125「KN」 PTP包装デザイン変更のお知らせ
発売元:ヤクルト本社 製造販売元:小林化工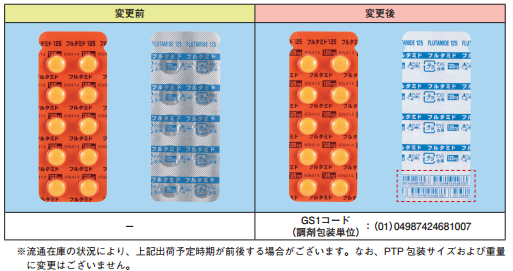
<感想>毎日飲む薬は14錠にならないかなと思います。わたしはもらったときにばらさないので、14錠包装だと飲み忘れが少なくなると思います。対応している薬剤もあります。
リンク先: http://www.yakult.co.jp/ph/news/files/?type=news&id=139883549775.pdf - 抗てんかん剤トピナ®の新たな剤形「トピナ®細粒10%」の発売について
協和発酵キリン
<概要>2014年5月13日、抗てんかん剤「トピナ®細粒10%」を発売。一部の小児や高齢者など錠剤を飲みにくいてんかん患者さんに対しても服用しやすく、服薬アドヒアランスの向上が期待されます。
<感想>医者からみて患者さんが薬を飲むのがンプライアンスで、患者がICに基づき自発的に薬を飲むのがアドヒアランスだそうです。アドヒアランス向上は患者さんが飲みやすい、飲みたくなるということだそうです。
リンク先: http://www.kyowa-kirin.co.jp/news_releases/2014/20140501_01.html - 高い挿入性・処置性能と、高画質を兼ね備えた細径内視鏡下部消化管用処置用スコープ「EC-580RD/M」
富士フイルム
<概要>挿入性と処置性能を高め、当社独自の画像センサー「スーパーCCD ハニカム™」による高画質を実現した下部消化管用処置用スコープ「EC-580RD/M」を、本日より富士フイルムメディカル株式会社(社長:平井 治郎)を通じて発売。
処置中は、処置する部位を明瞭にするためにウォータージェットノズルから出した水や消化管内の粘液などの吸引、処置具の出し入れを鉗子口から何度も繰り返します。本製品は、細径化しながらも鉗子口径3.2mmを確保し、処置具の出し入れを容易にするとともに、高い吸引性能を両立しました。また、ウォータージェットノズルと鉗子口の配置を工夫し、目的部位への送水と処置具での処置を必要最小限の動作で切り替えることができます。さらに、内視鏡先端部の湾曲角210°を実現。小回り・旋廻性能に優れているため、大腸内にある輪状ひだの裏側など観察しにくい部位の観察が容易になります。
<感想>開腹、開胸手術は交通事故に遭ったぐらいのダメージを受けると聞いたことがあります。(話は具体的にみえますが、どれぐらいの衝撃かよくわからない表現ですね。)術後1か月程度入院していたのはそのダメージから開腹するため。それを考えると内視鏡手術というのは患者の負担が少ない手術なんですね。
リンク先: http://www.fujifilm.co.jp/corporate/news/articleffnr_0872.html?ref=rss - がん治療薬HF10の第II相臨床試験実施申請資料を米国食品医薬品局へ提出
タカラバイオ
<概略>米国でがん治療薬HF10の第II相臨床試験を実施するため、本年4月30日(米国時間)に、米国食品医薬品局(FDA; Food and Drug Administration)に臨床試験実施申請資料(IND; Investigational New Drug)を提出しました。本試験では、治癒切除不能または転移性悪性黒色腫を対象とし、HF10とIpilimumab(商品名:YERVOY®)を併用投与した際の有効性、安全性、免疫学的検査などの評価を行う予定です。
<感想>HF10は、単純ヘルペスウイルスで、がん細胞で特異的に増殖するとされています。動物実験レベルでは免疫応答も誘導されることから投与されていない場所の腫瘍に効果が期待されます。正常細胞に対する影響は0とは証明されていないので、投与法は腫瘍内投与となっています。この仮説はとても魅力的ですが、まだ越えるべき壁は大きいと思います。昔、ミニブタのランゲルハンス島細胞を人へ応用することを研究していました。世界でいくつかの研究所と争っていたのですが、ミニブタのDNA(RNAだったかな)にヒトのウイルスに対応する配列があることがわかり、あっという間に研究は中止されてしまいました。
リンク先: http://www.takara-bio.co.jp/news/2014/05/01.htm
- 液状細胞診を利用したHPV併用検診サービス開始のお知らせ
ジェネティックラボ
<概要>ジェネティックラボ(代表取締役社長:福永健司、北海道札幌市)は、2014 年 6 月 1 日から、液状細胞診を利用したヒトパピローマウィルス(HPV)併用検診サービスを開始いたします。
液状細胞診用に採取した検体を発がん性の HPV を発見する検査に用いることによって、細胞の採取が一度で済み、受診者の負担を最小限に抑えることを可能とするもの。液状細胞診は従来法の直接塗抹法による細胞診に比べ、異型細胞の検出率が向上します。
<感想>ということです。
リンク先: http://www.gene-lab.com/new/post_73.html
きょうはここまで。
お気に入りの記事を「いいね!」で応援しよう
[プレスリリース] カテゴリの最新記事
-
子ども庁に関して 2021年04月09日
-
少年庁 いい人 奇策 2021年04月02日
-
麻生大臣 物忘れ 自閉症スペクトラム 2021年03月22日
【毎日開催】
15記事にいいね!で1ポイント
10秒滞在
いいね!
--
/
--
© Rakuten Group, Inc.









