医療用医薬品 0
[プレスリリース] カテゴリの記事
全841件 (841件中 601-650件目)
< 1 ... 8 9 10 11 12 13 14 15 16 17 >
-
次世代白内障手術装置 術中の眼内圧変動を減少させる独自の灌流制御システムを搭載
次世代白内障手術装置 術中の眼内圧変動を減少させる独自の灌流制御システムを搭載 CENTURION® VISION SYSTEM 7月 22日発売 ~安全性と効率性を高次元で融合し、手術医と患者様に最良の結果を提供~出典:プレスリリース 日本アルコン株式会社(本社:東京都港区、代表取締役社長: 松村誠一郎)は、白内障手術装置「CENTURION® VISION SYSTEM」を7月22日(火)より発売します。当製品は、手術中に変化する灌流圧を自動的かつ継続的にモニタリングする業界初のシステムを搭載し、眼内圧の変動による術中のリスクを低減させることで、手術の安全性と効率性の向上に寄与します。 従来は灌流液を注入するボトルを高い位置に吊るし、ボトルを上下させて重力を変えることで手術中の眼内圧をコントロールしていましたが、術中に瞬時に灌流液の量や灌流圧を変化させることはできませんでした。 Active Fluidics™ テクノロジーは、灌流バッグを本体内部の 2 枚のプレート間に設置し、手術装置本体が検知した流体の変化に応じて、灌流バッグを加圧減圧することで、灌流圧を調整し、手術中の眼内空間を安定的に確保します。これにより、手術中の眼内圧変動が低減され、手術医が設定した適切な眼内圧を維持することで、手術の安全性向上に寄与します。 これはは安全性が上がることでしょう。ただし、1台2,580万円
2014年07月18日
コメント(0)
-
一目惚れの分子メカニズム 異性の存在が性ホルモンの分泌を変える仕組みを解明
一目惚れの分子メカニズム異性の存在が性ホルモンの分泌を変える仕組みを解明出典:プレスリリース 早稲田大学教育・総合科学学術院/先端生命医科学センター(TWIns)のグループは、異性の存在が性ホルモンの分泌を変化させる新しい神経機構を明らかにしました。これまで社会環境の違いが、脳にどのような変化をもたらして人間や動物の行動や生理状態を変化させるのかは不明でしたが、ウズラを用いた本研究により雄が雌を見ると脳内で注意や覚醒に重要な神経伝達物質であるノルエピネフリンの分泌が急性的に高まり、GnIHの分泌を増やすことにより、男性ホルモンの血中濃度を下げることが分かりました。ノルエピネフリンとGnIHは人間や多くの動物に共通して存在することから、私たちヒトを含めた哺乳類でも同じ仕組みが存在することが考えられ、私たちが一目ぼれするときの神経機構に繋がる発見となりました。 人間も社会的な情報によって行動や生理状態は瞬時に変化します。例えば、異性と同性の前では態度や行動が変わってしまうことや、素敵な異性を前にすると性ホルモンの分泌が変化することは知られています。しかしながら、社会環境の違いが、脳にどのような変化をもたらして人間や動物の行動や生理状態を変化させるのかは不明でした。 異性の存在が、ノルエピネフリンやGnIHを介して、性ホルモンの分泌を瞬時に変化させる新しい神経機構が解明されました。本研究成果は、雌の存在を認知する際に視覚に大きく依存する動物モデルとして、鳥類のウズラから得られたものですが、ノルエピネフリンとGnIHは人間や多くの動物に共通して存在することから、私たちヒトを含めた哺乳類でも同じ仕組みが存在することが考えられます。本研究成果は、一目ぼれするときの神経機構や分子メカニズムの解明に貢献するものです。 一目惚れなのかな?必ずGnIH出るのならば、異性をみればみんな一人惚れする?
2014年07月18日
コメント(0)
-
ヒトとマウスの甘味受容体の機能の違いを解明
ヒトとマウスの甘味受容体の機能の違いを解明- ヒトの客観的な味覚評価法の構築に向けて -出典:プリスリリース 味を受け取る基本的な仕組みは、味の感受性の個体差が少ないマウスを利用することで解明されてきており、甘味や苦味は舌の細胞にあるセンサーが感知していること、センサーはそれぞれの味に対応した受容体と呼ばれる膜タンパク質であることが明らかになってきました。近年、味の感受性は動物ごとに異なるとの報告もなされるようになってきたところです。 今回、農研機構、理化学研究所と岡山大学は、細胞膜上の甘味受容体を検知する方法を開発して、ヒトとマウスでは甘味受容体が細胞内で合成されてから細胞膜へ移動する仕組みが全く異なることを発見しました。この結果は、ヒトならではの甘味を受け取る仕組みがあることを示唆しています。今後は、ヒトの味覚受容体を使って簡便で客観的な味覚評価技術を開発し、食品の味の評価に活用する予定です。 今まではマウスがおいしいと感じるものを、一番いいものとして扱ってきたけれども、やはり専門家の官能評価を優先するべきと言うことですかね。 いま、「神狩り2」(「クオリア」という概念も扱ったSFです)を読んでいるところなの色々迷います。
2014年07月17日
コメント(0)
-
弊社カラーコンタクトレンズに関する安全性についての見解
弊社カラーコンタクトレンズに関する安全性についての見解 出典:プレスリリース 本年 5 月 22 日付で、独立行政法人国民生活センターよりカラーコンタクトレンズの安全性に関するテスト結果が発表されました。また、日本コンタクトレンズ学会主催の第 57 回日本コンタクトレンズ学会総会においては、「カラーコンタクトレンズ障害を解剖する」と題したシンポジウムが開催されました。 弊社製品フレッシュルック®デイリーズ®イルミネート®及びフレッシュルック®デイリーズ®に関しまして、十分な酸素透過性、レンズ表面の平滑性が確保されており、色素のレンズ表面への露出も認められないと認識しております。 また、フレッシュルック®デイリーズ®およびフレッシュルック®デイリーズ®イルミネート®の発売開始以来、製品が原因で引き起こされた重篤な角膜障害は報告されておりません。さらに、日本アルコンでは 24 時間 365 日、オペレーターがユーザー様からのお問い合わせに対応しており、(ビジョンケアコール電話番号:0120-389103) 万が一、医療機関あるいはユーザー様より、製品の安全性に関するご連絡をいただいた場合は、社内の手続きに則り速やかに対応しております。 よって弊社といたしましては、製品に同梱されております添付文書に従った適切な使用と、眼科医による処方ならびに定期的な検査を受けていただくことで、安全にご使用いただけるコンタクトレンズであると考えております。 添付文書も大丈夫と言い切ったのはアルコンが初めてじゃないでしょうか。
2014年07月17日
コメント(0)
-
Googleと「スマートレンズ」技術供与契約を締結
Googleと「スマートレンズ」技術供与契約を締結 出典:プレスリリース ノバルティスは、同社のアイケア部門であるアルコンとGoogle Inc.の部門の間で、あらゆる眼の医療用途を目的とした Google の「スマートレンズ」技術ライセンス供与契約を締結したことを発表しました。世界規模の課題に新たなソリューションを見出す専門チーム、Google[x]との契約締結により、アルコンは、Google の「スマートレンズ」技術を発展させ、商品化する機会を得ました。同技術はアイケアのあり方を変え、アルコンの研究開発およびコンタクトレンズ・眼内レンズ(IOL)におけるグローバルなリーダーシップをさらに強化する可能性を秘めています。なお、今回の取引は、独占禁止法に関する承認を条件とします。 糖尿病患者の疾患管理を支援します。これは、スマートコンタクトレンズを用いて眼内の涙液測定データをモバイル機器にワイヤレス送信することで、身体への負担を最小限に抑えつつ、常に血糖値レベル測定を行うことを可能とします。 眼鏡なしでは文字が読めない老眼患者に対して、視力矯正調節機能を有するスマートレンズをコンタクトレンズ、または屈折性白内障治療に用いる IOLとして利用することで、手元に自然に焦点を合わせる眼機能回復を支援します。 老眼用のスマートレンズは興味あるところですが、老眼でどれぐらいの人がコンタクトレンズを使っているんでしょうか?
2014年07月17日
コメント(0)
-
テルモ、閉鎖式輸液システム「シュアプラグAD」シリーズを発売
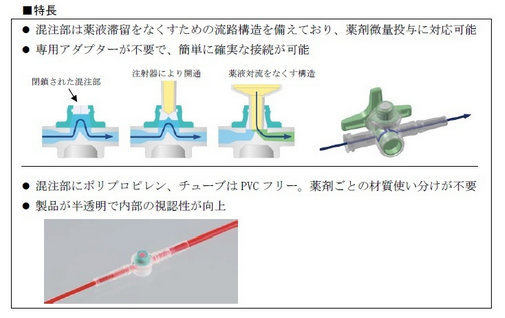
院内の各部署の様々な点滴ニーズに対応テルモ、閉鎖式輸液システム「シュアプラグAD」シリーズを発売 出典:プレスリリース テルモは、薬剤微量投与に対応可能な構造を採用した閉鎖式輸液システム「シュアプラグAD」シリーズを、このほど全国の医療機関向けに本格販売を開始しました。 製品の混注部は、薬液滞留をなくすために独自に開発した新構造を採用しており、薬剤の微量投与にも対応可能です。また、注射器や点滴器具を接続する際に専用のアダプターは不要で、簡単にかつ迅速に薬液を注入できるようになります。これにより物品管理もしやすくなり、操作間違いなどのリスクの低減など、経済面、臨床面での価値をもたらすことが期待できます。 このような工夫はもっと評価されていいと思います。
2014年07月17日
コメント(0)
-
“花色素ポリフェノールEX※1”配合育毛剤が 女性の育毛および発毛に有効であることを確認
“花色素ポリフェノールEX”配合育毛剤が女性の育毛および発毛に有効であることを確認― 第32回日本美容皮膚科学会 総会・学術大会で発表 ― 出典:プレスリリース サントリー健康科学研究所は、花色素ポリフェノールEX(シアニジン、デルフィニジン、ペラルゴニジンの3種のアントシアニジンを“花色素ポリフェノール”と称し、その含有エキスを混合配合したポリフェノールエキスを“花色素ポリフェノールEX”と呼称しています)を配合した育毛剤が女性の育毛および発毛に有効であることを確認しましたので、第32回日本美容皮膚科学会 総会・学術大会(7月12-13日、千葉県)にて発表しました。 ヒトの毛乳頭細胞を用いて、“花色素ポリフェノール”(シアニジン・デルフィニジン・ペラルゴニジン)の育毛機能を調べました。育毛機能は毛乳頭細胞増殖活性、VEGF産生促進作用およびFGF-7産生促進作用を指標に評価しました。 シアニジンに毛乳頭細胞増殖活性、デルフィニジンにVEGF産生促進作用、ペラルゴニジンにFGF-7産生促進作用が確認され、“花色素ポリフェノール”には育毛作用を有する可能性が示唆されました。 薄毛、抜け毛が気になる女性22名(40~65歳)を対象に、医薬部外品有効成分および“花色素ポリフェノールEX”等を配合した育毛剤を1日2回、12週間継続して使用いただき、対象者全員の頭頂部の毛髪画像をデジタルマイクロスコープによって定期的に撮影することで、試験期間中の育毛効果を評価しました。 頭頂部の非軟毛数は、“花色素ポリフェノールEX”配合育毛剤使用12週間後に平均で1cm2当たり約10本の増加が認められました。頭頂部の総毛髪数(非軟毛+軟毛)においても、使用12週間後に平均で1cm2当たり約20本の増加が認められました。また成長期毛率は増加し、休止期毛率は減少していました。 In Vitroは陽性対象がおいてあるので、増加量に関しての評価が可能ですが、人の試験では陽性対象がない上、経時変化でどんな検定しているか分からないので、評価不能です。
2014年07月17日
コメント(0)
-
アルツハイマー病での役割も示唆されている神経幹細胞に関する成果が専門誌Development に掲載されました。
アルツハイマー病での役割も示唆されている神経幹細胞に関する、創薬モデル動物開発研究プロジェクトチーム(津田玲生リーダー)とマサチューセッツ医科大学との共同研究の成果が専門誌Development に掲載されました。 出典:プレスリリース 成人の脳では古い神経細胞が脱落するのを代償する形で新たな神経細胞が産生されています。一方、アルツハイマー病(AD)の脳では、この神経細胞を供給するシステムのどこかに異常があり、脳の機能が正常に働かないと考えられています。 REST のショウジョウバエ相同因子である Charlatan(Chn)が中腸を作り出す幹細胞で働いていることを見いだしました(Development 誌7月号)。本成果により、幹細胞には進化的に共通した調節機構が存在することが解り、Chn の機能を明らかにすることにより神経幹細胞から神経細胞への供給メカニズムの理解につながると考えられます。このように、ショウジョウバエというモデル動物を使った研究は AD の発症メカニズム解明のために役立っています。 オリジナルのアブストラクトも読んでみましたが、タイトルと実験内容のつながりが分かりませんでした。勉強不足ですいません。
2014年07月16日
コメント(0)
-
細胞に「食べる」機能を付与
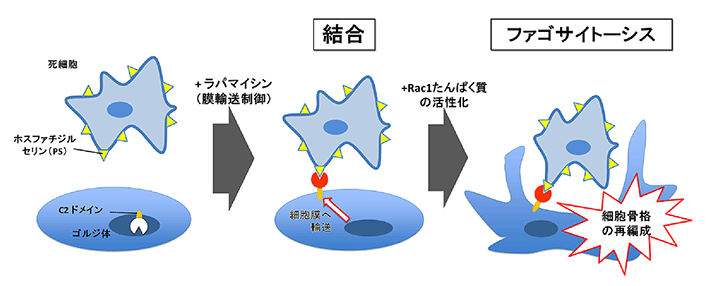
細胞に「食べる」機能を付与~細胞に新機能を付与する新しい研究ツール~ 出典:プレスリリース 不要になった細胞は、貪食細胞と呼ばれる細胞のファゴサイトーシスという現象によって「食べ」られ、貪食細胞内で消化、除去されます。 FKBP、FRBは、有機小分子ラパマイシン(rapamycin)の添加によって結合する性質を持っています。このような実験系に基づいて、これまでに「細胞内部」の重要な生命現象を速い時間スケールで制御する実験系の開発が精力的に行われてきました。その一方で「細胞表面」の情報伝達を速い時間スケールで制御する実験系というのは、これまでにほとんど開発が行われておらず、有用な手法の確立が強く望まれていました。 目的とする機能性たんぱく質を、細胞内小器官であるゴルジ体の膜上に集積させておき、任意のタイミングで細胞膜に輸送されるたんぱく質と結合させることで、細胞膜外に発現させる実験系を構築することを目指しました。 Giantin(ジャイアンティン)のゴルジ体膜貫通部位とK-Ras(K-ラス)の細胞膜標的配列の組み合わせであれば輸送効率が高いことを見いだしました。膜輸送を利用するという性質上、この局在の変化を伴う摂動系は15分~45分という時間を要しますが、現在ある細胞表面提示の摂動系としては最も速いものです。井上准教授らはこの手法をDISplay(dimerization-induced surface display)と名づけました。 でDISplay法を適用した細胞内で、Rac1を活性化させることとしました。すると、C2ドメインが細胞表面にあり、かつRac1が活性化した細胞は、死細胞を細胞内に取り込んでおり、ファゴサイトーシス現象が起こることが分かりました。 「DISplay」法は、細胞に付与した新しい機能を分単位で発現させることを可能とする点で非常に画期的といえます。今後の展開としては、DISplay法をさらに改良することでファゴサイトーシスの効率と精度を高めること、またそうした次世代型DISplay法を適用することで、将来的にがん細胞などの病原細胞を生体内でファゴサイトーシスできるような人工細胞を作製し治療に応用することが挙げられます。 C2ドメインが特定の細胞を捕まえることになれば、ミクロの決死隊ですね。 あと「食べる」を消化の方を想像してとんでもない技術ができたのかなと思いましが。この技術はとてもすごいのですが。 遺伝子レベルでの解明は設計図を見ているだけで、体内ではほんとに動くのかっていつも思っているので、こういう研究、好きです。
2014年07月16日
コメント(0)
-
大塚製薬 新規抗精神病薬「ブレクスピプラゾール」 統合失調症と大うつ病補助療法の治療薬として米国FDAに申請
大塚製薬 新規抗精神病薬「ブレクスピプラゾール」 統合失調症と大うつ病補助療法の治療薬として米国FDAに申請 出典:プレスリリース 大塚製薬と H.ルンドベック A/は、2014 年 7月 11日、米国 FDAに「ブレクスピプラゾール」の販売承認申請を行いましたのでお知らせします。申請した適応症は、統合失調症単剤療法と大うつ病補助療法です。 本申請は、フェーズ 2とフェーズ3試験において6,500名以上が登録されそのうち 5,300名に「ブレクスピプラゾール」が投与された 7 つの臨床試験をもとに行いました。今回申請したデータが申請要件を満たすと米国FDAから評価された場合、本申請の正式な承認申請受理は本年 9月に確認できる見込みです。 ポストアリピプラゾールですか。ちょっと不思議なのはフェーズ2、3試験で6,500名以上が登録され、5,300名がブレクスピプラゾールが投与されているというところです。よほど効果が期待できるので、1:1割り付けではなかったのかな。
2014年07月16日
コメント(0)
-
プラザキサ®に対する特異的中和剤を、米国食品医薬品局(FDA)が「画期的治療薬」に指定
プラザキサ®に対する特異的中和剤を、米国食品医薬品局(FDA)が「画期的治療薬」に指定出典:プレスリリース 米国食品医薬品局(FDA)は、ベーリンガーインゲルハイムが開発中の中和剤idarucizumab(ヒト化抗体フラグメント)を、「画期的治療薬」に指定しました。idarucizumabは、プラザキサ®の抗凝固作用に対する特異的中和剤として現在開発が進められています。 現在グローバルで進行中のREVERSE-AD試験では、臨床現場でプラザキサ®を服用中で、従来の治療で対処困難な出血を発症した、あるいは緊急処置を要する患者を対象にこの中和剤を評価します。35ヵ国以上の500を超える施設で実施される予定で、新規経口抗凝固剤に対する治験開発中の中和剤について、患者を対象に評価する初めての臨床試験です。 プラザキサ®は、新世代の経口抗凝固剤の中で初めて広範に承認を受けた薬剤であり、急性および慢性の血栓塞栓症の予防/治療における高いアンメット・メディカル・ニーズに対応することができる直接トロンビン阻害剤(DTI)です5,6。直接トロンビン阻害剤は、血栓形成プロセスにおいて中心的な役割を果たす酵素であるトロンビンの活性を特異的に阻害することにより、強力な抗血栓作用を発揮します7 。様々な凝固因子を介して多様な作用を示すビタミンK拮抗薬とは異なり、プラザキサ®は有効かつ予測可能で再現性のある抗凝固作用を示します。 接着剤はそれをはがすものが開発されないと発売されないと聞いたことがあります。ヘパリンに変わりうるプラザキサ®に関しても、出血時の対応薬が開発されることはとても意味があると思います。
2014年07月16日
コメント(0)
-
アストラゼネカのプロトンポンプ阻害剤「ネキシウム®」小児への適応拡大に関する臨床試験開始
アストラゼネカのプロトンポンプ阻害剤「ネキシウム®」小児への適応拡大に関する臨床試験開始出典:プレスリリース アストラゼネは、プロトンポンプ阻害剤(以下、PPI)「ネキシウム®カプセル」および「エソメプラゾールマグネシウム水和物」混濁液用顆粒剤の2剤型について、小児における胃潰瘍、十二指腸潰瘍、逆流性食道炎などの胃酸関連疾患の適応拡大を目的とした臨床試験を開始いたしました。 本試験では、1~14歳までの小児を対象に、ネキシウム®カプセルおよびエソメプラゾールマグネシウム水和物の混濁液用顆粒剤10mg、および20mgの安全性、薬物動態、薬力学および有効性を検討します。 海外では、エソメプラゾールマグネシウム水和物は、米国、カナダ、スウェーデンをはじめ、70カ国以上で小児への使用が認められています。また、混濁液用顆粒剤は米国で2006年10月20日に1~11歳向けとして初めて承認されています。 小児の地検はむずかしいので、大変と思います。今回は臨床薬理試験だけで適応を取りに行く方針なのでしょうか。その後NSAIDとの併用というのはげすの勘ぐり?
2014年07月16日
コメント(0)
-
理事会声明 小児(集中治療における人工呼吸中の鎮静)におけるプロポフォールの使用に関して
理事会声明 小児(集中治療における人工呼吸中の鎮静)におけるプロポフォールの使用に関して日本集中治療医学会出典:プレスリリース1、2 当学会の薬事・規格・安全対策委員会では、4 月 30 日に本事例についてホームページ上で注意喚起する一方、小児集中治療委員会では 3 月にまず小児集中治療専門施設に対し人工呼吸中の鎮静におけるプロポフォール使用のアンケート調査を実施しました。その後、本学会専門医研修認定施設に対しても、同様のアンケート調査を行い、6月末にその調査結果が理事会に報告されました。その内容を理事会で検討し、本日(7 月 14 日)、ホームページ上で公表することになりました。本調査結果より、我が国において小児の集中治療における人工呼吸中の鎮静にプロポフォールの使用が複数の施設で行われていることが明らかとなりました。 当学会は、本調査結果を受けて、小児(集中治療における人工呼吸中の鎮静)に対するプロポフォールの医学的妥当性および安全性を代替薬との比較も含めて検討する研究班を立ち上げることに致しました。 日本集中治療医学会認定専門医研修認定 ICU と PICU において、鎮静薬としてのプロポフォール使用状況を調査した。プロポフォールは、成人集中治療では一般的に使用され、小児集中治療においても単回投与使用に加え、持続投与による鎮静も稀ではない現状があった。 プロポフォールはM.ジャクソンが睡眠薬代わりに使用して、なくなったので、一般には知られるようになったと思います。 不思議な点が2つ、ICUにいるような人工呼吸をしているような小児の患者では検査が継続的に行われており、何かあればすぐに対処できたのではないか? 報告書は単にアンケートを行い、これから検討しますとあります。調査時に代替薬の調査がなく、プロポフォール以外では本当に安全なのかがよく分かりません。患者はもしかすると毎日発生しているかもしれないのに、こんなにゆっくりな対応でいいのでしょうか。また、調査に基づき、学会が発表したリコメンドはエビデンスとしては低く、禁忌であるリスクよりも本当にベネフィットがあると考える人が多いのであれば、製薬メーカーに働きかけて、臨床試験を行うべきでしょう。
2014年07月15日
コメント(0)
-
アステラス製薬 下痢型過敏性腸症候群治療剤「イリボー®錠/イリボー®OD錠」 日本での効能・効果追加申請に関するお知らせ
アステラス製薬 下痢型過敏性腸症候群治療剤「イリボー®錠/イリボー®OD錠」 日本での効能・効果追加申請に関するお知らせ 出典:プレスリリース アステラス製薬は、下痢型過敏性腸症候群治療剤「イリボー®錠2.5µg、同5µg/イリボー®OD 1)錠2.5µg、同5µg」(一般名:ラモセトロン塩酸塩)について、本日、女性における下痢型過敏性腸症候群2)に関する効能・効果追加の申請をしましたので、お知らせします。 「イリボー®錠/イリボー®OD錠」は、5-HT3受容体を選択的に阻害することで、消化管運動亢進に伴う便通異常(下痢・排便亢進)を改善するとともに、大腸痛覚伝達を抑制し、腹痛及び内臓知覚過敏を改善することが期待されています。 イリボーの男性に対する審査報告書では 本薬の薬物動態、有効性及び有害事象の発現頻度において男性と女性では異なる傾向が認められており、提示された臨床試験成績からは女性に対する本薬の至適用量は明確になっておらず、女性に対する有効性及び安全性は確立していないと考える。 薬物動態について、男性に対する女性の幾何平均値比[95%信頼区間]は、Cmax1.511[1.271,1.797]及び AUCinf 1.745[1.439, 2.114]であり、いずれも 1を含まなかったため、有意な性差が認められると判断された。 以上から、本薬で認められている薬物動態に性差が認められた理由は代謝過程、特に薬物代謝酵CYP1A2 の影響が大きく関与しているものと考えられる。 ということで、男性のみの許可でした。今年は再審査結果が公開されており、 総合評価 機構は、以上の安全性及び有効性の評価に基づき、カテゴリー1(薬事法第 14条第 2項第 3号イからハまでのいずれにも該当しない。)と判断した。(2014年3月24日再審査) この薬は便秘時に始めると、重篤な有害事象につながる可能性があります。女性の場合は血中濃度も高くなるようですし、注意して使う薬剤になりそうです。
2014年07月14日
コメント(0)
-
小動物用核磁気共鳴イメージングシステムの運用
小動物用核磁気共鳴イメージングシステムの運用出典:プレスリリース この度OISTでは、小動物における生体の代謝や機能といった高度な生体情報の解析を可能にする、小動物用核磁気共鳴イメージングシステムを導入し、施設の運用準備を開始しました。解像度の高さを決める静磁場強度において、最高レベルの性能を持つ同システムの導入は、国内において本学が2例目です。現在、システム利用に向けて学内での調整を進めており、将来的には学外機関の研究活動にも寄与するものと期待されます。 臨床画像診断で広く用いられている核磁気共鳴撮像(MRI)は、生体を傷つけることなく、内部を可視化する診断機器の一つです。MRIは、主に生体内の水素原子核の磁気共鳴現象を捉えます。磁気共鳴現象とは、磁場の中で原子核が特定の周波数の電磁波と共鳴を起こす現象のことを指します。MRIでは、この共鳴によって生じる電磁波の強度と周波数を基に物質の違いを画像化します。そのため脳や内臓、筋肉など、水素原子を多く含む水が豊富な領域において、鮮明な画像が得られ、脳腫瘍や脳梗塞の検出に優れています。画像の元となる電磁波の強度は、用いる静磁場の強さ(テスラ)にほぼ比例し、得られる情報量に大きく影響します。医療用としては1.5テスラのMRIが広く普及していますが、本システムは、11.7テスラという国内最大磁場強度を誇り、極めて多くの情報を得ることができます。そのため、本システムはマウスなどの小型の動物においても、形態情報のみならず、代謝や機能に至る様々な生体情報の解析に優れた性能を発揮します。 生きたままで色々分析できるのは、代謝系の薬に関してはとても有用です。
2014年07月11日
コメント(2)
-
国際アルツハイマー病学会における 新たなアルツハイマー病研究開発データの発表について
国際アルツハイマー病学会における 新たなアルツハイマー病研究開発データの発表について出典:プレスリリース 武田薬品工業と Zinfandel Pharmaceuticalsは、2014 年 7 月 12 日から 17 日までデンマーク コペンハーゲンにおいて開催される国際アルツハイマー病学会でTOMMORROW 試験の最新データを発表。 TOMMORROW 試験認知機能が正常な高齢者を対象とした、アルツハイマー病に起因する軽度認知機能障害の 5 年以内の発症リスクを予見するバイオマーカーを用いた評価手法(TOMM40 遺伝子型、アポリポタンパク質 E 遺伝子型および年齢で構成されるアルゴリズムを使用して特定する)を検証するとともに、同評価手法により発症リスクが高いと診断された高齢者において、低用量 AD-4833(一般名:ピオグリタゾン)の投与による同疾患の発症遅延効果を評価する臨床第 3 相試験。2013 年 8 月に武田薬品とジンファンデル社が開始。 試験開始1年だと、どんなデータが出るんでしょう?
2014年07月11日
コメント(0)
-
肥満に伴う代謝異常とリゾリン脂質の関わりを解明
肥満に伴う代謝異常とリゾリン脂質の関わりを解明出典:プレスリリース 肥満に伴う脂肪組織の肥大や全身の代謝異常に、リゾホスファチジン酸を作る酵素であるENPP2(オートタキシン)が関わっていることを明らかにしました。ENPP2は白色脂肪組織だけでなく、熱産生やエネルギー代謝に重要な褐色脂肪組織・骨格筋にも作用があり、糖代謝を制御していました。解析には新たに開発した二光子顕微鏡による生体分子イメージングを用いています。 ENPP2とは、別名オートタキシンといい、癌細胞の遊走に重要な、つまり癌を呼び寄せる作用のある酵素として見つかりました。ENPP2はリゾリン脂質という特殊な脂質(リゾホスファチジン酸)を作るだけでなく、ENPP2自体も多くの作用があります。今回の研究で、ENPP2の肥満に対する関わりが明らかになりました。 ENPP2は多くの臓器で発現が見られますが、脂肪組織、特に(前駆)脂肪細胞で多く作られています。そこで、ENPP2の生体での作用を明らかにするために、ENPP2の全身欠損マウス、脂肪細胞特異的欠損マウス、脂肪細胞特異的過剰発現マウス、の3種類を作成しました。ENPP2ヘテロ欠損マウス、脂肪細胞特異的ENPP2欠損マウスでは高脂肪食に伴う肥満、脂肪組織増殖が抑えられており、「やせたマウス」ができました。さらに、体重の抑制に加えて、肥満に伴う糖尿病の著明な改善がみられました。さらに、いずれのマウスでも褐色脂肪組織の機能が改善しており、全身のエネルギー消費量が増加していました。 ENPP2は直接インスリン作用を低下(阻害)させる他、脂肪細胞の分化・増殖にも関わっていました。これらの作用は、ENPP2によって生合成される脂質の働きだけでは説明できず、ENPP2の直接的な作用が考えられています。 オートタキシンは色々な効果を現す酵素として認識しています。生産物はリゾホスファチジン酸ですが、その中間過程で色々な補酵素を消費したりするからと思います。 「やせたマウス」の寿命とか糖尿病以外の病気、特に脳卒中の増加に興味があります。ある目的を持って今回のようなマウスを作ることができますが、寿命、生殖能力、知能ぐらいは抑えておいてデータベース化する意義はあるのではないでしょうか。
2014年07月11日
コメント(0)
-
iPS細胞誘導技術を応用して人工大腸がん幹細胞を作製することに成功
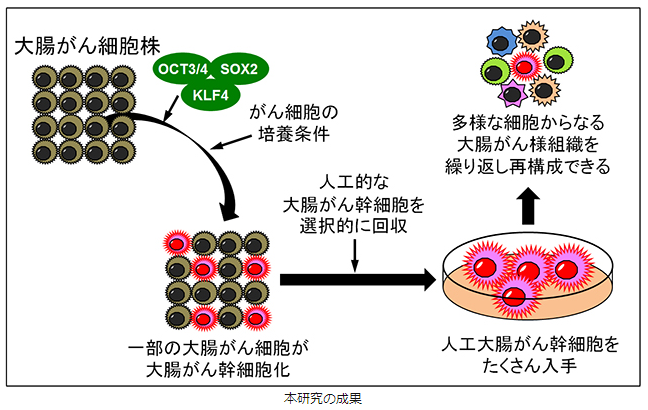
iPS細胞誘導技術を応用して人工大腸がん幹細胞を作製することに成功出典:プレスリリース 大嶋野歩 医学研究科/iPS細胞研究所研究員、坂井義治 医学研究科教授、山田泰広 iPS細胞研究所教授と、青井貴之 神戸大学医学研究科内科系講座iPS細胞応用医学分野特命教授らの共同研究グループは、iPS細胞誘導技術をがん研究に応用することで、人工的に大腸がん幹細胞を作製することに成功しました。 本グループは、人工的にがん幹細胞を作製することで、がん幹細胞を豊富に入手することができれば、がん幹細胞研究を推進することができると考え、本研究を行いました。その結果、iPS細胞誘導の際に用いられる遺伝子(OCT3/4, SOX2, KLF4)を大腸がん細胞株に導入した後、iPS細胞作製とは異なる培養環境を用いることで、一部のがん細胞に大腸がん幹細胞でみられる特徴を獲得させることに成功し、人工大腸がん幹細胞と名付けました。 さらに、この人工大腸がん幹細胞を選択的に回収する方法も開発しました。また、この人工大腸がん幹細胞を詳しく調べた結果、ヒトがん組織中のがん幹細胞と同様の特徴を示すことを確認しました。 最近、癌の新しい知見が続々出てきます。がん細胞は間葉細胞をまわりに身をつけて冬眠しているとか、免疫をすり抜けるためのタンパクを出しているとかです。 今回の発見もその一つに今後入ってくる可能性があります。がん幹細胞は一般のがん細胞とどれだけ違っているかとか、基礎的な研究がまだまだ、必要になります。既存の抗悪性腫瘍剤のスペクトラムの見直しも必要でしょう。 治療に結びつくのが、がん幹細胞が大腸癌様組織を再構成するステップ、がん幹細胞の抗悪性腫瘍薬剤の効果(これは一からやっておくべきだと思います。幹細胞が裸の状態であれば低用量で効果を示し、安全域が広がる可能性があると思うからです。その方が医療費も安くなります。ただ、臨床応用には新たなターゲット療法が必要になるかもしれません。ただ選択的に大腸がん細胞を回収できるのですから、レーダーはすでにあるので、それに対してロケットをどう飛ばすかだけだと安直に考えます。)
2014年07月11日
コメント(0)
-
国内初の当年予測 2014年のがん罹患数、死亡数予測公開
国内初の当年予測 2014年のがん罹患数、死亡数予測公開出典:プレスリリース 独立行政法人国立がん研究センターがん対策情報センターは、本年2014年に新たにがんと診断される罹患数と死亡数の予測をがん情報の総合サイト「がん情報サービス」にて7月10日に公開しました。 これまで、罹患数においては地域がん登録による全国がん罹患モニタリング集計2010年が、死亡数においては人口動態統計により2012年の実測値が、それぞれ最新統計として公開されていますが、いずれも集計に時間を要し数年遅れでの公開のため、今現在と直近の変化を知ることが出来ませんでした。予測数値は、現在のがん対策を継続した場合を前提に算出するため、後に公開される当該年の実測値と突き合わせることにより、それまでに実施されたがん対策の評価・分析を行うことが可能となります。 今回の2014年予測は、罹患数は全国がん罹患モニタリング集計の年齢階級別がん罹患数(1975~2010年全国推計値)を、死亡数は人口動態統計がん死亡数(1975~2012年実測値)を用いて算出しました。今後、2016年に施行されるがん登録推進法により罹患数の実測数値の集計が可能となれば、データソースがより確かな数値となり、予測数値の精度も上がると思われます。今後も予測精度を検証しつつ、ニーズに沿ったがん統計情報を整備してまいります。 この予測からの考察がどのような背景から考察されるかによって、 恣意的に使えるデータであることに気をつける必要があります。と前振りをしておいて私の考察 胃癌が相変わらず罹患数で1位です。ピロリの除菌の効果はあったのでしょうか。 肺がんは喫煙率の低下にもかかわらず、増加傾向にあります。罹患数ではついに大腸癌を抜いてしまいました。たばこ以外にもっと大きなリスクが隠れているのではないでしょうか。 高齢化のリスクは他の要因を上回る? 他の病気で死ななければ結局癌あるいはその合併症で死ぬ? 肝臓癌の死亡数は膵癌に抜かれました。罹患数ではまだ肝臓癌の方が多いと言うことは、早期発見、治療の進歩が肝がんでは進んだ可能性があるの? 膵癌の煙草のリスクは糖尿病よりも高いように記載されているが、喫煙率は低下し、糖尿病が急速に増加している中での膵癌の増加は煙草と、糖尿病のリスクの見方を変える必要はないでしょうか。 と煙草を援護するようなことを書いていますが、禁煙を勧めることには反対ではありません。煙草の税金を上げて、煙草農家への転業資金と健康保険にのみ使用するのであれば、1本1500円にぐらいにすることを望みます。(その資金がどこに行っているか分からない状態ではたばこ税の値上げは反対です)
2014年07月11日
コメント(0)
-
科学技術振興機構が植物由来生分解性樹脂製造技術開発の成功を認定
科学技術振興機構が植物由来生分解性樹脂製造技術開発の成功を認定出典:プレスリリース カネカは、2009年1月に独立行政法人科学技術振興機構より受託した、独創的シーズ展開事業「委託開発」の開発課題「植物由来生分解性樹脂」(製品名:カネカ バイオポリマー アオニレックスⓇ)の開発に対し、JSTより開発成功の認定を受けました。 当社高砂工業所にて2011年5月より稼働を開始した生産実証試験設備で、連続運転による培養生産性、培養後収率について目標を達成しました。また、製造した樹脂を用いて設計した農業用マルチフィルム(雑草抑制、地表乾燥防止、温度調整などを目的として畑に張る農業用フィルムのこと。現在は主に石油由来のポリエチレン系樹脂が使用されている。生分解性樹脂は回収作業や廃プラ処理が不要なため、今後の農業用マルチフィルム原料として期待されている。)、はグリーンプラ識別表示可能な配合で、既存石油由来生分解性フィルムと同等以上の物性が得られているなどの基準を達成しました。 農業が原油の値段に左右されるのを少しでも減らせることができるので大変有用な技術だと思います。
2014年07月10日
コメント(0)
-
テラ株式会社、医療法人社団医創会が共同で新規がん抗原サーバイビンペプチド及びMAGE-A4ペプチドを用いた樹状細胞ワクチン「バクセル(R)」の臨床試験を開始
テラ株式会社、医療法人社団医創会(セレンクリニック東京)が共同で新規がん抗原サーバイビンペプチド及びMAGE-A4ペプチドを用いた樹状細胞ワクチン「バクセル(R)」の臨床試験を開始出典:プレスリリース テラ及び医療法人社団医創会は共同研究契約を締結しました。この共同研究契約に基づき、テラはセレンクリニック東京と共同で、がんの患者を対象とする、新規がん抗原サーバイビンペプチド及びMAGE-A4ペプチドを用いた樹状細胞ワクチン「バクセル®」の臨床試験を開始いたします。 本臨床試験に用いるサーバイビンペプチド及びMAGE-A4ペプチドは、本特許を使用したMHCクラスI+MHCクラスII拘束性のハイブリッドロングペプチドであり、がんに対する免疫をこれまで以上に活性化することができる次世代のがん抗原ペプチドです。本臨床試験は、サーバイビンペプチド及びMAGE-A4ペプチドを用いた樹状細胞ワクチン「バクセル®」の安全性及び有効性の評価を行い、新規がん抗原の早期実用化に繋げてまいります。 セレンクリニック東京を含む医療法人社団医創会 セレンクリニックグループは、樹状細胞ワクチン「バクセル®」において3,528症例(2014年6月末時点)の治療実績を持ち、テラの契約医療機関の中で最多の実績を持ちます。また、テラと共同で過去の臨床データを解析し、論文発表や学会発表を行うことでより良い治療をがん患者のみなさまへ提供できる取り組みを推進しています。 よくわからない。3,528例も使用例があるのならば、製造販売承認できると思うのですが。
2014年07月10日
コメント(0)
-
アステラス製薬:アゾール系抗真菌剤イサブコナゾール 米国での承認申請に関するお知らせ
アステラス製薬:アゾール系抗真菌剤イサブコナゾール 米国での承認申請に関するお知らせ出典: プレスリリース アステラス製薬は、スイス バシリア社と共同で開発を進めているアゾール系抗真菌剤イサブコナゾールについて、アステラスファーマUS, Inc.が、「侵襲性アスペルギルス症及びムーコル症」の効能・効果で米国食品医薬品局(FDA)に販売許可申請を提出しましたので、お知らせします。 イサブコナゾールは、侵襲性アスペルギルス症及びムーコル症の適応症に関し、FDAからQualified Infectious Disease Product(QIDP)指定を受けています。米国ではQIDP指定により、優先審査と5年間の独占販売期間の延長が認められます。また、両適応症に関し、希少疾病用医薬品としての指定も受けています。 SECURE試験は無作為化二重盲検試験です。アスペルギルス又は他の糸状真菌による侵襲性の真菌感染症に対する一次治療として、ボリコナゾールに対する統計的な非劣性を検証することが試験の目的ですが、包括解析対象の 516 例において、イサブコナゾールは投与 42 日目までの総死亡率の主要評価項目を達成しました(イサブコナゾール群:18.6%に対し、ボリコナゾール群:20.2%)。両群の95%信頼区間の差は、事前に規定された非劣性の基準である10%の範囲内でした。 日本でもボリコナゾール(ブイフェンド:ファイザー)との同等性試験で承認されるのかな?
2014年07月10日
コメント(0)
-
全可視光の利用と発生した水素・酸素の分離を同時に可能にする 人工光合成システムの開発に成功
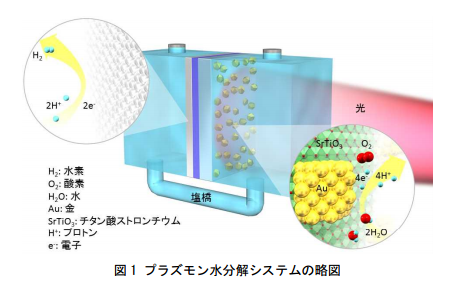
全可視光の利用と発生した水素・酸素の分離を同時に可能にする 人工光合成システムの開発に成功 出典:プレスリリース 再生可能エネルギーである太陽光エネルギーを安定的に貯蔵でき,かつ運搬も容易な化学エネルギー(化学物質)に変換する人工光合成の研究は,人類が直面する環境・エネルギー問題を解決するためのキーテクノロジーになると期待されています。 北海道大学電子科学研究所の研究グループは,首都大学東京,北海道大学大学院理学研究院と共同で光アンテナ機能を有する金属を担持した酸化物半導体基板を用い,従来の人工光合成では利用することができなかった 650〜850nm の可視・近赤外光も利用可能な人工光合成の開発に成功しました。 さらに,基板の表面と裏面に異なる金属を配置する極めて単純なシステムにより水を光分解し,それぞれの面から水素と酸素を分離して取り出すことに成功し,従来とは異なる方法論で水素の分離が可能であることを示しました。 こういう研究こそ進んで欲しいものです。
2014年07月10日
コメント(0)
-
1ナノメートルの人工分子マシン1個を「見て、触る」 - 光学顕微鏡による1分子モーションキャプチャ -
1ナノメートルの人工分子マシン1個を「見て、触る」- 光学顕微鏡による1分子モーションキャプチャ - 出典:プレスリリース ビーズプローブ光学顕微鏡1分子運動計測法(1分子モーションキャプチャ法)」は従来生体内でエネルギー変換を行う分子(生体分子マシン)の機能を解明するために考案された手法である。光学顕微鏡で可視化できるサイズのビーズを観察対象生体分子マシンに取り付けて、 “モーションキャプチャ”のマーカーのように用いるこの方法では、生体分子マシンの運動の方向性や一歩で進むサイズ、発生する力など他の計測では解らない多くのことが明らかになるため、人工的に作製した分子マシン(人工分子マシン)への適用が待たれていた。 しかしながら、人工分子マシンのサイズは生体分子マシンの1/10の1ナノメートル程度で、分子の小型化が引き起こすプローブの結合効率の低下やビーズと基板間の強い相互作用などの問題があり、本手法をそのまま適用するのは困難であった。 東京大学大学院工学系研究科は、自然科学研究機構岡崎統合バイオサイエンスセンター/分子科学研究所、物質・材料研究機構高分子材料ユニット有機材料グループと共に、大きさが1ナノメートルである人工分子マシン1分子のモーションキャプチャに成功した。研究グループは、サイズの小型化の問題点を考慮して従来の手法を改良することで、分子内の2枚の板状の部分がホイールのように回転(人工分子ベアリング)するダブルデッカーポルフィリン分子1個の回転運動を記録した。さらに、ビーズに外力をかけることで分子1個の運動を操作することにも成功した。 人工分子マシン1個の振る舞いを「見て、触り」ながら性能評価できるこの手法は、人工分子マシンの目標の一つ「力を発生して運動する人工分子モーター」の実証に適用できる現在唯一の方法である。将来、例えば光で駆動する分子モーターを作製し、生体分子モーターと接続することによって、生体のさまざまな化学反応を光で操作できるテーラーメイドなエネルギー変換技術が可能になると期待される。 こういう研究好きです。
2014年07月10日
コメント(0)
-
鞭毛モーターの規則的配列機構を解明 -鞭毛を動かす"エンジン"が正しい間隔で並ぶ仕組み発見-
鞭毛モーターの規則的配列機構を解明 -鞭毛を動かす"エンジン"が正しい間隔で並ぶ仕組み発見-出典:プレスリリース 東京大学大学院理学系研究科、、東京工業大学資源化学研究所研究グループは、名古屋大学エコトピア科学研究所、東京工業大学生命理工学研究科、コネチカット大学ヘルスセンター、マサチューセッツ大学メディカルスクールとの共同研究により、真核生物の鞭毛を動かすエンジンであるタンパク質「ダイニン」が、鞭毛を構成するタンパク質繊維「微小管」上に規則的に並ぶ仕組みを解明した。 「外腕ダイニン」の根元に存在する「ドッキング複合体」の性質に着目し、それ自体が約24nmの長さで、微小管上の決まった位置に数珠つなぎで結合することを突き止めた。ドッキング複合体が作った24nm周期の上に外腕ダイニンが乗ることで、ダイニンの24nm周期の結合ができあがる。鞭毛の構築メカニズムの理解だけでなく、外腕ダイニンの欠陥が主因と考えられているヒト疾患「原発性繊毛不動症候群」の研究に役立つと期待される。 ヒトの繊毛は気道から肺にかけて、不要物をはき出す役割を果たしているので、「原発性繊毛不動症候群」の患者は気管支拡張症などをきたします。
2014年07月10日
コメント(0)
-
シロアリの後腸に共生バクテリアによる新たな代謝経路を発見
シロアリの後腸に共生バクテリアによる新たな代謝経路を発見-シロアリのセルロース代謝経路の全体像が明らかに-出典:プレスリリース 理化学研究所(理研、野依良治理事長)と琉球大学(大城肇学長)は、オオシロアリに13C安定同位体標識化セルロースを与え、NMR(核磁気共鳴)法で代謝物を網羅的に追跡することで、腸管内の共生微生物群によるセルロース代謝経路を解析しました。その結果、新たな代謝経路を発見するとともに、シロアリと腸管内微生物群およびシロアリ個体同士の共生における栄養交換メカニズムの一端を解明しました。 共同研究チームは、陸上生態系モデルであるシロアリに、13C安定同位体標識化セルロースを餌として与え、その代謝経路を2次元NMR法により、宿主から共生微生物群までの全階層で可視化しました。その結果、これまで遺伝的解析などにより個々に予測されていた代謝経路の全体像を明らかにすることに成功するとともに、後腸の共生バクテリアによる新たな代謝経路を発見しました。さらに、必須アミノ酸を他の個体との栄養交換で摂取する栄養獲得経路も発見しました。 シロアリは植物が炭酸固定したセルロースを共生微生物で分解し、共生バクテリアが固定した窒素も利用しアミノ酸などに代謝する。栄養交換で他個体にも炭素・窒素資源が運ばれる。近年、ヒトの健康維持を意識した腸内微生物群の解析が盛んに行われているが、シロアリやその他野生動物の共生微生物群の解析も重要である。この際、高速DNAシーケンサーを利用し遺伝子のカタログをそろえるだけでなく、微生物群が織り成す代謝反応場を丸ごと解析する技術が有効に働く。 こういう測定法はもっと進んで欲しいものです。細菌叢による代謝等も、丸ごと可視化できるので大変有用だと思います。設計図だけ見せられるよりは、建った家で中身をみてみたい。その第一歩だと思います。 iPS細胞が病人を救うなら、この研究は地球を救うかもしれないというのは決して誇張じゃないと思います。
2014年07月09日
コメント(0)
-

貼付け型ウェアラブル生体センサ「Silmee™ Bar type」の発売について
貼付け型ウェアラブル生体センサ「Silmee™ Bar type」の発売について 出典:プレスリリース 当社は、人体に貼り付けて、心電位、脈波、体動、皮膚温を測定する生体センサ「SilmeeTM Bar type」を製品化し、大学・研究機関・企業向けに9月から国内で販売を開始します。 新製品は、ゲルパッドで胸部に貼りつけることで、心電位・脈波・体動・皮膚温という生体情報を同時に連続計測できる防水小型のウェアラブル生体センサです。計測したデータを元に、心拍間隔、脈波間隔、体動量、姿勢を算出し、Bluetooth®通信を介してスマートフォンやタブレットに結果を表示します。また、当社は制御・通信を行うインターフェース仕様「SilmeeTM API」をパートナーに提供し、多様な応用システム・サービスの開発をサポートしてヘルスケア分野のオープン・イノベーションを推進します。 非薬事品の為、診断、治療を目的とした販売、授与はできません。実証実験・評価用としての使用を想定しています。 この商品を評価するために購入するの?連続使用時間約24時間も定義によりますが、連続測定だと短いと思います。 ジム等の方が、需要があるような気がします。(企業というのがこれを指しているのかもしれません。)
2014年07月09日
コメント(0)
-
移乗アシスト装置“ロボット介護推進プロジェクト”採択決定
移乗アシスト装置“ロボット介護推進プロジェクト”採択決定− 北九州市の介護施設における実証評価の実施 −出典:プレスリリース 安川電機は、平成25年度より経済産業省が推進する「ロボット介護機器開発・導入促進事業」に参加し、介護ベッドと車いす間の移乗をアシストする装置を平成26年2月に開発を完了しています。 平成26年度も本開発事業に継続的に参加しており、経済産業省と公益財団法人テクノエイド協会が実施している「ロボット介護推進プロジェクト」にこのたび採択されました。今年度秋には北九州市内の介護施設に本移乗アシスト装置を導入し実証評価を実施します。 販売開始時期は平成28年を予定しています。 見た目大きいですね。でも人がやる力仕事を機械に任せることは喜ばしいと思います。
2014年07月09日
コメント(0)
-
無線通信機能搭載の血糖計や体重計の測定データを、電子カルテに自動転送する機能などを搭載した機能拡張版
無線通信機能搭載の血糖計や体重計の測定データを、電子カルテに自動転送する機能などを搭載した機能拡張版出典:プレスリリース オムロン ヘルスケアは、血圧や体温、SpO2(動脈血酸素飽和度)などの測定バイタルデータを電子カルテに自動転送する「スポットチェックモニタ HBP-1600(以下HBP-1600)」に、新たに無線通信機能搭載の血糖計や体重計の測定データを電子カルテに自動転送する機能などを搭載した機能拡張版を、2014年7月18日から発売します。 このたび、新たに他社製の無線通信機能搭載の血糖計や体重計に対応。他社製品との連動を強化しました。これまで、USB通信機能を搭載した他社の血糖計は利用できましたが、新たにRFIDを内蔵した他社の血糖計との連動が可能になります。測定後、血糖計をスポットチェックモニタ本体にかざすだけで、測定データが転送されて本体画面に表示されます。データを確認後、スポットチェックモニタ本体の送信ボタンを押すと測定データは電子カルテに転送されます。さらに、体重計のデータ取り込みソフトにも対応を開始。専用の受信モジュールと組み合わせて使うことで、ZigBee通信機能を搭載した他社の身長体重計や手すり付きの体重計で測定したデータを、電子カルテに転送することができます。 これは便利。少なくとも転記ミスはなくなるでしょう。だた、電子カルテにきちんと転送しているかの目視は怠らない方がいいと思います。
2014年07月09日
コメント(0)
-
「セレキノン®S」 新発売(九州・沖縄地区限定)のお知らせ
-日本初の「過敏性腸症候群(IBS)の再発症状改善薬」-「セレキノン®S」 新発売(九州・沖縄地区限定)のお知らせ出典:プレスリリース 田辺三菱製薬は、 OTC医薬品として日本で初めて「過敏性腸症候群(Irritable Bowel Syndrome、以下「IBS」)の再発症状改善」の効能を取得した「セレキノン®S」(要指導医薬品*)を7月10日より九州・沖縄地区の薬局・ドラッグストアで新発売いたします。 「セレキノン®S」は当社が開発した「トリメブチンマレイン酸塩」を配合するOTC医薬品で、腸の運動を調節することにより、ストレスによって繰り返す下痢や便秘といったIBSの症状を改善します。IBS患者さんに対してセルフメディケーションにおける新しい治療の選択肢を提供し、QOLの改善に貢献いたします。 どうして九州・沖縄地区限定なんでしょうか?
2014年07月08日
コメント(0)
-
Simvastatin for the Prevention of Exacerbations in Moderate-to-Severe COPD
中等症~重症の慢性閉塞性肺疾患の増悪予防におけるシンバスタチン出典:プレスリリース 後ろ向き研究では,スタチンにより慢性閉塞性肺疾患(COPD)の増悪の発生率と重症度,入院率,死亡率が低下することが示されている.われわれは,大規模多施設共同無作為化試験において,増悪の予防におけるシンバスタチンの有効性を前向きに調査した. シンバスタチン(40 mg/日)とプラセボを比較する無作為化比較対照試験として,「COPD の増悪予防におけるシンバスタチンの前向き無作為化プラセボ対照試験(STATCOPE)」をデザインした.主要評価項目は年間の増悪発生率とした.対象は,40~80 歳で,COPD(1 秒量 [FEV1] 80%未満,1 秒率 [FEV1/努力肺活量] 70%未満と定義)を有し,10 箱・年以上の喫煙歴があり,過去 1 年以内に酸素補給あるいはグルココルチコイドまたは抗菌薬の投与を受けているか,COPD による救急受診または入院のいずれかの既往を有する患者を適格とした.糖尿病または心血管疾患を有する患者と,スタチンを服用中,または成人治療第 3 委員会(ATP III)の基準に基づき服用する必要がある患者は除外した.参加者は 45 施設で 12~36 ヵ月間治療を受けた. COPD 患者 885 例を登録し,約 641 日間追跡した.44%は女性であった.患者の平均年齢(±SD)は 62.2±8.4 歳,FEV1 は予測値の 41.6±17.7%,喫煙歴は 50.6±27.4 箱・年であった.試験完了時における低比重リポ蛋白コレステロール値は,シンバスタチン投与を受けた患者のほうがプラセボ投与を受けた患者よりも低かった.平均増悪回数/人・年はシンバスタチン群とプラセボ群で同程度であり,それぞれ 1.36±1.61,1.39±1.73 であった(P=0.54).初回増悪までの日数の中央値も同程度であり,それぞれ 223 日(95%信頼区間 [CI] 195~275),231 日(95% CI 193~303)であった(P=0.34).非致死性の重篤な有害事象の発生回数/人・年も同程度であり,シンバスタチン群 0.63 件,プラセボ群 0.62 件であった.プラセボ群の 30 例とシンバスタチン群の 28 例が死亡した(P=0.89).慢性閉塞性肺疾患の増悪予防におけるスタチンもこれで「無用」という結論が出たと思います。後ろ向き研究で効果があり、前向き研究では効果がないというのはどういうことで生じるのでしょうか。コントロールパネルの問題かな?後ろ向き研究の場合は選択バイアスが入るのかな?
2014年07月08日
コメント(0)
-
Rosuvastatin for Sepsis-Associated Acute Respiratory Distress Syndrome
敗血症関連急性呼吸促迫症候群に対するロスバスタチン出典:文献 急性呼吸促迫症候群(ARDS)では,肺やほかの臓器の炎症が,生命に関わる臓器不全を引き起こす可能性がある.3-ヒドロキシ-3-メチルグルタリル補酵素 A 還元酵素阻害薬(スタチン)は,炎症反応を修飾することができる.先行する観察研究では,敗血症患者の臨床転帰がスタチンによって改善することが示唆された.われわれは,ロスバスタチン投与により,敗血症関連 ARDS の重症患者の臨床転帰が改善するという仮説を立てた。 多施設共同試験において,敗血症関連 ARDS 患者を,二重盲検下でロスバスタチンの経腸投与を行う群とプラセボを投与する群に無作為に割り付けた.主要評価項目は,自宅退院まで,また医療施設に入所していた場合は試験 60 日目までの死亡率とした.副次的評価項目は,28 日目までの人工呼吸器を使用しなかった日数(患者が生存し自発呼吸をしていた日数)と,14 日目までの臓器不全のない日数などとした。 この試験は,予定されていた 1,000 例のうち 745 例が登録された時点で,無益性のため中止された.60 日医療施設内死亡率にも(ロスバスタチン群 28.5%,プラセボ群 24.9%,P=0.21),人工呼吸器を使用しなかった平均日数(±SD)にも(ロスバスタチン群 15.1±10.8,プラセボ群 15.1±11.0,P=0.96),群間で有意差は認められなかった.両群の人口統計学的特性と主要な生理学的特性はよく一致していた.ロスバスタチン治療は,プラセボと比較して,14 日目までの腎不全のない日数が少ないこと(10.1±5.3 対 11.0±4.7,P=0.01)と,14 日目までの肝不全のない日数が少ないこと(10.8±5.0 対 11.8±4.3,P=0.003)に関連していた.ロスバスタチンは,血清クレアチンキナーゼが正常上限の 10 倍を超える確率の上昇に関連しなかった. 全く効果がなかったと言うことで、ARDSはこれで決着となるのではないでしょうか?肝不全と腎不全に関しても統計的には有意かもしれませんが、臨床的には無意味だと思います。
2014年07月08日
コメント(0)
-
infomity「臨床試験支援サービス」でイメージングCRO事業に参入
infomity「臨床試験支援サービス」でイメージングCRO事業に参入出典:プレスリリース コニカミノルタ株式会社(本社:東京都千代田区、社長:山名昌衛、以下 コニカミノルタ)は、医療ICTサービスプラットフォーム「infomity(インフォミティ)」において臨床試験支援システム「Trial BOX」を開発し、2014年7月より「臨床試験支援サービス」を開始しました。これによりイメージングCRO (Contract Research Organization)事業に参入します。 画像に関しては結構色々な部分で判断基準になっており、判定委員会に画像を持ち込んで判断していただくのもかなり手数がかかるので、良い商品だと思います。 ただし、監査証跡が結構面倒な気がします。
2014年07月07日
コメント(0)
-
CHMPがベータアミロイドプラークのPETイメージング用 ビザミルTM(フルテメタモールF18注射剤)のEUによる承認を勧告
CHMPがベータアミロイドプラークのPETイメージング用 ビザミルTM(フルテメタモールF18注射剤)のEUによる承認を勧告出典:プレスリリース GEヘルスケア(英チャルフォントセントジャイルズ)は2014年6月27日、欧州医薬品庁ヒト用医薬品委員会(CHMP)から肯定的意見を得たことを発表しました。これはビザミルTM(フルテメタモールF18注射剤)に対する販売承認の付与を勧告するものです。ビザミルTMは、アルツハイマー病(AD)およびその他の認知障害が疑われる認知症成人患者を対象に、脳内ベータアミロイド老人斑沈着の密度を評価するポジトロン断層撮影法(PET)用放射性医薬品です。ビザミルTMは診断のみを用途とし、臨床評価と組み合わせて使用するものです。アルツハイパーに関しては脳内βアミロイドは診断には使えるが、アミロイドを除去しても認知症は治らないという文献を読んだ記憶があるのですが、探しても見つからないので、夢だったのかもしれません。
2014年07月07日
コメント(0)
-
VCU Newsに当社RQ-10の医師主導治験に関する記事が掲載されました
VCU Newsに当社RQ-10の医師主導治験に関する記事が掲載されました。出典:プレスリリース VCU PMDC: Virginia Commonwealth University, Parkinson’s and Movement Disorders Centerは当社と共同研究契約を締結し、当社の所有するセロトニン5-HT4受容体部分作動薬(RQ-10)の医師主導治験を行っております。この度、本件に関する記事が同大学のニュースサイトに掲載されましたのでお知らせいたします。 詳しくはVCU Newsのサイトをご覧ください。本治験では、VCU PMDCのレスリー・クラウド医師の下、RQ-10のパーキンソン病患者に併発する胃不全麻痺に対する有効性評価を行います。 当社は、本治験の成果として、RQ-10が胃不全麻痺や便秘などの多くの機能性消化器疾患に対して、将来的な治療オプション提供の可能性を示せることを期待しております。 FDAに治験届けを出すのはラクオリアがスポンサーと読み取ったのは誤り?
2014年07月07日
コメント(0)
-
国産初の血友病インヒビター止血治療用製剤の製造販売承認取得について
国産初の血友病インヒビター止血治療用製剤の製造販売承認取得について 出典:プレスリリース 一般財団法人 化学及血清療法研究所(本所:熊本市、理事長:宮本誠二、以下「化血研」)は、インヒビターを保有する血友病患者向けの止血治療用バイパス製剤(一般名:乾燥濃縮人血液凝固第X因子加活性化第VII因子、販売名:バイクロットⓇ配合静注用、以下「本剤」)の製造販売承認を2014年7月4日付で取得しましたのでお知らせ致します。 インヒビターを保有する血友病患者の止血治療にあたっては、第VIII因子や第IX因子が関与する凝固経路を迂回(バイパス)して血液凝固反応を促進し、止血を図る機能を有するバイパス製剤が用いられています。 血友病患者さんに補充療法以外の治療がないものかと思います。
2014年07月06日
コメント(0)
-
インフリキシマブ(遺伝子組換え)製剤のバイオ後続品の製造販売承認取得について
インフリキシマブ(遺伝子組換え)製剤のバイオ後続品の製造販売承認取得について出典:プレスリリース 日本化薬は、2014年7月4日、Celltrion, Inc.及びCelltrion Healthcare Co., Ltd.と共同で開発を進めておりました、インフリキシマブBS点滴静注用100mg「NK」(開発コード:CT-P13)について、製造販売承認を取得いたしました。本剤は国内で最初に承認された単クローン抗体のバイオ後続品です。 インフリキシマブBS点滴静注用100mg「NK」は、関節リウマチ、炎症性腸疾患等の自己免疫疾患治療において重要な役割を果たしているインフリキシマブ(遺伝子組換え)製剤のバイオ後続品です。既に韓国、欧州を含む25か国で販売されております。日本化薬は、2010年11月にセルトリオングループと日本における共同開発・販売に関する契約を締結後、開発に着手してまいりました。 バイオ後続品がそろそろ市場に出回ってきました。製造施設の問題があるにしても、高価な薬剤が少しでも安価に入手できることは喜ばしいことです。
2014年07月06日
コメント(0)
-
爪白癬治療剤「クレナフィン®爪外用液10%」の国内製造販売承認取得について
爪白癬治療剤「クレナフィン®爪外用液10%」の国内製造販売承認取得について出典:プレスリリース 科研製薬株式会社(本社:東京都文京区、社長:大沼 哲夫、以下「科研製薬」)は、爪白癬治療剤「クレナフィン®爪外用液10%」(一般名:エフィナコナゾール、以下「クレナフィン®」)について、本日、皮膚糸状菌(トリコフィトン属)による爪白癬の効能・効果で製造販売承認を取得しましたのでお知らせいたします。 「クレナフィン®」は、科研製薬が創製した新規トリアゾール系化合物エフィナコナゾールを主成分とし、真菌の細胞膜構成成分であるエルゴステロールの生合成を阻害することにより抗真菌活性を発揮する日本初の外用爪白癬治療剤です。2つの国際共同治験(第III相臨床試験)において、1日1回塗布による有効性・安全性が確認されており、2012年10月に製造販売承認申請を行っておりました。 今までの爪白癬治療薬は、患部に届くことが難しいという点から経口剤が用いられいました。この経口剤は他剤との相互作用が教科書になるぐらいに強いものです。しかし、このニュースリリースだけではエフィナコナゾールそのものが爪に対する浸透性が高いのか、製剤に工夫があるのかよく分かりません。
2014年07月05日
コメント(0)
-
前立腺がん治療薬「ジェブタナ®点滴静注60mg」の 製造販売承認取得について
前立腺がん治療薬「ジェブタナ®点滴静注60mg」の 製造販売承認取得について 出典:プレスリリース サノフィは、 2014年7月4日、「前立腺癌」の効能・効果で「ジェブタナ®点滴静注60mg」(一般名:カバジタキセル アセトン付加物、以下「ジェブタナ®」)の製造販売承認を厚生労働省より取得したことをお知らせいたします。 「ジェブタナ®」は細胞内の微小管に作用して、細胞増殖を阻害する抗がん剤です。有効な治療法が限られているドセタキセル治療後の前立腺がん患者さんに対して、「ジェブタナ®」は全生存期間の延長を示した数少ない薬剤の一つです。本剤は、海外で実施した第III相試験(TROPIC試験, NCT00417079)において、全生存期間の有意な延長を示しました(全生存期間の中央値がミトキサントロン併用群の12.7か月に対してカバジタキセル群は15.1か月 [ハザード比=0.70 (95%信頼区間:0.59-0.83); P<0.0001])。 「ジェブタナ®」は、厚生労働省の「医療上の必要性の高い未承認薬・適応外薬検討会議」において、医療上の必要性が高い薬剤と評価され、2012年4月に厚生労働省より開発要請を受けました。その後、海外で実施した第III相試験結果、国内第I相試験結果等に基づき、2013年7月承認申請を行い、優先審査品目として審査され、本日承認されました。 カバシタキシルとドテタキセルを比較したらどうなるでしょうか。ドテタキセル治療後の再発例を対象にしているから効果はナイーブの時よりも弱いと思いますが、ドテタキセル治療後再発が必ずしもドテタキセルに耐性を持っているかは確かめられていないので、もしかするとです。理由はカバシタキシルとドテタキセルとの構造式、及び薬理作用がよく似ているからです。かつ比較試験が行われていないからです。
2014年07月05日
コメント(0)
-
4価髄膜炎菌ワクチン(ジフテリアトキソイド結合体)「メナクトラR筋注」日本国内での製造販売承認取得について
4価髄膜炎菌ワクチン(ジフテリアトキソイド結合体)「メナクトラR筋注」日本国内での製造販売承認取得について出典:プレスリリース サノフィは、2014年7月4日、厚生労働省より髄膜炎菌ワクチン「メナクトラ®筋注」[一般名:4 価髄膜炎菌ワクチン(ジフテリアトキソイド結合体)、以下「メナクトラ®」]の製造販売承認を取得しましたのでお知らせいたします。 メナクトラ®は、髄膜炎菌(血清型A,C,Y及びW-135)による侵襲性髄膜炎菌感染症(IMD:Invasive Meningococcal Disease)を予防するワクチンです。本ワクチンは、2010 年の「医療上の必要性の高い未承認薬・適応外薬検討会議」における審議の結果、医療上の必要性が高いと判断されました。サノフィは厚生労働省から開発要請を受け、メナクトラ®の臨床開発を行い、日本で初めて承認を取得しまた。 ということです。
2014年07月05日
コメント(0)
-
ヒト型抗ヒトPD-1モノクローナル抗体「オプジーボ®点滴静注20mg、100mg」 根治切除不能な悪性黒色腫に対する製造販売承認取得のお知らせ
ヒト型抗ヒトPD-1モノクローナル抗体「オプジーボ®点滴静注20mg、100mg」 根治切除不能な悪性黒色腫に対する製造販売承認取得のお知らせ出典:プレスリリース 小野薬品工業は、ヒト型抗ヒトPD-1モノクローナル抗体「オプジーボ®点滴静注20mg、100mg、以下、オプジーボ」について、2014年7月4日、根治切除不能な悪性黒色腫の治療薬として製造販売承認を取得しましたのでお知らせします。 オプジーボはヒト型抗ヒトPD-1 モノクローナル抗体です。PD-1 は、リンパ球の表面にある受容体の一種で、生体において活性化したリンパ球を抑制するシステム(負のシグナル)に関与しています。がん細胞は、このシステムを利用して免疫反応から逃れているという研究成績が報告されています。オプジーボは、リンパ球を抑制するPD-1 の働き(PD-1 と結合するPD-L1 およびPD-L2 との相互作用)を抑制することで、がん細胞を異物と認識してこれを排除する免疫反応を亢進することにより有効性が期待されている薬剤です。なお、オプジーボはPD-1を標的とする治療薬としては、世界で初めて製造販売承認を取得した薬剤となります。 日本における進行期の悪性黒色腫に対する標準薬物療法は、現在、抗悪性腫瘍剤ダカルバジンの単剤療法のみです。つきましては、オプジーボの早期使用が必要な場合を想定し倫理的な観点から、薬価基準収載までの期間、薬剤提供準備が整い次第、本剤第II相臨床試験実施施設のうち薬剤提供が受け入れ可能である一部の施設に限定して、本剤を無償で提供することにいたしました。 2013年のBREAKTHROUTH OF THE YEARはがん免疫療法でした。PD-1モノクローナル抗体もその中で取り上げられています。まずは、悪性黒色腫できちんとデータを取ることを期待します。 他の癌に使って薬害なんてことにならないよう。日本が世界に先駆けて承認したのだから。
2014年07月05日
コメント(0)
-
前立腺癌治療剤「ザイティガ®錠 250mg」 日本国内での製造販売承認取得のお知らせ
前立腺癌治療剤「ザイティガ®錠 250mg」 日本国内での製造販売承認取得のお知らせ出典:プレスリリース アストラゼネカは、7月4日付けで、ヤンセンファーマが経口前立腺癌治療剤「ザイティガ®錠 250mg 」(一般名:アビラテロン酢酸エステル)の国内製造販売承認を取得しましたことをお知らせいたします。 ザイティガ®錠は、CRPCを適応とし、アンドロゲンの生合成に必要な酵素であるCYP17を、精巣のみならず、副腎や前立腺がん組織内でも選択的に阻害することで抗腫瘍効果を示すCYP17阻害剤です。これにより、がん細胞に作用するアンドロゲンレベルをさらに抑制します。本剤は、2014年1月現在、欧米をはじめ世界87カ国で承認されています。 薬剤去勢の新しい薬剤ですが、去勢抵抗性前立腺癌への進行が減るかもしれない。 前はンドロゲンの生合成阻害には精巣での選択性を求められていたように思います。 この方向が進展するとHMG-CoAリダクターゼ阻害剤の使用が真剣味をおびるのでは。データはそこそこありますし。
2014年07月05日
コメント(0)
-
尋常性乾癬治療の配合外用剤「ドボベット®軟膏」承認取得のお知らせ
尋常性乾癬治療の配合外用剤「ドボベット®軟膏」承認取得のお知らせ 出典:プレスリリース 協和発酵キリンは、レオ ファーマが2014年7月4日に、尋常性乾癬治療剤「ドボベット®軟膏」の国内製造販売承認を取得したとの連絡を受けましたのでお知らせします。 ドボベット®軟膏は活性型ビタミンD3であるカルシポトリオール水和物と副腎皮質ホルモン(以下「ステロイド」)であるベタメタゾンジプロピオン酸エステルの配合外用剤であり、昨年8月、レオ ファーマが厚生労働省に承認申請を行っていたものです。 これは、混ぜる手間以外に何があるのでしょう?
2014年07月05日
コメント(0)
-
新規慢性閉塞性肺疾患(COPD)治療剤「アノーロ®エリプタ®」 承認取得のお知らせ
新規慢性閉塞性肺疾患(COPD)治療剤「アノーロ®エリプタ®」 承認取得のお知らせ出典:プレスリリース グラクソ・スミスクラインは、2014年7月4日、「アノーロ®エリプタ®」が慢性閉塞性肺疾患(慢性気管支炎、肺気腫)の気道閉塞性障害に基づく諸症状の緩解(長時間作用性吸入抗コリン剤及び長時間作用性吸入β₂刺激剤の併用が必要な場合)の適応で承認されたことをお知らせいたします。 COPDのこのレジメも一杯でました。ディバイスぐらいしか差が分からないのですが。
2014年07月05日
コメント(0)
-
「スタレボ®配合錠 L50、L100」の製造販売承認を取得
「スタレボ®配合錠 L50、L100」の製造販売承認を取得服薬錠数を減らして患者さんの服薬時の負担を軽減するレボドパ、カルビドパ、エンタカポンの配合剤出典:プレスリリース ノバルティス ファーマは、2014年7月4日、ドパミンの前駆体であるレボドパ、ドパ脱炭酸酵素阻害剤(DCI)であるカルビドパ水和物、および末梢COMT(カテコール-O-メチル基転移酵素)阻害剤であるエンタカポンの3成分を1剤に配合した「スタレボ®配合錠 L50、L100」(以下「スタレボ」)の製造販売承認を取得しました。本剤の適応症は、「パーキンソン病〔レボドパ・カルビドパ投与において症状の日内変動(wearing-off現象)が認められる場合〕」です。「スタレボ」は、2008年より国内で開発が始められ、その後、2012年に「医療上の必要性の高い未承認薬・適応外薬検討会議」での検討結果に基づき厚生労働省より開発要請を受けました。 この配合剤は本当に臨床錠の有用性があると思います。
2014年07月05日
コメント(0)
-
抗悪性腫瘍剤/ALK 阻害剤「アレセンサ®」 「ALK 融合遺伝子陽性の切除不能な進行・再発の非小細胞肺癌」に 対する製造販売承認を取得
抗悪性腫瘍剤/ALK 阻害剤「アレセンサ®」 「ALK 融合遺伝子陽性の切除不能な進行・再発の非小細胞肺癌」に 対する製造販売承認を取得出典:プレスリリース 中外製薬は、ALK 阻害剤アレクチニブ塩酸塩カプセル-販売名『アレセンサ®カプセル20mg、同40mg』(以下、「アレセンサ®」)について本日、厚生労働省より「ALK 融合遺伝子陽性の切除不能な進行・再発の非小細胞肺癌」を効能・効果として製造販売承認を取得したことをお知らせいたします。 「アレセンサ®」は、中外製薬およびF. ホフマン・ラ・ロシュ社(以下、ロシュ社)が提唱するバイオマーカーや診断ツールを用いて効果が期待できる患者さんに適切な薬剤を選択する、個別化医療(PHC:Personalized Healthcare)に合致した薬剤です。 中外製薬は、国内で行われた「アレセンサ®」の第I/II相臨床試験(以下、本臨床試験)の成績等を基に、「ALK 融合遺伝子陽性の切除不能な進行・再発の非小細胞肺癌」に対する製造販売承認申請を2013年10月7日に行いました。今回の承認はこれらの試験成績に基づいています。なお、2013年9月13日に「ALK 融合遺伝子陽性の切除不能な進行・再発の非小細胞肺癌」を予定効能・効果として希少疾病用医薬品の指定を受け、優先審査品目に指定されており、製造販売承認申請から約9カ月で承認取得となりました。 「アレセンサ®」は、中外製薬鎌倉研究所で創製された経口のALK 阻害剤です。非小細胞肺癌患者さんの2~5%にALK 融合遺伝子が発現すると報告されており、この融合遺伝子を有する細胞は恒常的にALKのキナーゼ活性が上昇し、細胞が腫瘍化していると考えられています。「アレセンサ®」は、このキナーゼ活性を選択的に阻害することにより、腫瘍細胞の増殖を阻害しアポトーシスを誘導することで、抗腫瘍効果を発揮します。 第I相パートにおいて、用量制限毒性の発現が認められなかったことから、最大投与量である1回300mgの1日2回投与が推奨用量として決定されました。また、同用量にて実施した第II相パートにおいて、奏効率は93.5%(95%信頼区間:82.1~98.6%)でした。 93.5%は抗菌剤みたいな奏効率です。まあ個別化医療を標榜するならばこれぐらいは効果を示して欲しいものです。ALK 融合遺伝子の発現が2~5%か。使用成績調査(全例調査)1,000例を集めるのにどれぐらいかかるのかな。 生存はどれぐらい出るか楽しみなところです。 ALK融合遺伝子の発現がなければ、薬理学上は全く効果がないはずです。この薬も日本で先駆けて承認されましたが、この奏効率に目がくらんで変な報道が行われてい、患者さんがその間違った報道につられて、医者に処方を要求するなんてことが起こらないことを切に願います。ALK融合遺伝子がない患者さんに使われて、死亡例が出て「薬害」なんていわれたら目も当てられません。
2014年07月05日
コメント(0)
-
嫌気性菌感染症治療剤「アネメトロ®点滴静注液500mg」 製造販売承認を取得
嫌気性菌感染症治療剤「アネメトロ®点滴静注液500mg」 製造販売承認を取得出典:プレスリリース ファイザーは、2014年7月4日、嫌気性菌感染症治療剤「アネメトロ®点滴静注液500mg」(一般名:メトロニダゾール)の製造販売承認を取得しました。 「アネメトロ点滴静注液500mg」は、ニトロイミダゾール系の抗菌薬で、菌体または原虫内の酸化還元系の反応によって還元されてニトロソ化合物となり、このニトロソ化合物が偏性嫌気性菌または原虫に対して強い抗菌活性や抗原虫活性を有します。 メトロニダゾールは、国内外において各種ガイドラインや教科書で嫌気性菌感染症に対して推奨されている標準的な治療薬です。国内では、メトロニダゾール経口剤(フラジール®内服錠、塩野義製薬)は「トリコモナス症(腟トリコモナスによる感染症)」を適応症として1961年に承認されました。2007 年以降、ヘリコバクター・ピロリ感染症、細菌性腟症、嫌気性菌感染症、感染性腸炎、アメーバ赤痢、ランブル鞭毛虫感染症に対して追加承認を取得しています。 メトロニダゾールの注射剤は国内の各種団体から開発の要望が挙げられ、2010年4月27日の「医療上の必要性の高い未承認薬・適応外薬検討会議」において、嫌気性菌感染症およびアメーバ赤痢に対する医療上の必要性が高いと評価され、開発企業の募集が行われました。 ファイザー株式会社では、公募リストにあった本剤に対する高い医療ニーズを踏まえ、未承認薬の解消によって医療に貢献すべく、本剤を開発することとし、臨床試験を実施し、承認申請を行った結果、「嫌気性菌感染症」、「感染性腸炎(偽膜性大腸炎を含む)」および「アメーバ赤痢」を適応症として、今回、製造販売承認を取得しました。 ということです。
2014年07月05日
コメント(0)
-
「イーケプラ®点滴静注500mg」 国内承認取得 4歳以上のてんかん患者さんの服薬継続に寄与
「イーケプラ®点滴静注500mg」 国内承認取得 4歳以上のてんかん患者さんの服薬継続に寄与出典:プレスリリース 大塚製薬とユーシービージャパン は、「イーケプラ点滴静注500mg」(一般名:レベチラセタム、以下「イーケプラ点滴静注」)の国内における製造販売承認を7月4日に取得しました。「イーケプラ点滴静注」の効能・効果は、経口投与ができない場合の一時的な代替製剤として経口製剤に準ずるものです。 てんかんは、乳幼児から高齢者まで幅広い年代で発症する病気で、国や地域によって性別や人種による発症率に大きな違いはなく、およそ100人に1人という発症頻度も変わりません。日本には約100万人のてんかん患者さんがいると言われていますが、適切な診断と薬物治療によりおよそ70%の患者さんはてんかん発作のない通常の生活を送ることができます。 日本において「イーケプラ錠250mgおよび同500mg」は、2010年7月に「他の抗てんかん薬で十分な効果が認められない成人てんかん患者の部分発作(二次性全般化発作を含む)に対する抗てんかん薬との併用療法」の効能・効果で最初の承認を取得後、2013年5月に4歳以上の適応(小児用量の追加)の承認を取得しました。また、2013年6月に承認された「イーケプラドライシロップ50%」は水に溶かして飲むドライシロップ製剤であるため、小児の患者さんのみならず、高齢者を含む成人患者さんで錠剤を飲みにくい場合にも使用できます。また、成長過程にある4歳以上の小児てんかん患者さんの体重に合わせた用量調整が可能となりました。更に2014年3月にてんかん患者の「部分発作に対する単剤療法(二次性全般化発作を含む)」の効能・効果で一部変更承認申請を行いました。「イーケプラ®」は、国内で既に約10万人を超える患者さんに使用されています。 祇園のてんかん発作による暴走等により、道路交通法が改定され、今年の6月1日から施行となっています。 最近糖尿病の低血糖発作による事故がよく報道されています。 1件の事故で判断するのではなく、事故リスクが健常人の事故リスクを上回ることでどうするかを考えるべきと思います。 日本ではそんなデータがないのかもしれませんが、なければ取るべきです。第3回日本視野学会学術集会が先月末に行われました。「有効視野:交通事故と運転行動に関するエビデンス」岡村 和子(科学警察研究所)という演題がありました。EU研究IMMORTALのメタ解析で、交通事故の発生リスクは視力と事故の関係を扱った79件の研究を見ても低視力に強いリスクはない。視野障害がある人には、禁止されなくても自発的な運転調整をする傾向がある。 視野では:軽度から中程度まででは運転に問題はない。しかし、垂直方向に障害があると走行位置保持に困難を訴える。 運転免許の医学適性について:運転アセスメントの必要性がある訓練や限定(昼間のみや、地域だけなど)をかけることも今後は検討できる今後ではなく、検討を始めて欲しいな。私は左側に視野欠損があるので、免許は取りませんでした。
2014年07月05日
コメント(0)
-
百日せき、ジフテリア、破傷風、及び急性灰白髄炎(ポリオ)を予防する4種混合ワクチン『スクエアキッズⓇ皮下注シリンジ』の国内製造販売承認取得のお知らせ
百日せき、ジフテリア、破傷風、及び急性灰白髄炎(ポリオ)を予防する4種混合ワクチン『スクエアキッズⓇ皮下注シリンジ』の国内製造販売承認取得のお知らせ出典:プレスリリース 第一三共とサノフィは、第一三共のグループ会社である北里第一三共ワクチンが、百日せき、ジフテリア、破傷風、及び急性灰白髄炎(ポリオ)を予防する4種混合ワクチン(以下「本ワクチン」)の国内製造販売承認を取得しましたことをお知らせいたします。 本ワクチンは、北里第一三共ワクチンの沈降精製百日せきジフテリア破傷風混合ワクチン(DPTワクチン)とサノフィパスツールの不活化ポリオワクチン(ソークワクチン)(eIPV:Enhanced Inactivated Poliomyelitis Vaccine)をプレフィルドシリンジに充填した製剤で、不活化ポリオワクチン(ソークワクチン)を含む4種混合ワクチンとして日本で初めて承認されました。 現在四種混合ワクチンは化血研、阪大微研、田辺三菱、アステラスから販売されているますが、不活化ポリオが、セービン株となっています。
2014年07月05日
コメント(0)
-
2型糖尿病治療剤「カナグル®錠100mg」の国内製造販売承認取得のお知らせ
2型糖尿病治療剤「カナグル®錠100mg」の国内製造販売承認取得のお知らせ出典:プレスリリース 田辺三菱製薬と第一三共は、2014年7月4日、田辺三菱製薬がSGLT2阻害剤「カナグル®錠100mg」(一般名:カナグリフロジン水和物、以下「カナグル®錠」)に関し、2型糖尿病を効能・効果として国内における製造販売承認を取得したことをお知らせいたします。 「カナグル®錠」は、田辺三菱製薬が創製した世界初の経口SGLT阻害物質T-1095をルーツとする日本発のSGLT2阻害剤です。本剤は、腎臓の尿細管において糖の再吸収に関与するトランスポーターであるSGLT2(ナトリウム-グルコース共輸送体2)を阻害することで、糖の再吸収を抑制、尿中に過剰な糖を排泄し、優れた血糖低下作用を示す薬剤です。 海外では、本剤の導出先であるヤンセン・ファーマシューティカルズが、2013年3月に、成人の2型糖尿病患者の治療薬「INVOKANA®(製品名)」として米国で承認を取得し、現在(2014年6月時点)では、米国を含め、欧州、カナダ、オーストラリアなど、世界40ヵ国以上で承認を受けています。 「カナグル®錠」は、田辺三菱製薬が製造販売を行い、田辺三菱製薬と第一三共が共同でプロモーションを行います。 これで5番目のSGLT2阻害剤スーグラ (イプラグリフロジン) 2014年4月発売 アステラス製薬、壽製薬、MSDフォシーガ ( タパグリフロジン) 2014年5月発売 プリストル、アストラゼネカ、小野薬品工業ルセフィ (ルセオグリフロジン) 2014年5月発売 大正富山、大正、ノバルティスデベルザ (トホグリフロジン) 2014年5月発売 サノフィ、興和カナグル (カナグリフロジン) 2014年7月承認 田辺三菱、第一三共 イーライリリーはエンバグリフロジンを2013年10月に申請しています。 脱水に気をつける必要があるとのSGLT2阻害薬の適正使用に関する委員会から勧奨を受けています。
2014年07月05日
コメント(0)
全841件 (841件中 601-650件目)












