医療用医薬品 0
[プレスリリース] カテゴリの記事
全841件 (841件中 801-841件目)
-
血液凝固検査試薬 「リアスオートP-FDP」を発売
血液凝固検査試薬 「リアスオートP-FDP」を発売出典:プレスリリース シスメックス株式会社(本社:神戸市、代表取締役会長兼社長:家次 恒 以下「シスメックス」)は、このたび血液凝固検査分野の「全自動血液凝固測定装置 CSシリーズ、CA-7/8000、CA-1500、CA-6/550、コアグレックス800」で使用可能な新たな試薬 「リアスオートP-FDP」を発売します。 このたび発売する「リアスオートP-FDP」は、FDP検査に使用され、血液の凝固・線溶亢進状態の把握に用いられます。播種性血管内凝固症候群(DIC)や血栓症の診断に重要な検査であり、Dダイマー検査との組み合わせにより、DICの病型分類にも有用と言われています。 また、本試薬では高値まで測定可能となり、これまで再検査を要していた高値検体を、1回の検査で測定することができ、迅速に測定することが可能となります。また、DIC病型分類の把握における有用性の向上を目指し、フィブリノゲン分解産物への反応性の向上を独自の技術により実現しました。 【新製品の概要】 販売名: リアスオートP-FDP 使用目的: 血漿または血清中フィブリノゲンおよびフィブリン分解産物(FDP)の測定 発売時期: 2014年5月 保険点数: 120点 高値が予想される場合に、薄める手間が省けるのがメリットです。
2014年05月29日
コメント(0)
-
「アミノインデックス技術」を用いた、生活習慣病に関連する リスクの高い集団の抽出の可能性について学会発表
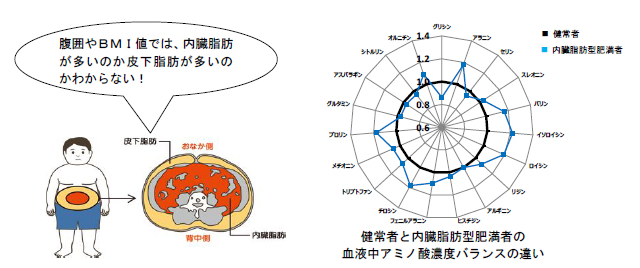
「アミノインデックス技術」を用いた、生活習慣病に関連する リスクの高い集団の抽出の可能性について学会発表出典:プレスリリース味の素は、三井記念病院総合健診センターの山門實特任顧問を中心としたグループとの共同研究で、「アミノインデックス技術」を用いて、生活習慣病に関連するリスク(内臓脂肪蓄積、脂肪肝、食後高インスリン血症)の高い集団を採血検査だけで抽出できることを確認しました。この研究成果は、第68回日本栄養・食糧学会大会(2014年5月30日(金)~6月1日(日)に北海道江別市の酪農学園大学にて開催)において発表される予定です。なお、本件は同学会大会のトピックス演題に選定されました。今回、20代~80代の人間ドック受診者約4,000名を対象に、血液中のアミノ酸濃度のバランスと様々な検査指標の関連を解析した結果、「アミノインデックス技術」による指標値の分布と既存の手法によりリスクが高いという結果になる分布が、同様の傾向を示しました。この結果から、生活習慣病に関連するリスクの高い集団の抽出に、「アミノインデックス技術」が応用できる可能性が示唆されました。 なお、当社は、「アミノインデックス技術」を活用し、2011年4月より、採血検査(約5ml)だけで6種類のがんのリスクスクリーニングができる検査サービス「アミノインデックス® がんリスクスクリーニング(AICS)」を事業化しています。これからも、100年にわたるアミノ酸研究の知見を活用して「アミノインデックス技術」の研究を推進し、がんや生活習慣病のリスク低減や、医療費削減の一助となることを目指します。さらに、今後、「アミノインデックス技術」を高齢者の栄養管理、運動などにも領域を広げ、人々の健康な生活に貢献します。 被爆もないしいい方法だと思います。偽陰性がどれぐらいあるかは知りたいところです。
2014年05月29日
コメント(0)
-
米国において制吐剤「ALOXI®」の小児適応に関する承認取得
米国において制吐剤「ALOXI®」の小児適応に関する承認取得出典:プレスリリース エーザイ株式会社は、このたび、米国における制吐剤「ALOXI®」(一般名:パロノセトロン塩酸塩)について、生後1カ月~17歳までの小児における初回および反復的な催吐性を有するがん化学療法(高度な催吐性を有するがん化学療法を含む)による急性の悪心・嘔吐(CINV)の予防に係る適応追加が、米国食品医薬品局(Food and Drug Administration: FDA)より承認されたことをお知らせします。小児がんの罹患年齢のピークは1歳未満といわれる中で、本剤は生後1~6カ月までの乳児におけるCINVに関する適応を有する初めての薬剤となります。 今回の承認は、FDAからの小児臨床試験実施要請書(Written Request)に応じて実施された、オンダンセトロンとの無作為化、二重盲検の非劣性試験に基づいています。主要評価項目である化学療法後24時間以内に嘔吐や吐き気がなく、制吐剤の投与も必要としない完全奏功率は、オンダンセトロン投与群の58.6%に対して、「ALOXI®」投与群(20mcg/kg、静注単回投与)は59.4%でした。有害事象発生頻度は両投与群とも同等であり、「ALOXI®」に関連する有害事象で最も頻度が高いものは頭痛でした。本試験では、小児における体重あたりの本剤投与量が成人に比較して高く設定されましたが、安全性プロファイルはこれまで成人において確認されているものと同様でした。また、本臨床データについては、小児臨床試験実施要請書に基づく有用性が認められ、本剤の米国における独占期間は6カ月間延長され、2015年10月13日まで存続します。CINVはChemotherapy Induced Nausea and Vomitingです。小児に関して効能を取るのを依頼されてもやはり対照薬をおいたRCTというのがすごいですね。オンダセトロンは、この記事を見る限りは乳児に効能はないわけですから。(プラセボ対照はますます倫理的ではないですが)
2014年05月29日
コメント(0)
-
バイエル薬品 経口抗凝固剤イグザレルト® 錠について 静脈血栓塞栓症の治療・再発抑制に対する効能追加を承認申請
バイエル薬品 経口抗凝固剤イグザレルト® 錠について 静脈血栓塞栓症の治療・再発抑制に対する効能追加を承認申請出典:プレスリリース バイエル薬品株式会社は本日、経口抗凝固剤(選択的直接作用型第Xa 因子阻害剤)「イグザレルト®錠」(一般名:リバーロキサバン)について、静脈血栓塞栓症(VTE:venous thromboembolism)の治療および再発抑制に対する効能追加の承認申請を厚生労働省に行いました。 イグザレルト®は 2012 年 4 月に、「非弁膜症性心房細動患者における虚血性脳卒中及び全身性塞栓症の発症抑制」を効能・効果として発売されました。海外(米国、欧州等)では、非弁膜症性心房細動患者における脳卒中・全身性塞栓症の発症抑制などのほか、VTE の治療および再発抑制の適応でも承認されています。ということです
2014年05月28日
コメント(0)
-
やっぱり 生姜は冷えに効く
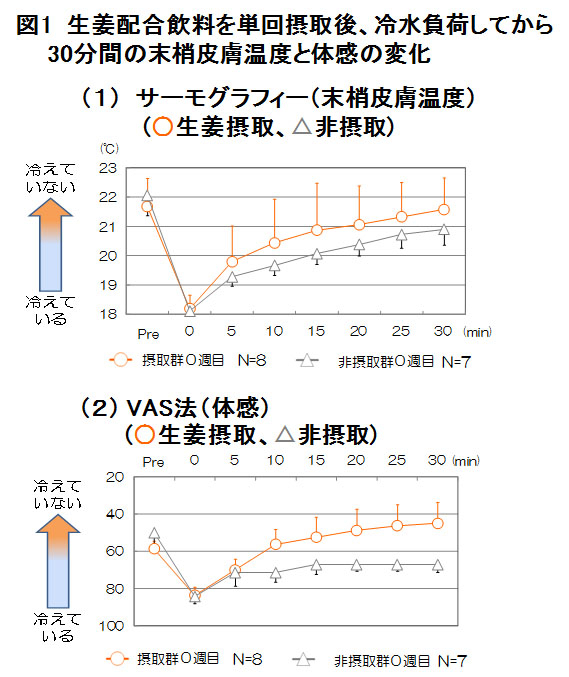
ノエビアグループは、生姜配合飲料の摂取が冷え性に有効であることを見出しました。出典:プレスリリース 現代の生活においては、過度の冷房、運動不足、睡眠不足、ストレスなど、冷えを引き起こす要因が多く見受けられます。特に、基礎代謝や血液循環を担う筋肉量が少ない女性は、男性より冷えに悩みやすいと言われています。 漢方医学では経験的に冷え性に対して生姜が利用されてきました。生姜は発汗促進、血行促進の他、咳止め、解熱や消化器系の機能亢進、腹痛や便秘の解消など、様々な効能が知られています。健常成人女性15名を、1.生姜配合飲料摂取群(8名)と2.非摂取群(7名)に分けました。そして、単回摂取試験と4週間の継続摂取試験の2つを実施しました。 温度と湿度がコントロールされた部屋に入室後、左足を撮影部位としたサーモグラフィー(用語説明*1)と、VAS(Visual Analogue Scale)法(用語説明*2)を実施し、冷えの状態と体感を評価しました。その後、1.摂取群は生姜配合飲料50mlを、2.非摂取群は水50mlを摂取しました。摂取後、両足を15℃の水に1分間浸漬しました。冷水負荷後、30分後まで5分間おきに測定を実施しました。冷水負荷前後を比較し、単回摂取の効果を評価しました。 単回摂取試験翌日より4週間、1.摂取群は生姜配合飲料50mlを毎日就寝前に摂取しました。その後、単回摂取試験と同様の冷水負荷試験を実施しました。単回摂取(0週目とする)の試験結果と比較し、継続摂取の効果を評価しました。 非摂取群でも4週目に改善効果があるようにみえます。特にVAS法での結果にその経過が顕著と思えます。あと検定方法はどのように行ったかも学会発表で質問が出そう、こういう経時データは各時間でt-検定を行うと、実験そのものを疑われます。単回投与試験はどちらの測定法でも投与法のばらつきが大きいように思えます。このような場合は一人が引っ張っている可能性があるので、生データをプロットし平均値を結ぶか、箱ひげ図でグラフを書くべきだと思います。★税込5000円以上ご注文で送料無料★常盤薬品工業 眠眠打破 50ml
2014年05月28日
コメント(0)
-
味の素の新甘味料「アドバンテーム」 欧州と米国で食品添加物認可を取得
味の素の新甘味料「アドバンテーム」 欧州と米国で食品添加物認可を取得出典:プレスリリース 味の素は、新甘味料「アドバンテーム」について、欧州委員会と米国食品医薬品局(FDA)の食品添加物認可を取得しました。(欧州委員会の認可取得は2014年5月14日、FDAの認可取得は2014年5月19日) 「アドバンテーム」は、当社が独自開発したアミノ酸系高甘味度甘味料で、砂糖の20,000~40,000倍の甘味度を持ち、味質の改善やコストダウンなど、食品や飲料など幅広い分野に新しい価値を提供します。「アドバンテーム」はフレーバーの安全性評価制度である米国FEMA GRASを2010年6月に取得、米国やFEMAに準拠しているアセアン・南米各国で、風味を増強させる風味改良剤(Flavor Modifier)として、既に販売されています。今回の、欧州委員会およびFDAの食品添加物認可取得により、多目的に使用できる甘味料として、卓上甘味料や、焼き菓子、ソフトドリンク、デザート、ジャム、チューインガムなど、幅広い食品に使えるようになります。 なお、日本国内でも食品添加物の認可申請中で、認可取得後に日本国内でも販売を開始する予定です。 さて、砂糖とアドバンテームでは糖尿病の発症に差があるのでしょうか?砂糖の摂取が糖尿病の最大リスクであることは間違いないと思います。(ベネフィットが上回っているので、砂糖はたばこのように叩かれることはありませんが)1日の砂糖の使用量を一定に保ち、それ以上の甘みはアドバンテームに置き換え群と全部砂糖群で糖尿病発症率の(別にアドバンテームに限るわけではないですが)比較なんてことを試みるヒトは、コストベネフィットと製薬メーカーの非協力からまあ夢物語でしょう。暴論ですが、少々の(1%未満)発がん性は糖尿病の発生率およびそれに対する医療費を考えると許してもいいのではないでしょうか。
2014年05月28日
コメント(0)
-
統合失調症治療薬 Asenapine(アセナピン)の臨床第III相試験結果のお知らせ
統合失調症治療薬 Asenapine(アセナピン)の臨床第III相試験結果のお知らせ出典:プレスリリース Meiji Seika ファルマ株式会社は、MSD株式会社と共同開発を進めている非定型抗精神病薬に分類される統合失調症治療薬asenapine(国際一般名称)の臨床第III相試験のうち、プラセボ対照二重盲検比較試験の結果が得られましたのでお知らせします。今回の試験は、日本、韓国および台湾の20歳以上65歳未満の急性増悪期の統合失調症患者を対象に、asenapineの2用量群(5mg 1日2回もしくは10mg 1日2回)およびプラセボ群(1日2回)の3群に分け、6週間服用後に、主要評価項目としてPANSSを用いて、症状の改善効果を検証することを目的に実施しました。その結果、asenapineの2用量でプラセボ群に対して有意な症状の改善効果を示しました。臨床第III相試験のうち、長期投与試験は現在実施中です。当社は、日本国内における本剤の統合失調症の適応取得を目的とした製造販売承認申請を2015年中に行う予定であり、承認取得後の販売・流通およびプロモーションは、当社が単独で実施します。 asenapineはアメリカでは総合失調症と双極性障害に関して適応を有しており、Saphris(R)名で販売されている。EUでは双極性障害には効能を取っているが、総合失調症には効果が弱いとして効能をえられていなし。EUでの販売名はSycrest(R)。
2014年05月28日
コメント(0)
-
FDA急性心不全治療薬RLX030に対して追加エビデンスが必要と言及
FDAが急性心不全治療薬RLX030に対する審査完了報告通知を発行出典:プレスリリース ノバルティスは、本日、米国食品医薬品局(FDA)より、急性心不全(AHF)治療薬RLX030(一般名:serelaxin)の生物学的製剤承認申請(Biologics License Application:BLA)について、米国における承認のためには有効性を示すさらなるエビデンスが必要とする審査完了報告通知(Complete Response Letter:CRL)を受領したと発表しました。RLX030は、主要な第III相臨床試験であるRELAX-AHF試験を含む臨床開発プログラムの中から、第II相と第III相臨床試験の有効性と安全性データをもとに、FDAへ承認申請されました。ノバルティスは、6,300名を上回る患者さんが参加予定であるRELAX-AHF-2試験などの大規模なグローバル臨床開発プログラムにより、引き続き急性心不全を対象とするRLX030の有効性データを構築していく予定です。なお、本邦においては、RLX030の第II相臨床試験を実施中であり、日本はRELAX-AHF試験とRELAX-AHF-2試験に含まれておりません。リラキシン受容体作動薬1であるRLX030は、男女双方に存在し、妊娠中の女性で増加して心血管需要の高まりに身体が対処するのを助ける生体ホルモン(ヒトリラキシン2)の遺伝子組み換え型です。RLX030には、血管を拡張させる、水分貯留を減少させるなど複数の効果があります。また、心臓と主要な臓器への損傷を低減する可能性を示唆するエビデンスもあります。これは、急性心不全発現時に起こる損傷の連鎖を考慮する場合に、特に重要と考えられます。 多分翻訳中だと思いますが、CHMPからも追加のエビデンスを提出するよう勧告を受けています。心不全の際の生体反応ではなく、妊娠中の生体反応の解析から見つかったユニークなものです。それ故、色々抑えなくてはいけないことが多いのでしょう。
2014年05月28日
コメント(0)
-
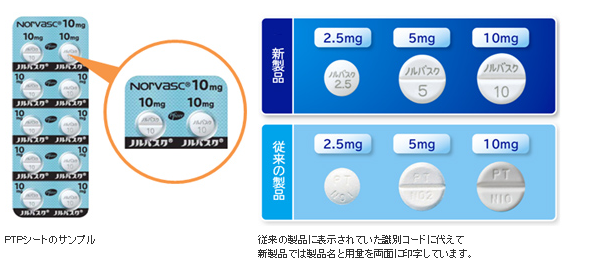
ノルバスク®錠 誤飲・取り違え予防のために “つたわるフォント”で製品名と用量を錠剤に両面印字
ノルバスク®錠 誤飲・取り違え予防のために “つたわるフォント”で製品名と用量を錠剤に両面印字出典:プレスリリース ファイザー株式会社(本社:東京都渋谷区、社長:梅田一郎)は、持続性カルシウム拮抗薬「ノルバスク®錠2.5mg/5mg/10mg」(一般名:アムロジピンベシル酸塩)に、製品名と用量を両面印字した新しい錠剤の製造・出荷を6月より順次開始いたします。 いい試みですね。PTPからこぼれたときとか、PTPだけで保管しているときに、最近は薬局から写真をくれますが、見やすいです。各メーカが追従してもらうことが望まれます。
2014年05月27日
コメント(0)
-
うつ病起こすアストロサイトを特定
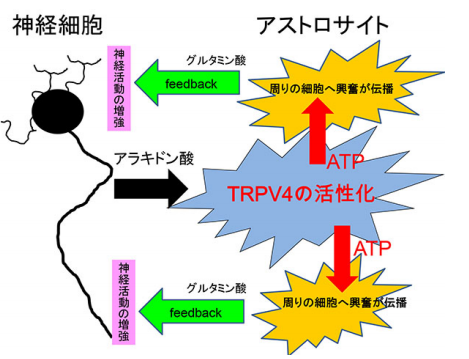
神経活動を調節する特殊な細胞集団を発見―TRPV4 陽性アストロサイトを介した神経活動の増強―出典:プレスリリース(群馬大) 今回、脳内に神経活動を調節できる特殊なアストロサイト集団が存在することを突き止め、この特殊な細胞がどのような分子機序で神経活動を調節しているのかを解明しました。温度センサー・脂質センサーとして知られるTRPV4 分子に注目。脳内では、TRPV4 がアストロサイトの一部のみに発現していることをつきとめました。脳内で神経細胞が活動すると脂質の一種であるアラキドン酸が産生します。これを少数だけ存在するTRPV4 陽性アストロサイトがキャッチすると伝達物質である ATPを放出することが分かりました。このATPを介して、周りのアストロサイトへと次々に興奮信号が伝播し、それらのアストロサイトから別の伝達物質であるグルタミン酸が放出し、神経活動が増強することを突き止めました(図1)。 アストロサイトが ATPやグルタミン酸という伝達物質を放出し、神経活動を調節することが示されたことで、脳梗塞のように神経興奮を抑制しないと、次々に神経細胞が死んでしまう一刻を争う病態において、今回の知見をいかし、アストロサイトの活動をブロックすることでその神経細胞死を防げる可能性が見いだされました。 昨年、脳内アストロサイトからのATP 放出量が減少することで鬱病が発症することが発見されたが、どのアストロサイトが ATP を放出するのかという大変重要な点が未解明のままだった。今回、TRPV4 陽性のアストロサイトが ATP を放出することを見いだしたので、これらアストロサイトの性質をさらに詳細に解析していくことで、鬱病発症の分子メカニズムを明らかに出来る。 この現象を非侵襲下で測定できるようになると、新型うつと従来のうつの区別ができるかもしれません。脳梗塞の脳保護薬としてはエダラボンが効能を持っています。アストロサイトの活性を抑制するONO-2506(arundic acid)はフェーズII/III試験において有効性を確認できず開発中止となっています。 直接的な効果を期待するにはアラキドン酸やグルタミン酸の制御受容体に直接作用しなくてはならないので、抗体等では局所到達性の問題が立ちふさがるような気がします。
2014年05月25日
コメント(0)
-
血管の老化は、筋肉のエネルギー消費を妨げることを発見
血管の老化は、筋肉のエネルギー消費を妨げることを発見 ~肥満や糖尿病を悪化させている可能性~出典:プレスリリース 新潟大学の南野 徹 教授らは、高カロリー食投与によって引き起こされた血管老化が、筋肉でのエネルギー消費を阻害することをマウスの実験で発見しました。 老化した血管が骨格筋におけるエネルギー消費を妨げることを発見しました。通常筋肉では、血流から糖(グルコース)を取り込んで、細胞内のミトコンドリアと呼ばれる小器官でエネルギーを作り出します。しかし、高カロリーの食事を投与された糖尿病病態モデルマウスでは、血管細胞が老化することで、筋肉への糖輸送や、筋肉におけるミトコンドリアの合成能が障害されていることが分かりました。この障害によって余剰となったカロリーが内臓脂肪として蓄積し、肥満や糖尿病がさらに悪化すると考えられます。 これまで、糖尿病で合併する血管障害は、糖尿病の病態の結果と考えられていました。しかし今回の成果で、血管の細胞老化によって肥満や糖尿病がさらに進行する悪循環を引き起こしている可能性を示しました。糖尿病の肥満は血管の老化から生じている可能性をマウスで示しています。細胞老化のキーファクターp53はがん抑制遺伝子でもあるため、p53そのものを治療標的とすることは難しいと思われますがp53の癌抑制機序とそのカウンターを研究する価値はあると思います(プレスリリースの意見とは異なっています)。
2014年05月25日
コメント(0)
-
バルサルタン/シルニジピン配合剤「アテディオ®配合錠」の新発売のお知らせ
バルサルタン/シルニジピン配合剤「アテディオ®配合錠」の新発売のお知らせ出典:プレスリリース 持田製薬は、5月23日、高血圧症治療用のバルサルタン/シルニジピン配合剤 「アテディオ®配合錠」の販売を開始しましたのでお知らせいたします。本剤は、味の素製薬と持田製薬が共同で開発し、本年3月24日に味の素製薬が製造販売承認を取得し、本日、薬価基準に収載されました。味の素製薬が製造販売元で、販売は持田製薬が行います。 「アテディオ®配合錠」はN型カルシウムチャネルブロック作用を有する持続性カルシウム拮抗降圧薬シルニジピンとアンジオテンシンII受容体拮抗薬バルサルタンとの本邦初の配合剤です。異なる機序の薬剤を組み合わせることで、優れた降圧効果が期待されます。包装 : 100錠(PTP)、140錠(PTP)、500錠(PTP)、500錠(バラ)薬価 : 1錠 134.2円製造販売承認日 : 2014年3月24日薬価基準収載日 : 2014年5月23日発売日 : 2014年5月23日製造販売元 : 味の素製薬株式会社販売 : 持田製薬株式会社カルシウム拮抗剤はあまりにゾロ新が出すぎて、12番目のものはジェネリック扱いで薬価が付いたと記憶しています。 薬価算定は新医療用配合剤の特例(「自社品の薬価」+「他者品のうち最も高い薬価」×0.8で算定。結果として1日薬価は併用の8割となっています。
2014年05月25日
コメント(0)
-
選択的 SGLT2阻害剤「ルセフィ®錠2.5mg」「ルセフィ®錠 5mg」の発売について
選択的 SGLT2阻害剤「ルセフィ®錠2.5mg」「ルセフィ®錠 5mg」の発売について 出典:プレスリリース 大正製薬は、2型糖尿病治療薬として選択的 SGLT2阻害剤「ルセフィ®錠 2.5mg、ルセフィ®錠 5mg」を本日発売しましたのでお知らせいたします。 「ルセフィ®錠」は、腎尿細管において糖の再吸収を行う輸送体であるナトリウム-グルコース共輸送体 2 (sodium-glucose cotransporter 2; SGLT2)を選択的に阻害することにより、糖を尿と共に体外に排泄し、血糖値を低下させる新しいタイプの薬剤です。 「ルセフィ®錠」は、日本国内での 2 型糖尿病患者を対象とした第 3 相臨床試験の結果、単剤投与ならびに既存の 6 種類の経口血糖降下薬との併用投与において優れた血糖改善効果を示し、52 週間にわたり減弱することなく効果を維持するとともに、良好な安全性プロファイルを有することが確認されました。 ルセフィ®錠は、大正製薬が創製及び製造販売承認を取得し、販売を当社の連結子会社である大正富山医薬品、およびノバルティス ファーマが行います。 薬 価:ルセフィ®錠 2.5mg 205.50 円 ルセフィ®錠 5mg 308.30 円 承 認 日:2014 年 3月 24日 薬価基準収載日:2014 年 5月 23日 販 売 開 始 日:2014 年 5月 23日 2型糖尿病という適応を取るためには6種類の併用試験が必要ということです。ノバルティスのプレスリリースは見つけられませんでした。発売が遅れるのかもしれません。
2014年05月25日
コメント(0)
-
2型糖尿病治療薬「フォシーガ®錠5mg、10mg」 新発売のお知らせ
2型糖尿病治療薬「フォシーガ®錠5mg、10mg」 新発売のお知らせ出典:プレスリリース アストラゼネカ株式会社と小野薬品工業株式会社は、1日1回経口投与の2型糖尿病治療薬「フォシーガ®錠5mg、10mg(一般名:ダパグリフロジンプロピレングリコール水和物)」を本日発売しましたのでお知らせいたします。フォシーガ®錠は、腎尿細管でのグルコース再吸収を制御するナトリウム・グルコース共輸送体2(sodium-glucose cotransporter 2: SGLT2)に対する選択的かつ可逆的な阻害剤であり、血液中の過剰なグルコースを尿と共に体外へ排出させ、血糖を低下させる薬剤です。本剤は、インスリンを介さずに空腹時血糖および食後高血糖を改善します。本剤は2型糖尿病治療薬として承認された世界で最初のSGLT2阻害剤です。 薬価: フォシーガ®錠 5mg 205.50円/錠 フォシーガ®錠 10mg 308.30円/錠製造販売承認日: 2014年3月24日薬価基準収載日: 2014年5月23日発売日: 2014年5月23日製造販売元: ブリストル・マイヤーズ株式会社販売提携: アストラゼネカ株式会社販売元: 小野薬品工業株式会社 薬価はアステラスのスーグラ(R)錠との類似薬効比較方式(I)で決定。薬価算定資料に外国価格が記載されていますが、常にアメリカが一桁違います。フォシーガ錠は11.57ドルです。
2014年05月24日
コメント(0)
-
MSD株式会社 経口2型糖尿病治療薬「ジャヌビア®錠」 「2型糖尿病」を効能・効果とした一部変更承認を取得
MSD株式会社 経口2型糖尿病治療薬「ジャヌビア®錠」 「2型糖尿病」を効能・効果とした一部変更承認を取得出典:プレスリリース MSDは、本日、経口2型糖尿病治療薬「ジャヌビア®錠(一般名:シタグリプチンリン酸塩水和物)」について、「2型糖尿病」を効能・効果とした一部変更承認を取得しました。これによりジャヌビア®錠は、すべての経口2型糖尿病治療薬およびインスリン製剤との併用療法が可能となりました。 ジャヌビア®錠は、日本初のDPP-4阻害薬として2009年12月に発売いたしました。1日1回の投与で選択的にDPP-4を阻害し、活性型インクレチンを増加させることで血糖依存的な血糖低下効果を示します。 既存の糖尿病治療薬との併用療法において、速効型インスリン分泌促進薬との併用療法の適応はありませんでしたが、両剤の併用試験結果を受け、『経口血糖降下薬の臨床評価方法に関するガイドライン』に基づき、2013年8月に効能・効果の一部変更承認申請を行っていました。新規作用機序の2型糖尿病の新薬が出るたびに、第2相試験で網羅的に併用試験をしなければならないのは面倒な感じがします。併用は必要なくて、取って代わるものこそが新薬ってのは言い過ぎですか?
2014年05月24日
コメント(0)
-
グラクソ・スミスクライン株式会社 新たな慢性閉塞性肺疾患(COPD)治療剤 ウメクリジニウムを日本で承認申請
グラクソ・スミスクライン株式会社新たな慢性閉塞性肺疾患(COPD)治療剤ウメクリジニウムを日本で承認申請出典:プレスリリース グラクソ・スミスクラインはエリプタ®デバイスを使用して吸入する長時間作動型抗コリン剤、ウメクリジニウムについて、慢性閉塞性肺疾患(以下COPD)の効能効果で厚生労働省へ承認申請を行ったことを発表致します。 ウメクリジニウムは、2014年4月28日に欧州、また2014年4月30日に米国にてIncruse ™Ellipta™として承認されました。尚、本剤は2014年以降もその他の国で順次申請されていく予定です。 先月ウメクリジニウム/ビランテロールについて、COPD治療薬として承認申請しています。単剤が未承認だから追加で承認申請したのかな?
2014年05月24日
コメント(0)
-
新規の核酸アナログ製剤「テノゼット®錠300mg」 B型慢性肝疾患の適応で新発売
新規の核酸アナログ製剤「テノゼット®錠300mg」B型慢性肝疾患の適応で新発売出典:プレスリリース グラクソ・スミスクライン株式会社は、5月23日付で、同社の抗ウイルス化学療法剤「テノゼット®錠300mg」(一般名:テノホビル ジソプロキシルフマル酸塩錠、以下「テノゼット®錠」)が薬価収載されたことを受け、同日より発売いたしました。「テノゼット®錠」は、米国Gilead Sciences社により開発されたB型慢性肝疾患治療薬です。GSKグループはGilead Sciences社との契約に基づき、日本におけるB型慢性肝炎治療薬としての独占的開発権および販売権の供与を受けています。 本剤は2014年4月に改訂された平成26年B型C型慢性肝炎・肝硬変治療のガイドライン2において、35歳以上のB型慢性肝炎患者の第一選択薬のひとつとして推奨されました。 製品名 テノゼット®錠300mg一般名 テノホビル ジソプロキシルフマル酸塩錠承認取得日 2014年3月24日発売日 2014年5月23日薬価 300mg 1錠:996.50円効能・効果 B型肝炎ウイルスの増殖を伴い肝機能の異常が確認されたB型慢性肝疾患におけるB型肝炎ウイルスの増殖抑制用法・用量 通常、成人にはテノホビル ジソプロキシルフマル酸塩として1回 300 mgを1日1回経口投与する。ブリストルのバラクルード錠と類似薬効比較方式(II)で薬価算定。補正加算はなし。
2014年05月24日
コメント(0)
-
抗がん剤 BBI608 の結腸直腸がんを対象にした第III相国際共同治験について 新規の患者登録中止のお知らせ
抗がん剤 BBI608 の結腸直腸がんを対象にした第III相国際共同治験について新規の患者登録中止のお知らせ 出典:プレスリリース 大日本住友製薬株式会社(本社:大阪市、社長:多田 正世)は、開発中の抗がん剤として開発中の「BBI608」の結腸直腸がんを対象とした第III相国際共同治験(CO23 試験、以下「本試験」)において、新規の患者登録および登録済みの患者さんへの投与を中止することとなりましたので、お知らせいたします。 独立安全性モニタリング委員会が、97 例の登録患者を対象とした本試験の中間解析を実施しました。その結果、安全性の問題は認められませんでしたが、DCR(病勢コントロール率)において、あらかじめ定められたクライテリア(判断基準)を達成しなかったため、新規の患者登録および登録済みの患者さんへの投与を中止することが勧告されました。なお、すでに本試験に参加した約 280 例については、新たな投与を中止いたしますが、今後、主要評価項目である OS(全生存期間)で評価いたします。 BBI608はがん細胞に加えて、がん幹細胞にも作用して抗腫瘍効果を出すとされている。 第III相試験で効果の点で中止勧告かつ現在投与中のひとも投与中止ということでどれぐらいのマージンをおいていたのか興味あるところです。 OSに関しては投与中止後も検討するとのことですが、病勢が進行している場合はすぐに、病勢が治まっているヒトは再発時に他の治療が入ります。プロトコールが有効であるならば次の治療開始時期はある程度一定条件のもとになりますが、中止するとかなりばらばらの段階で次の状態にすすむと考えられ、すごいバイアスがかかるきがします。 作用点ががん幹細胞にもあるということで、一度BBI608でたたけば延命するということでしょうか? 効果の出ている患者ボランティアまで投与中止するのかに関しては、投与継続を提案しているところと回答していました。 テレカンファランス 最初のQAしか聞いてません。(45分はきつい)
2014年05月24日
コメント(0)
-
骨吸収抑制剤「アレディア®」、骨形成不全症の治療薬として 効能・効果、用法・用量追加の承認を取得
骨吸収抑制剤「アレディア®」、骨形成不全症の治療薬として効能・効果、用法・用量追加の承認を取得効能・効果、用法・用量追加の承認を取得 出典:プレスリリース ノバルティス ファーマは、本日、骨吸収抑制剤「アレディア®点滴静注用15mg/同30mg」(一般名:パミドロン酸二ナトリウム水和物、以下「アレディア」)について、新たに骨形成不全症の効能又は効果、用法及び用量追加の承認を取得しました。 「アレディア」は、破骨細胞に対して骨吸収抑制作用を示すビスフォスフォネート剤であり、骨形成不全症の患者さんに投与することで、骨量の増加及び骨折率の低下が認められています。 「アレディア」は、1989年にイギリスで発売されて以来、2014年3月時点で世界37カ国で承認されています。日本では、初のビスフォスフォネート剤として、1994年に「悪性腫瘍による高カルシウム血症」を効能又は効果として発売された後、2004年に「乳癌の溶骨性骨転移(化学療法、内分泌療法、あるいは放射線療法と併用すること)」に対する効能・効果、用法・用量の追加承認を取得しています。
2014年05月24日
コメント(0)
-
新規抗悪性腫瘍剤「ロンサーフ®配合錠」薬価収載ならびに新発売のお知らせ
新規抗悪性腫瘍剤「ロンサーフ®配合錠」薬価収載ならびに新発売のお知らせ 出典:プレスリリース 大鵬薬品工業株式会社は、抗悪性腫瘍剤「ロンサーフ®配合錠T15・T20」(一般名:トリフルリジン・チピラシル塩酸塩、開発コード:TAS-102、以下本剤)が、本日薬価収載されましたことをお知らせします。発売は5月26日(月)を予定しています。 大鵬薬品が創製した経口のヌクレオシド系抗悪性腫瘍剤であり、国内第II相臨床試験結果に基づき、「治癒切除不能な進行・再発の結腸・直腸癌(標準的な治療が困難な場合に限る)」を効能・効果として、本年3月24日に世界に先駆けて国内で製造販売承認を取得しました。 また、治癒切除不能な進行・再発の結腸・直腸がん患者を対象に実施されている国際共同第III相臨床試験(試験名:RECOURSE)において、本剤がプラセボ投与群に対し、主要評価項目である全生存期間を有意に延長する結果が得られました。この結果に基づき、今後欧米においても申請を予定しています。【製造承認日】2014年3月24日【薬価収載日】2014年5月23日【発売予定日】2014年5月26日【 包 装 】ロンサーフ®配合錠T15:PTP包装:20錠(10錠× 2)、60錠(10錠× 2 × 3) ロンサーフ®配合錠T20:PTP包装:20錠(10錠× 2)、60錠(10錠× 2 × 3)【 薬 価 】ロンサーフ®配合錠T15:2,489.60円 ロンサーフ®配合錠T20:3,340.90円2レジメン以上の前治療歴を有し、かつ抗EGFRモノクローナル抗体製剤を含めて多の標準治療がない治療ラインで選択肢の一つとなっていることと世界に先駆けて日本で最初に承認されたことから、薬価は営業利益率に10%加算。 日本の比較試験ではプラセボ1:TAS-102群2の不均等割り付け。海外試験も不応例に関するプラセボ対照試験。TS-1のように胃癌でファーストラインは狙わないのか?イリノテカン以来の日本発の制がん剤、標準治療の一つに日本主導の臨床試験で組み込まれることを望みます。今の標準化学療法はフッ化ピリミジン系薬剤、イリノテカン、オキサリプラチン、ベバシズマブ、KRAS遺伝子に変異のない野生型の場合では抗EGFRモノクローナル抗体のうちイリノテカンとオキサリプラチンは日本発ですが標準治療に組み込まれた試験は海外主導でした。(イリノテカンの最初の扱いを見ていれば手を出すヒトはいないですが。)
2014年05月24日
コメント(0)
-
腎臓の希少疾病ADPKD患者さんのための錠剤 「サムスカ®錠30mg」を国内で発売
腎臓の希少疾病ADPKD患者さんのための錠剤「サムスカ®錠30mg」を国内で発売 出典:プレスリリース 大塚製薬は、「腎容積が既に増大しており、かつ、腎容積の増大速度が速い常染色体優性多発性のう胞腎の進行抑制」の効能・効果に使用する「サムスカ®錠30mg(一般名:トルバプタン)」を既存の7.5mg錠及び15mg錠に加え新たな製剤として2014年5月29日から発売します。 既に2014年3月24日に既存の7.5mg錠及び15mg錠に対して、この新効能・効果が追加承認され医療現場で使用され始めていますが、患者さんの服用錠剤数を少なくして利便性をより向上させるために、この度、高含量の30mg錠を発売します。
2014年05月24日
コメント(0)
-
「ランマークⓇ皮下注120mg」の骨巨細胞腫に関する効能追加承認取得のお知らせ
「ランマークⓇ皮下注120mg」の骨巨細胞腫に関する効能追加承認取得のお知らせ出典:プレスリリース 第一三共は、「ランマークⓇ皮下注120mg」(一般名:デノスマブ(遺伝子組換え))の骨巨細胞腫に関する承認事項一部変更承認を本日取得しましたのでお知らせいたします。用法・用量 通常、デノスマブ(遺伝子組換え)として120mgを第1日、第8日、第15日、第29日、その後は4週間に1回、皮下投与する。 デノスマブは、ヒト型モノクローナル抗体で、RANKリガンド(破骨細胞の形成、機能及び生存に必須の蛋白質)を標的とする世界初の抗体製剤です。当社は、本抗体を創製したAmgen Inc.(米国)から日本国内での開発・販売権を2007年に取得し、2012年4月に多発性骨髄腫・固形癌骨転移による骨病変の治療剤として「ランマークⓇ皮下注120mg」の製品名で発売、さらに2013年6月には骨粗鬆症治療剤として「プラリアⓇ皮下注60mgシリンジ」の製品名で発売しております。また、乳癌術後補助療法および関節リウマチに関する国内第3相臨床試験をそれぞれ推進しております。
2014年05月24日
コメント(0)
-
前立腺癌治療剤 「イクスタンジ®カプセル」 新発売のお知らせ
前立腺癌治療剤 「イクスタンジ®カプセル」 新発売のお知らせ出典:プレスリリース アステラス製薬は、経口アンドロゲン受容体シグナル伝達阻害剤「イクスタンジ®カプセル 40mg」(一般名:エンザルタミド、以下「イクスタンジ®カプセル」)について、去勢抵抗性前立腺癌の効能・効果で、日本において本日発売しましたので、お知らせします。 包装 イクスタンジ®カプセル 40mg:56カプセル(14カプセル×4シート)薬価 イクスタンジ®カプセル 40mg(40mg 1カプセル):3,138.80円薬価収載日 2014年5月23日発売日 2014年5月23日去勢抵抗性前立腺癌についての新薬ということで、原価計算方式となり 40mg1,575.70円と算定され、外国価格の調整がついて最終的に薬価は3,138.80円となった。用法・用量は160mgを1日1回なので、1日薬価は12,555.2円 4週間で351,545.60円。 去勢抵抗性前立腺癌になっても去勢状態の維持を目的に薬物去勢は継続されるので、今までの治療に月40万円プラスになることになります。 ドセタキセルは70mg/m2を3週に1回 薬価は80mg 59,156.00円で概略月88,753.00円(ジェネリックの場合は57,720.00円) これは製造販売後臨床試験でドセタキセルとの比較試験を実施して臨床的有用性を出しておかないと、経済的にはドセタキセルが有利。 斜体で記載しているのは個人的意見です。間違い等も入っている場合もありますので、参考にとどめてください。
2014年05月24日
コメント(0)
-
「カンゾウ葉エキス」に肌のアンチエイジングの可能性
肌細胞の老化モデルで、サーカディアンリズムが乱れることを解明リズムの乱れを補正し、肌のコラーゲン産生を高める天然素材を発見出典:ロート製薬 プレスリリース ロート製薬は、「再生美容」や「機能性素材の探索」をテーマに掲げる研究拠点「ロートリサーチビレッジ京都」で肌のサーカディアンリズムについて、体内時計(R)をつかさどる「時計遺伝子」に着目して研究を行い、肌細胞の老化モデルではサーカディアンリズムが乱れていることを確認しました。また、リズムの乱れを遺伝子レベルで補正し、かつ肌のコラーゲン産生を促進する素材として「カンゾウ葉エキス」を発見しました。夜の肌細胞レベルでのリズムの乱れは、エイジングに伴う肌機能低下のメカニズムの一つと考えられます。本研究結果は今後、アンチエイジング製品開発に応用していきます。 体内時計はロート製薬の登録商標(第5093717号)なんですね。サーカディアンリズムは体内時計と訳さずに概日リズムと訳すのが多いのはこの理由?繊維芽細胞に過酸化水素処理したものを、細胞老化モデルとしています。老化モデルでは概日モデルが乱れて、夜にもPER1(時間遺伝子)のmRNA発現が下がらなかった。Type1コラーゲンの産生量はPER1のmRNAと逆の動きをしており、細胞老化モデルではコラーゲンの産生が落ちていました。カンゾウ葉エキスは細胞老化モデルにおいて、夜に時間遺伝子を低下させ、コラーゲンの産生を増やしました。 概日リズムあるいは時計遺伝子が肌細胞にどのような影響を与えているのかは更に研究が必要ですが、カンゾウ葉エキスが肌のアンチエイジングに使える可能性がありそうです。 カンゾウ葉エキスに関してはすでにEstrogen induces VEGF-A expression in hair follicle dermal papilla cells.として日本皮膚科学会第37回学術大会で報告されるなど様々な効果が明らかになっています。すでに化粧品の成分として認められています。
2014年05月23日
コメント(0)
-
帝國製薬 経口抗アレルギー剤を導入
帝國製薬、経口抗アレルギー剤に関するライセンス契約締結の件出典:プレスリリース 帝國製薬はJ. Uriach(スペイン)と同社が保有する経口抗アレルギー剤「Rupatadine錠(ルパタジン錠)の日本における開発、販売に関するライセンス契約を締結。ルパタジンは国内未承認医薬品(新有効成分)で、その錠剤は欧州を中心に「Rupafin」のブランド名で世界50カ国以上で販売されている。海外での適応症はアレルギー性鼻炎および蕁麻疹で、その用法は10mgを1日1回経口投与となっている。 ルパタジンは第二世代の抗ヒスタミン薬。12歳以上の成人および小児のアレルギー性鼻炎および慢性蕁麻疹の適用を有している。 脳関門を通過しないために鎮静作用が少ないとされる第二世代の抗ヒスタミン薬としてはエピナスチン塩酸塩(アレジオン)、ロラタジン(クラリチン)、塩酸フェキソフェナジン(アレグラ)、塩酸セチリジン(ジルテック)が日本で発売されている。アレジオン、アレグラについてはOTC化されている。
2014年05月23日
コメント(0)
-
イーライリリー 1日1回投与インスリン 第3相試験でポジティブな結果
2型糖尿病患者を対象とした3つの第III相試験においてイーライリリー社のBASAL INSULIN PEGLISPROがインスリングラルギンに対してHBA1C値の低下における優越性を示す2015年第1四半期までに米国及び欧州の規制当局へ承認申請の見込み プレスリリース (クリックするとプレスリリースが開きます) 5月12日1型及び2型糖尿病の1日1回投与治療薬として開発中のbasal insulin peglispro (BIL)に関して、2型糖尿病患者を対象として完了した3つの第III相試験について、ポジティブなトップライン結果を発表しました。全3試験で主要有効性評価項目であるヘモグロビンA1c(HbA1c)値 低下において、インスリングラルギンに対し 非劣性が達成されました。主要評価項目達成を受けてHbA1c値低下の優越性を検討したところ、全3試験で、インスリングラルギンと比較してBILは統計学的に有意なHbA1c値低下を示しました。 対象とした2型糖尿病患者インスリ未治療 (IMAGINE-2)持続型インスリンと食前インスリンを併用している患者 (IMAGINE-4)持続型インスリンで治療中の患者 (IMAGINE-5) これらの臨床試験では、副次的評価項目として夜間低血糖発現率及び体重の変化を評価しました。全3試験で、BIL投与群はインスリングラルギン投与群と比較して夜間低血糖発現率が統計学的に有意に低下しました。さらに、BIL投与群では、体重増加は同等か統計学的に有意に少ないことが示されました。 臨床検査値の変化BIL投与群にわずかではあるが統計学的に有意なトリグリセリドの上昇が認められました。IMAGINE-4及びIMAGINE-5では、インスリングラルギン投与群と比較して、わずかではあるが統計学的に有意なHDL(高比重リポ蛋白)コレステロールの低下が付随して認められました。この所見はIMAGINE-2では認められませんでした。IMAGINE-2及びIMAGINE-4では、LDL(低比重リポ蛋白)コレステロールの変化量にBIL投与群とインスリングラルギン投与群で統計的な有意差は認められませんでした。IMAGINE-5においては、BIL投与群はインスリングラルギン投与群と比較して、52週目でのLDLの有意な低下を認めました。肝酵素ALT(アラニン・アミノトランスフェラーゼ)の基準値上限の3倍超の上昇を示した被験者は、BIL投与群でインスリングラルギン投与群よりも多く認められました。IMAGINE-2及びIMAGINE-5では、一部の被験者を対象にMRIによる肝脂肪の測定を行いました。インスリン未治療の2型糖尿病患者を対象とした臨床試験(IMAGINE-2)では、BIL投与群の肝脂肪量はベースラインからの変化を認めませんでしたが、インスリングラルギン投与群では肝脂肪量のベースラインからの減少が認められました。持効型インスリンで治療中の2型糖尿病患者を対象とした臨床試験(IMAGINE-5)では、BIL投与群で肝脂肪量はベースラインから増加し、26週目以降に安定しました。インスリングラルギン投与群では、臨床試験期間中に肝脂肪量の変化を認めませんでした。 これまでに完了した2型糖尿病患者を対象とした試験の解析から、有害な心血管イベントの発現率はBIL投与群とインスリングラルギン投与群で同程度であることが示されました(95%信頼区間の上限は1.8未満であった)。 インスリン投与が1日1回で済むということで、インスリングラルギンが大変重宝されています。それにもう一つラインナップが増えて、インスリングラルギンがアレルギー等で使えない患者さんには朗報と思います。
2014年05月22日
コメント(0)
-

サルでもお返しをする人を認識する。
神経科学研究の進歩に貢献するマーモセットの社会的知性を明らかに独立行政法人国立精神・神経医療研究センター名古屋大学プレスリリース 神経科学研究の進歩に欠かせない新世界ザルの一種である小型の「マーモセット」が、高い他者認知能力を持つことを実験によって明らかにし、英国の科学誌「Biology Letters」に発表しました。 これまで身体の大きなフサオマキザルでは道具を使用したり、優れた記憶能力を持つなど社会的認知能力が高いことが知られていましたが、今回の研究成果により、体重300g前後で道具を使用せず記憶能力も劣るマーモセットにおいてもフサオマキザルと同様の社会認知能力を有することが示されました。マーモセットは小型で扱いやすく、繁殖力が高いという性質から、モデル動物として高い有用性を持っていることが知られています。 この結果は、マーモセットが社会的知性や対人性に問題を持つ自閉症や発達障害の研究推進に道を開くものであり、学術的にも高い意義を持つと考えられます。 ノドジロオマキザル(Wikipediaより) ピグミーマーモセット(Wikipediaより) マーモセットは一夫一妻性で、父親も子育てに参加したり、食物を分け与えたりと協力的であり、緊密な社会性を有していることが知られています。 実験に使用した4頭のマーモセットはいずれも、互恵性を示す演技を見た後では、二人の人物から同じ割合で食物を取りましたが、非互恵性を示す演技の後には、非互恵的な演技者(A)から食物を受け取ることを避ける傾向にありました 互恵性とは、互いに相手に利益や恩恵を与え合う性質があることをさす。多くの霊長類は集団内で他個体に毛繕いをするが、されたほうは直後でなくても毛繕い仕返すのが一般的である。 ロジカルな思考力や記憶能力に優れる一方、他者認知能力や社会的知性に問題がある自閉症の脳機能解明に、マーモセットが役に立つ可能性を示唆しています。 マーモセットはワシントン条約付属書IIに分類されているため、 入手は困難なので、非侵襲的検査しか実施できないのは残念。
2014年05月22日
コメント(0)
-
5月16日のプレスリリース
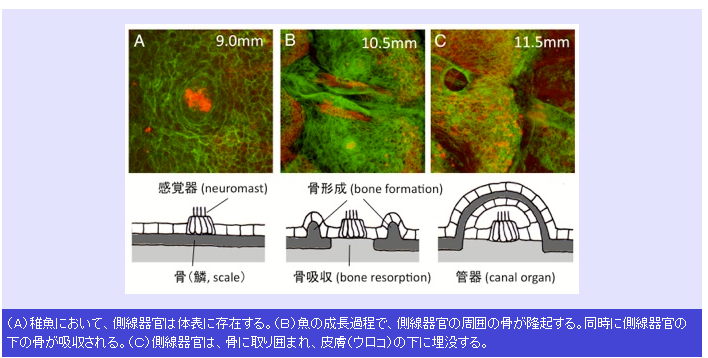
高血圧症治療剤「カンデサルタン錠『あすか』」に関する事業化契約の締結についてあすか製薬 武田薬品工業<概要>カンデサルタン「あすか」は、武田薬品が同社の高血圧症治療剤「ブロプレス®錠」(一般名:カンデサルタン シレキセチル、以下「ブロプレス」)の特許権等をあすか製薬に許諾したオーソライズド・ジェネリック(Authorized Generic:AG)です。本年2月、あすか製薬は、厚生労働省よりカンデサルタン「あすか」の製造販売承認を取得し、6月の薬価収載に向けて薬価申請を行っています。本契約に基づき、カンデサルタン「あすか」の薬価基準収載後、あすか製薬は本剤を発売し、医療機関に情報提供を行います。一方、武田薬品は、本剤をあすか製薬から仕入れ、特約店に販売する物流業務に特化します。その他、契約内容の詳細については開示しておりません。<感想>オリジンをもつ会社がジェネリック販売(物流ですが)に係わるという契約です。一般的にジェネリック医薬品は原薬およびその含有量は同じですが、添加物や製剤化過程が異なります。生物学的同等性試験で担保は取っていますが、その点にこだわる人もあることが事実です。今回の場合は原薬・添加物、製造方法が同一のAuthorized Generic(AG)なのでその点は問題ないことになります。武田薬品工業もあすか製薬からロイヤリティが取れるので、金銭面でメリットがあります。安全性情報の収集、提供に関してもあすか製薬の場合は納めて終わりではないと思われますので、ジェネリック医薬品の拡大の一手段になるかもしれません。リンク先:http://www.takeda.co.jp/news/2014/20140516_6561.html米国臨床腫瘍学会年次集会における TAK-700(一般名:orteronel)の臨床第3相試験の最新データについて 武田薬品工業<概要>化学療法を受けていない転移性・去勢抵抗性前立腺癌患者を対象とした本試験では、プレドニゾンとTAK-700併用群は、プレドニゾンとプラセボ併用群と比較し、二つの主要評価項目のうちの一つである画像上での無増悪生存期間(rPFS: radiographic Progression Free Survival)において30%の有意なリスク減少を示しました。もう一方の主要評価項目である全生存期間(OS:Overall Survival)においては、TAK-700併用群はプラセボ併用群と比較し、中央値で1.9ヶ月の改善を示したものの、統計学的な有意差はみられませんでした。<感想>前立腺癌が再発するまでの期間は長くなりますが、トータルの生存期間はステロイド単独と変わらないとの結果です。現在は再発した場合の薬剤はないので、こういうことになっていると思います。再発した場合に有効な(生存期間をプラセボあるいは既存治療より延長する)薬剤がある場合にはこの結果はまた評価が変わります。リンク先:http://www.takeda.co.jp/news/files/20140516_02_jp.pdf弊社社員の医師主導臨床研究の関与への関与について協和発酵キリン<概要>腎性貧血治療薬「ネスプ注射液」に係る医師主導臨床研究で問題発生データの入力の代行、臨床検査結果に個人情報が含まれているのに社員が保管、臨床検査結果に対する解析を行った、3点が問題。<感想>医師主導臨床研究を行った医師は新聞で大きく取り上げられていましたが、薬剤販売会社にも問題があったということです。営業本部が情報を抱え込んでいたということも問題視されています。医師主導臨床研究に関してはデータマネージメント(DM)や解析に関して予算をきっちり取っていない、品質管理の概念が薄いなど医師側に大きな問題があります。それを製薬企業におまえのところの薬を使ってやっているからなんとかせいと医師が押しつけます。DM、解析、品質管理はただでできません。またこれを怠るということは協力してくれた患者ボランティアに対する感謝の気持ちが医師にないことから生じています。主体が製薬企業の場合でもこの構造は変わりません。(極論です)リンク先:http://www.kyowa-kirin.co.jp/news_releases/2014/pdf/20140516_01.pdf骨リモデリングによるゼブラフィッシュ側線器官の形成メカニズム国立遺伝研究所<概要>ゼブラフィッシュの側線器官(感丘)は、稚魚期には体表にありますが(図A)、魚の成長過程において、骨組織であるウロコの中に取り込まれます(管器、図C)。我々は、この移行過程において、骨形成と骨吸収(骨リモデリング)が行われていることを明らかにしました(図B)。さらに、ウロコの移植実験と突然変異体解析から、(1)側線器官が骨リモデリングに必要であること、また、(2)骨リモデリングは側線器官の成長に必要であること、を示しました。これらの結果は、感覚器(神経組織)と骨(結合組織)は、密接に相互作用しながら、形態形成を行っていることを示しています。<感想>感覚器と骨(神経組織と結合組織)の関係を魚のウロコを使って確かめたものです。この研究の優れているのはウロコという外部にある骨組織を観察することで生体が生きている状態で研究をしているところです。リンク先:http://www.nig.ac.jp/Research-Highlights/1468/1510.html免疫応答の要となる分子の閾値(いきち)決定機構を解明理化学研究所<概要>B細胞の情報伝達経路である「CARMA1-TAK1-IKK」は、B細胞のシグナル伝達をNF-κBに仲介するアダプター分子「CARMA1」と、リン酸化酵素の「TAK1」および「IKK」とで構成され、これらが連携して細胞内で情報を伝達しNF-κBを活性化します。研究グループはこの経路について詳細な分子動態の計測を行い数理モデル化し、シミュレーション解析しました。この結果、TAK1がCARMA1のリン酸化を介してIKK活性をさらに増幅する、という「正のフィードバック(図の黒線)」制御を行っており、これがNF-κBのいき値を決定していることが分かりました。さらに、このメカニズムによるNF-κBのいき値活性の制御を1細胞レベルで検証しました。B細胞受容体を刺激したところ、一定の刺激量以上だとNF-κBの核内移行が「起きる、起きない(0か1)」のデジタルに制御されている、つまりいき値が存在することが認められました。<感想>体内でもアナログ-デジタル変換が行われているということです。がんやアトピー性皮膚炎の新しい切り口ができるかもしれません。理化学研究所は税金を使っているから成果を出さなくてはならない、という意見は反対。利益を追求する私企業で基礎研究はどうしても軽視されます。国の基礎体力をつけるためには必要な国の投資だと思います。ただし、その恩恵を受けた企業はきちんと税金を払うだけでなく、寄付という形で国の科学研究費に投資するべきだと思います。そこから医師主導臨床研究の資金を出すことにすれば、最近の問題発生の予防になると思います。リンク先:http://www.riken.jp/pr/press/2014/20140516_2/digest/白血球「好塩基球」の喘息における新メカニズムを解明独立行政法人理化学研究所<概要>マウス生体内で起きるアレルギー反応での好塩基球の役割を解析するため、好塩基球を欠損させたマウスと、好塩基球由来のインターロイキン「IL-4」だけを欠くマウスを準備しました。通常、システインプロテアーゼを投与すると、肺に炎症の原因となる白血球一種の好酸球が大量に集まり、ムチンという粘液の産生が誘導されて喘息症状が現れます。ところが、好塩基球を欠損させたマウスにシステインプロテアーゼを投与しても喘息症状は現れず、肺への好酸球の集積やムチンの産生も抑制されました。喘息症状の抑制はIL-4だけを欠くマウスでも確認され、この結果、好塩基球から産生されるIL-4の重要性が示されました。NH細胞の活性化には好塩基球から産生されるIL-4が必要であり、システインプロテアーゼで誘導される喘息では、好塩基球とNH細胞の共同作業が必要であることが明らかになりました。<感想>ぜんそくに関しては発作予防、発作軽減の薬はほぼ完成形にあると思います。ぜんそくそのものの治療に突破口を開くかもしれません。ただし、免疫機能を調節するわけですから、この切り口では思いもよらない副作用が発生するかもしれません。リンク先:http://www.riken.jp/pr/press/2014/20140516_1/digest/成熟した脊髄内での神経細胞新生に成功 -神経組織再生の高効率化に期待-京都大学<概要>脊髄での神経細胞産生を亢進して脊髄損傷による下肢の麻痺を大幅に改善することに成功しました。成熟した脊髄では神経細胞産生は厳密に阻害されており、治療には細胞移植が必要と考えられていました。今回の結果は、内在神経幹細胞の神経細胞産生能力を活性化するだけでも損傷を治療できる可能性を示しました。<感想>これが人に応用できればすごいことだと思います。iPSも裸足で逃げ出す成果だと思います。車いすの人が立って歩ける可能性があるからです。神経組織は再生しないというのが定説でしたが、厳重に再生を抑えている仕組みがあり、それを解除すれば再生する。なぜ再生させないようになっているかに関しての知見が集まればこの発見を人に応用する際の副作用を予見できると思います。リンク先:http://www.kyoto-u.ac.jp/ja/news_data/h/h1/news6/2014/140516_1.htm超ルイス酸性分子の開発に成功東京工業大学<概要>このボリニウムイオンの高い反応性を示す結果として、特異な二酸化炭素の活性化反応も見出した。ボリニウムイオンの溶液に二酸化炭素ガスを混合すると、二酸化炭素の炭素原子にボリニウムイオンのメシチル基が移り、かつ酸素を一つ失ったカチオン化合物が速やかに生成した(図3)。すなわちこの反応では、二酸化炭素の酸素原子がホウ素により奪われている。この特異な反応は、強いルイス酸中心であるボリニウムイオンのホウ素原子が、二酸化炭素の酸素原子に配位することから進行すると考えられる。<感想>素人考えですが、人工光合成(二酸化炭素から酸素を作る)ができるのではと思いました。リンク先:http://www.titech.ac.jp/news/2014/027678.html今日はここまで
2014年05月17日
コメント(1)
-

5月9日のニュースリリース
昨日は決算の発表がたくさんありました。パイプラインに関しての情報もありますが、それは省略。 昼に光合成、夜に細胞分裂が起こるのはなぜか?その謎を解明!国立遺伝研究所<概要> なぜ、そのような時間帯の制限が存在するのでしょうか。それはどのような仕組みによるのでしょうか。遺伝学研究所の宮城島進也特任准教授らは、細胞分裂の観察が容易な単細胞性の藻類(真核生物の紅藻)を用いて、その謎を突き止めることに成功しました。 紅藻は、光合成を行う水生生物で、夜、細胞分裂が起こることが知られています。宮城島特任准教授らは、まず、細胞分裂の進行をオンにするスイッチは何かを調べました。生物の細胞内に、概日リズムを刻む生物時計(細胞内時計)が存在することはよく知られているのですが、その時計に連動したスイッチがあるはずなのです。そして、詳しく解析した結果、E2Fと呼ばれるタンパク質がスイッチとしてはたらくことで、細胞分裂は夜引き起こされることが明らかになりました。 光合成を行う生物の細胞では、ミトコンドリアや葉緑体が活動する時間帯と細胞分裂が起こる時間帯が分けられることで、活性酸素の子孫細胞に与えるダメージが、最小限にとどめられているのではないかという推測が得られたのです。<感想>エネルギーを産出するさい、酸素がその過程に含まれている限りは過酸化物質による酸素毒を避けることはできない。今までは過酸化物質除去の部分を取り上げることが多かったと思いますが、細胞分裂という繊細な作業は時間帯を避けるということ。睡眠が体の成長、アンチエイジングに重要であるということの理論的後押しをする可能性に期待。リンク先:http://www.nig.ac.jp/Research-Highlights/1468/1506.htmlゆっくり食べると食後のエネルギー消費量が増えることを発見<概要>急いで食べる時に比べて、ゆっくり食べる方が食後のエネルギー消費量が増加することを明らかにした。300kcalのブロック状の食品をできるだけ急いで食べると、その後、90分間のエネルギー消費量は体重1kg当り平均7calだった一方、食塊がなくなるまでよく噛んで食べた時には180calと有意に高い値だった。また、消化管の血流もゆっくり食べた時の方が有意に高くなったことから、ゆっくり食べると消化・吸収活動が増加することに関連してエネルギー消費量が高くなったものと推察される。<感想>基礎代謝量の1割を占める食事誘発性体熱産生が20倍以上になるということです。結構大きいのでは 0.18×50×3×360=9720kcal ゆっくり噛むだけで50kgのひとはこれぐらい変わる。(脂肪で1kgぐらいかな)。基礎代謝を上げることはなかなか難しいのでダイエットにはいいかと。リンク先:http://www.titech.ac.jp/news/2014/027599.html
2014年05月10日
コメント(0)
-
5月7日のプレスリリース
2014年米国消化器病週間における酸関連疾患治療薬ボノプラザンフマル酸塩の最新試験データの発表について武田薬品工業<概要>2014年5月3日から6日まで、米国イリノイ州シカゴで開催された「米国消化器病週間(Digestive Disease Week)」において、ボノプラザンフマル酸塩(開発コード:TAK-438)の5つの臨床第3相試験結果をポスター発表しました。ボノプラザンフマル酸塩は、当社が創製したカリウムイオン競合型アシッドブロッカー(Potassium-Competitive Acid Blocker : P-CAB)と呼ばれる新しいカテゴリーの酸分泌抑制薬であり、胃壁細胞における酸分泌の最終段階に位置するH+, K+-ATPase(プロトンポンプ)をカリウムイオンと競合的に阻害することにより、強力かつ持続的な酸分泌抑制作用と、投与早期からの効果発現を示します。<感想>有効性はタケプロンを対象に非劣性を証明。有害事象の発生率は同じ。NSID長期投与の胃潰瘍再発率はタケプロンよりも有意に押さえた(5.5 ⇒ 3.3%)ということ。有効性はタケプロンで90%超えているので、優越性を示す必要がないとは思うが、潰瘍再発率で5%が3%と優位性が統計学的に有意性が示されているが、無再発が94.5%が96.7%になったということは医学的に優位性があるのでしょうか?新規作用機序をもつ薬剤ではありますが、有害事象のパターンは同じで、有効性に差がない場合に有効性加算はとれるのでしょうか?メリットはプロトンポンプ阻害薬がアレルギーで使えない人に使えるだけ?(ちょっと極論)リンク先:http://www.takeda.co.jp/news/2014/20140507_6461.html経口アンドロゲン受容体阻害剤エンザルタミド 米国FDAからの追加適応申請受領通知、優先審査に指定アステラス製薬米国メディベーション社と共同で開発・商業化を進めている経口アンドロゲン受容体阻害剤エンザルタミド(一般名、欧米での製品名:XTANDI®、開発コード:MDV3100)について、米国食品医薬品局(FDA)から、化学療法施行歴のない転移性去勢抵抗性前立腺がんの追加適応症での医薬品承認事項変更申請を受領した旨の通知を受けました。当該申請には優先審査が適応され、通知された審査終了目標日(PDUFA Date)は、2014年9月18日です。なお、エンザルタミドは現在、米国において、ドセタキセルによる化学療法施行歴を有する転移性去勢抵抗性前立腺がんの治療薬として承認を取得しています。化学療法施行歴のない転移性去勢抵抗性前立腺がん患者1,700名以上を対象に実施したプラセボ対照試験である第III相PREVAIL試験の結果に基づいています。<感想>去勢抵抗性の定義はホルモン療法(抗アンドロゲン剤)が長期継続によるホルモン抵抗性になったものも含むので、去勢抵抗性の前立腺がんになぜアンドロゲン受容体阻害剤が効くのか不思議といえば不思議。核内移行とDNA結合、活性化補助因子の動員を抑制するということですが、元になるテストステロンが去勢により生産されていないのに・・・リンク先:http://www.astellas.com/jp/corporate/news/detail/fda-3.html世界初の不可逆的ErbBファミリー阻害剤「ジオトリフ®錠」 新発売、EGFR遺伝子変異陽性の手術不能又は再発非小細胞肺癌の効能・効果で日本べーリンガーインゲルハイム<概要>EGFR遺伝子変異陽性の手術不能又は再発非小細胞肺癌の効能・効果で、4月17日に薬価収載された経口の抗悪性腫瘍剤/チロシンキナーゼ阻害剤「ジオトリフ®錠 20mg/同30mg/同40mg/同50mg」(以下「ジオトリフ®錠」、一般名:アファチニブマレイン酸塩)を本日5月7日より発売。<感想>審査報告書によれば、死亡例は海外のピボタル試験では13/175、日本では0/54。日本人に多いグレード3以上の副作用は下痢、発疹/ざ瘡および爪の異常であるが、休薬・減量・投与中止でコントロール可能であった。海外の死亡には間質肺疾患様事象が原因となる場合が多かった。下痢では臨床試験中には死亡例はみられていないが、named use programmeで死亡例が2例報告されているが、いづれも下痢に対する適切な治療を受けられず、天気に大きな影響を与えたと思われる。経口剤ですからね。一人暮らしで下痢を発症して、トイレでそのままなんてことが、発売後には増えるのじゃないですかね。間質性肺炎に関しては適応が肺がんなので定期的に通院していればかなり避けることができるでしょうが。皮膚のなかで、SJSが出ていますが、転帰不明というのはどうしてかな?死亡例はないし、重篤有害事象だから最終観察時未回復でないと問題が生じるのではないか?当初は800例の製造販売後調査を予定されたが、重篤な有害事象を評価可能な例数として専門協議において1500例とされた。リンク先:http://www.boehringer-ingelheim.jp/news/ プレスリリース http://www.info.pmda.go.jp/shinyaku/P201300171/ 審査報告書HP-3060(経皮吸収型アレルギー性鼻炎治療剤)の 国内第II相臨床試験結果のお知らせ久光製薬<概要>アレルギー性鼻炎を有する成人を対象に、本剤の薬物動態、有効性および安全性について、プラセボ対照の試験を実施しました。その結果、安定した薬物濃度を維持するとともに、有効性の主要評価項目でプラセボ投与群との間に統計学的有意差をもって改善が確認されました。また、安全性に関して重篤な副作用は認められませんでした。 本結果を踏まえ、第III相臨床試験で有効性の検証を行うとともに、長期投与時の安全性および有効性を確認します。<感想>はいそうですか。経皮吸収は期待される選択肢ですが、もう少し具体的な内容を記載してもいいのではないかと思います。リンク先:http://www.hisamitsu.co.jp/company/pdf/news_release_140507.pdf 医薬品第一部会の議事録が公開されていますが、2013年8月2日版です。審査報告書がわかるといえばいいのですが、薬価収載までには公開してほしいと思います。 今日はここまで。
2014年05月08日
コメント(0)
-
5月6日のプレスリリース
5月6日は振替休日だったので、国内ではプレスリリースを見つけることができませんでした。海外で1つだけ US FDA approves EPANOVA for the treatment of adults with severe hypertriglyceridaemiaAstraZeneca Global<概要> the US Food and Drug Administration (FDA) has approved EPANOVA (omega-3-carboxylic acids) as an adjunct to diet to reduce triglyceride levels in adults with severe hypertriglyceridaemia (triglyceride levels greater than or equal to 500 mg/dL).The FDA approval was based on data from a clinical development programme that included positive results from the Phase III EVOLVE (EpanoVa fOr Lowering Very High triglyceridEs) trial, which examined the efficacy of EPANOVA in lowering triglycerides and other key lipid parameters in patients with very high triglycerides. The effect of EPANOVA on the risk of pancreatitis or on cardiovascular mortality and morbidity has not been determined.<感想>トリグリセライド血症治療薬の目的は血中トリグリセライドを下げることではありません。膵臓炎や心血管系の発生率の低下と心血管系による死亡リスクの低下です。高血圧用薬やスタチン系を代表とするコレステロール血症も同様に、心血管系のリスク低下、脳血管系のリスクの低下が治療の目的です。プラセボとの比較試験がいくつかあって、メタアナリシスがポジのAとなるのは大変な道のりではあるけれども、それがなければ薬価をつけないとなれば高血圧とスタチンだけでもすごい医療にの節減にはなるのですがね。(極論ですよ、誤解なきよう。サロゲートエンドポイントでは少なくともBでなければ承認されませんから。)今日はここまで
2014年05月07日
コメント(0)
-
5月5日のプレスリリース
Novartis drug Signifor® LAR shows superior efficacy in acromegaly patients not controlled on first generation somatostatin analogues.Novartis<概要>Phase III data show patients on pasireotide LAR achieved greater biochemical control, as measured by both GH and IGF-1 levels, versus control group.These data, supported by a previously published Phase III study, are the basis for worldwide regulatory filings for pasireotide LAR in the treatment of acromegaly.<感想>末端肥大症に新薬登場です。クッシング症候群ですでの効能を有しているSigniforが待った肥大症で良好な試験結果を得ました。リンク先:http://www.novartis.com/newsroom/Landmark Study Shows Once-Monthly Long-Acting Therapy INVEGA® SUSTENNA® (paliperidone palmitate) Significantly Delayed Time to Relapse in Patients with Schizophrenia Compared to Daily Oral Antipsychotic.Johnson & Johnson<概要>the results of its landmark PRIDE (Paliperidone Palmitate Research In Demonstrating Effectiveness) trial. PRIDE is the first prospective, randomized clinical trial to compare schizophrenia medications within the context of many “real world” issues in the treatment of schizophrenia, including some of the most challenging circumstances – recent incarceration and substance abuse.INVEGA® SUSTENNA® showed statistical superiority against the primary endpoint, delaying relapse in patients with schizophrenia, as well as in reducing overall relapse, compared to the most commonly used treatments, daily oral antipsychotics (median 416 days vs. median 226 days; P = 0.011). The risk of relapse was 1.4 times higher (95% CI: 1.09, 1.88, P=0.011) in the oral group versus the INVEGA® SUSTENNA® group<感想>ヤンセンの月1注射のゼプリオンにブルーレターが出たところです。(頻度は臨床試験を上回るものではなかったと思います。)この手の薬は重大な副作用が出たときにどうやって中和するのでしょうか?リンク先:http://www.jnj.com/news/all/GREER® Laboratories, Inc. Launches ORALAIR®, the First and Only Sublingual Allergy Immunotherapy Tablet with a Mix of Five Grass Allergens for the Treatment of Grass Pollen Allergy<概要>Grass allergies are the most common seasonal allergy in the United States1,2 and most people are allergic to more than one type of grass.3 ORALAIR is the first and only FDA approved oral allergy immunotherapy tablet that includes a five grass, mixed pollens allergen extract. These grasses are widely distributed throughout the U.S.<感想>花粉症の舌下減感作療法。アメリカ向けなので、抗原が日本向けではありません。リンク先:http://www.greerlabs.com/files/ORALAIR-Launch-Day-4-30-14.pdf Kinex Receives US FDA Allowance for Oratecan, an Oral Form of Irinotecan with Enhanced Gastrointestinal Absorption, the Second U.S. IND Based on the Orascovery Technology Platform<概要>Kinex Pharmaceuticals, Inc. announced today that the United States Food and Drug Administration (FDA) has allowed its Investigational New Drug (IND) application for Oratecan, an oral form of an approved anti-cancer drug irinotecan with enhanced oral absorption.<感想>イリノテカンの経口剤の第1相試験が開始。Kinexは色々な制がん剤の経口化を研究している会社。FDA INDはパクリタキセルの経口化に続いて2剤目。昔制がん剤の開発をしているときに前期第2相試験が終わったときに世話人の先生からこの制がん剤は切れすぎる、経口剤としては危険が伴うので注意を伴う。ということをいわれたことを思い出しました。注射は医者の監視下で投与されますが、経口は医師の管理外で投与されることに警笛を鳴らしてもらったのだと思います。リンク先:http://www.kinexpharma.com/kinex-receives-us-fda-allowance-for-oratecan-an-oral-form-of-irinotecan-with-enhanced-gastrointestinal-absorption-the-second-u-s-ind-based-on-the-orascovery-technology-platform/今日はここまで。
2014年05月06日
コメント(0)
-
5月3日のプレスリリース
Merck and Endocyte Announce Independent DSMB Recommends Vintafolide PROCEED Phase 3 Trial Be Stopped for Futility Following Interim Analysis<概要>The Data Safety Monitoring Board (DSMB) of the PROCEED trial has completed a pre-specified, interim futility analysis and the DSMB recommended that the trial be stopped because vintafolide did not demonstrate efficacy on the pre-specified outcome of Progression-Free Survival (PFS) in patients with platinum-resistant ovarian cancer. PROCEED is a Phase 3 randomized, double-blind clinical trial, evaluating vintafolide in combination with pegylated liposomal doxorubicin (PLD) compared to PLD plus placebo for the treatment of folate receptor-positive, platinum-resistant ovarian cancer. The primary endpoint of the trial was PFS <感想>英語まんまですいません。日本ではVintafolideはMK-8109という治験コードで第1相試験が今年2月に始まったばかり。MK-8109はビンカアルカロイドと葉酸の複合体。MK-8109は卵巣がん他の葉酸受容体の過剰発減を生じているがん細胞に選択性を持たしています。Etarfolatideという卵巣がんにおける葉酸受容体の過剰発現を検出できる放射線画像診断用イメージング剤でターゲットを確認してから投与を行います。第2相試験の結果でEMAに製造販売承認新姓を行っています。PROCEED試験が中間解析でプラセボに対して無増悪生存期間の延長をえられないことがDSMBより勧告されたので、これから先に進むのはとても難しくなりました。リンク先:http://www.mercknewsroom.com/news-release/oncology-newsroom/merck-and-endocyte-announce-independent-dsmb-recommends-vintafolide-p (MerckのNews) http://www.clinicaltrials.jp/user/search/directCteDetail.jsp?clinicalTrialId=10939 (MK-8109 日本第1相試験の概要)FDA Issues Complete Response Letter for PLUMIAZ™, Investigational Medicine for Epilepsy Cluster SeizuresACORDA THERAPEUTICS<概要>U.S. Food and Drug Administration (FDA) has issued a Complete Response Letter (CRL) for the New Drug Application (NDA) for PLUMIAZTM (diazepam) Nasal Spray for the treatment of people with epilepsy who experience cluster seizures.A CRL is a communication from the FDA that informs a company that their review of the NDA is complete and the application cannot be approved in its present form. The Company is currently developing a response to address the items outlined in the letter.<感想>発作群発てんかんの点鼻薬がFDAが承認しなかったというニュースです。リンク先:http://ir.acorda.com/investors/investor-news/investor-news-details/2014/FDA-Issues-Complete-Response-Letter-for-PLUMIAZ-Investigational-Medicine-for-Epilepsy-Cluster-Seizures/default.aspxきょうはここまで
2014年05月04日
コメント(0)
-
5月2日のニュースリリース
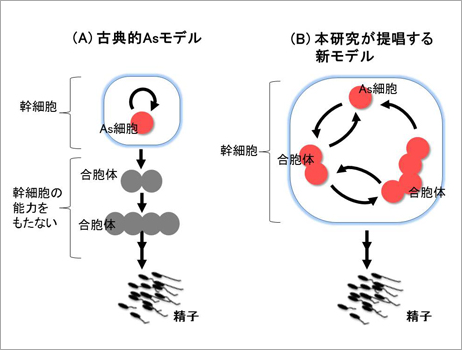
NF-κBデコイオリゴを用いたアトピー性皮膚炎治療薬の開発戦略を変更 新たな製剤技術を検討アンジェスMG<概要>塩野義製薬は平成 25年 6月より、株式会社メドレックス(本社:香川県東かがわ市、代表取締役社長 松村 眞良、以下、メドレックス)の経皮製剤技術を用いた NF-κBデコイオリゴのアトピー性皮膚炎治療薬について第I相臨床試験を実施してきました。今回、この試験データを分析した結果、現行の製剤については第II相臨床試験には進まず、臨床開発の成功確率を高める目的で新たな製剤技術の検討を行うことを決定。NF-κBデコイオリゴは通常の低分子医薬品に比べてサイズの大きな分子であり、医薬品として最適の効果を得るためには NF-κB デコイオリゴを効率的に皮膚透過させる製剤技術との組み合わせが重要となります。<感想>どんなにいい薬でも標的に届かなければ無効です。今回のNF-κBは免疫反応を強める遺伝子のスイッチ。デコイは遺伝子の働きを抑える短い核酸。短いといっても分子量は大きいし、立体構造が重要と言うことで、アンジェスも苦労しているようですね。スイッチを止めれば、生体のフィードバックが利いて他の経路から情報が行く可能性(実はこれが病気だったりして)もあるので、スイッチを入れてから電気がつくまでの経路(情報伝達系、効果発現系)に対する現在の薬の方が私は好きです。リンク先:http://www.anges-mg.com/pdf.php?pdf=100725.pdf精子幹細胞の知られざる性質が明らかに ~幹細胞は異なる状態を繰り返し行き来する~基礎生物学研究所 生殖細胞研究部門<概要>「精子幹細胞は、タイプの異なる細胞(As細胞と合胞体)がお互いの状態を繰り返し行き来しながら、どちらも区別なく幹細胞として機能する」という新説を提唱しました。<感想>実験方法は精巣ライブイメージング法で8000時間の映像と数理モデルの一致から結論にいたっています。こつこつとマウスの精巣を写し続けて新しい知見をえた研究者に脱帽です。ヒトの男性不妊の究明やその治療薬に貢献することを願います。リンク先:http://www.nibb.ac.jp/press/2014/05/02.html細胞外マトリクスの形態形成における新たな働きの発見独立行政法人理化学研究所<概要>成長期のヒトの血管系では、拍動の刺激に応じて血管内の細胞の再配置や増殖が起き、血流が最適化されるように管の形状が変化します。ところが、胚発生において血液循環が始まる前に、すでに血管はある程度適正な形状を獲得しています。気管に蓄積する細胞外マトリクスの性質を調べたところ、粘性の高いゾル状態の成分と弾性を持ったゲル状態の成分が存在していることが分かりました。これらの成分を損なう条件や、気管上皮細胞の管腔側の細胞膜(アピカル細胞膜)が過剰に拡大するショウジョウバエの変異体では、気管が過剰に伸長することが知られています。そこで、これらの変異体の解析データをもとに、気管形成の仕組みをシミュレーションする物理モデルを作りました。気管の長さと形状の安定は、気管の上皮細胞膜の拡張力と細胞外マトリクスの弾性力が拮抗することによって決まる、という仕組みが明かになりました。この成果は、細胞外マトリクスの形態形成に関わる新しい機能の発見であり、細胞が生物の管状組織を形作る細胞生物学的な見地からも興味深い発見。<感想>典型的な基礎研究。当たり前のようなことに疑問をもち、その原因を確かめるということは、すぐに臨床応用ができるものではありませんが大切なことです。この知見から臨床応用を思いつくのは別の才能と思いますが、その才能もこの発見がなければ不可能です。リンク先:http://www.riken.jp/pr/press/2014/20140502_1/横浜市立大学医学群 石ヶ坪教授らの研究グループが、ベーチェット病発症に細菌が関与していることを遺伝学的に証明横浜私立大学<概要>日本人・トルコ人計約5,000例の患者・健常人の検体を解析しました。細菌成分を認識する分子など自然免疫に関わる遺伝子11個と、ゲノムワイド関連解析でみつかった10個の遺伝子のエキソンを、次世代シーケンサーを用いて解析したところ、グラム陰性菌の成分やグラム陰性菌やグラム陽性菌の成分の受容体変異の分布が、ベーチェット病においては、健常人と比較して、これらの細菌に対する反応が異なる可能性があります。また、家族性地中海熱の原因遺伝子MEFV*5 M694V(694番目のパイリンという蛋白質のメチオニンがバリンに置換)を持つひとではベーチェット病になりやすいことが証明されました。<感想>現在のベーチェット病の治療は軽度の場合はコルヒチン、重篤な場合はステロイドやサイクロスポリンが使われます。TNF-α抗体も処方される場合があります。今回の研究は細菌の受容体の変異が明らかにしました。治療はその変異した受容体を元に戻すことか、変異受容体が細胞内でどのようなシグナルを出しているかがわかれば、そのシグナルを元に戻す、あるいは調節することが考えられます。TNF-α抗体がその役割を果たしているのかもしれません。リンク先:http://www.yokohama-cu.ac.jp/res_pro/researcher/小児の遺伝性疾患「ファンコニ貧血」病態の完全解明への一歩 ~キー分子FANCD2に会合するCtIPタンパク質の同定~京都大学<概要>小児遺伝性疾患「ファンコニ貧血」(FA)の病態の解明を目指しており、今回、ファンコニ貧血に関連したキー分子であるFANCD2が、DNA修復機構において中心的役割をはたすCtIPタンパク質を結合し、その制御を行うことを発見。「ファンコニ貧血症」は、まれながらDNA損傷修復の欠損による典型的な病態として有名であり、「家族性乳がん」と原因遺伝子が共通であることなどから、学術的な重要性が高く、注目されている疾患。骨髄における造血幹細胞の維持と白血病化を防ぐしくみである「DNA損傷修復」の具体的メカニズムを明らかにし、病態の理解をさらに深めるために有意義<感想>ちょっとずれますが、「家族性乳がん」をもつ男は「ファンコニ貧血」を発症するのか?がんは遺伝的要素が高いと言われていましたが、今回の「家族性乳がん」のように遺伝子が特定されているものを除けば、食生活の類似性の方が発がんに関与していると言われています。リンク先:http://www.kyoto-u.ac.jp/ja/news_data/h/h1/news6/2014/140502_2.htmがん細胞が集団で浸潤するための分子メカニズムを解明名古屋大学<概要>がん細胞集団に存在する細胞が、自身の前に細胞がないことを関知し、インテグリンβ1の発現を促進。インテグリンβ1の発現が、がん細胞が集団として周りの細胞に浸潤していくことが重要であることを証明。<感想>細胞集団がインテグリンβ1を発現する先頭細胞群に率いられ、転移していくという仮設です。インテグリンβ1の発現を抑制すれば転移が防げるかもしれません。昔は細胞間接着を失い、一細胞レベルで転移するという仮説が主流でした。15年ぐらい前の話です。がん細胞を生きたまま観察できるようになり、この仮説は力を失いました。今日は大学のプレスリリースが多かったので基礎の話が主となりました。今日はここまで。
2014年05月03日
コメント(0)
-
5月1日のプレスリリース
フルタミド錠125「KN」 PTP包装デザイン変更のお知らせ発売元:ヤクルト本社 製造販売元:小林化工<感想>毎日飲む薬は14錠にならないかなと思います。わたしはもらったときにばらさないので、14錠包装だと飲み忘れが少なくなると思います。対応している薬剤もあります。リンク先:http://www.yakult.co.jp/ph/news/files/?type=news&id=139883549775.pdf抗てんかん剤トピナ®の新たな剤形「トピナ®細粒10%」の発売について協和発酵キリン<概要>2014年5月13日、抗てんかん剤「トピナ®細粒10%」を発売。一部の小児や高齢者など錠剤を飲みにくいてんかん患者さんに対しても服用しやすく、服薬アドヒアランスの向上が期待されます。<感想>医者からみて患者さんが薬を飲むのがンプライアンスで、患者がICに基づき自発的に薬を飲むのがアドヒアランスだそうです。アドヒアランス向上は患者さんが飲みやすい、飲みたくなるということだそうです。リンク先:http://www.kyowa-kirin.co.jp/news_releases/2014/20140501_01.html高い挿入性・処置性能と、高画質を兼ね備えた細径内視鏡下部消化管用処置用スコープ「EC-580RD/M」富士フイルム<概要>挿入性と処置性能を高め、当社独自の画像センサー「スーパーCCD ハニカム™」による高画質を実現した下部消化管用処置用スコープ「EC-580RD/M」を、本日より富士フイルムメディカル株式会社(社長:平井 治郎)を通じて発売。処置中は、処置する部位を明瞭にするためにウォータージェットノズルから出した水や消化管内の粘液などの吸引、処置具の出し入れを鉗子口から何度も繰り返します。本製品は、細径化しながらも鉗子口径3.2mmを確保し、処置具の出し入れを容易にするとともに、高い吸引性能を両立しました。また、ウォータージェットノズルと鉗子口の配置を工夫し、目的部位への送水と処置具での処置を必要最小限の動作で切り替えることができます。さらに、内視鏡先端部の湾曲角210°を実現。小回り・旋廻性能に優れているため、大腸内にある輪状ひだの裏側など観察しにくい部位の観察が容易になります。<感想>開腹、開胸手術は交通事故に遭ったぐらいのダメージを受けると聞いたことがあります。(話は具体的にみえますが、どれぐらいの衝撃かよくわからない表現ですね。)術後1か月程度入院していたのはそのダメージから開腹するため。それを考えると内視鏡手術というのは患者の負担が少ない手術なんですね。リンク先:http://www.fujifilm.co.jp/corporate/news/articleffnr_0872.html?ref=rssがん治療薬HF10の第II相臨床試験実施申請資料を米国食品医薬品局へ提出タカラバイオ<概略>米国でがん治療薬HF10の第II相臨床試験を実施するため、本年4月30日(米国時間)に、米国食品医薬品局(FDA; Food and Drug Administration)に臨床試験実施申請資料(IND; Investigational New Drug)を提出しました。本試験では、治癒切除不能または転移性悪性黒色腫を対象とし、HF10とIpilimumab(商品名:YERVOY®)を併用投与した際の有効性、安全性、免疫学的検査などの評価を行う予定です。<感想>HF10は、単純ヘルペスウイルスで、がん細胞で特異的に増殖するとされています。動物実験レベルでは免疫応答も誘導されることから投与されていない場所の腫瘍に効果が期待されます。正常細胞に対する影響は0とは証明されていないので、投与法は腫瘍内投与となっています。この仮説はとても魅力的ですが、まだ越えるべき壁は大きいと思います。昔、ミニブタのランゲルハンス島細胞を人へ応用することを研究していました。世界でいくつかの研究所と争っていたのですが、ミニブタのDNA(RNAだったかな)にヒトのウイルスに対応する配列があることがわかり、あっという間に研究は中止されてしまいました。リンク先:http://www.takara-bio.co.jp/news/2014/05/01.htm液状細胞診を利用したHPV併用検診サービス開始のお知らせ ジェネティックラボ<概要>ジェネティックラボ(代表取締役社長:福永健司、北海道札幌市)は、2014 年 6 月 1 日から、液状細胞診を利用したヒトパピローマウィルス(HPV)併用検診サービスを開始いたします。液状細胞診用に採取した検体を発がん性の HPV を発見する検査に用いることによって、細胞の採取が一度で済み、受診者の負担を最小限に抑えることを可能とするもの。液状細胞診は従来法の直接塗抹法による細胞診に比べ、異型細胞の検出率が向上します。<感想>ということです。リンク先:http://www.gene-lab.com/new/post_73.htmlきょうはここまで。
2014年05月02日
コメント(0)
-
4月30日のニュースリリース
大塚製薬、新規抗結核薬 「DeltybaTM」(デルティバ)多剤耐性結核の適応症で欧州にて承認取得大塚製薬<概要>大塚製薬が独自に創製した新規抗結核薬「Deltyba」(デルティバ)が初めて承認され、多剤耐性結核の治療が欧州で可能となる。1971年大塚製薬初の治療薬研究所設立時、当時社長の大塚明彦(現大塚ホールディングス代表取締役会長)が掲げた最初の研究テーマのひとつが結核であった。大塚製薬は抗結核薬の開発に最も多くの投資をしている。<感想>リファンピシン以来の抗結核薬。抗痛風剤のアロプリノールに次ぐ新薬が出るまで時間がかかりましたが、これもそれに匹敵するぐらい期間が空いていると思います。リンク先:http://www.otsuka.co.jp/company/release/2014/0430_01.html血小板減少症治療薬に関するライセンス契約の終了について小野薬品工業、日産化学工業<概要>小野薬品と日産化学工業は、2014年 4 月 30 日をもって新規血小板減少症治療薬に関するライセンス契約を終了することに合意しましたので、お知らせいたします。 NIP-022は日産化学が創製した新規血小板減少症治療薬です。造血因子であるトロンボポエチンの受容体を活性化することにより血小板数を増加させる、経口投与が可能な低分子化合物です。<感想>日産化学工業は医薬品に関してリパロ(スタチン)、ランデル(Ca拮抗薬)といった実績持っています。特許を取って、製薬メーカーに開発を任せるというスタンスで、製薬メーカー内では変わったポジションを持っています。血小板減少症に関しては抗悪性腫瘍剤の血球系副作用は白血球がG-CSF+抗生物質である程度対応できるようになってきただけに、血小板減少症の対応は原因薬剤の投与中止がメインで、重症の場合はステロイドやγ-グロブリンの大量療法、出血時の血小板輸血の現状を打破し、ブレークスルーがえられる可能性があると思うのですが。G-CSF併用で投与量、投与期間を延長し、結果として効果の増強がえられた抗悪性腫瘍剤もあると聞きます。リンク先:http://www.ono.co.jp/jpnw/PDF/n14_0430.pdfCOPD 治療薬1日1回吸入「ウルティブロ®ブリーズへラー®」の LANTERN 試験の結果 および中国での承認申請の時期についてそーせいグループ<概要>ノバルティス社へ導出しているグリコピロニウム臭化物(開発コード:NVA237、製品名:シーブリ®ブリーズへラー®、(以下、「シーブリ」))を含有する1日1回吸入の「ウルティブロ®ブリーズへラー®」(開発コード:QVA149、インダカテロールマレイン酸塩 110μg/グリコピロニウム臭化物 50μg(以下、「ウルティブロ」))につきまして、導出先のノバルティス社が第III相臨床試験である直接比較 LANTERN 試験の結果を発表しました。LANTERN 試験は、中国、アルゼンチン、チリおよび台湾 6の 56 施設において実施された、26週間の無作為、二重盲検、平行群間比較試験です。当試験では、過去一年以内に増悪を経験または未経験の中等症から重症の COPD 患者さん 741 人を対象に SFC に対する「ウルティブロ」の有効性と安全性が評価されました。<概要>抗コリン薬とβ2刺激剤の併用なので、組み合わせは色々あるともいますが、吸入なので別々は煩雑。配合剤となっていますが、本当にいい組み合わせかどうかは最近は問われないようです。リンク先:http://www.sosei.com/pdf/press_jp_20140430_462.pdf国際総合科学群教授大関泰裕の糖鎖生物学研究ユニットが、理研バイオ解析チームと共に、スフィンゴ糖脂質の糖鎖構造を解読し腫瘍細胞の増殖抑制を惹起する、全く新規なレクチン"MytiLec"の一次構造を決定!横山私立大学<概要>軟体動物二枚貝のムラサキイガイから、Fabry病の蓄積物やO157菌毒素の標的として知られるグロボトリオース(Gb3)スフィンゴ糖脂質に結合し、本糖鎖を発現するリンパ腫細胞を選択的に殺傷するMytiLecレクチンタンパク質を発見。糖鎖結合の仕組みを原子レベルで解析していくことで、Gb3スフィンゴ糖脂質に結合したMytiLecからどのようなシグナルが発信され、リンパ腫細胞が死んでいくのかなど、細胞機能に関する生命科学の新たな知見が解明されていく可能性があります。<感想>抗体系の抗悪性腫瘍剤あるいはそのキャリアーになる可能性があると思いますが、いかんせん分子量が大きい。生体内で腫瘍が1細胞レベルで発生したときにその成長を止めることを既にやっているという仮説はいかがでしょう。リンク先:http://www.yokohama-cu.ac.jp/res_pro/researcher/ PQBP1遺伝子変異が関与する知的障害の原因を解明東京歯科医科大学<概要>知的障害の発症にpolyglutamine-tract binding protein 1 (PQBP1)遺伝子の変異が関与することに着目し、PQBP1 タンパク質の機能障害が生じる原因を解明しました。PQBP1遺伝子の変異によって生じる知的障害は、YxxPxxVLモチーフが欠損することでPQBP1がRNAスプライシングに於いて正常に機能しないことが原因と考えられます。RNAスプライシングは脳神経機能分子を含む様々な遺伝子の発現に重要な役割を果たすことが知られており、今後の研究進展により、知的障害の分子メカニズム理解と治療開発につながることが期待されます。 <感想>もやもやするなぁ。PQB1たんぱく質の生体内での働きを明確にした方がいいと思います。リンク先:http://www.tmd.ac.jp/archive-tmdu/kouhou/20140430.pdfSall1は活性化因子及び抑制因子として働いて腎臓ネフロン前駆細胞と初期ネフロンを維持している熊本大学<概要>Sall1がネフロン前駆細胞の自己複製と維持に必須であることを見いだしました。腎臓発生分野は2013年末に、ヒトiPS細胞からネフロン前駆細胞の誘導に成功しています。今回の研究で得られたネフロン前駆細胞の維持機構に関する知見は、ネフロン前駆細胞を人為的に増幅する技術開発に向けた基盤として極めて有用です。<感想>幹細胞やiPS細胞あるいはSTAT細胞(まだ分かりませんが)がある臓器の細胞に分化したのち、どんなふうに臓器を形成していくかにはまだ大きな壁があると思います(最初のSTAT細胞で100年かかると小保方さんが言っていたのはこのあたりかもしれません)非常に荒っぽい言い方をすると頸椎障害で車いす生活になった人に幹細胞を頸椎神経に振りかけてやると神経が修復し、車いすが不要になることはひとで明らかにされている(非常に非倫理的な実験ですけれども)、皮膚もそうかもしれません。その他の臓器は前駆細胞がどのように臓器になっていくかはわかっていません。この研究はそれにひとつの道具を提供(腎臓に限られますが)したことになります。この研究だけでも12年かかっています。リンク先:http://www.imeg.kumamoto-u.ac.jp/newpress/np70.htmlケトプロフェン(外皮用剤)の妊娠中における使用について厚生労働省 医薬品・医療機器安全性情報第312号<概要>ケトプロフェン製剤の妊娠中の使用については,坐剤及び注射剤は既に妊娠後期の女性への使用が禁忌とされていますが,外皮用剤については禁忌とされていませんでした。妊娠中の女性がケトプロフェンのテープ剤を使用し,胎児に胎児動脈管収縮等の副作用が起きた症例が新たに集積したことから,医薬品医療機器総合機構(以下,「PMDA」という。)は妊婦に対する更なる注意喚起の必要性について対応を検討しました。妊娠後期の女性がケトプロフェンのテープ剤1日1枚を1週間使用して胎児に動脈管収縮が起きた症例があること,また,これまでの国内症例の集積や既にケトプロフェンの坐剤及び注射剤で妊娠後期の女性が禁忌になっていることも踏まえると,テープ剤についても坐剤及び注射剤と同様の注意喚起が必要と判断しました。また,テープ剤以外の外皮用剤についても同様の事象が起こる可能性があるため,厚生労働省はケトプロフェンの全ての外皮用剤の製造販売業者に対し,平成26年3月25日付で妊娠後期の女性への使用を禁忌とするよう使用上の注意の改訂を指示しました。<感想>テープ剤でも血管内に発現し、胎児に影響を与えるのは知らなかったのでびっくり。この副作用は命に関わるものではないので、いいと言えばいいですが、胎児毒性のある薬剤はたとえテープ剤であっても注意が必要と言うことですね。ただし、発生率がわかりませんので、リスクがどれぐらいなのかよくわかりませんが。薬局でも売っているので妊婦の方は気をつけてください。リンク先:http://www1.mhlw.go.jp/kinkyu/iyaku_j/iyaku_j/今日はここまで
2014年05月01日
コメント(0)
-
4月29日のプレスリリース
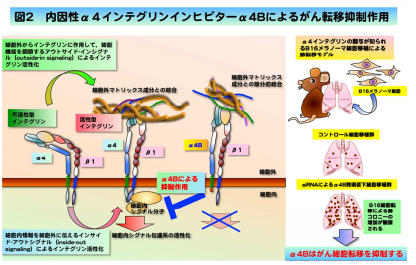
昭和の日だったせいか、企業のプレスリリースは見つかりませんでした。幹細胞の多能性に関わるレトロトランスポゾン由来のRNA理化学研究所<概要>これまで知られていなかった数千種類のRNAがiPS細胞やES細胞の核内で発現していることを見いだし、その一部が幹細胞に特徴的な多能性の維持に関与している可能性があることを明らかにしました。ゲノムに存在するレトロトランスポゾン由来の配列は、大多数が機能を持たない「ジャンクDNA」とこれまで考えられてきました。ES細胞やiPS細胞において、レトロトランスポゾンの断片が活性化し、そこから転写されるRNAが多能性の維持に関与していることを示す今回の発見は、幹細胞においてncRNAが重要な役割を果たしていることを示唆します。今後さらにNASTsの機能を解明することで、幹細胞特有の転写制御ネットワークの理解が深まり、iPS細胞から目的細胞を効率よく分化させる方法の開発などへの応用が期待できます。リンク先:http://www.riken.jp/pr/press/2014/20140429_1/#fig3<感想>細胞をガラス管に通して酸性環境で培養すると、レトロトランスポゾンの断片が活性化し、そこから転写されるRNAが多能性の維持をしてるのかな?理化学研の研究だから、あの細胞も検討していたりして。 今日はこれだけ
2014年04月30日
コメント(0)
-
4月28日のプレスリリース
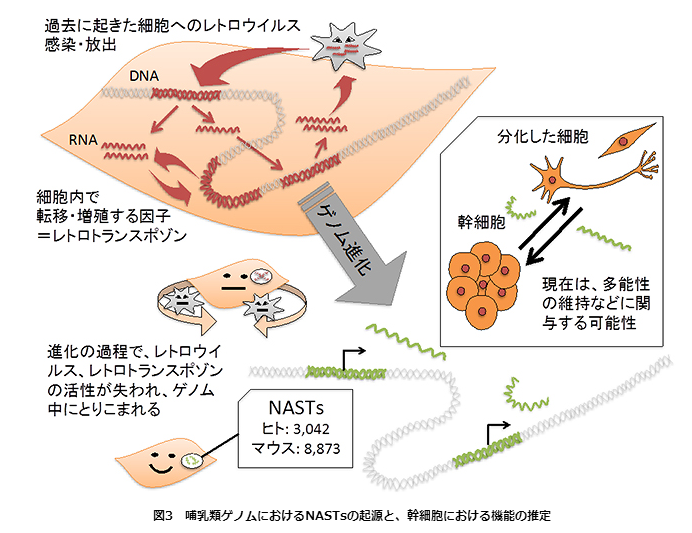
リンク先の後のURLをクリックするとリンク先に飛ぶようにしました。テバ社と武田薬品におけるパーキンソン病治療薬ラサジリンに関する 日本での提携について 武田薬品工業<概要>テバ社が保有するパーキンソン病治療薬ラサジリン(一般名、以下「ラサジリン」)の日本における製品化に関する契約を締結しましたのでお知らせします。 ラサジリンは、ドーパミンの分解酵素であるモノアミン酸化酵素 B(MAO-B)の働きを阻害することによって、脳内のドーパミン濃度を高め、本疾患に特徴的な運動症状などを改善する薬剤です。<感想>パーキンソン病という語句が効能効果に出てくる薬剤は85品目とかなり多いですが、L-dopaが基本でそれに追加の壁はまだまだ破れていないような気がします。テバ社は世界最大のジェネリック企業で有名ですが中枢神経系などのスペシャリティ医薬品もやっているんですね。リンク先:http://www.takeda.co.jp/news/2014/20140428_6441.html (武田) http://www.teva.jp/news/2014/pdf/0428.pdf (テバ)2014年日本リウマチ学会総会・学術集会にて抗TNF-α抗体「セルトリズマブ ペゴル(一般名)」の国内臨床試験における総合的疾患寛解、および長期的な身体機能及び健康関連QOL改善効果について発表アステラス製薬<概要>PEG化*1抗TNF-α(腫瘍壊死因子α)抗体「セルトリズマブ ペゴル」(一般名、日本での製品名「シムジア®皮下注200mgシリンジ」、以下「シムジア®」及び欧米での製品名Cimzia®)の関節リウマチを対象とした国内臨床試験(J-RAPID及びHIKARI試験)の成績を基に追加解析を行いComprehensive Disease Remission(CDR)、および長期的な身体機能及び健康関連QOL改善効果について、2014年4月24、25、26日に東京で開催された日本リウマチ学会総会・学術集会にて発表しました。<感想>「シムジア®」は2013年3月に発売されています。自己注射も可能なプレフィルドシリンジ。TNF-α抗体でリウマチの治療はかなり進みました。インフォームドコンセントからアドフィアランス(患者が積極的に治療方針の決定に参加し、その決定に従って治療を受けること)の概念も本物になりつつあります。リンク先:http://www.astellas.com/jp/corporate/news/detail/2014tnf-qol.htmlロシュ社、欧州にて中等度から重度の関節リウマチ患者さんにより自由度の高い治療を提供するRoACTEMRAの新しい皮下注製剤の承認を取得中外製薬<概要>他のリウマチ薬に対する、忍容性が低い、または治療反応が得られなかった中等度から重度の関節リウマチ(RA)患者さんに対するRoACTEMRA(tocilizumab)の皮下注製剤の承認を、欧州委員会より取得したことを発表。<感想>TNF-α抗体に続くIL-6受容体抗体です。プレフィルドシリンジは2013年に承認されています。リンク先:http://www.chugai-pharm.co.jp/hc/ss/news/detail/20140428140000.html2型糖尿病治療薬「ビデュリオン®」~ペン型製剤を国内承認申請アストラゼネカ<概要>2型糖尿病治療薬「ビデュリオン®皮下注用(一般名:エキセナチド)」のペン型製剤を国内で製造販売承認申請いたしました。ビデュリオン®皮下注は、GLP-1受容体作動薬であるエキセナチドを有効成分とする世界で初めての週1回投与の2型糖尿病治療薬です。週1回の投与で安定かつ優れた血糖コンロトール改善効果を示し、アドヒアランスの向上が期待できます。<感想>2型糖尿病のターゲットも増えてきました。週1回の投与ですむならかなりコンプライアンスが上がるのでしょう。リンク先:http://www.astrazeneca.co.jp/media/pressrelease/Article/20140428がん細胞転移を抑制する新たな細胞接着制御メカニズムを解明 北海道大学<概要>細胞接着レセプターα4 インテグリンのスプライシングバリアントα4B を同定した。α4B はα4 インテグリンの関与が知られるメラノーマがん細胞転移を抑制した。α4B はα4 インテグリンの関与が知られるメラノーマがん細胞転移を抑制した。 <感想>なかなかヒトでは聞かなかった血管新生抑制剤もようやく使われるようになったし、転移抑制剤も日の目を見る日も近いと思います。ただ無増悪生存期間が腫瘍評価項目と考えられるので、プロトコールを考える人は大変だと思います。リンク先(直接PDFが出ます):http://www.hokudai.ac.jp/news/140428_pr_pharm.pdfきょうはここまで。
2014年04月29日
コメント(0)
-
4月23日のプレスリリース
バイエル社のリオシグアト 肺動脈性肺高血圧症の治療薬として効能追加承認申請を日本において提出バイエル薬品<概要>日本において、リオシグアトの肺動脈性肺高血圧症(PAH)に対する効能追加承認申請を行いました。PAH は、進行性の病態であり、肺動脈の血圧が大幅に上昇し、心不全や死亡に至ることがあります。リオシグアトは、2014 年 1 月に生命を脅かす別の型の肺高血圧症である慢性血栓塞栓性肺高血圧症(CTEPH)の経口治療薬として、「アデムパス®錠」の販売名で厚生労働省から承認を取得しています。単剤療法、または PAH 治療に使用する他の特定の薬剤[エンドセリン受容体拮抗薬(ERA)または非経静脈的プロスタサイクリン誘導体(PCA)など]との併用療法のいずれにおいても、第 III相臨床試験において PAH を対象に臨床的に重要な複数の評価項目全体を通じて有意な臨床的有効性が速やかかつ持続的に認められた経口治療薬です。リオシグアトは、歩行可能距離を有意に延長し、心臓や肺の機能を向上させ、日常活動時の呼吸を楽にします。 その結果リオシグアトを投与した PAH 患者において疾患の重症度が持続的に改善することが示されました。<感想> 肺高血圧症(PH)特に肺動脈性高血圧症(PAH)の新薬が続々と出てきます。予後が不良なので、いいことです。リンク先:http://byl.bayer.co.jp/html/press_release/2014/news2014-04-23.pdfサラシア属植物抽出物が平成25年度「食品の機能性評価」において食後血糖上昇抑制の機能で、総合評価「B」を取得 森下仁丹<概要>森下仁丹株式会社(本社:大阪市中央区/代表取締役社長:駒村純一)は、公益財団法人日本健康・栄養食品協会(所在地:東京都新宿区) が実施する平成 25 年度「食品の機能性評価」に、「サラシア属植物抽出物」をサラシア属植物普及協会として応募し、厳正なる審査の結果、総合評価「B」を取得しました。評価した機能: 食後血糖上昇抑制<感想>健康食品は保健機能食品(国が制度を創設して機能表示等を許可したものと)、といわゆる健康食品に分かれます。医薬品の場合、重大な副作用が出た場合は医薬品副作用救済制度がありますが、健康食品にはありません。伝聞調の表現は、逆に効果がないと考えた方がいいのかもしれません。また、医薬品成分が入っている場合もありますが、含有量などの品質管理が十分でない場合もありますので、GMPマークがついているものを選んだ方が無難です。リンク先:http://www.jintan.co.jp/pdf/bhp_file.pdf「ナノピア® eTDM メトトレキサート」 新発売のお知らせ積水メディカル<概要>積水メディカル株式会社(社長:田頭 秀雄、本社:東京都中央区、以下積水メディカル)は、血中薬物濃度測定用試薬である「ナノピア® eTDM メトトレキサート」を4月8日に新発売しましたのでお知らせします。「ナノピア® eTDM メトトレキサート」は、 抗悪性腫瘍薬(抗がん剤)であるメトトレキサートの血中濃度測定用試薬です。ホモジニアスエンザイムイムノアッセイを測定原理とし、生化学自動分析装置での簡便測定が可能です。測定時間も約10分間と迅速であり、調製不要な液状試薬であるために、緊急検査にも対応することが可能です。<感想>体外診断用医薬品でないのが残念。自動分析装置で使えるので、便利。リンク先:http://www.sekisuimedical.jp/news/release/140423.html熱帯熱マラリア原虫の増殖阻害薬候補物質の開発東京大学大学院農学生命化学科<概要>硫酸化ジェランは新規の材料から合成された熱帯熱マラリア原虫の増殖阻害薬の候補物質であるため、この薬剤機序の解明を行うことで、新たなマラリア治療薬の開発につながることが期待されます。<感想>今のマラリア治療薬はお酒が飲めないので、新薬に期待。リンク先:http://www.a.u-tokyo.ac.jp/topics/2014/20140423-1.htmlICHQ4B ガイドラインに基づく事項別付属文書(製剤均一性試験法)について厚生労働省医薬食品局審査管理課長<概要>日米 EU 医薬品規制調和国際会議(ICH)において、「ICHQ4B ガイドライン(平成 21 年 5 月 26 日付け薬食審査発第 0526001 号厚生労働省医薬食品局審査管理課長通知)」の事項別付属文書として、別添のとおり製剤均一性試験法について、付属文書(以下「本文書」という。)がとりまとめられました。<感想>日米EUなんですね、日米欧とおもいこんでました。リンク先:http://wwwhourei.mhlw.go.jp/hourei/doc/tsuchi/T140423I0010.pdf
2014年04月24日
コメント(0)
-
4月22日のプレスリリース その2
追加です。 製薬企業による臨床研究支援の在り方に関する基本的考え方日本製薬工業協会 協会会員向け<概要> 本年 4 月 11 日には報告書「高血圧症治療薬の臨床研究事案を踏まえた対応及び再発防止策について」が取りまとめられたが、この検討の過程においては、製薬企業に対しても、今後の臨床研究支援の在り方に関し、指摘や要請が行われている。 ○自社医薬品の臨床研究に対する資金提供や物品供与等の支援は、契約により実施すること。○臨床研究における客観性と信頼性を確保するためには、利益相反関係に十分留意の上、支援を行うこと。○今後自社医薬品に関する臨床研究に対する資金提供の支援方法としては用いないこと。<感想>「奨学寄付金」が本来の趣旨に則り使われるには越したことはありません。契約をきちんとして行えば、うまくいくかな?テレビでお金をもらうと手心を加えたくなるなんてお医者さんには契約だろうと寄附金だろうと同じような気がします。解析担当者の個人的な犯罪みたいにいわれていたけど、監査とか品質管理はそれがわからなかったこと自体が薬事法違反のような・・・リンク先:http://www.jpma.or.jp/about/basis/code/また明日。
2014年04月23日
コメント(0)
-
お薬のプレスリリース 4月22日分
今日からお薬関係のニュースリリースの概要と感想を書くことにしました。新規抗悪性腫瘍剤 ET-743(トラベクテジン)が悪性軟部腫瘍患者を対象とした第II相臨床試験において無増悪生存期間の延長目標を達成大鵬薬品工業<概要>抗悪性腫瘍剤ET-743(一般名:トラベクテジン、欧州販売名:Yondelis®、以下本剤)が、染色体転座が報告されている組織型の悪性軟部腫瘍患者を対象とした第II相臨床試験において、無増悪生存期間の延長目標を達成したことをお知らせします。<感想>大鵬薬品工業はFT-207からティーエスワンにいたる自社開発の抗悪性腫瘍剤と導入品の二本柱でやっている会社。今回は導入品。悪性軟部腫瘍は稀少なので、承認も早いかもしれません。リンク先:http://www.taiho.co.jp/corporation/news/2014/20140422.html分子標的DDS技術を用いた線維症治療薬 肝硬変治療薬の第I相試験にてヒトへの投与を完了日東電工(Nitto)<概要>2008年から 札幌医科大学の新津洋司郎特任教授と共同で、肝硬変をはじめとする臓器線維症治療薬の開発を進めてまいりました。2013年6月より米国で治験第I相試験を開始し、このたび健常人に対する投与を完了致しました。引き続き第I/II相試験にて患者様への安全性と薬効の検証を行います。線維化の原因を選択的に抑えるsiRNAを薬物として用い、ビタミンA誘導体を標的化剤として患部にのみ選択的に送達する(薬物の送達と作用の双方に特異性を有する)安全性を志向する薬です。また、線維症の根本的な治療に繋がる世界初の薬。<感想>特発性肺線維症の薬としては塩野義製薬の「ピレスパ®錠」がありますが、これは線維化の進行を止めるだけ。臓器線維化に関しては東北大名誉教授の京極方久先生(病理)が「治せんわけがない、細胞は入れ替わるのだから」という言葉を思い出します。富士フイルムをはじめとしてフィルム関連の企業が製薬によく進出しています。第II相以降はどこかの製薬メーカと組むのでしょう。「薬物の送達と作用の双方に」といえば中外製薬の「カドサイラ®」、ビタミンAにあたるのが「トラスツズマブ(ハーセプチン®)リンク先:http://www.nitto.com/jp/ja/press/2014/0422.jspアテローム切除型血管形成術用カテーテル「ニプロ DCA」製造販売承認取得のお知らせニプロ<概要>ニプロ株式会社は、虚血性心疾患の狭窄または閉塞した冠動脈に対して、回転する小型内蔵型カッターで病変部を切削してアテロームを取り込み、体外に取り出すことを目的としたカテーテル「ニプロ DCA」の医療器機の製造販売承認を、2014年3月26日に取得しましたのでお知らせいたします。<感想>虚血性心疾患のカテーテル治療は風船を膨らませる「バルーン術」、小さな金属の網をつける「ステント治療」、石灰化した血管内のコレステロールの塊を砕く「ロータープレータ」、カテーテルのさきのカッターで塊を取り除くDCA(Directional Coronary Atherectomy)があります。最近はエキシマレーザーを使って細胞を砕いてしまうというのもあります。どれにしても再狭窄が問題です。リンク先:http://www.nipro.co.jp/ja/news/2014/document/140422.pdf世界初の化学発光酵素免疫測定法によるproPSA測定試薬 アクセス ハイブリテック p2PSA(研究用試薬) 発売ベックマン・コールター<概要>世界初の化学発光酵素免疫測定法によるproPSA測定試薬「アクセス ハイブリテック p2PSA」を、2014年5月1日(木)に発売します。前立腺特異抗原(PSA)のうち、[-2]proPSAは最も前立腺がんに特異的であると報告されています。「アクセス ハイブリテック p2PSA」は、血清中の [-2]proPSA 濃度を測定する研究用試薬です。<感想>わざわざ、研究用試薬と断っているのは健康保険が利かないからと思います。(厚労省の認可が必要)PSA抗原は一般的は健診でも測定することがあるぐらいメジャーです。前立腺腫瘍は前立腺針生検を行って確定としますが、グレーゾーンの場合の針生検が減らせるかもしれません。針生検は針で細胞をとるので、場所が悪ければ偽陰性になるし、変なところに刺すと出血が起こるので、無駄な生検を減らせるのはいいことだと思います。リンク先:http://www.beckmancoulter.co.jp/press/140422.html 今日はここまで
2014年04月23日
コメント(0)
全841件 (841件中 801-841件目)